Identifikasi dan Keragaman Genetik Longtail Tuna (Thunnus tonggol) Yang Didaratkan di PPI Kedonganan dan PPP Muncar Menggunakan Marka D-loop Mitokondria
on
Journal of Marine and Aquatic Sciences 7(1), 94-102 (2021)
Identifikasi dan Keragaman Genetik Longtail Tuna (Thunnus tonggol) Yang Didaratkan di PPI Kedonganan dan PPP Muncar Menggunakan Marka D-loop Mitokondria
Enex Yuniarti Ningsih a*, Elok Faiqoh a, Ida Ayu Astarini b, Putu Dian Pertiwi c, Andrianus Sembiring c, Ni Luh Astria Yusmalinda c, Muhammad Danie Al Malik c
a Program Studi Ilmu Kelautan, Fakultas Kelautan dan Perikanan, Universitas Udayana, Badung, Bali – Indonesia b Program Studi Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Badung, Bali – Indonesia c Biodiversitas Indonesia (Bionesia), Denpasar, Bali – Indonesia
* Penulis koresponden. Tel.: +62-818-060-01419
Alamat e-mail: yuniartiningsih3@gmail.com
Diterima (received) 12 Juli 2019; disetujui (accepted) 2 November 2021; tersedia secara online (available online) 2 November 2021
Abstract
Longtail tuna (Thunnus tonggol) is one of the oceanodromus neritic species and the migration pattern follows the water currents. Currently, this species has not been widely studied in Indonesian waters, so it is nesessary to study the identification of morphology and genetic diversity. The molecular approach employed in this study is DNA barcoding using mitochondrial D – loop locus. This study can explain the importance of species genetic information in stability and resilience. This study aims to determine the identification of morphology, phylogenetic and genetic diversity of longtail tuna at two locations in PPI Kedonganan, Bali dan PPP Muncar, Banyuwangi. The molecular analysis was done in several stages, i.e DNA extraction, Polymerase Chain Reaction, electrophoresis and sequencing. Based on the result of sequencing and analysis, 33 samples of longtail tuna was found. The result of phylogenetic tree reconstruction from two locations showed one clade with genetic distance value among longtail tuna species ranging from 0.000 – 0.042 for all close kinship samples. The haplotype diversity (Hd) value of longtail tuna was 0.9905 and nucleotide diversity (π) was 0.020. The high value of genetic diversity indicated that two longtail tuna populations have a high survival ability to adapt on environmental changes. Index fixation analysis (Fst) has a value of 0.0299, p -value > 0.05. The index fixation value indicated no significant population difference. The result of this study can be use as basic data in planning genetic conservation strategies with sustainable fisheries management efforts.
Keywords: longtail tuna; genetic marker; mtDNA; sequencing
Abstrak
Longtail Tuna (Thunnus tonggol) merupakan salah satu spesies tuna neritik yang bersifat oseanodromus dan pola migrasi mengikuti arus perairan. Hingga saat ini, penelitian spesies ini belum banyak dilakukan di Perairan Indonesia sehingga perlu adanya pengkajian identifikasi morfologi dan keragaman genetik. Pendekatan molekuler yang digunakan dalam penelitian ini adalah DNA barcoding menggunakan lokus D – loop mitokondria. Pemahaman hal tersebut dapat menjelaskan arti penting dari pengetahuan informasi genetik suatu spesies dalam stabilitas dan ketahanan populasi. Tujuan penelitian ini adalah untuk mengetahui identifikasi morfologi, filogenetik dan keragaman genetik pada longtail tuna di dua lokasi berbeda yaitu PPI Kedonganan, Bali dan PPP Muncar, Banyuwangi. Analisis molekuler yang dilakukan yaitu tahapan ekstraksi DNA, Polymerase Chain Reaction, elektroforesis dan sekuensing. Berdasarkan hasil sekuensing dan analisis didapatkan 33 sampel longtail tuna. Hasil rekonstruksi pohon filogenetik dari dua lokasi pengambilan sampel memperlihatkan satu clade dengan nilai jarak genetik antar spesies longtail tuna berkisar 0.000 – 0.042 yang semua sampel memiliki hubungan kekerabatan dekat. Nilai keragaman haplotipe (Hd) longtail tuna sebesar 0.9905 dan keragaman nukleotida (π) sebesar 0.020. Nilai keragaman genetik yang tinggi menunjukkan bahwa kedua populasi longtail tuna memiliki kemampuan bertahan hidup yang tinggi untuk beradaptasi dengan perubahan lingkungan. Analisis indeks fiksasi (Fst) memiliki nilai sebesar 0.0299, p – value > 0.05. Nilai indeks fiksasi menunjukkan bahwa tidak ada perbedaan populasi yang
signifikan. Hasil analisis ini dapat digunakan sebagai data dasar dalam perencanaan strategi konservasi genetik dengan upaya pengelolaan perikanan berkelanjutan.
Kata Kunci: tongkol abu – abu; penanda genetik; mtDNA; sekuensing
Ikan Tuna merupakan salah satu komoditas perikanan terbesar ketiga di Indonesia (Firdaus, 2018). Menurut FAO (2016), dari hasil penangkapan ikan tuna secara global mencapai 7.7 juta ton/tahun dengan total hasil tangkapan Indonesia mencapai 16% dari total produksi global. Ikan Tuna dengan genus Thunnus, menguasai lebih dari 80% komoditas di pasar internasional. Longtail Tuna (Thunnus tonggol) merupakan salah satu spesies tuna neritik yang bersifat oseanodromus dan pola migrasi mengikuti arus perairan (Wagiyo dan Febrianti, 2015; Hidayat dan Noegroho, 2018).
Perairan Selat Bali adalah salah satu daerah penangkapan ikan (fishing ground) yang memiliki potensi sumberdaya hayati laut yang tinggi dalam bidang perikanan. Hasil tangkapan di Perairan Selat Bali didaratkan dibeberapa wilayah, seperti PPI Kedonganan dan PPP Muncar. Kedua tempat ini adalah tempat pendaratan utama bagi kapal – kapal yang beroperasi di sekitar perairan tersebut.
Restiangsih dan Hidayat (2018) melaporkan terjadi penurunan produksi tangkapan longtail tuna di Indonesia, dimana pada tahun 2005 produksi sebesar 121.792 ton/tahun meningkat pada tahun 2007 sebesar 145.587 ton/tahun dan mengalami penurunan hingga tahun 2014 sebesar 55. 589 ton/tahun. Dilihat dari intensitas produksi longtail tuna mengalami penurunan yang cukup signifikan, kondisi ini dikhawatirkan akan menyebabkan terjadinya penurunan variasi genetik longtail tuna dan adanya kesalahan dalam identifikasi estimasi hasil tangkapan. Upaya yang dapat dilakukan untuk mengantisipasi hal tersebut adalah melalui pendekatan genetik. Pendekatan genetik dapat dilakukan dengan menggunakan identifikasi molekuler dalam menentukan identitas spesies dan status hidup suatu populasi.
Penelitian spesies ini belum banyak dilakukan di Perairan Indonesia, sehingga perlu dilakukan pengkajian mengenai identifikasi morfologi dan keragaman genetik. Pemahaman tersebut dapat menjelaskan arti penting dari pengetahuan informasi genetik suatu spesies dalam stabilitas
dan ketahanan populasi. Informasi genetik didapatkan dari pengkajian identifikasi molekuler menggunakan teknik DNA barcoding. DNA barcoding merupakan salah satu metode yang dapat digunakan dalam identifikasi suatu organisme yang sulit untuk dibedakan secara morfologi dengan cepat dan akurat (Galimberti et al., 2013). Teknik ini menggunakan salah satu penanda genetik yaitu D – loop mitokondria. D – loop atau yang dikenal dengan control region adalah salah satu segmen DNA yang memiliki proses replikasi dan transkripsi mtDNA dengan tingkat mutasi dan laju polymorfisme yang tinggi, sehingga menyebabkan urutan nukleotida yang sangat bervariasi antar individu (Pedrosa-Gerasmio et al., 2012). Penanda genetik ini telah terbukti sangat sensitif dalam mendeteksi struktur genetik populasi migrasi ikan (Pertiwi dkk., 2015). Penggunaan penanda genetik D – loop telah banyak digunakan dalam beberapa penelitian sebelumnya, seperti Thunnus obesus (Nugraha, 2009), Thunnus albacares (Wu et al., 2010), Thunnus tonggol (Willette et al., 2016).
Berdasarkan uraian, penelitian ini dilakukan untuk mengetahui identifikasi morfologi, filogenetik dan keragaman genetik longtail tuna (Thunnus tonggol) yang didaratkan di PPI Kedonganan dan PPP Muncar menggunakan marka D – loop Mitokondria.
Penelitian ini dilakukan pada bulan Desember 2018 sampai Maret 2019. Pengambilan sampel longtail tuna (Thunnus tonggol) sebanyak ± 20
ekor/lokasi (Cohen et al., 2007) di PPI Kedonganan, Bali dan PPP Muncar, Banyuwangi (Gambar 1). Analisis molekuler dilakukan di Biodiversitas Indonesia (Bionesia), Bali.
-
2.2 Alat dan Bahan
Peralatan yang digunakan dalam penelitian ini, antara lain glove, plate numeric, tray, tube, microtube,
strips tube PCR, api bunsen, mikro pipet, tips, gelas beker, pinset, vortex, heating block, transiluminator, centrifuge, thermal cycler, neraca analitik, mesin elektroforesis, microwave dan kamera. Bahan yang digunakan etanol 95%, larutan Chelex 10%, ddH2O, 10x PCR buffer, MgCL2, primer CRK, primer CRE, PE Amplitaq, dNTPs bubuk agarosa, low mass ladder, loading dye, dan biotium.
-
2.3 Pengambilan Sampel
Pengambilan sampel longtail tuna (Gambar 2) dilakukan dengan mengambil bagian sirip dada (pectoral fin) atau sirip ekor (caudal fin). Sampel di simpan dalam tube yang berisi larutan etanol 95%. Kemudian masing – masing tube sampel diberikan label.

Gambar 2. Thunnus tonggol (Sumber : Bionesia)
-
2.4 Analisis Molekuler
-
2.4.1. Ekstraksi
-
Ekstraksi dilakukan dengan menggunakan larutan Chelex 10% (Walsh et al., 1991). Jaringan sampel
diambil ± 2 mm dan dimasukan kedalam tube yang berisikan larutan Chelex 10%, kemudian di vortex selama ± 15 detik dan centrifuge selama ± 1 menit. Setelah itu, diinkubasi di dalam heating block dengan suhu 95°C selama 1 jam.
-
2.4.2. PCR (Polymerase Chain Reaction)
Proses amplifikasi DNA menggunakan enzim taq Polymerase dan primer forward CRK 5’-AGC TCA GCG CCA GAG CGC CGG TCT TGT AAA-3’ , primer reverse CRE 5’-CCT GAA GTA GGA ACC AGA TG-3’ (Lee et al., 1995). Pengaturan tahapan PCR meliputi denaturasi awal pada suhu 80°C selama 10 detik, denaturasi pada suhu 94°C selama 30 detik, annealing pada suhu 50°C selama 30 detik, extention pada suhu 72°C selama 45 detik (Barber et al., 2006). Tahapan PCR ini dilakukan pengulangan sebanyak 38 siklus.
-
2.4.3. Elektroforesis
Pengecekan kualitas produk DNA dengan menggunakan media gel agarosa. Bahan pembuatan gel agarosa adalah 0.75 gram bubuk agarosa dan 75 ml buffer dimasukan ke dalam gelas beker kemudian dipanaskan di dalam microwave selama 4 menit. Gel agarosa dituangkan kedalam cetakan yang telah dipasangkan sisir untuk pembuat sumur dan diamkan selama 60 menit. Setelah mengeras, gel dimasukan ke dalam mesin
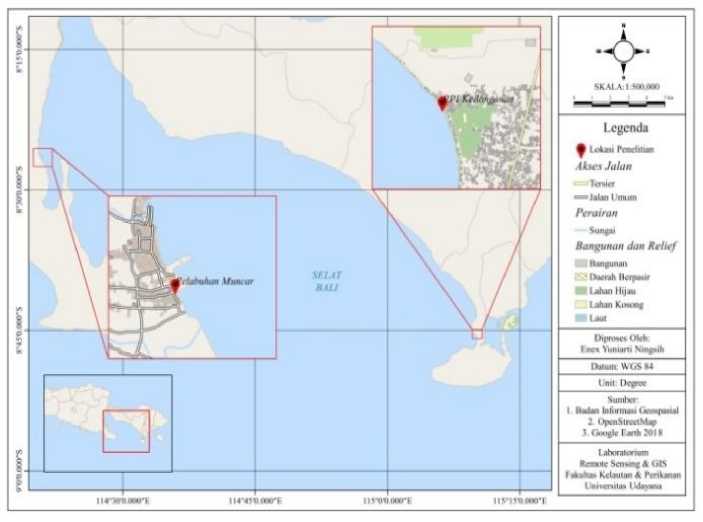
Gambar 2. Peta Lokasi Penelitian
elektroforesis, kemudian tambahan 2μl biotium, 1μl loading dye ke masing – masing sampel. Nyalakan mesin elektroforesis selama 30 menit dengan tegangan 100V dan kecepatan arus 200A. Hasil produk PCR dikirim ke DNA Sequencing Facility.
-
2.5 Analisis Data
Identifikasi secara morfologi menggunakan buku identifikasi Market Fishes of Indonesia (White et al., 2013). Untuk analisis molekuler pada hasil sekuen mtDNA control region menggunakan software MEGA 7. Pada software ini dilakukan proses penjajaran sekuen untuk melihat kemiripan antar sekuen dengan menggunakan Clustal W serta identifikasi molekuler menggunakan Basic Local Alignment Search Tool (BLAST) pada GenBank (http://www.ncbi.nih.gov).
Analisis filogenetik mengunakan software MEGA 7, dengan metode Maximun Likelihood model evolusi kimura 2 – parameter dan bootstrap 1000 kali pengulangan. Analisis keragaman genetik pada data sekuen menggunakan software DnaSP 5.10 (Librado and Rozas, 2009). Berdasarkan Nei (1987), deskripsi hasil analisis keragaman genetik terbagi menjadi 2 yaitu keragaman haplotipe (Hd) dan keragaman nukleotida (π). Analisis populasi menggunakan software Arlequin ver. 3.5 (Excoffier and Lischer, 2010).
Hasil pendugaan menggunakan metode identifikasi morfologi, total sampel yang ditemukan dari dua lokasi pengambilan sampel adalah 45 sampel longtail tuna yang kemudian di analisis secara molekuler. Hasil analisis molekuler menunjukkan bahwa 42 sampel dari total sampel longtail tuna berhasil dianalisis, sementara 3 sampel tidak dapat dianalisis. Hal ini, disebabkan oleh beberapa faktor antara lain kegagalan proses amplifikasi DNA, dimana primer yang digunakan tidak menempel pada DNA target secara spesifik, rusaknya DNA pada jaringan sampel, DNA hasil ekstraksi kurang bagus, dan percampuran reagen PCR yang tidak sempurna. Sampel yang berhasil dianalisis molekuler dapat dilihat pada Tabel 1.
Tabel 1
Total sampel dari PPI Kedonganan dan PPP Muncar.
|
Lokasi |
Ident Morfolo gi |
Identifikasi Genetik |
Tidak dapat diana lisis | ||
|
T. tongg ol |
T. albacare s |
E. Affin is | |||
|
Muncar |
21 |
15 |
3 |
- |
3 |
|
Kedong anan |
24 |
18 |
1 |
5 |
- |
|
Total Sampel |
45 |
33 |
4 |
5 |
3 |
Sampel yang berhasil dianalisis molekuler memiliki panjang fragmen DNA berkisar antara 473 – 499 bp dengan nilai identity berkisar 95% – 99%. Menurut Leray et al. (2013), persentase identity minimal untuk menyatakan suatu spesies adalah 97%. Nilai identity juga dipengaruhi oleh panjang fragmen DNA sampel yang dimiliki.
Menurut nelayan dan penjual ikan di PPI Kedonganan dan PPP Muncar, hasil identifikasi morfologi pada sampel BIO06.048.003 – BIO06.048.018, BIO06.011.002 – BIO06.011.018, BIO06.014.001, BIO06.013.001, BIO06.001 – BIO06.016.005 adalah Ikan Nyareng sebutan masyarakat lokal. Hal ini didukung oleh hasil analisis molekuler adalah Thunnus tonggol yang mempunyai nama nasional tongkol abu – abu atau longtail tuna. Hasil identifikasi morfologi pada sampel BIO06.048.019 – BIO06.048.021, BIO06.011.013, BIO06.005 – BIO06.011.006, BIO06.014 – BIO06.011.016 diduga terjadi ketidakcocokan deskripsi awal yang disebabkan oleh penggunaan sampel berupa potongan tubuh ikan. Setelah di analisis molekuler menunjukkan bahwa sampel yang awalnya diduga longtail tuna (Thunnus tonggol) adalah Thunnus albacares dan Euthynnus affinis yang mempunyai nama nasional tuna sirip kuning dan tongkol (Tabel 2).
-
3.2 Analisis Filogenetik Longtail Tuna
Hasil rekonstruksi pohon filogenetik longtail tuna dengan menggunakan penanda genetik D – loop mitokondria pada kedua lokasi (Gambar 3), dinyatakan dalam satu clade yang sama yaitu clade 1 (T. tonggol). Berdasarkan hasil perbandingan dengan database menunjukkan nilai kisaran 97% -99% (Tabel 2). Hasil analisis jarak genetik antar sampel longtail tuna dalam satu clade adalah 0.000 – 0.042, yang memperlihatkan kekerabatan yang
Tabel 2
Hasil identifikasi spesies tuna berdasarkan database GenBank menggunakan Basic Local Alignment Search Tool (BLAST) sampel tuna
|
No. Lokasi Kode Sampel Hasil BLAST |
Panjang Sekuen Query cover (%) Ident (%) |
|
1 BIO06_048_003 Thunnus tonggol 2 BIO06_048_004 Thunnus tonggol 3 BIO06_048_005 Thunnus tonggol 4 BIO06_048_006 Thunnus tonggol 5 BIO06_048_007 Thunnus tonggol 6 BIO06_048_008 Thunnus tonggol 7 § BIO06_048_009 Thunnus tonggol 8 § BIO06_048_010 Thunnus tonggol 9 OS BIO06_048_011 Thunnus tonggol 10 BIO06_048_013 Thunnus tonggol 11 I BIO06_048_014 Thunnus tonggol 12 CR BIO06_048_015 Thunnus tonggol 13 BIO06_048_016 Thunnus tonggol 14 BIO06_048_017 Thunnus tonggol 15 BIO06_048_018 Thunnus tonggol 16 BIO06_048_019 Thunnus albacores 17 BIO06_048_020 Thunnus albacores 18 BIO06_048_021 Thunnus albacores |
484 98 99.12 473 100 98.68 491 96 98.9 484 98 98.68 485 98 98.91 472 100 98.67 483 97 98.23 473 100 98.9 472 99 99.11 476 99 99.56 473 100 98.68 484 97 98.9 483 98 98.91 468 99 99.33 473 99 99.56 473 100 99.12 472 100 99.11 485 98 98.46 |
|
19 BIO_06_011_002 Thunnus tonggol 20 BIO_06_011_003 Thunnus tonggol 21 BIO_06_011_004 Thunnus tonggol 22 BIO_06_011_005 Euthynnus affinis 23 BIO_06_011_006 Euthynnus affinis 24 BIO_06_011_007 Thunnus tonggol 25 BIO_06_011_008 Thunnus tonggol 26 BIO_06_011_009 Thunnus tonggol 27 BIO_06_011_010 Thunnus tonggol 28 £ BIO_06_011_011 Thunnus tonggol 29 o- BIO_06_011_012 Thunnus tonggol 20 cS BIO_06_011_013 Thunnus albacores 31 S BIO_06_011_014 Euthynnus affinis 32 OS BIO_06_011_015 Euthynnus affinis 33 ≡ BIO_06_011_016 Euthynnus affinis 34 BIO_06_011_017 Thunnus tonggol 35 BIO_06_011_018 Thunnus tonggol 36 BIO06_014_001 Thunnus tonggol 37 BIO06_013_001 Thunnus tonggol 38 BIO06_016_001 Thunnus tonggol 39 BIO06_016_002 Thunnus tonggol 40 BIO06_016_003 Thunnus tonggol 41 BIO06_016_004 Thunnus tonggol 42 BIO06_016_005 Thunnus tonggol |
472 99 99.56 484 97 98.9 473 99 98.23 473 100 99.54 471 100 99.54 473 100 98.23 470 100 98.44 472 99 98.44 469 99 99.55 471 99 98 469 99 98.43 444 100 98.59 499 94 96.58 474 100 95.24 474 99 99.54 473 100 98.68 470 100 97.58 471 100 97.78 473 100 97.35 487 97 97.59 475 99 98.01 474 99 98.23 474 99 98.90 467 99 99.10 |
|
dekat antar sampel yang berasal dari PPI Kedonganan dan PPP Muncar. Semakin kecil jarak genetik suatu spesies maka semakin dekat hubungan kekerabatan dan begitu pula sebaliknya. |
Hal ini didukung dengan nilai bootstrap sebesar 80 pada percabangannya, dimana jika nilai bootstrap antara 70 – 100 menunjukkan peluang terjadi perubahan susunan pada clade rendah. Sebaliknya, |
80
81
55∣BI006 048 016 Muncar I Bl∞6 048 017 Muncar
' - BιoO6 048 004 Muncar
I— BIO06011007 Kedonganan
-BιoO6 048 003 Muncar
I BlO 06 011 017 Kedonganan ^∣ i BIO 06 011 004 Kedonganan SiL B∣ogg 016 001 Kedonganan
i— BioO6.O48.OO7 Muncar
86
BICXK 016 003 Kedonganan p BI006 014 001 Kedonganan
L BI006 016 002 Kedonganan
B∣oO6O48OO6 Muncar
BI006 048 014 Muncar
■ - BIO 06 011 008 Kedonganan l- BI006.048.009 Muncar
821BIO 06 011 003 Kedonganan .BI006 048.015 Muncar
- BIO 06 011 018 Kedonganan
lBιoO6 048 005 Muncar
BI006 048 008 Muncar
BI006 016 004 Kedonganan
' BI006 016 005 Kedonganan
— BIO 06 011 012 Kedonganan
BIOO6.O48.013 Muncar
BI006 048 018 Muncar
— BIO 06 011 002 Kedonganan
- BIO 06 011 010 Kedonganan
KC3133O21 Thunnus tonggol haplotype 3 D-Ioop partial sequence mitochondrial.
- BIC06 048.010 Muncar
L 81006 048 011 Muncar
Clade 1 T. torι°°ol
----BIO 06 011 009 Kedonganan
— BIO 06 011 011 Kedonganan
BI006013O01 Kedonganan
----BICO6.048 02I Muncar
∣ T. albacares
KC165861 1 Thunnus albacares haplotype 15 D-Ioop partial sequence mιtochondnal
-BIO 06 011 OtSKedonganan ∣ .
JN655119 1 Eulhynnus affinιs haplotype 130 D-Ioop partial sequence mitochondrial I ^' ^pri/S
002
Gambar 3. Rekonstruksi pohon filogenetik menggunakan metode maximum likelihood dengan kimura – 2 parameter dari 2 lokasi yaitu PPI Kedonganan, Bali dan PPP Muncar, Banyuwangi.
jika nilai bootstrap ≤ 70 maka peluang perubahan susunan clade tinggi (Prehadi et al., 2015).
Setiap clade yang terbentuk menunjukkan perbedaan spesies. Pada clade besar, masih terdapat clade kecil yang menunjukkan adanya perbedaan basa nukleotida antar individu. Menurut Verawati (2015), hal ini dapat terjadi akibat dari kondisi lingkungan yang mempengaruhi materi genetik suatu individu. Disertai dengan penambahan data sekuen GenBank dengan no accession KC313302.1 (Thunnus tonggol), KC165861.1 (Thunnus albacares), dan JN655119.1 (Euthynnus affinis) yang dijadikan pembanding dalam penentuan spesies.
Distribusi sampel longtail tuna dalam satu clade ini diduga karena adanya pengaruh dari faktor geografis yang sama. Mengindikasikan kedua lokasi pengambilan sampel longtail tuna ini adalah satu keturunan dan kemungkinan besar perairan tersebut adalah jalur migrasi longtail tuna, yang mengakibatkan kedua lokasi menjadi mirip secara genetik. Hasil ini serupa dengan penelitian yang dilakukan oleh Willette et al. (2016), yang tidak menemukan adanya perbedaan genetik di Perairan Laut Cina Selatan berdasarkan pohon filogenetik longtail tuna. Beberapa penelitian pada spesies tuna lainnya seperti Wijana dan Mahardika (2010), pada spesies tuna sirip kuning di Philipina dan Spanyol
dan Kunal et al. (2013), pada spesies tuna sirip kuning di Perairan India.
-
3.3 Keragaman Genetik Longtail Tuna
Jumlah haplotipe longtail tuna berbeda dari dua lokasi penelitian, dimana sampel longtail tuna dari PPI Kedonganan dengan jumlah 18 sampel mempunyai 17 haplotipe dan PPP Muncar dengan jumlah 15 sampel mempunyai 13 haplotipe. Hasil tersebut menunjukkan terdapat beberapa sampel mempunyai sekuen identik didukung oleh nilai keragaman genetik yang tinggi sebesar 0.9905. Nilai keragaman nukleotida (π) yang rendah sebesar 0.020, berarti hampir setiap sampel merupakan haplotipe berbeda dengan perbedaan nukleotida antar sampel sangat kecil. Hasil analisis keragaman genetik longtail tuna ini disajikan pada Tabel 3. Analisis populasi menunjukkan hasil Fst yang tidak signifikan (Fst = 0.0299, p – value > 0.05). Hal ini, menunjukkan adanya indikasi bahwa tidak ada perbedaan populasi longtail tuna.
Tingginya nilai keragaman genetik longtail tuna di kedua lokasi penelitian serupa dengan penelitian yang telah dilakukan Willette et al. (2016) di Perairan Laut Cina Selatan. Hasil penelitian ini juga serupa dengan penelitian ikan pelagis lainnya yang memiliki nilai keragaman genetik tinggi seperti nilai keragaman genetik tuna mata besar di Perairan Samudera Hindia sebesar 0.8136 (Nugraha, 2009), tuna sirip kuning di Perairan India sebesar 0.998 (Kunal et al., 2013), tuna sirip kuning di Perairan Maluku Utara dan Ambon sebesar 0.990 (Akbar dkk., 2014) dan tuna mata besar di Perairan Indonesia bagian barat (0.999), tengah (0.998) dan timur (0.997) (Pertiwi et al., 2017).
Tabel 3
Jumlah sampel (n), jumlah haplotipe (Hn), keragaman haplotipe (Hd), keragaman nukleotida (π) longtail tuna (Thunnus tonggol) di PPI Kedonganan dan PPP Muncar.
|
Populasi |
n |
Hn |
Hd |
π |
|
Muncar |
15 |
13 |
0.9809 |
0.017 |
|
Kedonganan |
18 |
17 |
0.9934 |
0.022 |
|
Dua populasi |
33 |
29 |
0.9905 |
0.020 |
Tingginya keragaman genetik longtail tuna di perairan ini diduga disebabkan oleh beberapa faktor antara lain; ukuran populasi besar, kemampuan migrasi dan adaptasi terhadap
kondisi lingkungan. (1) faktor pertama, populasi longtail tuna yang berukuran besar memungkinkan adanya perkawinan acak (interbreeding) antar individu dengan individu lain, baik dengan genotip yang sama maupun berbeda. Dengan adanya perkawinan acak ini, dapat membantu meningkatkan frekuensi alel pada keturunan berikutnya dan melindungi tidak terjadinya penurunan populasi. Pendugaan persebaran longtail tuna pada perairan tertentu dapat mengakibatkan penangkapan sub – populasi dalam jumlah kecil. Beberapa penelitian menemukan adanya penangkapan pada sub – populasi dari jenis – jenis tuna lainnya seperti Nugraha (2009), menjelaskan bahwa dengan pengkajian 190 sampel tuna mata besar ditemukan 5 sub – populasi yang diduga berasal dari dua populasi yaitu populasi Samudera Hindia dan Samudera Pasifik. (2) Faktor kedua adalah kemampuan migrasi, dimana keragaman genetik suatu populasi akan meningkat jika mendapatkan pengaruh aliran gen dari populasi lain. (3) Faktor ketiga, kemampuan adaptasi setiap individu dipengaruhi oleh perubahan kondisi lingkungan, dimana sebagian besar keberadaan ikan tuna di pengaruhi oleh suhu permukaan laut dan klorofil – a. Pola persebaran suhu permukaan laut dan klorofil – a mengindikasikan terjadinya upwelling. Upwelling menggambarkan kelimpahan dan distribusi fitoplankton di suatu perairan (Barata dkk., 2014). Fitoplankton menentukan tinggi rendahnya produktifitas perairan dan keberadaan ikan kecil yang menjadi makanan dari ikan tuna (Padmaningrat dkk., 2017). Hal tersebut, dapat mempengaruhi sifat tampak (fenotip) suatu individu disamping ditentukan oleh sifat dalam (genotip). Hal ini, didukung oleh penelitian Hartoko (2010), yang menemukan aktivitas migrasi pada beberapa spesies tuna dipengaruhi oleh kondisi oseanografi seperti suhu, kedalaman, klorofil – a, salinitas dan pola arus.
Tingginya keragaman genetik longtail tuna menghasilkan keturunan dengan berbagai karakteristik yang dapat menunjukkan kemampuan dalam beradaptasi terhadap perubahan lingkungan dan mengurangi kemungkinan kerusakan gen (seperti penyakit) dalam populasi. Keragaman genetik tinggi patut dipertahankan agar tetap terjaga kelestariannya, sehingga tidak terjadi kepunahan. Meskipun diketahui beberapa spesies tuna merupakan salah satu sumberdaya komersil yang tinggi dan menjadi ikan target dalam penangkapan.
Penangkapan yang dilakukan secara terus menerus pada beberapa spesies tuna tertentu, dapat menimbulkan dampak buruk pada struktur populasi dan penurunan keragaman genetik suatu spesies tuna. Hal ini, memberikan pandangan bahwa perlu adanya strategi untuk menjaga kelestarian keanekaragaman hayati melalui pendekatan genetik. Upaya yang dapat dilakukan dalam menjaga kelestarian keanekaragam hayati antara lain; (1) pengendalian batasan ukuran minimal tangkapan pada setiap penangkapan, (2) batasan waktu penangkapan, dimana
penangkapan dilakukan pada saat puncak musim tuna, sehingga dapat menghindari terjadinya overfishing. Sumberdaya genetik merupakan kunci penting bagi suatu spesies untuk dapat bertahan hidup demi keberlanjutan sumberdaya alam di masa yang akan datang. Sesuai dengan pernyataan Santoso (2016), keragaman genetik mempunyai dampak potensial secara langsung maupun tidak pada individu spesies, populasi, komunitas dan ekosistem.
Hasil analisis menunjukkan bahwa kedua populasi longtail tuna memiliki tipe haplotipe beragam sebanyak 29 haplotipe dan nilai keragaman genetik tinggi sebesar 0.9905, sehingga memberikan peluang pada longtail tuna untuk mampu beradaptasi terhadap perubahan lingkungan. Rekonstruksi pohon filogenetik menunjukkan pencampuran populasi dengan nilai Fst yang tidak menunjukkan perbedaan yang signifikan pada kedua lokasi tersebut.
Ucapan terimakasih
Penulis mengucapkan terimakasih kepada United States Agency for International Development (USAID) melalui Enhanced Engagement in Research (PEER) Science Program (AID – OAA – A – A – 11 – 00012) yang telah mendanai penelitian ini, serta Biodiversitas Indonesia (Bionesia) atas segala fasilitas dan laboratorium dalam penelitian ini.
Daftar Pustaka
Akbar, N., Zamani, N. P., & Madduppa, H. H. (2014). Keragaman genetik ikan tuna sirip kuning (Thunnus albacares) dari dua populasi di Laut Maluku, Indonesia. Depik Jurnal Ilmu–ilmu Perairan, Pesisir dan Perikanan, 3(1), 65–73.
Barata, R. B. Y., Setyono, H., & Harsono, G. (2014). Dinamika upwelling dan downwelling berdasarkan variabilitas suhu permukaan laut dan klorofil–a di Perairan Selatan Jawa. Jurnal Oseanografi, 3(1), 57–66.
Barber, P. H., Erdmann, M. V., & Palumbi, S. R. (2006). Comparative phylogeography of three codistributed stomatopods: origins and timing of regional lineage diversification in the Coral Triangle. Evolution. 60(9), 1825–1839.
Cohen, L., Manion, L., & Morrison, K. (2007). Research methods in education. (6th ed.). New york, USA:
Routledge.
Excoffier, L., & Lischer, H. E. L. (2010). Arlequin suite ver 3.5: a new series of programs to perform
population genetics analyses under Linux and
Windows. Molecular Ecology Resources, 10(3), 564–567.
FAO. (2016). The states of world fisheries and aquaculture. Rome, Italy: Food and Agriculture Organization.
Firdaus, M. (2018). Profil perikanan tuna dan cakalang di Indonesia. Buletin Ilmiah Marina Sosial Ekonomi Kelautan dan Perikanan, 4(1), 23–32.
Galimberti, A., Mattia, F. D., Losa, A., Bruni, I., Federici, S., Casiraghi, M., Martellos, S., & Labra, M. (2013). DNA barcoding as a new tool for food traceability. Food Research International, 50(1), 55–63.
Hartoko, A. (2010). Spatial distribution of Thunnus.sp, vertical and horizontal sub–surface multilayer
temperature profiles of in–situ agro float data in Indian Ocean. Journal of Coastal Development, 14(1), 61–74.
Hidayat, T., & Noegroho, T. (2018). Biologi reproduksi ikan tongkol abu–abu (Thunnus tonggol) di Perairan Laut Cina Selatan. BAWAL Widya Riset Perikanan Tangkap, 10(1), 17–28.
Kunal, S. P., Kumar, G., Menezes, M. R., & Meena, R. M. (2013). Mitochondrial DNA analysis reveals three stocks of yellowfin tuna Thunnus albacares (Bonnaterre, 1788) in Indian waters. Conservation Genetics, 14(1), 205–213.
Lee, W. J., Conroy, J., Howell, W. H., & Kocher, T. D. (1995). Structure and evolution of teleost mitochondrial control regions. Journal of Molecular Evolution, 41(1), 54–66.
Leray, M., Yang, J. Y., Meyer, C. P., Mills, S. C., Agudelo, N., Ranwez, V., Boehm, J. T., & Machida, R. J. (2013). A new versatile primer set targeting a short fragment of the mitochondrial COI region for metabarcoding metazoan diversity: application for characterizing coral reef fish gut contents. Frontiers in Zoology, 10(1), 34.
Librado, P., & Rozas, J. (2009). DnaSP v5: a software for comprehensive analysis of DNA polymorphism data. Bioinformatics, 25(11), 1451–1452.
Nei, M. (1987). Molecular Evolutionary Genetics. New York, USA: Colombia University Press.
Nugraha, B. (2009). Studi tentang genetika populasi ikan tuna mata besar (Thunnus obesus) hasil tangkapan tuna longline yang didaratkan di Benoa. Tesis. Bogor, Indonesia: Program Studi Magister Sains, Program Pascasarjana Institut Pertanian Bogor.
Padmaningrat, K. B., Karang, I. W. G. A., & As–syakur, A. R. (2017). Aplikasi sistem informasi geografis (SIG) dan penginderaan jauh untuk pemetaan daerah tangkapan ikan tuna mata besar di Selatan Jawa dan Bali. Journal of Marine and Aquatic Sciences, 3(1), 70–83.
Pedrosa-Gerasmio, I. R., Babaran, R. P., & Santos, M. D. (2012). Discrimination of juvenile yellowfin (Thunnus albacares) and bigeye (T. obesus) tunas using mitochondrial DNA control region and liver morphology. PloS One, 7(4), 1–7.
Pertiwi, N. P. D., Nugraha, B., Sulistyaningsih, R. K., Jatmiko, I., Sembiring, A., Mahardini, A., Cahyani, N. K. D., Anggoro, A. W., Madduppa, H. H., Sutikno, A., Barber, P. H., & Mahardika, G. N. (2017). Short
communication: Lack of differentiation within the bigeye tuna population of Indonesia. Biodiversitas Journal of Biological Diversity, 18(4), 1406–1413.
Pertiwi, N. P. D., Mahardika, I. G. N. K., & Watiniasih, N. L. (2015). Optimasi amplifikasi DNA menggunakan metode PCR (Polymerase Chain Reaction) pada ikan karang famili Pseudocromidae (Dottyback) untuk identifikasi spesies secara molekuler. Jurnal Biologi Udayana, 19(2): 1–5.
Prehadi, P., Sembiring, A., Kurniasih, E. M., Rahmad, R., Arafat, D., Subhan, B., & Madduppa, H. H. (2015). DNA barcoding and phylogenetic reconstruction of shark species landed in Muncar fisheries landing site in comparison with Southern Java fishing port. Biodiversitas Journal of Biological Diversity, 16(1), 55–61.
Restiangsih, Y. H., & Hidayat, T. (2018). Analisis
pertumbuhan dan laju eksploitasi ikan tongkol abu– abu, Thunnus tonggol (Bleeker, 1851) Di Perairan Lautan Jawa. BAWAL Widya Riset Perikanan Tangkap, 10(2), 111–120.
Santoso, W. Y. (2016). Signifikansi preventive expenditures valuation dalam bioprospeksi sumberdaya genetik di Indonesia. Jurnal Pengelolaan Sumberdaya Alam dan Lingkungan, 6(1), 86–96.
Verawati, I. (2015). Identifikasi molekuler, keragaman genetik dan karakteristik habitat siput laut (Nudibranchia) dari beberapa populasi di Indonesia. Skripsi. Bogor, Indonesia: Program Studi Ilmu Kelautan,
Departemen Ilmu dan Teknologi Kelautan Institut Pertanian Bogor.
Wagiyo, K., & Febrianti, E. (2015). Aspek biologi dan parameter populasi ikan tongkol abu–abu (Thunnus tonggol) di Perairan Langsa dan sekitarnya. BAWAL Widya Riset Perikanan Tangkap, 7(2), 59–66.
Walsh, P. S., Metzger, D. A., & Higuchi, R. (1991). Chelex 100 as a Medium for Simple Extraction of DNA for PCR–Based Typing from Forensic Material.
Biotechniques, 10(4), 506–513.
White, W. T., Last, P. R., Dharmadi, Faizah, R., Chodrijah, U., Prisantoso, B. I., Pogonoski, J. J., Puckridge, M., & Blaber, S. J. M. (2013). Market fishes of Indonesia (jenis–jenis ikan di Indonesia). Canberra, Australian: Australian Centre for International
Agricultural Research.
Wijana, I. M. S., & Mahardika, I. G. N. (2010). Struktur genetik dan filogeni yellowfin tuna (Thunnus albacares) berdasarkan sekuen DNA mitokondria control region sitokrom oksidase I pada diversitas zone biogeografi. Jurnal Bumi Lestari, 10(2), 270–274.
Willette, D. A., Santos, M. D., & Leadbitter, D. (2016). Longtail tuna Thunnus tonggol (Bleeker, 1851) shows genetic partitioning across, but not within, basins of the Indo–Pasific based on mitochondrial DNA.
Journal of Applied Ichtyology, 32(2), 318–323.
Wu, G. C. C., Chiang, H. C., Chou, Y. W., Wong, Z, R., Hsu, C. C., Chen, C. Y., & Yang, H. Y. (2010).
Phylogeography of yellowfin tuna (Thunnus albacares) in the Western Pacific and the Western Indian Oceans inferred from mitochondrial DNA. Fisheries Research, 105(3), 248–253.
© 2021 by the authors; licensee Udayana University, Indonesia. This article is an open access article distributed under the terms and conditions of the Creative Commons Attribution license (http://creativecommons.org/licenses/by/3.0/).
J. Mar. Aquat. Sci. 7: 94-102 (2021)
Discussion and feedback