UJI IDENTIFIKASI IBUPROFEN PADA OBAT HERBAL DENGAN KLT-SPEKTROFOTODENSITOMETRI
on
Uji Identifikasi Ibuprofen pada Obat Herbal dengan KLT-Spektrofotodensitometri (Temaje I
G.D. B., I N.K. Widjaja, K.D. Cahyadi, Gelgel W.)
UJI IDENTIFIKASI IBUPROFEN PADA OBAT HERBAL DENGAN KLT-SPEKTROFOTODENSITOMETRI
I G.D.B. Temaja, I N.K. Widjaja, K.D. Cahyadi, I M.A.G. Wirasuta
Jurusan Farmasi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana
Korespondensi: Dr.rer.nat. I Made Agus Gelgel Wirasuta, M. Si., Apt
Jurusan Farmasi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana Jalan Kampus Unud-Jimbaran, Jimbaran-Bali, Indonesia 80364 Telp/Fax: 0361-703837
Email: mgelgel1@yahoo.de
ABSTRAK
Belakangan ini, terjadi peningkatan tren penggunaan obat herbal di masyarakat. Melihat kecenderungan tersebut, beberapa pihak yang tidak bertanggungjawab memanfaatkannya sebagai peluang untuk meraih keuntungan yaitu dengan menambahkan bahan kimia obat (BKO) ke dalam produk obat herbal untuk meningkatkan efek obat tersebut. Ibuprofen adalah salah satu BKO yang sering ditambahkan secara illegal ke dalam obat herbal. Oleh karena itu, perlu dilakukan uji identifikasi ibuprofen pada obat herbal untuk mengontrol kualitas obat herbal dan menjamin perlindungan konsumen. Tujuan penelitian ini adalah mengembangkan metode KLT-Spektrofotodensitometri untuk identifikasi senyawa ibuprofen pada obat herbal.
Ekstraksi sampel dilakukan dengan menggunakan kolom SPE C8-Cation Exchange dan fraksinya dipisahkan menggunakan 2 sistem KLT yang berbeda yaitu sistem TE dan TF. Kemudian, plat KLT dipindai pada panjang gelombang 210 nm menggunakan TLC Scanner 3 (Camag-Mutenz-Switzerland) untuk dibuat kromatogramnya. Spektrum masing-masing puncak dibaca pada rentang panjang gelombang 190 – 400 nm. Identifikasi senyawa dilakukan berdasarkan nilai hRfc dan korelasi spektrum in situ-nya dengan spektrum standar pada library Camag WinCats.
Hasil uji identifikasi menunjukkan bahwa fraksi yang didapatkan mengandung ibuprofen. Validasi metode mencakup spesifisitas dengan kemurnian spektrum puncak > 0,99958, presisi (hRf dan Area Under Curve (AUC)) dengan koefisien variansi (KV) < 2%, linearitas dengan r > 0,99907 dan sdv < 5%, serta Limit of Detection (LOD) 21,22ng.
Kata kunci: identifikasi, ibuprofen, TLC-Spektrofotodensitometri, SPE
-
1. PENDAHULUAN
Belakangan ini, terjadi peningkatan tren penggunaan obat herbal di masyarakat. Melihat kecenderungan tersebut, beberapa pihak yang tidak bertanggungjawab memanfaatkannya sebagai peluang untuk meraih keuntungan yaitu dengan menambahkan bahan kimia obat (BKO) ke dalam produk obat herbal untuk meningkatkan efek obat tersebut.
Menurut laporan BPOM, telah ditemukan senyawa ibuprofen pada produk obat herbal yang memiliki khasiat sebagai penurun panas (BPOM RI, 2008). Ibuprofen memiliki sifat antipiretik yang merangsang pusat pengaturan panas di hipotalamus (bagian otak yang bersifat
sangat peka, salah satunya terhadap suhu) sehingga mengakibatkan vasodilatasi perifer dengan bertambahnya pengeluaran panas yang disertai dengan keluarnya banyak keringat (Tjay dan Rahardja, 2008).
KLT-Spektrofotodensitometri dilaporkan telah dapat digunakan untuk uji skrining dan konfirmasi pada analisis toksikologi (Wirasuta, 2012). KLT-Spektrofotodensitometri merupakan metode yang sederhana, murah, handal, dan memiliki spesifisitas yang cukup untuk uji konfirmasi (Flanagan et al., 2007). Adapun tujuan penelitian ini adalah mengembangkan metode KLT-Spektrofotodensitometri untuk identifikasi senyawa ibuprofen pada obat herbal.
-
2. MATERI DAN METODE
-
2.1 Alat
-
Peralatan gelas yang umum dipakai dalam laboratorium analisis, ballfiller, timbangan analitik (AND GR-200), oven (Memmert), alat pengaduk mekanik (Ika vibrax VXR basic), pompa vakum (Gast), manifold (Phenomenex), pH meter (Oakton), Linomat 5 (Camag-Muttenz-Switzerland), bejana kromatografi (Camag-Muttenz-Switzerland), Spektrofotodensitometer TLC-Scanner 3 (Camag-Mutenz-Switzerland).
-
2.2 Bahan
Bahan kimia dan pelarut yang digunakan mempunyai derajat kemurnian pro analisis (Merck-Germany) yaitu metanol, kalium dihidrogen fosfat (KH2PO4), natrium hidroksida (NaOH), asam asetat, n-heksana, diklorometana, isopropanol, amonium hidroksida, asam hidroklorida (HCl), etil asetat, kloroform, dan aquades. Fase diam yaitu plat aluminium TLC Silika Gel 60 GF254 (Merck-Germany). Kolom SPE Strata Screen C (Phenomenex). Senyawa standar ibuprofen (BPOM RI), salbutamol sulfat (Ferron Par Pharmaceutical), difenhidramin HCl (BPOM RI), diazepam (BPOM RI), klordiazepoksid, natrium diklofenak (Ferron Par Pharmaceutical), kodein (BPOM RI), bromheksin (BPOM RI).
-
2.3 Metode
-
2.3.1 Penyiapan Larutan
-
Larutan yang dibuat meliputi larutan NaOH 0,2 M, larutan dapar fosfat (KH2PO4) 0,1 M pH 6, larutan baku stok ibuprofen 2 mg/mL, larutan baku kerja ibuprofen 500 µg/mL, larutan standar pembanding dengan konsentrasi 5, 50, 100 dan 500 µg/mL, larutan fase gerak sistem TE (etil asetat: metanol: ammonia (85:10:5 %v/v)) dan TF (etil asetat), larutan standar senyawa pengkoreksi hRf masing-masing dengan konsentrasi 250 µg/mL (TF = klordiazepoksid, natrium diklofenak, dan diazepam; TE = salbutamol sulfat, kodein, difenhidramin HCl, dan bromheksin).
-
2.3.2 Metode Ekstraksi
-
A. Penyiapan Kolom SPE
Penyiapan Kolom SPE Strata Screen C mengacu pada metode yang dikembangkan oleh Purbandika (2011) yaitu dengan mengelusi kolom menggunakan 3 mL metanol, dilanjutkan dengan 3 mL air, dan 3 mL dapar fosfat 0,1 M pH 6. Laju elusi diatur 1,5 mL/menit menggunakan alat vakum sampai tersisa sedikit eluen untuk menjaga agar kolom tidak kering (Purbandika, 2011).
-
B. Penyiapan Sampel
Sebanyak 500 µL senyawa standar ibuprofen 50 µg/mL ditambahkan 500 µL dapar fosfat 0,1 M pH 6. Campuran dikocok dalam ultrasonic selama 30 menit.
-
C. Proses Ekstraksi
Proses ekstraksi dilakukan sesuai dengan metode yang dikembangkan oleh Purbandika (2011) dimana analit dielusi dengan menggunakan fase gerak metanol. Isolat ditampung kemudian diuapkan sampai kering pada suhu 60oC di atas tangas air. Ekstrak direkonstitusi dengan 100 μL metanol sehingga konsentrasi yang didapat sebesar 250 µg/mL.
-
2.3.3 Sistem Pemisahan Dengan KLT-Spektrofotodensitometri
Dua buah plat dengan ukuran 10 x 10 cm dicuci dan diaktivasi. Totolan awal 10 mm dari tepi kiri dan 10 mm dari bawah plat, lebar pita 3 mm, dan jarak antar noda 6 mm. Totolan 1 – 3 adalah sampel ekstraksi ibuprofen, standar pengkoreksi hRf ditotolkan pada noda ke-4, sedangkan standar pembanding ibuprofen pada noda ke-5 sampai dengan ke-12. Semua noda ditotolkan pada 2 plat yang terpisah. Plat pertama dielusi dengan fase gerak sistem TE dan plat kedua dengan fase gerak sistem TF. Chamber dijenuhkan sebelum dielusi selama 30 menit. Elusi dilakukan sampai jarak pengembangan 8 cm, kemudian plat dikeringkan pada suhu 60°C selama 10 menit di dalam oven. Plat yang sudah kering dipindai dengan spektrofotodensitometer TLC-Scanner 3 (Camag-Mutenz-Switzerland) pada panjang gelombang 210 nm dan spektrum masing-masing puncak dibaca pada rentang panjang gelombang 190 - 400 nm serta diuji kemurnian spektrumnya.
-
2.3.4 Analisis Data
Nilai hRfc diperoleh dengan mengacu pada Zeeuw et al (1992) yang mengkoreksi hRf dengan metode poligonal menggunakan senyawa standar pengkoreksi hRf. Modifikasi dilakukan pada senyawa standar pengkoreksi hRf yang digunakan menjadi salbutamol (hRfc = 20), kodein (hRfc = 35), difenhidramin (hRfc = 65), dan bromheksin (hRfc = 88) untuk sistem TE serta klordiazepoksid (hRfc = 10), diklofenak (hRfc = 27), dan diazepam (hRfc = 49), untuk sistem TF. Perhitungan hRfc dengan metode poligonal secara otomatis mengacu pada Wirasuta (2012) yang memanfaatkan WinCATS-Specllib-Tool (Camag -Switzerland).
Untuk memastikan identitas puncak kromatogram digunakan WinCATS-Specllib-Tool dengan melihat nilai hRfc yang didapatkan ± 11 untuk sistem TE dan ± 8 untuk sistem TF serta korelasi spektrum in situ analit dengan spektrum pada library. Nilai korelasi spektrum minimum ditetapkan sebesar 0,8 (Wirasuta, 2012).
-
2.3.5 Uji Validasi Metode Analisis
Validasi metode untuk analisis kualitatif mencakup spesifisitas, presisi, linearitas, dan batas deteksi (United Nations Office on Drugs and Crime, 2009).
-
A. Penentuan Spesifisitas, Linearitas, dan
LOD
Penotolan sampel dan standar untuk uji validasi dikerjakan pada prosedur 2.3.3. Noda dipindai pada panjang gelombang maksimum in situ ibuprofen (224 nm) pada library Camag (1999). Spektrum setiap puncak dipindai pada panjang gelombang 190 – 400 nm. Uji spesifisitas dilakukan dengan tes purity peaks 85% puncak (Camag, 1999).
-
B. Penentuan Presisi
Disiapkan 2 plat KLT dengan ukuran 7,5 x 10 cm yang telah dicuci dan diaktivasi sebelumnya. Penentuan presisi dilakukan dengan menggunakan 3 variasi konsentrasi (80, 100, 120 %) dengan 3 kali pengulangan (Harmita, 2004). Ditotolkan senyawa standar ibuprofen dengan 3 variasi massa penotolan (ng/totolan) berbeda (400, 500, dan 600 ng) dengan 3 kali pengulangan menggunakan alat Linomat 5. Plat dielusi seperti pada prosedur 2.3.3. Plat yang
sudah kering selanjutnya dipindai seperti pada prosedur 2.3.5 (A).
-
C. Perhitungan Nilai Parameter Validasi
Spesifisitas ditentukan dari kemurnian puncak dengan melihat korelasi spektrum pada Rf awal dengan Rf maksimum serta Rf maksimum dengan Rf akhir (Camag, 1999). Nilai korelasi spektrum minimum ditetapkan sebesar 0,999 (Indrayanto et al., 2009).
Nilai linearitas dilihat dengan membuat grafik antara konsentrasi dan AUC. Berdasarkan grafik tersebut ditentukan persamaan regresi linier (y = bx + a) dan koefisien korelasinya (r) dimana r yang ditetapkan diatas 0,999 (Lawson, 1996). Dengan persamaan regresi linear yang diperoleh, selanjutnya dihitung nilai simpangan baku residual S(y/x) dan batas deteksi (LOD).
Perhitungan presisi dilakukan terhadap hRf dan AUC senyawa pada 2 sistem KLT. Presisi dinyatakan sebagai standar deviasi (SD) dan koefisien variansi (KV) (Indrayanto et al., 2009).
-
3. HASIL DAN PEMBAHASAN
-
3.1 Uji Identifikasi
-
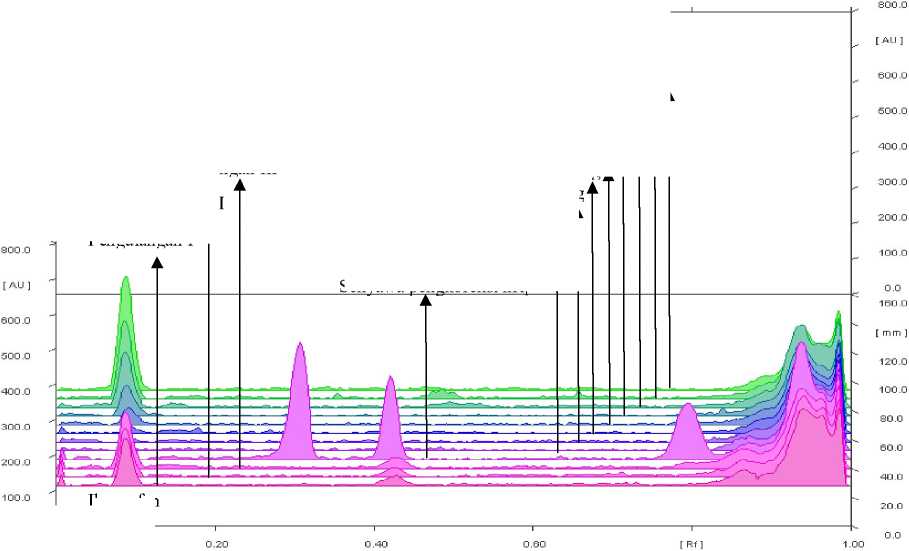
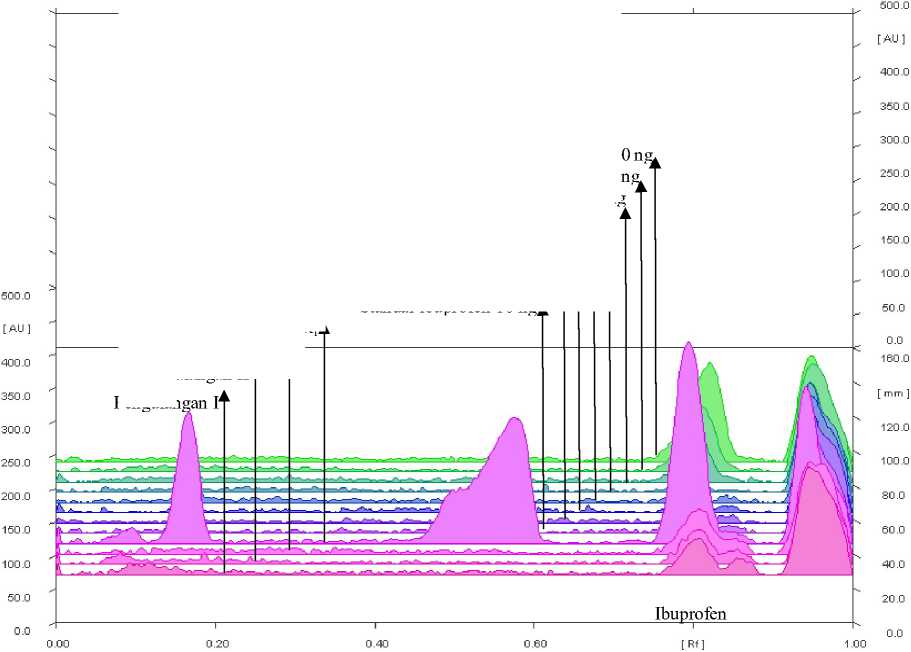
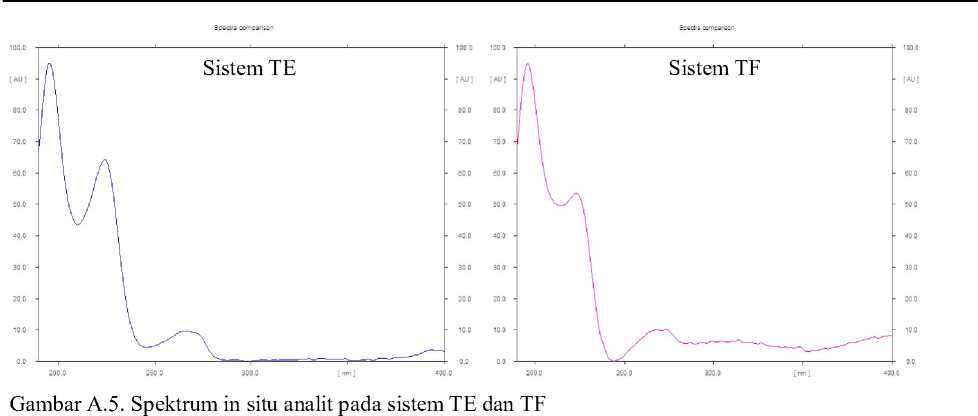
Kromatogram hasil elusi pada sistem TE dan TF dapat dilihat pada Gambar A.1 dan A.2. Nilai hRf dari masing-masing senyawa standar pengkoreksi hRf dapat dilihat pada Tabel B.1. Proses koreksi nilai hRf puncak fraksi hasil SPE menggunakan metode poligonal dilakukan secara otomatis dengan WinCATS-Specllib-Tool seperti pada Gambar A.3 dan A.4. Jumlah senyawa yang berada pada rentang hRfc ± error window dari masing-masing sistem KLT ini disebut dengan Hit Factor (HF). Adapun HF pada sistem TE maupun TF dapat dilihat pada Tabel B.2. Spektrum analit di kedua sistem KLT ditunjukkan oleh Gambar A.5.
Berdasarkan HF yang didapatkan, identifikasi dilakukan dengan memilih senyawa yang memiliki nilai korelasi spektrum analit dengan spektrum pada library Camag WinCats terbaik. Tabel B.3 menunjukkan hasil identifikasi yang dilakukan pada 2 sistem KLT. Dari hasil pada Tabel B.2 dan terlihat bahwa senyawa yang berada pada rentang hRfc ± 11 (error window TE) dan hRfc ± 8 (error window TF) dengan nilai korelasi spektrum 0,99729; 0,99752; 0,99842 pada sistem TE dan 0,92455;
0,94532; 0,93654 pada sistem TF adalah ibuprofen. Identifikasi yang dilakukan pada 2 sistem KLT seperti pada Tabel B.3 mendapatkan kesesuaian hasil baik pada sistem TE maupun TF dimana ibuprofen adalah senyawa pada fraksi hasil SPE.
-
3.2 Validasi Metode Analisis
Hasil uji spesifisitas dengan melihat kemurnian puncak dapat dilihat secara lengkap pada Tabel B.4. Dari hasil uji purity peaks menunjukkan bahwa puncak ibuprofen merupakan puncak murni dimana korelasi spektrum pada posisi Rf awal dengan Rf maksimum sebesar 0,99983; 0,99987; 0,99984 pada sistem TE dan 0,99963; 0,99952; 0,99975 pada sistem TF serta korelasi Rf maksimum dengan Rf akhir sebesar 0,99984; 0,99985; 0,99983 pada sistem TE dan 0,99962; 0,99958; 0,99983 pada sistem TF.
Hasil uji presisi dapat dilihat pada Tabel B.5 dan B.6. Uji presisi hRf dilakukan dengan n = 9 menghasilkan nilai KV < 2%. Uji presisi AUC dengan konsentrasi 80, 100, dan 120 % dengan 3 kali pengulangan menghasilkan nilai KV < 2%.
Persamaan regresi linear yang didapatkan adalah y = 5,2429x – 49,065 dengan r = 0,99907 dan sdv 4,17% pada sistem TE dan y = 5,3021x – 181,0223 dengan r = 0,99975 dan sdv 2,42% pada sistem TF. Batas deteksi (LOD) yang didapatkan adalah 21,22 ng.
-
4. KESIMPULAN
Sistem ini dapat digunakan untuk mengidentifikasi ibuprofen pada obat tradisional dengan spesifisitas (kemurnian spektrum) > 0,99958, linearitas dengan r > 0,99907 dan sdv < 4,17%, batas deteksi 21,22 ng serta presisi hRf dan AUC dengan KV < 2%.
UCAPAN TERIMA KASIH
Terima kasih dihaturkan kepada reviewer Ibu Ni Made Pitri Susanti, S.Farm., M.Si., Apt., dan Ibu Luh Putu Mirah Kusuma Dewi, SF., Apt., Lembaga Forensik dan Sains Kriminologi Universitas Udayana atas bantuan tempat dan alat dalam mendukung penelitian ini.
DAFTAR PUSTAKA
BPOM RI. (2008). Metode Analisis PPOMN th 2008. Jakarta: Balai Pengawas Obat dan Makanan Republik Indonesia.
Camag. (1999). Welcome to the CAMAG WinCats Tutorial: WinCats Planar Chromatography. Switzerland:
CAMAG.
Flanagan, R. J., A. Taylor., I. D. Watson, R. Whelpton. (2007). Fundamentals of Analytical Toxicology. New Delhi: John Wiley and Sons, Ltd. p. 131–134, 137– 139.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian, vol 1 (3). hal 117-135.
Indrayanto, G., M. Yuwono, Suciati. (2009). TLC: Validation of Analyses. Jack Cazes. Encyclopedia of Chromatography, Third Edition. (p. 2336–2339). London: Informa, Ltd.
Lawson Lary. (1996). Guidance Memo No. 96007: Evaluation of Calibration Curve Linearity. Virginia: Department of Environmental Quality Water Operations Commonwealth of Virginia, p. 1–2.
Purbandika, I M.D.M. (2011). Metode Ekstraksi Fase Padat (Solid Phase Extraction) Untuk Narkotika dan Psikotropika Dalam Urin. Skripsi. Universitas Udayana, Bukit Jimbaran. hal 44.
Tjay, T. H. & K. Rahardja. (2008). Obat-Obat Penting. Jakarta: PT Elex Media Komputindo. hal 314.
United Nations Office on Drugs and Crime. (2009). Guidance for the Validation of Analytical Methodology and Calibration of Equipment used for Testing of Illicit Drugs in Seized Materials and Biological Specimens. New York: United Nations. p. 8, 9, 10-13, 18, 19.
Wirasuta, I M.A.G. (2012). Chemical Profiling of Ecstasy Recovered From Around Jakarta By High Performance Thin Layer Chromatography (HPTLC)-Densitometry (In Press). Egypt J Forensic Sci, vol 2 (3). p. 97–104.
Zeeuw, R.A., J.P. Franke, F. Degel, G. Machbert, H. Schutz, J. Wijsbeek. (1992). Thin Layer Chromatographic Rf
Values of Toxicologically Relevant Substances on Standardized Systems. Jerman: VHC Verlagsgesellschaft mbH
APENDIKS A.
Pengulangan III
Pengulangan II
Pengulangan I
Senyawa pengkoreksi hRf
Ibuprofen
Standar ibuprofen 1000 ng
Standar ibuprofen 800 ng ▲
Standar ibuprofen 400 ng A
Standar ibuprofen 200 ng 4 T
Standar ibuprofen 100 nga T I I I
Standar ibuprofen 50 ng
Standar ibuprofen 20 ng
Standar ibuprofen 10 ng▲
0.00
Gambar A.1. Kromatogram hasil elusi dengan sistem TE
All tracks @ 210 nm
Pengulan
Standar ibuprofen 100
Standar ibuprofen 800 n
Standar ibuprofen 400 ng
Standar ibuprofen 200 ng
Standar ibuprofen 100 ng
Standar ibuprofen 50 ng
Standar ibuprofen 20 ng A
Standar ibuprofen 10 ng
Senyawa pengkoreksi hRf
Pengulangan III▲
Pengulangan II4 I
Gambar A.2. Kromatogram hasil elusi dengan sistem TF
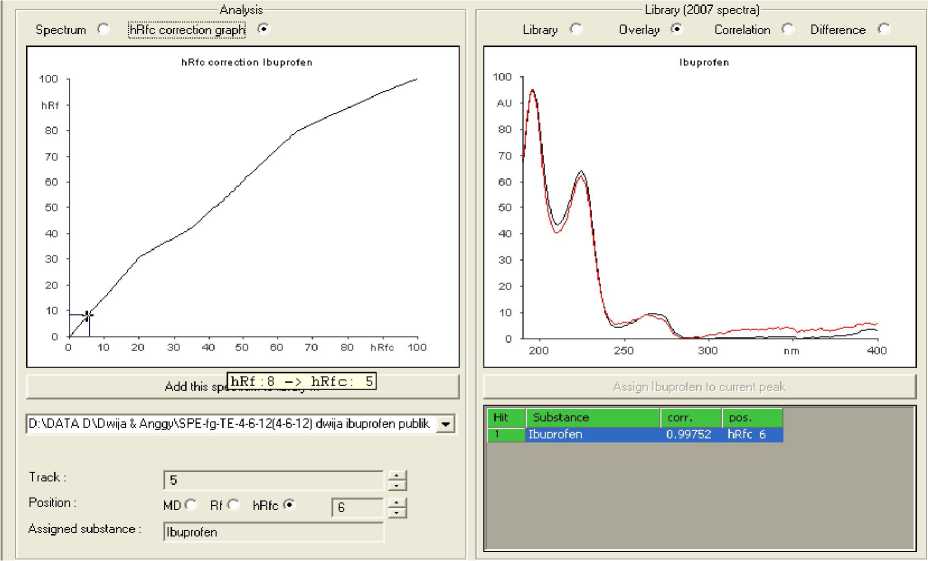
Gambar A.3. Contoh hasil koreksi hRf dengan metode poligonal dan korelasi spektrum analit terhadap spektrum library pada sistem TE
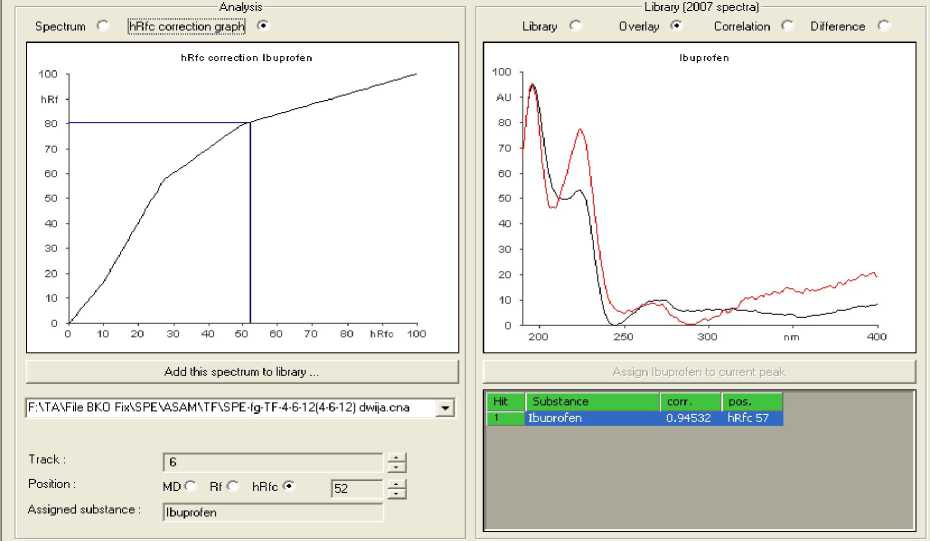
Gambar A.4. Contoh hasil koreksi hRf dengan metode poligonal dan korelasi spektrum analit terhadap spektrum library pada sistem TF
APENDIKS B.
Tabel B.1.Nilai hRf senyawa standar referensi sistem pada sistem TE dan TF
|
Senyawa Referensi |
hRf |
hRfc pustaka |
|
Sistem TE | ||
|
Salbutamol |
31 |
20 |
|
Kodein |
42 |
35 |
|
Difenhidramin |
80 |
65 |
|
Bromheksin |
94 |
88 |
|
Sistem TF | ||
|
Klordiasepoksid |
17 |
10 |
|
Diklofenak |
57 |
27 |
|
Diazepam |
79 |
49 |
Tabel B.2. Hit factor pada sistem TE dan TF
|
Sistem TE |
Sistem TF | ||||||
|
Pengulangan |
hRfc analit |
HF |
Korelasi Senyawa Posisi spektrum |
hRfc analit |
HF |
Senyawa |
Korelasi Posisi spektrum |
|
I |
6 |
1 |
Ibuprofen 0,99729 hRfc 6 |
52 |
1 |
Ibuprofen |
0,92455 hRfc 57 |
|
II |
6 |
1 |
Ibuprofen 0,99752 hRfc 6 |
52 |
1 |
Ibuprofen |
0,94532 hRfc 57 |
|
III |
6 |
1 |
Ibuprofen 0,99842 hRfc 6 |
52 |
1 |
Ibuprofen |
0,93654 hRfc 57 |
|
Keterangan: HF = |
Hit Factor; Posisi |
= nilai hRfc menurut library | |||||
|
Tabel B.3. Hasil identifikasi puncak pada 2 sistem KLT | |||||||
|
Sistem TE |
Sistem TF | ||||||
|
Pengulangan |
hRfc |
HF |
Senyawa dengan Korelasi kecocokan |
hRfc |
HF |
Senyawa dengan Korelasi kecocokan | |
|
analit |
spektrum terbaik |
analit |
terbaik |
spektrum | |||
|
I |
6 |
1 |
Ibuprofen 0,99729 |
52 |
1 |
Ibuprofen |
0,92455 |
|
II |
6 |
1 |
Ibuprofen 0,99752 |
52 |
1 |
Ibuprofen |
0,94532 |
|
III |
6 |
1 |
Ibuprofen 0,99842 |
52 |
1 |
Ibuprofen |
0,93654 |
Keterangan: HF = Hit Factor
Tabel B.4. Uji purity peaks
|
Pengulangan |
Senyawa yang ditandai |
r(s,m) |
Sistem TE r(m,e) Kemurnian |
r(s,m) |
Sistem TF r(m,e) |
Kemurnian | |
|
I |
Ibuprofen |
0,99983 |
0,99963 |
ok |
0,99984 |
0,99962 |
ok |
|
II |
Ibuprofen |
0,99987 |
0,99952 |
ok |
0,99985 |
0,99958 |
ok |
|
III |
Ibuprofen |
0,99984 |
0,99975 |
ok |
0,99983 |
0,99983 |
ok |
Keterangan: r(s,m) = korelasi spektrum Rf awal dibandingkan dengan Rf maks; r(m,e) = korelasi spektrum Rf maks dibandingkan dengan Rf akhir
|
Tabel B.5. Uji presisi hRf pada sistem TE dan TF | ||
|
Sistem KLT |
TE |
TF |
|
Rata-rata |
7 |
85 |
|
SD |
0 |
1 |
|
KV |
0 |
1,1764 |
Keterangan: SD = Standar Deviasi; KV = Koefisisen Variansi
Tabel B.6. Uji presisi AUC pada sistem TE dan TF
|
Massa Penotolan (ng) |
400 |
500 |
600 | |||
|
Sistem TE |
Sistem TF |
Sistem TE |
Sistem TF |
Sistem TE |
Sistem TF | |
|
Rata-rata |
2459,367 |
790 |
3127,467 |
2634,9 |
3755,9 |
3586,8 |
|
SD |
41,20829 |
10,66583 |
26,50987 |
47,37943 |
17,63888 |
68,49095 |
|
KV |
1,6755652 |
1,350105 |
0,847647 |
1,798149 |
0,469631 |
1,909528 |
Keterangan: SD = Standar Deviasi; KV = Koefisisen Variansi
16
Discussion and feedback