SINTESIS FOTOKATALIS ZnO-SiO2 DENGAN METODE SOL GEL UNTUK FOTODEGRADASI ZAT WARNA RHODAMIN B
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 17 (2), JULI 2023 DOI: https://doi.org/10.24843/JCHEM.2023.v17.i02.p5
p-ISSN 1907-9850
e-ISSN 2599-2740
SINTESIS FOTOKATALIS’ ZnO-SiO2MENGGUNAKANnMETODE SOL-GEL PADA FOTODEGRADASI ZAT WARNA RHODAMIN B
L. Nainggolan, I W. Sudiarta*, dan I W. Suarsa
Program Studi Kimia, Fakultas’ Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Kampus Bukit Jimbaran, Jimbaran, Bali, Indonesia
*Email: wayansudiarta@unud.ac.id
ABSTRAK
Penelitian mengenai sintesis ZnO-SiO2 dengan metode sol gel dan penggunaannya dalam mendegradasi zat warna tekstil Rhodamin B telah berhasil dilakukan. Penelitian ini bertujuan dalam mengetahui karakteristik dari komposit ZnO-SiO2, menentukan waktu optimum dan pH optimum fotodegradasi zat warna Rhodamin B. Karakterisasi fotokatralis meliputi analisis difraksi sinar-X (XRD) untuk kristalinitas, analisis morfologi permukaan dengan mikroskop elektron (SEM), analisis gugus fungsi dengan spektrofotometer infra merah (FTIR). Aktivitas fotokatalitik ditentukan dengan mengukur degradasi larutan Rhodamin B melalui pengukuran absorbansi Rhodamin B sisa dengan metode spektrofotometri UV-Visible. Hasil penelitian ini menunjukkan fotokatalis ZnO-SiO2 berhasil disintesis dengan ukuran kristal berkisar dari 15,51 – 82,71 nm, dengan rata-rata ukuran kristal sebesar 48,53 nm dan kristal berbentuk wurtzite (hexagonal). Fotodegradasi dipengaruhi oleh waktu penyinaran dan pH larutan. Fotodegradasi optimum terjadi pada pH 6 dan waktu penyinaran 3 jam, serta %D (persentase degradasi) 99,10 ± 0,42 %.
Kata kunci: fotodegradasi, karakterisasi, Rhodamin B, ZnO-SiO2
ABSTRACT
Research about the synthesis of ZnO-SiO2 with a sol-gel method and its use in degrading the textile dye Rhodamine B has been done. This research aims to know the characteristics of the ZnO-SiO2 composite and determine the optimum time and pH for the photodegradation of Rhodamine B dye. The photocatalytic characterization included X-ray diffraction (XRD) analysis for crystallinity, surface morphology analysis by electron microscopy (SEM), and analysis of the functional groups by using an infrared spectrophotometer (FTIR). The photocatalytic activity was determined by measuring the degradation of the Rhodamine B solution by measuring the absorbance of the remaining Rhodamine B using the UV-Visible spectrophotometry method. The results showed that the ZnO-SiO2 photocatalyst was successfully synthesized with crystal sizes ranging from 15.51 – 82.71 nm, an average crystal size of 48.53 nm and a wurtzite (hexagonal) structure. The photodegradation was affected by irradiation time and the pH of the solution. The optimum photodegradation conditions occurred at pH 6 and irradiation time of 3 hours, with the percentage of degradation (%D) of 99.10 ± 0.42%.
Keywords: characterization, photodegradation, Rhodamin B, ZnO-SiO2
PENDAHULUAN
Perkembangan teknologi dan ilmu pengetahuan mendorong tumbuhnya perindustrian di Indonesia. Salah satunya industri tekstil. Keberadaan industri tekstil menghasilkan keuntungan, seperti meningkatkan produk dan pendapatan dari industri itu sendiri serta mengurangi angka pengangguran masyarakat,. Produk tekstil dan industri tekstil adalah industri yang sangat penting dalam meningkatkan nilai perekonomian Indonesia. Berkembangnya industri tekstil berdampak pada produksi
limbah zat warna tekstil yang semakin meningkat (Maryadi, 2007).
Dalam permasalahan pencemaran air, limbah tekstil sangat berperan besar pada lingkungan, apalagi limbah dibuang ke lingkungan tanpa ada pengolahan terlebih dahulu. (Suwarsa, 1998). Menurut Toca-Herrera yang dikutip Hussein (2011), bahwa dalam bentuk limbah cair zat warna, akumulasi zat warna tekstil mencapai 75%. Zat warna yang banyak digunakan pada industri tekstil adalah metilen blue, metilen orange, congo red, remazol brilliant blue, Rhodamin B, dan lain sebagainya.
Rhodamin B merupakan satu dari banyak zat warna yang sering digunakan untuk keperluan pabrik kertas dan tekstil yang memberikan warna yang cerah dengan harga yang murah, dan mudah diperoleh, dan (Arief et al, 2007). Senyawa Rhodamin B banyak ditemukan dalam limbah cair hasil industri karena penggunaan Rhodamin B yang semakin meningkat. Limbah buangan Rhodamin B dapat menurunkan kualitas air dan dapat menimbulkan berbagai penyakit serius dalam tubuh jika terdapat di makanan atau diminuman yang kita konsumsi. Diperlukan suatu metode yang efisien dan efektif untuk mengurangi kandungan Rhodamin B dalam limbah cair dengan mengolah limbah tekstil sebelum dibuang ke lingkungan (Stockle, 2014).
Berbagai metode pengolahan limbah tekstil zat warna dikembangkan, salah satunya adalah metode adsorpsi, tetapi zat warna yang diadsorpsiiterakumulasi di adsorben mengakibatkan metode ini kurang efektif dan dapat menimbulkan permasalahan baru bagi lingkungan (Utubira, 2006). Sebagai alternatif digunakan metode fotodegradasi. Fotodegradasi adalah reaksi pemecahan kimia yang berlangsung dengan adanya sinar UV dan katalis dengan bantuan energi foton (Nogueira dan Jardim, 2005). Fotodegradasi membutuhkan katalis seperti CuO, ZnS, TiO2, dan ZnO karena bersifat semikonduktor (Wijaya et al., 2006). Banyak penelitian degradasi zat warna sintetis menggunakan fotokatalis TiO2, beberapa juga menggunakan semikonduktor ZnO. Sebagian semikonduktor memiliki celah pita yang cukup yang digunakan dalam proses fotokatalis, seperti ZnO (energi celahh = 3,4 eV); TiO2 (energi celahh = 3,2 eV) ; dan lain-lain. Dalam menggantikan TiO2 digunakan ZnO karna sama-sama memiliki mekanisme fotodegradasi yang cukup terjangkau (Sibarani et al, 2016).
Diker et al., (2011) menyatakan bahwa faktor yang mempengaruhi fotodegradasi suatu zat warna adalah pH, konsentrasi, massa dan waktu kontak. Pada penelitian Wei et.al (2011), memperoleh laju proses fotokatalitik TiO2-SiO2 akan meningkat dengan semakin besar nilai pH pada degradasi Rhodamin B. Nilai pH (derajat keasaman) adalah salah satu variabel yang penting pada pengolahan limbah cair zat warna. Adapun waktu kontak juga mempengaruhi aktivitas fotodegradasi.
Penelitian Abdul et al., (2016) menyatakan bahwa untuk meningkatkan proses
fotokatalik, dengan penentuan aktivitas fotokatalik dilakukan pencampuran SiO2 dengan fotokatalis semikonduktor lainnya. Ada beberapa kelebihan dari metode sol-gel yaitu: kemurnian tinggi, suhu relatif rendah, tidak bereaksi dengan senyawa sisa, dapat memperkecil kehilangan bahan akibat
penguapan, kehomogenan yang lebih baik, dan berkurangnya udara yang tercemar (Fernandez, 2011). Hasil komposit ZnO-SiO2 metode solgel dikarakterisasi menggunakan XRD untuk analisis kristalinitas, SEM untuk melihat morfologi dari fotokatalis, dan FTIR untuk mengidentifikasi gugus fungsi dari ZnO- SiO2. Uji aktivitas fotokatalik terhadap Rhodamin B dilakukan dalam variasi waktu kontak dan variasi pH.
MATERI DAN METODE..
Bahan.
Dalam pelaksanaan penelitian ini menggunakan bahan kimia yang berkualitas p.a (pro analisis): Rhodamin B
(C28H31N2O3Cl), Tetraetil Ortosilikat (TEOS), Seng Asetat Dihidrat (Zn(CH3COO)2.2H2O), Etanol 99,9%, Asam Klorida, Katalis NH3 25% (Merck), Akuades.
Peralatan
Peralatan yang digunakan dalam penelitian ini adalah: gelas beker, labu ukur, filler, pipet volume,,pipet tetes, batang pengaduk, pipet ukur, spatulla, neraca analitik, desikator, oven, cawan porselin, alu mortar, botol sampel gelap, pH meter, aluminium foil, kertas saring, plastik hitam, kotak radiasi, lampu UV, E-Liquid Magnetic Stirrer 6800 rpm, Stirrer Bar, Centrifuge Centurion Merk Kubota, Type: S700TR, Scaning Electron Mycroscopy,(SEM) Type: Inspect-S50 Merk FEI,, Forie Transform Infra-Red (FTIR), Type : IRPrestige 21; Merk Shimadzzu, X-Ray Difraction (XRD) Type: E’xpert Pro; Merk Pan Analytical,, UV-Visible Spectrophotometer Double Beam Merk Shimadzu, Type: UV-1800.
Cara Kerja
Sintesis komposit ZnO- SiO2 dengan metode sol-gel
Sintesis ZnO-SiO2 dengannmetode solgel terdiri dari hidrolisis, kondensasi dan aging, serta pengeringan (Fernandez, 2013). Pembuatan fotokatalis ZnO-SiO2 dilakukan
dengan penambahan 54 mL TEOS (tetraethyl orthosilicate), 33,00 g (Zn(CH3COO)2.2H2O) dan 200 mL etanol diaduk menggunakan pengaduk magnetik selama ±45 menit dalam gelas beker. Kemudian ditambahkan 4,67 mL NH3 dan 30 mL akuades sambil diaduk kembali selama ± 45 menit. Larutan gel di aging selama 3 hari. Setelah proses aging selanjutnya disaring dan dioven pada suhu 100°C sampai pelarut menguap seluruhnya. Jika dalam bentuk padatan maka terlebih dahulu dilakukan penggerusan untuk mendapatkan serbuk. Serbuk fotokatalis ZnO-SiO2 disimpan di dalam desikator sebelum dikarakterisasi dengan XRD, SEM, FTIR (Beganskiene et al., 2004).
Karakterisasi Fotokatalis ZnO-SiO2
Fotokatalis ZnO-SiO2 dikarakterisasi menggunakan X-RD untuk mengetahui tingkat kristalinitas fotokatalis yang terbentuk dan mengidentifikasi unsur dalam fotokatalis. Scanning Elektron Microscopy (SEM) untuk melihat morfologi dari fotokatalis, dan untuk mengidentifikasi gugus fungsi fotokatalis ZnO-SiO2 dengan FTIR (Fourierr Transform Infrra Red) (Thermo, 2001).
Penentuan waktu penyinaran optimum
Lima buah gelas beker 100 mL masing-masing diisi dengan 10 mL larutan Rhodamin B 100 ppm dengan keadaan yang dubungkus plastik hitam. Kemudian dimasukkan 0,1 g komposit ZnO- SiO2, dan dilakukan penyinaran UV sambil diaduk dengan pengaduk magnetic dengan variasi 1, 2, 3, 4, dan 5 jam. Pemisahan larutan yang mengandung sisa zat warna dari suspensi dilakukan dengan sentrifugasi dengan kecepatan 4000 rpm 8 menit. Kemudian masing-masing supernatant dianalisis dengan spektrometer UV-Vis pada panjang gelombang maksimum. Nilai absorbansi yang diperoleh selanjutnya disubstitusikan ke persamaan regresi linear kurva kalibrasi, untuk menghitung konsentrasi Rhodamin B. Nilai konsentrasi yang diperoleh, digunakan untuk menghitung persentase degradasi Rhodamin B. Nilai konsentrasi yang diperoleh, digunakan untuk menghitung persentase degradasi Rhodamin B dengan persamaan:
Persentase Degradasi (%D) = c^cr %100% (1) Keterangan:
Ca = Konsentrasi awal Rh B (sebelum radiasi) Cr = Konsentrasi Rh B setelah radiasi (t)
Berdasarkan nilai persentase degradasi, maka dapat diketahui waktu penyinaran optimum untuk degradasi Rhodamin B oleh fotokatalis ZnO-SiO2.
Penentuan pH larutan optimum
Enam beker glass 100 mL masing-masing diisi dengan 10 mL larutan Rhodamin B 100 ppm dengan keadaan dibungkus plastik hitam. Kemudian dimasukkan 0,1 g komposit ZnO- SiO2, dan dilakukan penyinaran UV sambil diaduk dengan pengaduk magnetic dengan variasi pH 3, 4, 6, 7, 8, dan 10 secara berurutan. Pengaturan pH dengan penambahan HCl untuk pH 3, 4, 6 dan NH3 untuk pH 8, 10. Masing-masing gelas beker ditambah 0,1 g komposit ZnO-SiO2, kemudian Gelas beker dimasukkan ke dalam kotak radiasi yang sudah ada pengaduk magnetiknya dan pembungkus plastik hitam dilepaskan. Fotodegradasi dilakukan selama waktu optimum (3 jam). Pada proses penyinaran larutan harus diaduk menggunakan pengaduk magnetik. Dilakukan sentrifugasi dengan kecepatan 4000 rpm 8 menit untuk pemisahan larutan yang mengandung sisa zat warna dari suspensi. Kemudian masing-masing supernatant dianalisis dengan spektrometer UV-Visible dengan panjang gelombang maksimum. Nilai absorbansi yang diperoleh selanjutnya disubstitusikan ke persamaan regresi linear kurva kalibrasi, untuk memperoleh konsentrasi Rhodamin B.
Desorpsi Rhodamin B
Komposit ZnO-SiO2 yang telah digunakan pada proses fotodegradasi pada kondisi optimum ditambah dengan 25 mL etanol, kemudian diaduk dengan magnetic stirrer dengan waktu 3 jam, selanjutnya disentrifugasi untuk memisahkan fotokatalis dengan cairan (supernatant). Rhodamin B yang terdesorpsi berada dalam supernatant diukur absorbansinya pada panjang gelombang maks dengan spektrofotometer UV-Vis (etanol sebagai blanko). Hasil absorbansi dibuat dalam persamaan regresi linier Rhodamin B (y = bx ± a), sehingga diperoleh konsentrasi Rhodamin B yang terdesorpsi.
HASIL DAN PEMBAHASAN
Fotokatalis ZnO-SiO2
Sol-gel adalah salah satu metode pembuatan fotokatalis yang sederhana untuk
mensintesis nanopartikel (Zawrah et al., 2009). Sintesis ZnO-SiO2 dengan metode sol-gel, ada tiga tahap yaitu hidrolisis,,kondensasi dan aging serta pengeringan dengan oven (Fernandez, 2013). Penambahan Zink Acetate dengan TEOS (Tetraethyl orthosilicate) membentuk silika’ ter-doping dalam ZnO. (Zn(CH3COO)2.2H2O) berfungsi sebagai prekursor (sumber Zn) sementara TEOS sebagai prekursor SiO2. Penambahan NH3 bertujuan untuk proses hidrolisis prekursor yang cepat. Etanol berfungsi sebagai pelarut karena jika direaksikan dengan (Zn(CH3COO)2.2H2O) akan menghasilkan Zn2+, etil asetat (CH3COOC2H5), dan air (H2O) dengan reaksi sebagai berikut:
Zn(CH3COO)2.2H2O + 2C2H5OH(aq) → Zn2+(aq) + 2CH3COOC2H5(aq) + 3H2O(aq)
Hidrolisis komposit ZnO-SiO2 memperoleh endapan putih. Kondensasi dan aging memperoleh gel. Proses pengeringan menghasilkan serbuk putih.
Hasil Karakterisasi Fotokatalis ZnO-SiO2X-Ray Difraction (XRD)
Hasil karakterisasi fotokatalis ZnO-SiO2 dengan X-RD (X-Ray Diffraction) bertujuan untuk mendapatkan ukuran partikel serta mengidentifikasi fasa kristalin dalam material. Tabung anoda digunkan untuk pengukuran X-RD dengan logam target Cu (λ =1,5418 nm). Karakterisasi X-RD untuk memperoleh struktur kristal dari ZnO-SiO2 yang terbentuk, dan dibandingkan dengan literatur. Gambar 2. merupakan perbandingan
karakterisasi ZnO menurut Sunardi (2020) dan hasil sintesis ZnO-SiO2 menggunakan X-RD.
Berdasarkan Gambar 1 perbandingan difraktogram ZnO-SiO2 hasil sintesis dan difraktogram hasil penelitian Sunardi (2020) mengindikasikan bahwa ZnO-SiO2 sudah terbentuk, ditunjukkan oleh puncak puncak tajam pada daerah 2θ = 10-30 yaitu 12,48°; 17,73° ; 22,31°; 37,25°; 38,03° merupakan puncak puncak kristal ZnO, sedangkan puncak melebar pada daerah 2θ = 20-30 yang berada pada dasar puncak puncak tajam menunjukkan kristal SiO2 yang berbentuk amorf. Hasil karakterisasi X-RD menunjukkan bahwa hasil penelitian ini sama dengan penelitian Sunardi (2020) yang menyatakan bahwa difraktogram X-RD nanokomposit SiO2/ZnO menunjukkan puncak pada 2θ yaitu 30,42°, 31,56°, dan 44,40° dan menghasilkan ukuran komposit dengan rentang ukuran 100-200 nm.
Ukuran kristal (D) dihitung dengan persamaan D = 0,9 .λ. dimana dari setengah βcos θ
lebar puncak maksimum X-RD diperoleh ukuran kristal sampel. Hasil perhitungan dengan persamaan scherre diperoleh range ukuran kristal berkisar dari 15,51 – 82,71
dengan ukuran kristal rata-rata berukuran nanopartikel sebesar 48,5281 nm. (Lampiran 2.) Nilai FulllWidth to Half Maximum (FWHM) berbanding terbalik dengan besar ukuran kristal, dan dipengaruhi oleh intensitas dari setiap bidang kristal. Semakin besar FWHM maka nilai ukuran kristal yang terbentuk akan semakin kecil, tetapi Semakin tinggi intensitas maka nilai FWHM semakin kecil.

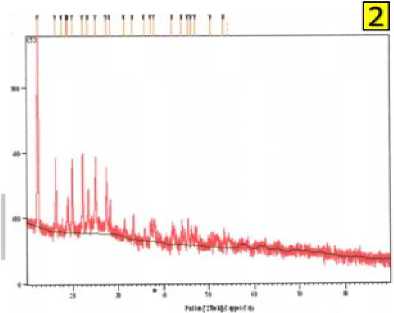
Gambar 1 Difraktogram:1.(a) Bahan Silika Murni, (b) Bahan ZnO Murni dan (c) SiO2/ZnO Nanokomposit dari Abu Vulkanik dan Limbah Seng , Sunardi (2020) dan 2.
Difragtogram ZnO-SiO2 Hasil Sintesis
Scanning Electron Microscopy (SEM)
Analisis ZnO-SiO2 dengan SEM yaitu untuk mengetahui komposisi dan morfologi hasil sintesis campuran silika (SiO2) yang merupakan partikel amorf dengan ZnO, dengan perbesaran sampai dengan 100.000 kali (skala 500 nm). Ukuran dan gambar morfologi padatan merupakan hasil analisis SEM. Hasil SEM pada Gambar 2 menunjukkan bahwa kristal yang terbentuk berupa material yang cukup seragam berupa lingkaran. Hasil ini sesuai dengan penelitian yang diterbitkan Sunardi (2020), dimana sintesis nanokomposit SiO2/ZnO memiliki rentang ukuran 100-200 nm dengan bentuk melingkar yang seragam.
Forrier Transform Infra Red (FTIR)
Spektra FTIR pada Gambar 3 menunjukkan adanya pita serapan SiO2 yang muncul pada gelombang 994,76 dan 1053,3. Pita serapan regangan ZnO berada pada gelombang 439,77 cm-1. Penyerapan sinar pada 439,77 menghasilkan serapan gugus Si-O-Si, dan serapan 994,76 menghasilkan gugus silanol.(Si-O-H) yang terkondensasi lebih lanjut ke siloksan (Si-O-Si) serta serapan kuat di gelombang 1053,30 untuk vibrasi asimetris .Si-O-Si. Puncak serapan gelombang 3414 cm-1 pada fotokatalis ZnO-SiO2 dengan serapan melebar diidentifikasi jadi vibrasi ulur gugus fungsi O-H ikatan hidrogen dari silika (SiO2).

Gambar 2. Foto SEM Fotokatalis ZnO-SiO2 (perbesaran 100.000 kali)
Hasil penelitian sejalan dengan hasil penelitian Saraswati (2014) yang menghasilkan daerah regangan serapan ZnO pada gelombang 400,00-500,00. Sunardi (2020) menyatakan bahwa spektrum SiO2 yang kuat menunjukkan adanya silika yang ditunjukkan dengan munculnya spektrum SiO2 dengan gelombang 993,340 dan 1109,070, sedangkan ZnO berada di gelombang 443,63 cm-1. Penelitian Maula (2015) menyatakan bahwa spektrum SiO2 yang kuat menunjukkan adanya silika, termasuk pembengkokan simetris Si -O- Si dengan bilangan,gelombang 470,60 cm-1 dan ,Si -O- Si pada 964,34 cm-1.

Gambar 3. Spektra FTIR Fotokatalis ZnO-SiO2
Waktu Penyinaran Optimum untuk Fotodegradasi Rhodamin B oleh Fotokatalis ZnO-SiO2
Gambar 4 menunjukkan terjadinya peningkatan persentase degradasi Rhodamin B seiring dengan peningkatan waktu penyinaran sinar UV. Intensitas cahaya yang diberikan pada system berhubungan dengan kenaikan persentase degradasi dan berbanding lurus dengan waktu. Apabila intensitas cahaya yang diberikan pada sistem cukup rendah (0-20 mW/cm2), maka reaksi fotodegradasi akan bergantung pada pembentukan hole elektron. Hal ini berarti, waktu radiasi sinar UV bergantung pada energi/foton dimana semakin lama maka semakin banyak energi pada permukaan ZnO dengan persentasi degradasi yang semakin besar (Nurhasanah, et.al., 2011).
Semakin besar intensitas cahaya yang diberikan, maka persentase degradasi dan dekolorisasi semakin tinggi (Kumar dan Pandey, 2017). Hasil optimasi penyinaran waktu degradasi menunjukkan perubahan warna pink menjadi bening dari jam ke-3. Kenaikan degradasi Rhodamin B terjadi pada menit ke-1 menuju jam ke-5. Setelah mencapai 3 jam, proses fotodegradasi tidak meningkat secara signifikan. Pada waktu 4 dan 5 jam persentase degradasi relatif stabil yang hanya memiliki selisih 0,36 %. Hal ini mungkin terjadi karena kemampuan komposit ZnO-SiO2 dalam mendegradasi rhodamin B sudah mencapai titik maksimal. Lambatnya laju degradasi polutan setelah waktu tertentu mencerminkan bahwa reaksi antara polutan dengan radikal hidroksil (•OH) sulit berlangsung. (Augugliaro et al., 2006).
Berdasarkan analisis tersebut, maka waktu penyinaran selama 3 jam dipilih sebagai waktu penyinaran optimum dengan persentase degradasi (%D) 98,96 ± 0,54.
100.00 τ O £ 99.00 --^ 98.00 -F3 S5 97.00 -Ω S 96.00 -
I 95.00 4----------1----------1-----------1-----------1-----------1----------1
" 0 1 2 3 4 5 6
l½ktu (jam)
Gambar 4. Kurva Hubungan Waktu Penyinaran dengan’ Persentase Degradasi

Nilai pH Optimum Fotodegradasi Rhodamin B oleh Fotokatalis ZnO-SiO2
Nilai pH optimum merupakan kondisi pH larutan yang dibutuhkan untuk memberikan persentase degradasi terbaik pada reaksi fotodegradasi Rhodamin B oleh fotokatalis ZnO-SiO2. Perbedaan kondisi pH larutan dapat menyebabkan perubahan muatan permukaan dan pergeseran potensial reaksi fotokatalis sehingga mempengaruhi proses degradasi zat warna kekuatan ionik, dan mempengaruhi proses adsorbsi. Hubungan antara nilai pH dengan persentase degradasi pada reaksi fotodegradasi Rhodamin B oleh fotokatalis ZnO-SiO2 ditunjukkan oleh Gambar 5.
Pada Gambar 5 menunjukkan Zat Rhodamin B terdegradasi lebih cepat pada pH asam dibandingkan dengan pH basa. Pada pH 4 mengalami penurunan persentase degradasi dan meningkat pada pH 6, kemudian mengalami penurunan dari pH 7 hingga pH 9. Leksono (2012) memperoleh hasil persentase degradasi optimum senyawa Rhodamin B menggunakan fotokatalis bentonite terpilar TiO2 sebesar 93,24% pada pH 3 (asam), sedangkan Saraswati (2014) memperoleh hasil degradasi optimum menggunakan ZnO-arang aktif sebesar 87,87% pada pH 4 (asam). zat warna Rhodamin B yang mempunyai muatan negative mudah ter-adsorpsi pada permukaan ZnO kondisi asam bermuatan positif. Interaksi elektrostatis ZnO dengan muatan positif dan Rhodamin B muatan negatif menghasilkan adsorpsi kuat yang diperoleh dari Silika dioksida. Sebaliknya ZnO akan bermuatan negatif pada pH basa yang mengakibatkan anion Rhodamin B mengalami gaya tolak-menolak. Rhodamin B termasuk dalam zat warna bermuatan negative pada pelarut air, karena itu pada pH basa Rhodamin B kurang efektif terdegradasi (Sibarani. 2016). Semakin banyak jumlah zat warna Rhodamin B yang teradsorpsi pada ZnO maka semakin banyak juga Rhodamin B yang terdegradasi pada kondisi asam oleh fotokatalis ini. Hal ini juga diperoleh Ayu et al. (2020) yang menyebutkan bahwa fotodegradasi zat tekstil Rhodamin B terjadi di suasana asam. Berdasarkan analisis tersebut, maka pH kerja optimum fotodegradasi Rhodamin B oleh fotokatalis ZnO-SiO2 yang dipilih adalah pH 6 dikarenakan persentase degradasinya relative konstan. Dimana pada pH 4 mengalami penurunan persentase degradasi yang berpengaruh pada kurang efektifnya pH 3. Selisih persentase degradasi (%D) antara pH 3
dan pH 6 hanya 0,3 % dengan %D optimum (pH 6) sebesar 99,10 ± 0,42 %.

Gambar 1. Kurva hubungan pH dengan persentase dgradasi (%D)
Fotokatalis Rhodamin B oleh ZnO-SiO2 dan Sinar UV
Berdasarkan data fotodegradasi pada kondisi optimum yaitu pada pH 6 dengan waktu penyinaran 3 jam diperoleh bahwa konsentrasi Rhodamin B dalam supernatant (kadar sisa) sebesar 0,90 mg/L. konsentrasi awal Rhodamin B sebesar 100 mg/L, sehingga konsentrasi yang terdegradasi sebesar 99,10 mg/L. Berdasarkan data konsentrasi tersebut maka diperoleh persentase degradasi Rhodamin B (%D) sebesar 99,10 ± 0,42 %.
Fotodegradasi Rhodamin B terjadi pada permukaan fotokatalis ZnO-SiO2 dengan perkiraan mekanisme fotokatalisis sebagai berikut:
ZnO + hυ → hvb+ + ecb-
O2+ ecb- → •O2-
hvb+ + H2O → OH- + H+
2O2•- + 2H2O → H2O2 + 2OH-+ O2
H2O + ecb- → OH- + •OH
C28H31N2O3Cl- + •OH → CO2 + H2O + senyawa sederhana lain (produk)
Radiasi UV (hv) mengenai ZnO pada ZnO-SiO2 memunculkan terjadinya electron dengan loncatan dari pita valensi selanjutnya ke konduksi pada logam. Loncatan elektron memenculkan lubang elektron (hole) dengan interaksi pada air sebagai pelarut dan bentuk radikal •OH. Sifat Radikal •OH ini adalah aktif dan mampu menguraikan target senyawa organik (Gustavson et al., 2010). Elektron pada pita konduksi bereaksi dengan Oksigen menghasilkan ion O2- yang selanjutnya
direaksikan dengan air dalam susana asam menghasilkan radikal •OH. Oksidator dan reduktor yang terbentuk akan mendegradasi zat warna sehingga menghasilkan CO2, H2O serta senyawa yang lebih sederhana (Batista et al., 2010).
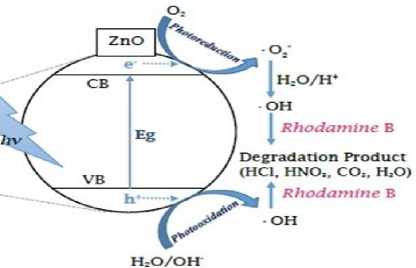
Gambar 2. Mekanisme Fotokatalisis Rhodamin B oleh ZnO-SiO2 dan Radiasi (Malato et al., 2002)
Reaksi degradasi fotokatalitik di permukaan semi-konduktor dengan melalui pemberi elektron dari substrat ke h+ (hole) dan memperoleh radikal pada substrat untuk menginisiasi reaksi-reaksi yang berantai). Jika oksidasi potensial h+ (hole) pada pita valensi cukup besar dalam mengoksidasi gugus hidroksil dan H2O dengan menghasilkan (•OH) radikal hidroksil.. Rhodamin B dalam fasa larutan teradsorpsi pada permukaan fotokatalis, selanjutnya dengan kehadiran radiasi UV yang menyinari katalis ZnO-SiO2 mengakibatkan terjadinya reaksi fotokatalisis Rhodamin B menjadi air dan gas CO2. Laju fotodegradasi Rhodamin B dipengaruhi oleh kecepatan Rhodamin B teradsorpsi pada permukaannya. Dalam peristiwa ini terjadi dekolorisasi Rhodamin B yang melibatkan dua peristiwa yaitu adsorpsi dan fotokatalisis/fotodegradasi, dimana proses fotokatalisis/fotodegradasi Rhodamin B menjadi senyawa lebih kecil lain lebih dominan, dan Rhodamin B yang masih terserap dalam fotokatalis setelah raksi fotokatalisis berhenti. Rhodamin B yang masih terserap tersebut dibuktikan dengan desorpsi, dimana diperoleh hasil desorpsi Rodamin B sebesar 0,0531 mg/L. Berdasarkan hasil desorpsi dapat diduga bahwa pada proses dekolorisasi sebagian besar merupakan hasil fotodegradasi dan sebagian kecil akibat Rhodamin B masih terperangkap dalam fotokatalis akibat adsorpsi. Dari 99,10 mg/L Rhodamin B yang terdekolorisasi, sekitar 0,0531 mg/L masih tertahan dalan fotokatalis.
Hal ini menunjukkan bahwa dekolorisasi (penghilang zat warna) didominasi oleh proses fotodegradasi.
SIMPULAN
Fotokatalis komposit ZnO-SiO2
berhasil disintesis dengan menggunakan metode sol-gel, didukung oleh hasil difraktogram X-RD dimana teridentifikasi pada 2 theta 20-30 muncul puncak dasar melebar yang merupakan puncak SiO2 yang amorf. Fotokatalis ZnO-SiO2 hasil sintesis mempunyai karakteristik ukuran Kristal antara 15,51 –
82,71 nm dan ukuran kristal rata-rata 48,5281 nm. Morfologi fotokatalis berupa lingkaran. Fotokatalis juga mempunyai gugus Zn - O, Sii-oO, Si -O- Si, dan Sii- OH. Fotodegradasi lebih sempurna berlangsung pada suasana asam dengan pH optimum pada pH 6. Semakin lama waktu penyinaran maka semakin tinggi kemampuan fotodegradasinya dengan waktu optimum kontak/penyinaran 3 jam. Persentase fotodegradasi Rhodamin B oleh ZnO-SiO2 pada kondisi optimum sebesar 99,10±0,42 % .
DAFTAR PUSTAKA
Arief, S., Safni, Roza, P. P. 2007, Degradasi Zat Warna Rhodamin Sonolisis
menggunakan Penambahan TiO2 Hasil Sintesis Sol Gel. Jurnal Riset Kimia. 1(1): 64-70
Batista, A. P. L., de Carvalho, H. W. P., Luz, G. H. P., Martins, P. F. Q. 2010. Preparation of Cu/SiO2 and Photocatalityc Activity to Degradation of Methylen Blue. Journallof Environment Chemistry. (8): 63-67
Diantariani, N. P., Widihati, I. A. G., Megasari, I. G. A. A. R. 2014. Fotodegradasi Metilen Biru dengan Katalis ZnO dan Sinar UV. Jurnal Kimia. 8(1): 137-143
Fernandez, R. 2012. Sintesis SiO2 dengan Metode Sol-Gel serta Aplikasinya terhadap Aktifitas Sitoksik Sel, Skripsi, Program Studi Kimia. FMIPA. Universitas Andalas,
Gustavson, E., dan Schuler A., 2010.
Photocatalys Degradation of Rhodamin B for TiO2 Composites. Thesis. Physics of Biological and Material Systems
Radiation Physics. University
Gothenburg
Husein, S., Umar. 2011., Penelitian Untuk Skripsi dan Tesis BisnissEdisi 11. Jakarta: PT. Grafindo Persada
Kumar. A, Pande., 2017. Photodegradation of Methylene Blue N in Aqueous and Solution Using Zinc Oxide and Titanium Dioxide. Desalination. 1-14
Madhu, G. M., Raj, R. A. L. A., Pai, K. V. K., Rao, S. 2007. Fotodegradation of Mehylene Blue Dye using UV/BaTiO3, UV/H2O2 and UV/H2O2/BaTiO3
oxidation processes. Indian Journal of Chemical Teknology. 14: 139-144
Maulana, I., 2015. Pengaruh Analisis Silika pada Aktivitas Fotokatalik Nanopartikel ZnO. Tesis. Jurusan Teknik Kimia, ITSN, Surabaya.
Sibarani, J., Purba, D. L., Suprihatin, I. E., Manurung, M. 2016. Fotodegradasi Zat Warna Rhodamin B dengan ZnO/Reagen Fenton/UV. Cakra Kimia (Indonesia E-jounal of Applied Chemistry). 4(1): 8494
Silviana dan Sunardi, 2020, Sintesis dan Karakterisasi Nanokomposit ZnO/SiO2 dari Seng dan abu vulkanik gunung berapi. Journal of Scientific and Applied Chemistry. 23(10): 365-369
Stockle, 2014. Lembar Keselamatan Data Rhodamin B (C.I. 45170). Darmstadt: Pan-Reac Appli-Chem, Jerman
Suwarsa, S.S. 1998. Penyerapan Zat Warna BR Red HE oleh Padi Jerami. JMS. 3(1): 3240.
Widiantini, N. L. P., Sibarani, J., Manurung, M. 2013. Studi Fotodegradasi Congo-Red dengan UV/ZnO/Reagen Fenton, Jurnal Kimia. 7(1): 82-90
Wismayanti, D., 2014, Pembuatan Komposit Arang Aktif -ZnO sebagai Fotokatalis dalam Mendegradasi Zat Metilen Biru, skripsi, Program studi Kimia, FMIPA, UNUD, Jimbaran.
You-ji, L., Wei, C. 2011.
Photocatalytic,Degradation of Rhodamin B using nano-crystalline TiO2 - zeolite surface composite catalysts, effect of photocatalytic condition to degradation efficiency. Catal. Sci. Technol. 1 (2011): 802–809
150
Discussion and feedback