PENURUNAN COD, BOD, TSS, AMONIA DAN KOLIFORM AIR LIMBAH RUMAH POTONG HEWAN DENGAN BIOFILTER AEROBIC FIXED-BED REACTOR DAN KLORINASI
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 16 (2), JULI 2022 DOI: https://doi.org/10.24843/JCHEM.2022.v16.i02.p07
p-ISSN 1907-9850
e-ISSN 2599-2740
PENURUNAN COD, BOD, TSS, AMONIA DAN KOLIFORM AIR LIMBAH RUMAH POTONG HEWAN DENGAN BIOFILTER AEROBIC FIXED-BED REACTOR DAN
KLORINASI
J. B. Butler, I. W. Budiarsa Suyasa* dan I. M. S. Negara
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Bukit Jimbaran, Badung, Bali, Indonesia
*Email: budiarsa_suyasa@unud.ac.id
ABSTRAK
Rumah potong hewan (RPH) menghasilkan limbah cair yang mengandung konsentrasi bahan organik yang tinggi yang dapat memberikan efek mencemari badan air dan lingkungan sekitar. Proses pengolahan limbah RPH dapat dilakukan secara biologis yaitu biofiltrasi dengan memanfaatkan mikroorganisme untuk meremediasi lingkungan serta pengolahan secara klorinasi. Upaya dalam pengolahan limbah cair terus dikembangkan. Penelitian ini bertujuan untuk menentukan efektivitas teknik pengolahan biofiltrasi pada Aerobic Fixed-Bed Reactor (AFBR) berbahan media batu apung dan kemudian dikombinasikan dengan klorinasi terhadap penurunan kadar COD, BOD, TSS, amonia, dan bakteri koliform. Metode yang digunakan adalah menggunakan biofilm hasil pembibitan pada batu apung dengan variasi penambahan suspensi aktif dan tanpa suspensi aktif, perlakuan sistem aerasi dengan variasi waktu pengolahan, serta penambahan kaporit dengan variasi dosis klor aktif. Hasil penelitian menunjukkan bahwa penambahan suspensi aktif pada proses pembibitan menghasilkan biofilm yang terbaik, serta efektif dalam menurunkan kadar COD, BOD, TSS, dan amonia. Penurunan kadar COD terbaik pada jam ke-36 yaitu 81,60 mg/L dengan efisiensi 57,45%, BOD pada jam ke-36 yaitu 24,67 mg/L dengan efisiensi 65,74%, TSS pada jam ke-42 sebesar 54,0 mg/L dengan efisiensi 85,66%, dan amonia pada jam ke-42 yaitu 1,5539 mg/L dengan efisiensi 88,29%. Klorinasi yang dilakukan setelah pengolahan dengan AFBR menghasilkan penurunan jumlah bakteri koliform dari 1.100 MPN/100 mL menjadi 0 MPN/100 mL dengen efisiensi 100%. Proses klorinasi tersebut menghasilkan dosis klor optimum yaitu 165 ppm dengan residu klor 28,80 mg/L. Dengan demikian, waktu pengolahan 36-42 jam pada AFBR kemudian dilanjutkan klorinasi dengan dosis klor 165 ppm relatif cukup efektif dalam menurunkan kadar COD, BOD, TSS, amonia, dan bakteri koliform air limbah RPH.
Kata kunci: amonia, biofilter, klorinasi, koliform.
ABSTRACT
Slaughterhouses produce wastewater containing high organic matter, which has the effect of polluting water and the surrounding environment. Slaughterhouse wastewater treatment can be done biologically, namely biofiltration, by utilizing microorganisms and chlorination. Efforts in wastewater treatment continue to be developed. This study aimed to determine the effectiveness of biofiltration processing techniques with an Aerobic Fixed-Bed Reactor (AFBR) with pumice stone media combined with chlorination to reduce the levels of COD, BOD, TSS, ammonia, and coliform bacteria. The method applied was to use biofilms from the seedings on pumice with variations of with or without the addition of active suspension, aeration system treatment with time variations, and the addition of chlorine with variations of active chlorine doses. The results showed that the addition of active suspension in the process produced the best biofilm, and was effective in reducing the levels of COD, BOD, TSS, and ammonia. The best reduction of COD levels was at the 36th hour at 81.60 mg/L with an efficiency of 57.45%, BOD at the 36th hour was 24.67 mg/L with an efficiency of 65.74%, TSS at the 42nd hour was 54.0 mg/L with an efficiency of 85.66%, and ammonia at the 42nd hour of 1.5539 mg/L with an efficiency of 88.29%. Chlorination after the treatment with AFBR resulted in a decreased number of coliform bacteria from 1,100 MPN/100 mL to 0 MPN/100 mL with 100% efficiency. The chlorination process resulted in the optimum chlorine dose of 165 ppm with a chlorine residual of 28.80 mg/L. Thus, the treatment for 36-42 hours on AFBR followed by chlorination with a chlorine dose of 165 ppm was relatively effective in reducing COD, BOD, TSS, ammonia, and coliform levels of bacteria in slaughterhouses wastewater. Keywords: ammonia, biofiltration, chlorination, coliform.
Keywords: ammonia, biofiltration, chlorination, coliform.
PENDAHULUAN
Kandungan bahan organik yang tinggi umum terkandung pada limbah cair pembuangan, seperti limbah rumah potong hewan. Kegiatan RPH membuang limbah cair yang mengandung bahan-bahan padat, lemak,.darah, tinja hewan, isi.rumen, serta.air cucian. Limbah ini dapat menjadi media pertumbuhan mikroorganisme dan mudah mengalami pembusukan. Dalam proses pembusukannya di dalam air, kandungan NH3 dan H2S yang tinggi akan menimbulkan bau yang tidak sedap serta dapat menyebabkan gangguan pada saluran pernapasan dan kehilangan selera makan (Widya et al., 2008).
Selain itu, terdapat berbagai mikroorganisme yang terkandung dalam limbah cair RPH yang dapat bersifat patogen, seperti kolifom dan E. coli (Tarntip dan.Thungkao,.2011; Ratnawati et al., 2016). Hal ini menandakan bahwa pengolahan limbah cair RPH yang kurang sempurna dapat berpotensi bahaya, karena kandungan bakteri-bakteri patogen yang merupakan bibit penyakit, selain itu dapat meningkatkan COD, BOD, TSS, minyak dan lemak, NH3, serta pH limbah cair (Aini et al., 2017).
Beberapa upaya yang dapat dilakukan dalam mengolah air limbah RPH adalah dengan cara sederhana seperti pengolahan biofilter aerob menggunakan media filter dan klorinasi.
Biofiltrasi aerobik memiliki prinsip yaitu mikroba tumbuh dan berkembang menempel pada.suatu.media.filter.dan.membentuk. biofilm dalam suatu reaktor (attached growth). Biofilter pada metode ini dapat dengan baik menyisihkan kadar BOD, COD, TSS, serta amonia dalam limbah cair (Wijeyekoon et al., 2000). Terdapat biofilter yang dapat digunakan sebagai media dalam pengolahan seperti batu apung. Hal ini dikarenakan batu apung memiliki rongga atau pori pada permukaan yang dapat menjadi wadah yang baik untuk mikroba dan bahan organik membentuk lapisan biomassa (Said, 2005).
Selain pengolahan limbah secara biologis, diperlukan metode lain untuk menurunkan jumlah bakteri patogen yang diduga terkandung pada limbah tersebut. Klorinasi merupakan metode yang baik
dilakukan dalam mengolah limbah cair. Untuk meningkatkan kualitas air limbah secara
kimia, dapat dilakukan metode
klorinasi.sehingga pada…akhirnya dapat mempengaruhi.parameter.bakteriologis.limba h (Busyairi et al., 2016).
Artikel kali ini menyampaikan hasil penelitian tentang penurunan COD, BOD, TSS, amonia, serta bakteri koliform limbah cair RPH dengan metode biofiltrasi aerobik kombinasi klorinasi. Metode biofilter yang digunakan adalah dengan Aerobic Fixed-Bed Reactor (AFBR) dengan media batu apung yang merupakan salah satu media yang baik untuk pembentukan biofilm. Metode klorinasi dapat menggunakan kaporit sebagai bahan dasar klor aktifnya. Penelitian ini bertujuan untuk mengetahui efektivitas terhadap baku mutu biofilm pada AFBR berbahan batu apung terhadap penurunan kadar COD, BOD, TSS, dan amonia, yang kemudian limbah RPH tersebut dilanjutkan ke perlakuan klorinasi untuk penurunan jumlah bakteri koliform.
MATERIAL DAN METODE
Bahan
Sampel air limbah rumah potong hewan (RPH) diperoleh dari usaha perternakan hewan bernama Cinde Laras berlokasi di Mengwi, Bali. RPH Cinde Laras menghasilkan limbah cair hasil pemotongan yang mengalir ke sungai, sawah, dan saluran pembuangan air rumah penduduk setempat.
Bahan kimia yang digunakan adalah KI, K2Cr2O7, Na2S2O3, MnSO4, H2SO4, NaN3, (NH4)2Fe(SO4)2, K2HPO4, KH2PO4, MgSO4, FeSO4, AgSO4, NaOH, Na3C6H5O7, NaOCl, NH4Cl, C5FeN6Na2O, C2H5OH, C6H5OH KMnO4, C2H2O4, glukosa, asam asetat glasial, Bile Green Lactose Broth (BGLB), indikator amilum, indikator ferron, akuades, dan kertas saring.
Alat
Aerobic Fixed-Bed Reactor (AFBR), batu apung, aerator, Erlenmeyer, pipet tetes, pipet volume, ball filler, gelas ukur, botol BOD, buret, statif dan klem, corong, neraca analitik, hotplate, seperangkat alat refluks, batang pengaduk, kaca arloji, oven, gelas Beker, tabung reaksi, rak tabung reaksi,
tabung durham, aluminium foil, dan spektrofotometer Uv-Vis.
Cara kerja
Penentuan Nilai COD
Sampel air sebanyak 25 mL dimasukkan ke labu refluks dan ditambah K2Cr2O7 0,025 N sebanyak 25 mL dan
dihomogenkan. Larutan ditambah 10 mL larutan AgSO4-H2SO4 dan ditambah beberapa batu didih. Campuran direfluks selama 90 menit. Setelah 90 menit, pemanas dimatikan dan campuran dibiarkan mendingin. Campuran ditambah akuades ± 80 mL.
Larutan ditambah beberapa tetes indikator ferroin, kemudian dititrasi dengan larutan (NH4)2Fe(SO4)2 sampai larutan dari biru kehijauan menjadi merah bata.
Penentuan Nilai BOD
Sampel air didalam botol BOD 100 mL lalu diberi MnSO4 dan alkali-iodida-azida masing-masing 1 mL. Botol BOD ditutup lalu dibolak-balik sebanyak 15 kali hingga homogen. Secara perlahan, 1 mL H2SO4 pekat dialirkan ke dalam sampel, kemudian larutan dihomogenkan kembali. Larutan 50 mL larutan dan.dimasukkan ke Erlenmeyer. Larutan dititrasi.dengan.Na2S2O3 0,25 N hingga menjadi. warna. kuning. pucat, lalu ditambahkan 3-5 tetes indikator amilum dan dititrasi hingga.warna biru hilang.
Penentuan Nilai TSS
Sampel air sebanyak 50 mL disaring pada kertas saring, kemudian kertas saring diletakan pada kaca arloji. Kaca arloji dimasukkan ke dalam oven 150°C selama 1 jam. Kertas saring ditimbang sampai konstan.
Penentuan Nilai Amonia Secara Spektrofotometri
Larutan standar amonia 0; 0,2; 0,4; 0,6; 0,8; dan 1 ppm dan sampel sebanyak 25 mL disiapkan. Larutan standar dan sampel ditambah larutan fenol 10% sebanyak 1 mL, natrium nitroprusida sebanyak 1 mL, lalu larutan pengoksidasi 2,5 mL. Masing-masing standar dan sampel ditutup dengan aluminium foil dan didiamkan selama 1 jam untuk pembentukan warna menjadi warna biru. Larutan standar dan sampel dianalisis menggunakan spektrofotometer Uv-Vis pada panjang gelombang 630 nm.
Sampling Sedimen Tanah
Sampling tanah sebagai sumber bibit suspensi aktif diambil di lokasi yang terpapar pembuangan air limbah rumah potong hewan secara random dengan ke dalaman ± 5 – 7 cm dari permukaan tanah, sampel dimasukkan ke dalam botol plastik kedap udara. Sampel disimpan di lemari pendingin sebelum dilakukan pembibitan (seeding) suspensi aktif.
Pembuatan Media Pertumbuhan Mikroorganisme (Nutrien)
Nutrien dibuat dengan (NH4)2[Fe(SO4)2], K2HPO4, KH2PO4, masing-masing 0,1 gram, MgSO4 dan FeSO4 masing-masing sebanyak 0,002 gram, dan glukosa sebanyak 2 gram. Campuran dilarutkan dalam 2 liter akuades hingga homogen.
Pembibitan Suspensi Aktif
Suspensi aktif dibuat dengan campuran sampel sedimen tanah sebanyak 2 gram dan media nutrien sebanyak 500 mL dalam gelas beaker 1000 mL. Pada dasar gelas, dialirkan oksigen menggunakan selang dan batu aerator. Suspensi aktif dibibitkan selama 7 hari.
Pembibitan Biofilm dalam AFBR
Pembibitan di lakukan pada bak aerasi kapasitas 50 L yang terdiri dari batu aerator, aerator, batu apung, dan papan penopang media batu apung. Pembibitan biofilm tanpa suspensi aktif, dimasukkan 5 L media nutrien dan 45 L air got ke dalam bak aerasi I. Pembibitan biofilm menggunakan suspensi aktif dimasukkan 5 L media nutrien, 500 mL suspensi aktif, dan 44,5 L air got ke bak aerasi II. Campuran pada bak tanpa suspensi aktif maupun dengan suspensi aktif kemudian diberi suplai oksigen menggunakan aerator, dan dilakukan pengukuran Mixed Liquor Suspended Solids (MLSS).
MLSS diukur dengan mengambil sampel air pada waktu pembibitan 0; 12; 24; 36; dan 42 jam. Sampel air pada bak aerasi tersebut diambil pada area dekat media filter batu apung sebanyak 25 mL, dan disimpan pada botol plastik kedap udara. Setiap sampel di saring menggunakan kertas saring, kertas saring ditimbang, kemudian dikeringkan dalam oven pada suhu 105°C selama 1 jam, lalu ditimbang hingga konstan.
Pengujian Kinerja AFBR
Aerobic Fixed-Bed Reactor (AFBR) terdiri dari bak sedimentasi dengan kapasitas 50 L dan bak aerasi kapasitas 50 L yang berisikan media biofilter batu apung yang telah melalui tahap pembibitan biofilm. Desain alat AFBR dapat dilihat pada Gambar 1.
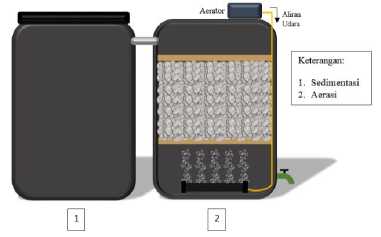
Gambar 1. Desain Alat AFBR
Pengolahan sampel limbah cair RPH pada Aerobic Fixed Bed Reactor (AFBR) dimulai dengan mengalirkan sampel ke bak sedimentasi dan didiamkan selama 24 jam. Hal tersebut bertujuan untuk mengendapkan padatan-padatan berat seperti sisa potongan daging ke dasar bak. Sampel air kemudian dialirkan ke bak aerasi yang berisikan biofilm pada media batu apung. Pengujian kinerja AFBR berdasarkan efisiensi biofilm dalam penurunan nilai karakteristik sampel limbah rumah potong hewan. Sampel air saat pengolahan diambil setiap 0; 12; 18; 24; 36; dan 42 jam. Setiap sampel tersebut dilakukan pengujian COD, BOD, TSS, serta amonia.
Klorinasi Hasil Pengolahan AFBR Penentuan Kadar Bahan Organik Total
Sampel air limbah RPH hasil pengolahan pada AFBR sebanyak 10 mL ditambahkan 90 mL akuades. Sampel lalu ditambahkan 2,5 mL H2SO4 8 N dan 10 mL KMnO4 0,01 N. Larutan dididihkan selama 10 menit, lalu.ditambah..10 mL.asam.oksalat
0,01 N..hingga.tidak.berwarna.
Larutan..kemudian..dititrasi..memakai…KMn O4 0,01 N hingga warna merah muda.
Pengujian Nilai Klor Aktif Dalam Larutan Kaporit dan Sampel
Kaporit...sebanyak…1 gram dilarutkan dengan 1 liter akuades, kemudian...diambil sebanyak..25...mL..dan..dimasukkan...ke..dala m Erlenmeyer. Larutan ditambahkan KI
sebanyak 1 gram dan 2,5 mL asam asetat glasial, lalu diteteskan larutan amilum hingga berwarna biru. Larutan dititrasi dengan Na2S2O3 0,0125 N hingg warna biru..hilang..Nilai klor aktif dihitung berdasarkan.jumlah Na2S2O3.yang dibutuhkan. Berdasarkan kadar BOT yang diperoleh, variasi dosis klor akan ditentukan Klorinasi dilakukan menggunakan variasi dosis larutan kaporit 145; 150; 155; 160; 165; 170; 175; dan 180 ppm. Nilai klor aktif sampel pada berbagai variasi dosis klor dilakukan dengan cara yang sama.
Uji Most Probable Number (MPN) Koliform
Sampel dibuat 3 kali pengenceran dalam gelas beker 100 mL. Pengenceran 1 (10-1), pengenceran 2 (10-2), dan pengenceran 3 (10-3). Sampel sebanyak 5 mL dari masing-masing pengenceran dan dimasukkan ke dalam tabung reaksi kemudian ditutup. Kemudian pada tabung reaksi yang baru dan steril, dimasukkan 1 mL sampel dan ditambahkan 2 mL media BGLB. Sampel dilakukan 3 kali percobaan untuk setiap pengenceran. Masing-masing tabung reaksi dimasukkan tabung durham dengan posisi mulut tabung di bawah, dan tabung reaksi ditutup. Tabung dibulak-balikan hingga tidak ada gelembung udara didalam tabung durham. Seluruh tabung reaksi diinkubasi dengan suhu 37°C selama 24 jam. Setelah itu, diamati pembentukan gelembung udara pada tabung durham. Dihitung nilai MPN/100 mL yang diperoleh.
HASIL DAN PEMBAHASAN
Sampel merupakan limbah cair yang diperoleh dari RPH di Kapal, Kecamatan Mengwi, Kabupaten Badung, Bali. Karakteristik awal sampel air dapat dilihat pada Tabel 1.
Tabel 1. Karakteristik Awal Air Limbah RPH
|
Parameter |
Nilai (ppm) |
Baku mutu (ppm)* |
|
COD |
191,76 |
100 |
|
BOD |
72,00 |
50 |
|
TSS |
502,00 |
200 |
|
Amonia |
13,26 |
5 |
Keterangan (*) = Pergub Bali No. 16 Tahun 2016
Berdasarkan Tabel 1., karakteristik limbah awal RPH menunjukkan nilai COD, BOD, TSS, dan Amonia melewati nilai batas baku mutu yang ditetapkan pada peraturan Gubernur Bali No. 16 Tahun 2016 tentang baku mutu lingkungan hidup dan kriteria baku kerusakan lingkungan hidup. Nilai karakteristik yang tinggi menandakan kualitas sampel air limbah ini tercemar.
Pembibitan Bioflm dalam AFBR
Pembentukan biofilm dilakukan pada bak aerasi berisikan biofilter batu apung, dengan variasi tanpa penambahan suspensi aktif (bak aerasi I) dan dengan suspensi aktif (bak aerasi II). Variasi pengukuran ini dilakukan untuk melihat pertumbuhan biomassa mikroba yang menandakan terjadinya pembentukan biofilm pada batu apung.
Parameter pengukuran dilakukan dengan memperhatikan nilai MLSS (Mixed Liquor Suspended Solid) dan waktu pertumbuhan mikroba hingga fase stasioner. Pengukuran MLSS bertujuan untuk mengetahui kuantitas padatan tersuspensi pada bak aerasi. Semakin tinggi nilai MLSS maka semakin banyak jumlah biomassa mikroba yang terdapat pada permukaan biofilter (Sari et al., 2013). Waktu optimal yang digunakan untuk pembibitan dapat dilihat dari nilai MLSS yang tertinggi (fase stasioner), karena pada nilai tersebut menunjukkan puncak pertumbuhan mikroorganisme tertinggi (Pradnyadari et al., 2018). Nilai MLSS yang diperoleh pada pembibitan biofilm disajikan pada Gambar 2.
Berdasarkan Gambar 2, terlihat bahwa seiring bertambahnya waktu pembibitan terjadi peningkatan nilai MLSS pada kedua bak aerasi..Penambahan nutrien sebagai makanan serta pemberian oksigen (aerasi) menunjang pertumbuhan biomassa mikroorganisme pada media biofilter (Dewi et al., 2019). Bak II yaitu bak dengan penambahan suspensi aktif, memiliki nilai MLSS yang lebih tinggi dari bak I, yang berarti pada bak II terjadi pertumbuhan biomassa yang lebih tinggi pula. Kondisi tersebut dapat disebabkan oleh banyaknya mikroorganisme yang berasal dari sedimen lumpur pada suspense aktif yang ditambahkan.
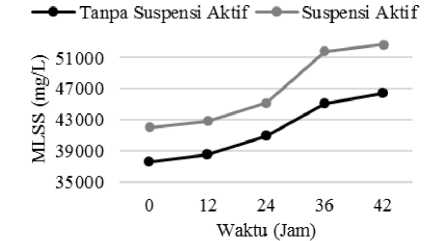
Gambar 2. Nilai MLSS pembibitan biofilm
Kandungan bahan organik pada air got tercemar yang digunakan menciptakan.suasana yang.baik untuk mikroba yang memerlukan bahan…organik tersebut untuk metabolismenya (Turista,.2017). Tingginya aktivitas dan jumlah mikroorganisme dalam mengurai bahan organik berkontribusi dengan tingginya biomassa yang dihasilkan (Dewi et al., 2019).
Nilai MLSS pada bak I dan II pada jam ke-0 menunjukkan 37.636 mg/L dan 42.032 mg/L yang kemudian terus meningkat hingga jam ke-36. Tahap ini menandakan pertumbuhan mikroba langsung dimulai yang disebut sebagai fase eksponensial. Pada fase ini, terjadi pembelahan sel dimana pada awalnya peningkatan jumlah sel lambat, tetapi kemudian pembelahan sel tersebut meningkat dengan cepat. Pada jam ke-36 sampai ke-42 ini, terjadi tahap yang disebut fase stasioner, setelah itu pembibitan dihentikan. Hal ini dikarenakan jumlah mikroba yang tinggi diinginkan untuk proses pengolahan air limbah tahap selanjutnya. Pada fase stasioner, nutrien yang dibutuhkan oleh bakteri telah berkurang dan jumlah sel yang membelah diimbangi oleh jumlah sel yang mati (Suyasa, 2015). Biofilm yang ditumbuhkan menggunakan suspensi aktif (bak II) menghasilkan MLSS tertinggi, sehingga biofilm ini digunakan untuk mengolah sampel limbah air RPH.
Kinerja AFBR dalam Pengolahan Limbah RPH
Karakteristik sampel pada berbagai variasi waktu disajikan pada Tabel 2, dan hasil kinerja pengolahan limbah cair RPH menggunakan AFBR berbahan batu apung pada Tabel 3.
Tabel 2. Karakteristik Sampel Air RPH pada Berbagai Variasi Waktu Pengolahan
|
Waktu (Jam) |
Parameter (mg/L) | |||
|
COD |
BOD |
TSS |
Amonia | |
|
0 |
174,08 |
67,33 |
388,00 |
10,52 |
|
12 |
155,04 |
66,67 |
292,00 |
8,36 |
|
18 |
144,16 |
60,67 |
236,00 |
5,72 |
|
24 |
121,04 |
48,67 |
144,00 |
5,20 |
|
36 |
81,60 |
24,67 |
72,00 |
3,58 |
|
42 |
92,48 |
25,33 |
54,00 |
1,55 |
|
Tabel 3. Kinerja AFBR terhadap Penurunan | ||||
|
COD, BOD,TSS, dan Amonia | ||||
|
Waktu |
Efisiensi Penurunan (%) | |||
|
(Jam) |
COD |
BOD |
TSS |
Amonia |
|
0 |
9,22 |
6,49 |
22,71 |
20,66 |
|
12 |
19,15 |
7,41 |
41,83 |
36,92 |
|
18 |
24,82 |
15,74 |
51,99 |
56,87 |
|
24 |
36,88 |
32,41 |
71,31 |
60,77 |
|
36 |
57,45 |
65,74 |
85,66 |
72,95 |
|
42 |
51,77 |
64,81 |
89,24 |
88,29 |
|
Efektivitas | ||||
|
Baku |
47,85 |
44,00 |
60,15 |
62,31 |
|
Mutu | ||||
Keterangan: Persentase efisiensi penurunan yang efektif terhadap baku mutu.
Efektivitas nilai baku diperoleh dari persentase perbandingan nilai parameter air limbah awal dengan nilai baku mutu tersebut. Kinerja AFBR dapat dikatakan efektif dalam mengolah limbah RPH, apabila efisiensi penurunan kadar sebuah parameter telah melampaui nilai efektivitas terhadap baku mutu parameter tersebut.
Tingginya jumlah oksigen yang dibutuhkan untuk mengoksidasi seluruh bahan kimia baik organik maupun anorganik dalam air menyebabkan tingginya nilai COD air (Saeni, 1989). Hasil pengolahan jam ke-36 merupakan hasil terbaik atau dengan penurunan kadar COD terbesar yaitu 110,16 mg/L dengan efisiensi 57,45%. Penurunan nilai tersebut disebabkan karena aktivitas mikroorganisme pada biofilm yang terjadi, seperti oksidasi untuk mendegradasi kandungan organik pada air limbah (Islamawati et al., 2018).
Hasil pengolahan BOD paling efisien pada waktu 36 jam yaitu sebesar 24,67 mg/L. Penurunan nilai tersebut dapat terjadi karena adanya proses degradasi dan penguraian bahan organik pada lapisan biofilm yang
melekat pada permukaan media batu apung, dibantu proses aerasi yang menyebabkan berkurangnya konsentrasi zat pencemar (Megasari et al, 2012).
Penurunan nilai TSS dapat terjadi dipengaruhi oleh proses sedimentasi yang telah dilakukan pada sampel air selama 24 jam. Pada proses sedimentasi tersebut, padatan tersuspensi yang berat terendapkan pada dasar bak sedimentasi. Nilai TSS terus menurun pada proses pengolahan dipengaruhi oleh filtrasi oleh media batu apung yang digunakan. Kandungan TSS limbah tersaring melalui celah media dan biofilm yang membungkus permukaan batu apung.
Menurut Said dan Muhammad (2014), pertumbuhan mikroorganisme pada lapisan biofilm yang sudah terbentuk akan terus berlangsung sehingga ketebalan lapisan biofilm bertambah. Pada kondisi ini, nutrien sebagai makanan dan oksigen tidak mampu mencapai permukaan padat biofilter yaitu batu apung. Hal ini menyebabkan lapisan biomassa akan terbagi menjadi dua, yaitu lapisan aerob dan lapisan anaerob. Pada zona aerobik terjadi proses nitrifikasi, dimana amonium akan dikonversi menjadi nitrat (NH4+ → NO3). Pada kondisi anaerobik akan terjadi proses denitrifikasi yakni nitrat diubah menjadi gas nitrogen (NO3 → N2). Sistem biofilm ini memudahkan proses penurunan kadar amonia tersebut.
Klorinasi
Sampel air limbah RPH akan dilanjutkan ke proses klorinasi setelah pengolahan menggunakan AFBR. Kombinasi sistem pengolahan air limbah ini bertujuan untuk memaksimalkan pengolahan, dimana klorinasi dimanfaatkan untuk menurunkan atau menghilangkan kadar bakteri koliform pada air limbah. Pengujian klorinasi kali ini menggunakan kalsium hipoklorit atau kaporit (Ca(OCl)2).
Kadar bahan organik total (BOT) sebelum klorinasi menjadi dasar penentuan dosis klor kaporit yang akan digunakan pada sampel pada proses klorinasi. Menurut Said (2007), bahan organik dapat meningkatkan kebutuhan klor karena keberadaannya menyebabkan penurunan efisiensi proses disinfeksi. Kadar BOT sampel limbah air RPH sebelum klorinasi adalah sebesar 166,7953 ppm. Dengan itu, ditentukan dosis
145 150 155 160 165 170 175 180
Dosis Klor Kaporit (ppm)
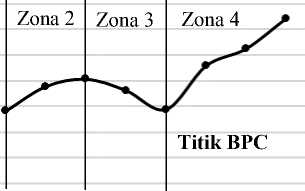
klor yang akan diaplikasikan pada sampel kali ini yaitu 145; 150; 155; 160; 165; 170; 175; dan 180 ppm. Kurva breakpoint chlorination (BPC) residu klor sampel dilihat pada Gambar 3.
70.00 ^ 60.00 ~ Ξ 50.00 § S 40.00 N - 30.00 1 20.00 £ 10.00 0.00
Gambar 3. Kurva BPC dosis klor kaporit
Pada Gambar 3, kurva terbagi menjadi 3 zona. Zona 1 merupakan zona terjadinya proses oksidasi senyawa yang mudah teroksidasi seperti logam, besi, dan mangan (Fe2+ dan Mn2+) menghasilkan nilai residu klor yang sangat kecil atau nol (Budiyono dan Sumardiono, 2013). Zona 2 merupakan zona klorin bereaksi dengan amoniak membentuk senyawa kloramin, dimana kloramin berkontribusi dalam proses disinfeksi. Pada zona 3, klorin mengoksidasi seluruh kontaminan termasuk kloramin. Hal ini menjelaskan penurunan nilai residu klor yang terkandung pada zona tersebut (Shovitri, 2011). Dosis klor 165 ppm merupakan titik BPC. Menurut Busyairi et al (2016) breakpoint ini dapat terjadi karena telah teroksidasinya zat organik maupun anorganik yang terkandung, sedangkan pembubuhan klor aktif terus berlangsung yang dapat dilihat dari nilai residu klor yang menurun pada 165 ppm. Pada BPC terjadi penurunan klor bebas, residu klor yang diperoleh sebesar 28,8031 ppm.
Klorinasi dilanjutkan ke tahap pengujian koliform dengan metode Most Probable Number (MPN). Pada perlakuan ini, koliform diuji pada sampel sebelum perlakuan klorinasi, dan 3 sampel setelah pelakuan klorinasi, yaitu sebelum breakpoint (155 ppm), breakpoint (165 ppm), dan sesudah breakpoint (175 ppm).
Sampel sebelum pengolahan dengan klorinasi mengandung 1.100 MPN/100 mL. Setelah pengolahan secara klorinasi dengan dosis klor 155; 165; dan 175 ppm, koliform sebesar 0 MPN/100mL dengan efisiensi
penurunan 100%. Hal ini menunjukkan klor pada kaporit (HOCl) efektif untuk mematikan bakteri koliform. Variasi dosis pada ketiga sampel tersebut menunjukkan hasil yang efisien dalam penghilangan bakteri koliform, namun dosis optimum nya adalah dosis breakpoint yaitu 165 ppm. Hal ini dikarenakan pada dosis tersebut residu klor yang dihasilkan paling sedikit diantara dosis sebelum breakpoint maupun sesudah. Residu klor yang terlalu tinggi dapat mencemari lingkungan lebih lanjut, namun konsentrasi residu klor pada titik breakpoint yang sedikit tersebut dianggap perlu untuk pembasmian kuman-kuman selanjutnya (Andhika, 2013).
SIMPULAN
Efisiensi waktu pengolahan pada Aerobic Fixed-Bed Reactor berbahan batu apung dengan penambahan suspensi aktif serta klorinasi dalam penurunan masing-masing parameter pada sampel air limbah rumah potong hewan adalah sebagai berikut: COD sebesar 57,45% selama 36 jam; BOD 65,74% selama 36 jam; TSS 89,24% selama 42 jam; amonia 88,29% selama 42 jam, bakteri koliform 100% dengan dosis klor 165 ppm pada waktu kontak 30 menit.
DAFTAR PUSTAKA
Andhika, J. D., Duta, Trijoko, Hanani, dan Yusniar. 2013. Kadar Sisa Chlor dan Kandungan Bakteri E. Coli Perusahaan Air Minum Tirta Moedal Semarang Sebelum dan Sesudah Pengolahan. Jurnal Kesehatan Masyarakat. 2(2): 19.
Budiyono dan Sumardiono, S. 2013. Teknik Pengolahan Air. Graha Ilmu:
Yogyakarta.
Busyairi, M., Dewi, P. D., dan Widodo, D. 2016. Efektivitas Kaporit pada Porses Klorinasi Terhadap Penurunan Bakteri Coliform dari Limbah Cair Rumah Sakit X Samarinda. Jurnal Manusia dan Lingkungan. 23(2): 156-162.
Dewi, W. T., Suyasa, W. B., Rai, N. 2019. Pengaruh Penambahan Lumpur Aktif pada Biofilter Anoksik-Oksik dalam Menurunkan Kadar Amonia Air Limbah Rumah Sakit. Ecotrophic.
13(2): 52-58.
Islamawati, D., Darundiati, Y.H., Dewanti, N. A. 2018. Studi Penurunan Kadar COD (Chemical Oxygen Demand)
Menggunakan Ferri Klorida (FeCl3) pada Limbah Cair Tapioka di Desa Ngempalk Margoyoso Pati. Jurnal Kesehatan Masyarakat. 6(6).
Megasari, R., Biyatmoko, D., Ilham, W., Hadie, J. 2012. Identifikasi Keragaman Jenis Bakteri pada Proses Pengolahan Limbah Cair Industri Minuman dengan lumpur Aktif Limbah Tahu, EnviroScienteae. 8(2): 89-101.
Peraturan Gubernur Bali Nomor 16 Tahun 2016. Baku Mutu Lingkungan Hidup dan Kriteria Baku Kerusakan Lingkungan Hidup bagi Usaha dan/atau Kegiatan Domestik.
Pradnyadari, I. G. A. L., Suyasa, I. W. B., dan Suastuti, N. G. A. M. D. 2018. Penyisihan Amonia Nitrit dan Nitrat dengan Biofilter Menggunakan Plastik Bekas sebagai Media Penopang Biofilm, Jurnal Media Sains. 2(2): 7682.
Saeni, M.S. 1989. Kimia Lingkungan. Bogor: IPB.
Said, N. I. 2007. Disinfeksi untuk Proses Pengolahan Air Minum. JAI. 3(1): 176179.
Said, N.I., Muhammad, R. 2014. Penghilangan Amoniak di dalam Air Limbah Domestik dengan Proses Moving Bed Biofilm Reactor (MBBR). JAI. 7(1): 46-52.
Sari, F.R., Raudhah, A., dan Abubakar, T. 2013. Perbandingan Limbah dan Lumpur Aktif Terdapat Pengearuh Sistem Aaerasi pada Pengolaham LIMBAH CPO. Konversi. Vol 2(1): 15.
Shovitri, M., Rosyidi, M.B., Nurhatika, S., dan Zulaika, E., 2011. Apakah
Breakpoint chlorination (BPC) selalu Aplikatif untuk Mengolah Limbah Cair Rumah Sakit. Jurnal Purifikasi. 12: 8392.
Suyasa, W.B., 2015. Pencemaran Air dan Pengolahan Air Limbah. Denpasar: Udayana University Press.
Turista, D. D. R. 2017. Biodegradasi Limbah Cair Organik Menggunakan
Konsorsium Bakteri. Stikes Utama Abdi Huseda Tulungagung. Jawa Timur.
181
Discussion and feedback