AKTIVITAS KOMBINASI EKSTRAK ETANOL KULIT MARKISA (Passiflora edulis Sims) DAN KULIT ALPUKAT (Persea americana Mill) TERHADAP KELARUTAN KALSIUM OKSALAT
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 15 (2), JULI 2021 DOI: https://doi.org/10.24843/JCHEM.2021.v15.i02.p01
p-ISSN 1907-9850
e-ISSN 2599-2740
AKTIVITAS KOMBINASI EKSTRAK ETANOL KULIT MARKISA (Passiflora edulis Sims) DAN KULIT ALPUKAT (Persea americana Mill) TERHADAP KELARUTAN KALSIUM OKSALAT
B. N. Widodo dan Tukiran*
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengentahuan Alam, Universitas Negeri Surabaya, Surabaya, Indonesia
*Email : tukiran@unesa.ac.id
ABSTRAK
Kulit markisa dan kulit alpukat mengandung senyawa bioaktif yang kompleks, termasuk kandungan kalium yang cukup tinggi di dalamnya. Senyawa flavonoid dapat berperan dalam peluruhan kalsium oksalat, membentuk senyawa kompleks yang mudah terlarut dalam air, serta kalium dapat memisahkan ikatan antara kalsium dengan oksalat. Penelitian ini memiliki tujuan untuk mengetahui keberadaan senyawa bioaktif dan daya larut dari kombinasi ekstrak kulit markisa dengan kulit alpukat terhadap kristal kalium oksalat. Simplisia kering kedua sampel diekstraksi menggunakan metode maserasi dengan perendaman dalam pelarut etanol 96%. Keberadaan senyawa bioaktif dalam ekstrak ditentukan dengan skrining fitokimia, kadar total flavonoid ditentukan menggunakan Spektrofotometri UV-Vis, sedangkan kadar kalium dan kalsium terlarut ditentukan menggunakan Spektrofotometri Serapan Atom (SSA). Penelitian dilakukan menggunakan metode Rancangan Acak Lengkap (RAL) dengan 7 perlakuan masing-masing 3 kali ulangan. Analisis data dilakukan dengan menggunakan analisis varian One way Anova, dilanjutkan dengan uji Duncan. Skrining fitokimia menunjukkan bahwa pada ekstrak etanol kulit markisa positif mengandung senyawa alkaloid, fenolik, flavonoid, saponin, tanin, steroid, dan triterpenoid, sedangkan ekstrak etanol kulit alpukat positif mengandung senyawa alkaloid, fenolik, flavonoid, saponin, tanin, steroid, dan triterpenoid. Kadar total flavonoid dalam ektrak kulit markisa dan kulit alpukat sebesar 3,2397 dan 3,0913 mg QE/gram sampel, sedangkan kadar kaliumnya sebesar 134,72 dan 47,56 mg/100 g sampel. Hasil analisis menunjukkan bahwa kombinasi ekstrak yang memiliki efek melarutkan paling besar adalah kombinasi ekstrak kulit markisa dan ekstrak kulit alpukat dengan perbandingan 3:1 mampu melarutkan 14,799 mg/L kalsium oksalat.
Kata kunci: flavonoid, kalium, kalsium oksalat, kulit alpukat, kulit markisa.
ABSTRACT
Passion fruit peel and avocado peel contain complex bioactive compounds, including a high potassium content in them. Flavonoid compounds can play a role in the breakdown of calcium oxalate, form complex compounds that are easily soluble in water, and potassium can separate the bonds between calcium and oxalate. This study aims to determine the presence of bioactive compounds and the solubility of the combination of passion fruit peel and avocado peel extract against potassium oxalate crystals. The dry simplicia of the two samples was extracted using the maceration method by immersing in 96% ethanol solvent. The presence of bioactive compounds in the extract was determined by phytochemical screening, the total of flavonoid contents were determined using UV-Vis Spectrophotometry, while the levels of potassium and dissolved calcium were determined using Atomic Absorption Spectrophotometry (AAS). The research was conducted using a Completely Randomized Design (CRD) method with 7 treatments each 3 replicates. Data analysis was performed using One way Anova, continued by Duncan's test. Phytochemical screening showed that the ethanol extract of passion fruit peel was positive for alkaloid, phenolic, flavonoid, saponin, tannin, steroid, and triterpenoid compounds, while the ethanol extract avocado peel was positive for alkaloid, phenolic, flavonoid, saponin, tannin, steroid, and triterpenoid compounds. The total flavonoid contents in the passion fruit peel and avocado peel extract were 3.2397 and 3.0913 mg QE/gram sample, while the potassium levels were 134.72 and 47.56 mg/100 g samples. The results of the analysis showed that the combination of extracts that had the greatest dissolving effect was the combination of passion fruit peel extract and avocado peel extract with a ratio of 3:1 which was able to dissolve 14.799 mg/L of calcium oxalate.
Keywords: avocado peel, calcium oxalate, flavonoids, passion fruit peel, potassium.
PENDAHULUAN
Indonesia merupakan negara dengan penderita gagal ginjal yang cukup besar. Menurut data dari Perhimpunan Nefrologi Indonesia (Permefri) sekitar 12,5% dari penduduk Indonesia mengalami penurunan fungsi ginjal dengan 150.000 orang karena hipertensi (Ali, Masi, & Kallo, 2017). Berdasarkan data WHO Country Health Profiles pada tahun 2012, penyakit ginjal sebagai penyebab kematian urutan ke-10 di Indonesia (World Health Organization, 2012). Penyebabnya sendiri paling besar diakibatkan oleh nefropati diabetik (52%), hipertensi (24%), kelainan glomerulopati primer (6%), asam urat (1), dan lainnya, serta 2% tidak diketahui penyebabnya. Penyakit ginjal ini 60% dialami oleh laki-laki (Moeloek, 2018).
Kalsium oksalat merupakan batu yang paling banyak dijumpai pada penderita batu ginjal dengan persentasenya 80%. Batu ginjal jenis lain yang juga ditemukan dalam penderita adalah batu kalsium fosfat, batu sistin, batu struvit, dan batu asam urat (Kurniasih, 2019). Pengobatan penderita batu ginjal biasanya ditujukan untuk memecah batu tersebut melalui pembedahan dan perawatan khusus. Penanganan termasuk penggunaan obat-obatan kimia, ESWL (Extracorporeal Shock Wave Lithotripsy) atau teknik benturan, operasi bedah, dan enduorologi. Selain sangat mahal, setiap metode pengobatan juga bisa memiliki kekurangan, seperti operasi dengan resiko infeksi yang tinggi atau kegagalan dengan terapi tambahan, serta penggunaan bahan obat-obatan kimiawi jangka panjang yang dapat merusak fungsi ginjal.
Beberapa alternatif jamu dan obat-obatan yang telah diteliti menggunakan beberapa jenis tanaman dapat melarutkan batu ginjal, di antaranya Kristianingsih dan Wiyono (2015) membuktikan bahwa ekstrak daun alpukat dan daun pandan wangi teruji mengandung flavonoid, keduanya dapat melarutkan kalsium batu ginjal secara in vitro. Winarti et al. (2014) menyatakan bahwa tingginya kadar kalium dalam ekstrak meniran dengan suasana yang asam memiliki kemampuan untuk melarutkan kalsium fosfat. Penelitian lain menunjukkan bahwa kombinasi ekstrak etanol dari daun sirsak dan tumbuhan pegagan secara in vitro juga dapat melarutkan kalsium pada batu ginjal (Swintari, Yuliet, & Khaerati, 2017). Menurut Cahyana (2015), ekstrak etanol daun tapak dara
dapat meluruhkan endapan kristal kalsium oksalat dan mencegah terjadinya agregasi kembali yang dilakukan secara in vitro.
Berdasarkan penelitian-penelitian tersebut, dapat ditemukan bahwa flavonoid berperan dalam peluruhan batu ginjal. Gugus hidroksil dapat bereaksi dengan kalsium pada batu ginjal membentuk khelat Ca-flavonoid yang mudah larut dalam air. Semakin banyak air yang terkandung dalam urin dapat membantu mempercepat larutnya batu ginjal (Winarti, Nuryanti, & Said, 2014). Selain itu, kalium juga merupakan mineral yang berperan pada proses terlarutnya kalsium dalam batu ginjal. Kalium akan bersaing dan memutus ikatan antara kalsium dan oksalat, sehingga kalium akan bergabung dengan oksalat membentuk garam yang mudah terlarut dalam air (Dewi, Walanda, & Sabang, 2016).
Buah markisa merupakan buah tropis dengan kandungan zat aktif yang tinggi pada bagian kulitnya, seperti flavonoid, alkaloid, pektin, dan polisakarida (Xiong, Li, Zheng, Hu, Cui, & Li, 2019). Kulit buah markisa segar mengandung kalium yang cukup tinggi, yaitu 178 mg/100 gram. Kulit buah markisa diidentifikasi memiliki total senyawa fenolik 4,67 mg GAE/g dan flavonoidnya sebesar 1,17 mg CE/g (Vuolo, Lima, & Junior, 2019). Selain buah markisa, buah alpukat juga dapat menjadi sumber kalium. Kandungan serat yang tinggi dapat mengatur keseimbangan kalium, serta kandungan antioksidan (Shalaby, Abu-Elsaad, & Ibrahim, 2020). Kulit alpukat terbukti mengandung senyawa metabolit sekunder seperti flavonoid, polifenol, tanin, saponin, alkaloid, dan antosianin (Harahap, 2019; Wahyuni, 2019).
Berdasarkan uraian di atas, peneliti berharap dapat mengetahui aktivitas ekstrak etanol kulit buah markisa yang dikombinasikan dengan kulit buah alpukat dalam melarutkan kalsium oksalat untuk mengetahui keefektifan kedua ekstrak tersebut.
MATERI DAN METODE
Bahan
Bahan-bahan dalam penelitian ini adalah kulit buah markisa, kulit buah alpukat, aquades, herbal Kejibeling, etanol 96%, (NH4)2C2O4, CaCl2, HCl pekat, serbuk Mg, NaCl 1%, gelatin 10%, FeCl3 1%, NH3, H2SO4 pekat, kloroform, asam asetat anhidrat, kuersetin, CH3COOK, AlCl3, HNO3 pekat.
Peralatan
Alat-alat dalam penelitian ini adalah ayakan mesh 40, toples, kertas saring, gelas kimia, gelas ukur, pipet tetes, plastik wrap, tabung reaksi, mortar alu, dan botol vial. Alat dan instrumen lain yang digunakan adalah neraca analitik, waterbath, kompor listrik, desikator, pompa vacuum, lemari pemanas, spektrofotometer UV-Vis, rotary evaporator, dan spektrofotometer serapan atom (SSA).
Cara Kerja
Persiapan Simplisia
Buah Markisa dan buah alpukat diperoleh dari desa Prambon, Tugu, Trenggalek. Buah yang didapatkan dicuci menggunakan air hingga bersih. Buah kemudian dipotong menjadi dua bagian lalu dikupas untuk memisahkan bagian kulitnya. Setelah itu, kulit dikeringkan dan dihaluskan hingga menjadi serbuk.
Pembuatan Ekstrak Etanol Kulit Buah Markisa dan Kulit Buah Alpukat
Ekstrak didapatkan dengan cara maserasi dingin menggunakan pelarut etanol 96%. Simplisia kering kulit markisa dan kulit alpukat masing-masing 500 gram direndam dengan pelarut dalam wadah tertutup rapat dalam waktu 24 jam. Hasil maserasi disaring dan didapatkan maserat dan diletakkan dalam wadah tertutup. Residu dilakukan maserasi kembali sebanyak 2 kali dengan pelarut etanol 96%. Maserat yang didapatkan kemudian dipekatkan menggunakan rotary evaporator hingga didapatkan ekstrak kental.
Skrining Fitokimia Ekstrak Etanol Kulit Buah Markisa dan Kulit Buah Alpukat
Skrining fitokimia pada ekstrak kulit markisa dan kulit alpukat dilakukan uji alkaloid, senyawa fenolik, flavonoid, saponin, tanin, steroid, dan triterpenoid.
Penentuan Kadar Total Flavonoid
Kurva standar kuersetin dibuat berdasarkan metode kolorimetri aluminium klorida (Chang, Yang, Wen, & Chern, 2002). Larutan kuersetin dibuat dengan konsentrasi 20, 40, 60, 80, dan 100 mg/L dalam pelarut etanol. Ekstrak sebanyak 1 mg dilarutkan dengan 1 ml etanol 96%. Selanjutnya, larutan dari berbagai konsentrasi (berlaku pada ekstrak) diambil 0,5 mL untuk ditambah 1,5 mL etanol 96% dan 0,1
mL AlCl3 10%. Sebanyak 0,1 mL kalium asetat (CH3COOK) 1M dan 2,8 mL aquades ditambahkan ke dalam larutan, kemudian diinkubasi selama 30 menit. Selanjutnya, absorbansi larutan standar dan sampel diukur menggunakan spektrofotometer UV-Vis dengan panjang gelombang 415 nm.
Persiapan Kristal Kalsium Oksalat
Kalsium oksalat yang akan digunakan sebagai kontrol diperoleh melalui reaksi pengendapan dengan mereaksikan (NH4)2C2O4 dengan CaCl2. Setelah endapan terbentuk, endapan dibebaskan dari H2SO4 menggunakan larutan ammonia. Kemudian endapan disaring dan dicuci dengan aquades. Endapan yang didapatkan kemudian dikeringkan pada suhu 60oC selama 4 jam (Kurniasih, 2019). Analisis kualitatif untuk membuktikan kristal kalsium oksalat yaitu dilakukan pemeriksaan kalsium yang diuji dengan HCl 10% dan (NH4)2C2O4 jenuh. Pemeriksaan oksalat diuji dengan HCl 10% dan padatan MnO2. Positif kalsium akan terbentuk endapan putih seperti kabut dan oksalat menunjukkan terbentuknya gas (Kristianingsih & Wiyono, 2015).
Pengujian Aktivitas Kelarutan Kalsium Oksalat
Pengujian kelarutan kalsium oksalat dilakukan secara in vitro, dilakukan dengan menyiapkan 7 tabung masing-masing berisi 10 mL aquades sebagai kontrol negatif (P0), obat herbal Kejibeling sebagai kontrol positif (P1), dan larutan kombinasi (MA). Masing-masing variasi ditambahkan 100 mg kristal kalsium oksalat, kemudian diinkubasi pada suhu 37ºC dengan waktu 5 jam dengan dilakukan pengocokan setiap 15 menit. Setelah diinkubasi sampel didiamkan hingga stabil, larutan disaring untuk memisahkan dengan endapannya (Cahyana, 2015). Selanjutnya, filtrat didestruksi menggunakan 8 mL HNO3 35% dan 2 mL H2O2 30% selama 45 menit. Sampel hasil destruksi masing-masing diambil 1 mL, kemudian dilakukan penambahan aquades hingga 10 mL. Larutan kemudian diukur absorbansi kadar kalsium terlarutnya pada panjang gelombang 422,7 nm menggunakan spektroskopi serapan atom (SSA). Larutan juga diukur kadar kalium dan kalsiumnya sebelum diberikan perlakuan (Susanti, Sukmawardani, & Musfiroh, 2016).
Analisis Data
Data yang didapatkan dari penelitian adalah konsentrasi kalsium terlarut setelah perlakuan. Data tersebut dilakukan analisis statistik menggunakan analisis varian One Way Anova dengan dilanjutkan uji Duncan guna menentukan perbedaan masing-masing kelompok uji.
HASIL DAN PEMBAHASAN
Hasil Ekstraksi
Simplisia kulit markisa dan kulit alpukat masing-masing sebanyak 500 gram diekstraksi menggunakan metode maserasi dingin dengan perendaman dalam pelarut etanol 96% dan dilakukan selama 3x24 jam. Etanol digunakan sebagai pelarut karena merupakan pelarut yang bersifat umum dan boleh digunakan untuk
Hasil Skrining Fitokimia
mengekstraksi dari tumbuhan herbal selain menggunakan air atau campuran etanol-air (BPOM, 2010). Maserasi menggunakan pelarut etanol 96% bertujuan untuk melarutkan senyawa aktif dalam simplisia, khususnya senyawa flavonoid. Flavonoid yang terdapat dalam tumbuhan biasanya ada dalam bentuk glikosida, sehingga dapat terlarut dalam pelarut etanol (Prayoga, Nocianitri, & Puspawati, 2019). Etanol dengan konsentrasi 96% lebih efektif digunakan karena kapang akan sulit tumbuh atau bahkan mati dalam etanol 20% atau lebih, selain itu etanol tidak beracun, netral, dan zat penganggu yang terlarut terbatas (Swintari, Yuliet, & Khaerati, 2017). Ekstrak kental yang dihasilkan dari sampel kulit markisa yaitu 74,618 gram dengan rendemen sebesar 14,3% dan kulit alpukat 90,166 gram dengan rendemen sebesar 17,4%.
Tabel 1. Hasil Uji Fitokimia Ekstrak Etanol Kulit Markisa dan Kulit Alpukat.
|
No. Identifikasi |
Hasil Reagen Kulit Kulit Pengamatan Markisa Alpukat |
|
Alkaloid a. Mayer . b. Wagner c. Dragendorff 2. Fenolik |
Mayer + + Endapan putih Wagner + + Endapan Jingga Dragendorff + + Endapan Cokelat NaCl 1% + + + Hijau kehitaman gelatin 10% |
|
HCl+Mg + + Cincin merah Aquades + + Busa FeCl3 1% + + Coklat/hijau kehitaman |
|
Terpenoid 6. a. Steroid b. Triterpenoid |
Liebermann- Burchard Ungu-hijau Kloroform + Warna merah H2SO4 antar permukaan |
Keterangan: Tanda “+” menunjukkan mengandung senyawa yang diuji, sedangkan tanda “-” menunjukkan tidak ada kandungan senyawa yang diuji
Skrining fitokimia dilakukan dengan tujuan untuk mengetahui keberadaan senyawa bioaktif yang terkandung dalam ekstrak etanol kulit buah markisa dan kulit buah alpukat. Analisis fitokimia yang dilakukan antara lain uji alkaloid, fenolik, flavonoid, saponin, tanin, dan terpenoid.
Data dari hasil skrining fitokimia yang diperoleh pada Tabel 1 menunjukkan bahwa ekstrak etanol kulit markisa dan ekstrak etanol kulit alpukat terbukti memiliki hasil uji yang sama, yaitu positif mengandung senyawa
bioaktif berupa alkaloid, senyawa fenolik, flavonoid, saponin, tanin, dan terpenoid. Hasil penelitian ini sesuai dengan hasil pengujian yang telah dilakukan oleh Wulandari et al. (2019) bahwa dalam ekstrak etanol kulit alpukat mengandung senyawa aktif alkaloid, senyawa fenolik, flavonoid, saponin, tanin, dan terpenoid, serta Jagessar (2017) dengan pelarut yang sama dapat melarutkan senyawa metabolit sekunder pada kulit buah markisa berupa alkaloid, senyawa fenolik, flavonoid, saponin, tannin, dan terpenoid. Kandungan suatu
senyawa dalam ekstrak tergantung pada sifat kepolaran senyawa dan pelarutnya. Kelarutan suatu senyawa dalam pelarut memiliki prinsip like dissolve like, yaitu senyawa polar akan dilarutkan oleh pelarut polar dan sebaliknya, senyawa non-polar akan dilarutkan oleh pelarut non-polar juga. Sifat etanol 96% yang semipolar dapat melarutkan beberapa senyawa metabolit sekunder dalam kulit markisa dan kulit alpukat.
Pembuatan Kristal Kalsium Oksalat
Sintesis kristal kalsium oksalat dilakukan dengan reaksi antara kalsium klorida dengan ammonium oksalat. Kemudian, larutan didiamkan selama semalam untuk memaksimalkan pembentukan kristal. Setelah kristal terbentuk, kristal digerus dan diayak untuk mendapatkan ukuran yang sama. Identifikasi kalsium oksalat bertujuan untuk memastikan bahwa kristal yang terbentuk merupakan endapan kalsium oksalat. Pemeriksaan kalsium dilakukan dengan melarutkan kristal ke dalam HCl 10% dan ditambah dengan ammonium oksalat jenuh. Terbentuknya endapan putih seperti awan menunjukkan adanya ion kalsium terlarut yang membentuk endapan kalsium oksalat kembali dengan oksalat jenuh. Pemeriksaan oksalat dilakukan dengan melarutkan kristal ke dalam HCl 10% dan ditambahkan dengan padatan MnO2. Timbulnya gelembung gas menunjukkan bahwa ion oksalat telah teroksidasi oleh MnO2 membentuk karbondioksida (CO2) (Kristianingsih & Wiyono, 2015).
Konsentrasi Ekstrak Efektif
Penelitian tentang efektifitas ekstrak kulit markisa dan kulit alpukat dalam melarutkan batu ginjal kalsium oksalat belum pernah diteliti sebelumnya, sehingga perlu diketahui konsentrasi masing-masing ekstrak yang paling efektif untuk selanjutnya dikombinasikan. Kedua ekstrak diuji keefektifannya pada konsentrasi 2%, 4%, 6%, 8%, dan 10% sebagai ekstrak tunggal. Aquades digunakan sebagai kontrol negatif dan obat herbal Kejibeling sebagai kontrol positif. Penggunaan aquades sebagai kontrol negatif ini bertujuan untuk memastikan bahwa kristal kalsium oksalat larut akibat perlakuan. Penggunaan obat herbal Kejibeling sebagai kontrol positif dikarenakan herbal ini merupakan ramuan tradisional yang
terbuat dari kombinasi ekstrak daun kejibeling, kumis kucing, dan daun meniran yang terbukti mampu melarutkan batu ginjal dan sudah banyak beredar di masyarakat. Konsentrasi kapsul herbal yang digunakan sesuai dengan aturan konsumsi yaitu 2 kapsul satu kali minum dengan konsentrasi 0,02%.
Semua kelompok diberikan perlakuan sesuai dengan prosedur yang ada. Perlakuan diberikan dengan menambahkan 100 mg serbuk kristal kalsium oksalat untuk menggantikan batu ginjal ke dalam 10 mL ekstrak. Penggunaan kristal kalisum oksalat sebagai pengganti batu ginjal dikarenakan kalsium oksalat merupakan batu yang paling sering ditemukan dari penderita batu ginjal dengan persentase sebesar 80% (Kurniasih, 2019). Selanjutnya, sampel diinkubasi pada suhu 37oC dengan waktu 5 jam dan dilakukan pengocokan setiap 15 menit. Perlakuan ini bertujuan untuk mendapatkan kondisi seperti halnya dalam tubuh. Pengocokan pada tahap ini dilakukan untuk mendapatkan kondisi yang sama seperti dalam ginjal dengan aliran urin, air, maupun gerakan akibat aktivitas tubuh (Winarti, Nuryanti, & Said, 2014).
Setelah itu, ekstrak disaring untuk memisahkan filtrat dan residu atau sisa kristal yang tidak terlarut. Filtrat hasil penyaringan kemudian didestruksi dengan HNO3 dan H2O2. Destruksi bertujuan untuk memecah ikatan pada senyawa organik antara unsur logam dengan unsur lainnya. Pemanasan pada proses destruksi bertujuan untuk mempercepat proses pemutusan ikatan organik pada larutan. Destruksi dapat dihentikan setelah larutan jernih yang menunjukkan semua konstituen senyawa organik telah terputus dan menyisakan logam (Swintari, Yuliet, & Khaerati, 2017). Setelah didestruksi, masing-masing sampel diambil 1 mL untuk diencerkan 10x. Pengenceran dilakukan untuk menurunkan konsentrasi dalam larutan sampel, sehingga tidak melebihi batas pengukuran yang dapat mengganggu keakuratan pengukuran. Selanjutnya sampel di analisis kadar kalsiumnya dengan Spektrofotometri Serapan Atom (SSA). Hasil pengukuran yang didapatkan merupakan absorbansi sampel setelah diencerkan, sehingga konsentrasi yang sebenarnya sebelum pengenceran dapat diketahui dengan mengkalikan konsentrasi terukur dengan faktor pengenceran.
Tabel 2. Kadar kalsium terlarut dalam ekstrak kulit alpukat dan ekstrak kulit markisa.
|
Perlakuan |
Rerata Ca Terlarut (mg/L) |
Perlakuan |
Rerata Ca Terlarut (mg/L) |
|
Aquades |
6,885 |
Kejibeling |
7,168 |
|
M 2% |
7,124 |
A 2% |
7,564 |
|
M 4% |
8,532 |
A 4% |
8,565 |
|
M 6% |
10,485 |
A 6% |
8,656 |
|
M 8% |
10,601 |
A 8% |
9,743 |
|
M 10% |
11,139 |
A 10% |
10,591 |
Keterangan: A= Ekstrak Kulit Alpukat, M= Ekstrak Kulit Markisa
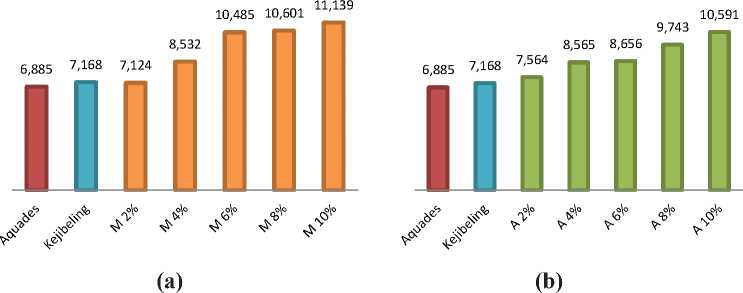
Gambar 1. Histogram kelarutan kalsium (mg/L) dalam ekstrak kulit markisa (a) dan ekstrak kulit alpukat (b).
Data hasil pembacaan kalsium terlarut menggunakan Spektrofotometri Serapan Atom (SSA) ditunjukkan pada Tabel 1 dan Gambar 1. Histogram ekstrak kulit markisa (Gambar 1a) menunjukkan konsentrasi 4%, 6%, 8%, dan 10% dapat melarutkan kristal kalsium oksalat lebih besar daripada kontrol positif Kejibeling 0,02% dan kontrol negatif. Ekstrak kulit markisa 10% memiliki potensi melarutkan kristal kalsium oksalat paling tinggi yang ditunjukkan dengan kadar kalsium terlarut 11,139 mg/L. Nilai tersebut menunjukkan nilai yang paling tinggi dibandingkan dengan konsentrasi yang lain dan kontrol positif. Pada histogram ekstrak kulit markisa menunjukkan bahwa semakin besar konsentrasi ekstrak yang digunakan maka semakin besar kadar kalsium terlarut.
Histogram ekstrak kulit alpukat (Gambar 1b) menunjukkan semua konsentrasi 2%, 4%, 6%, 8%, dan 10% dapat melarutkan kristal kalsium oksalat lebih besar daripada kontrol positif Kejibeling 0,02% dan kontrol negatif. Ekstrak kulit alpukat 10% memiliki potensi melarutkan kristal kalsium oksalat paling tinggi yang ditunjukkan dengan kadar kalsium terlarut 10,591 mg/L. Nilai tersebut menunjukkan nilai 126
yang paling tinggi daripada konsentrasi yang lain dan kontrol positif. Pada histogram ekstrak kulit alpukat menunjukkan bahwa semakin besar konsentrasi ekstrak yang digunakan maka semakin besar kadar kalsium terlarut.
Meningkatnya jumlah kalsium terlarut sebanding dengan penambahan konsentrasi ekstrak yang digunakan. Hal ini diduga akibat meningkatnya kandungan kalium, flavonoid, dan derajat keasaman (pH) ekstrak. Sesuai dengan pernyataan Winarti et al. (2014) bahwa meningkatnya konsentrasi ekstrak yang digunakan dalam perlakuan, maka kandungan flavonoid, kalium, dan derajat keasaman ekstrak akan meningkat, sehingga kemampuan ekstrak untuk melarutkan kalsium juga akan semakin tinggi.
Kombinasi Efektif
Kombinasi ekstrak yang digunakan ditentukan menggunakan metode Rancangan Acak Lengkap (RAL) dengan 7 perlakuan masing-masing 3 kali ulangan. Analisis kuantitatif kelarutan kalsium oksalat ditentukan dengan beberapa kelompok yaitu menggunakan aquades sebagai kontrol negatif, kapsul herbal Kejibeling sebagai kontrol positif, serta
kombinasi ekstrak kulit markisa dan ekstrak kulit alpukat. Kombinasi ekstrak kulit markisa (M) dan ekstrak kulit alpukat (A) tersebut adalah perlakuan 1 (P1) dengan perbandingan 0:4 atau ekstrak tunggal kulit alpukat, perlakuan 2 (P2) 1:3, perlakuan 3 (P3) 2:2, perlakuan 4 (P4) 3:1, dan perlakuan 5 (P5) 4:0 atau ekstrak tunggal kulit markisa. Data hasil pembacaan kalsium terlarut menggunakan Spektrofotometri Serapan Atom (SSA) dapat ditunjukkan pada Gambar 2. Histogram di atas
menunjukkan semua perlakuan kombinasi dapat melarutkan kristal kalsium oksalat lebih besar daripada kontrol positif Kejibeling 0,02% dan kontrol negatif. Perlakuan 4 memiliki potensi melarutkan kristal kalsium oksalat paling tinggi yang ditunjukkan dengan kadar kalsium terlarut 14,799 mg/L. Nilai tersebut menunjukkan nilai yang paling tinggi dibandingkan dengan konsentrasi yang lain dan kontrol positif.
Tabel 3. Kadar kalsium terlarut dalam kombinasi ekstrak kulit markisa (M) dan ekstrak kulit alpukat (A)
|
Perlakuan |
Rerata Ca Terlarut (mg/L) |
Notasi |
|
Aquades |
7,272 |
a |
|
Kejibeling |
7,341 |
b |
|
M:A (0:4) |
10,141 |
c |
|
M:A (1:3) |
12,750 |
d |
|
M:A (2:2) |
13,810 |
e |
|
M:A (3:1) |
14,799 |
f |
|
M:A (4:0) |
14,259 |
g |
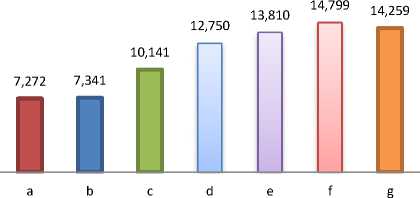
Gambar 2. Histogram kelarutan kalsium (mg/L) dalam ekstrak kombinasi.
Data yang didapatkan tersebut dianalisis statistik dengan One Way Anova dengan tingkat kepercayaan 95%, setelah itu dilanjutkan uji Duncan untuk menentukan perbedaan yang signifikan antar perlakuan. Berdasarkan analisis ragam (One Way Anova) diperoleh nilai p<0,05 yaitu dengan nilai 0,000, sehingga terlihat bahwa antar perlakuan terdapat perbedaan signifikan. Hal ini menunjukkan dengan adanya perlakuan berpengaruh terhadap besarnya jumlah kalsium terlarut. Setelah diketahui adanya perbedaan nyata antar kelompok, data dilanjutkan dengan uji Duncan.
Analisis statistik Duncan (berdasarkan data rerata kadar Ca terlarut dalam Tabel 3 dan
histogram di Gambar 2) menunjukkan bahwa terdapat perbedaan nyata antara a dengan b dan c. Kadar kalsium terlarut pada c masih lebih besar daripada a dan b. Nilai kadar kalsium terlarut oleh b lebih besar daripada a. Perbedaan nyata juga terjadi pada d dengan e, dimana kadar kalsium terlarutnya lebih besar daripada e. Demikian pula dengan g berbeda nyata dengan e, dengan kadar kalsium terlarut yang lebih besar. Sementara itu, f menunjukkan nilai yang berbeda nyata dengan perlakuan lainnya. Kadar kalsium terlarut pada perlakuan ini merupakan yang tertinggi.
Tabel 4. Data analisis kuantitatif pada ekstrak.
|
Parameter Ukur |
Ekstrak Kulit Markisa |
Ekstrak Kulit Alpukat |
|
Kadar Flavonoid |
3,2397 mg QE/g |
3,0913 mg QE/g |
|
Kadar Kalium |
134,72 mg/100g |
47,56 mg/100g |
|
Kadar Kalsium |
13,61 mg/100g |
15,69 mg/100g |
|
Derajat Keasaman (pH) |
4,2 |
5,3 |
Senyawa flavonoid dalam ekstrak berperan penting dalam proses kelarutan kalsium. Gugus fenolik dalam senyawa flavonoid maupun alkaloid dapat mengikat kalsium pada kristal yang menyebabkan terbentuknya senyawa khelat Ca-flavonoid. Senyawa ini merupakan kompleks yang mudah larut dalam air, sehingga kelarutan batu ginjal dapat berjalan cepat ketika semakin banyak air yang terkandung dalam urin. Senyawa fenolik tersebut akan mendonorkan hidrogen dan mengikat oksalat menjadi asam oksalat yang akan mudah larut (Winarti, Nuryanti, & Said, 2014). Data yang ditunjukkan pada Tabel 4 menunjukkan bahwa ekstrak tunggal kulit markisa memiliki kadar flavonoid yang lebih tinggi (134,72 mg/100 g ekstrak) daripada ekstrak tunggal kulit alpukat (3,0913 mg QE/g ekstrak), sehingga dapat mempengaruhi jumlah kalsium yang terlarut. Semakin besar konsentrasi ekstrak kulit markisa dalam larutan kombinasi akan meningkatkan jumlah kelarutan kalsium.
Selain itu, kalium juga merupakan mineral yang dapat mempengaruhi proses kelarutan kalsium oksalat. Kalium akan mendesak dan memisahkan ikatan kalsium dengan oksalat, sehingga kalium akan berikatan dengan oksalat dengan membentuk garam kalium oksalat yang mudah larut dalam air (Dewi, Walanda, & Sabang, 2016). Kalium adalah zat pereduksi yang kuat dengan nilai potensial reduksi standar kalium lebih rendah daripada nilai potensial reduksi standar kalsium, sehingga kalium akan mudah mendesak dan mereduksi kalsium. Nilai potensial reduksi standar kalium adalah -2,90 volt dan kalsium adalah -2,71 volt (Chang, 2003). Kalium terletak lebih ke kiri daripada kalsium dalam deret volta yang menyebabkan kalium lebih reaktif dan mudah melepaskan elektron. Hal inilah yang menyebabkan kalium dapat mendesak pemutusan ikatan kalsium dengan oksalat membentuk senyawa kalium oksalat (Permata, Angkat, & Wahyuni, 2017). Data yang ditunjukkan pada Tabel 4 menunjukkan bahwa kadar kalium dalam ekstrak tunggal kulit markisa lebih tinggi
(3,2397 mg QE/g ekstrak) daripada ekstrak tunggal kulit alpukat (47,56 mg/100 g ekstrak). Semakin besar konsentrasi yang digunakan menyebabkan semakin tinggi pula kadar kalium dalam ekstrak, sehingga akan meningkatnya jumlah kelarutan kalsium.
Sifat keasaman suatu larutan juga termasuk salah satu faktor yang dapat mempengaruhi kelarutan kristal kalsium oksalat. Kelarutan senyawa garam yang dibentuk oleh asam lemah dapat dipengaruhi oleh tingkat keasaman (pH) larutan. Contoh garam tersebut adalah garam oksalat, garam karbonat, dan garam fosfat. Ion hidrogen dari senyawa tersebut akan bergabung dengan anion dari garamnya membentuk asam lemah yang akan meningkatkan kelarutan (Day & Underwood, 1999). Ekstrak tunggal kulit markisa memiliki keasaman yang lebih kuat daripada ekstrak tunggal kulit alpukat, sehingga meningkatnya keasaman akan meningkatkan jumlah kalsium yang terlarut.
Perlakuan 1 (P1) merupakan ekstrak tunggal kulit alpukat memiliki kelarutan kalsium paling rendah dengan kadar kalsium terlarut sebesar 10,141 mg/L. Berdasarkan data pada Tabel 4, ekstrak kulit alpukat memiliki kadar flavonoid, kadar kalium, dan derajat keasaman yang lebih rendah daripada ekstrak tunggal markisa, hal ini dibuktikan dengan kadar kalsium terlarut oleh perlakuan 5 (P5) yang lebih besar daripada perlakuan 1 (P1). Jumlah kalsium terlarut dalam perlakuan 5 (P5) lebih kecil daripada perlakuan 4 (P4) diduga karena adanya senyawa lain akibat kombinasi antara ekstrak kulit markisa dan kulit alpukat yang menjadikan lebih efektif dalam melarutkan kalsium.
Berdasarkan penelitian yang telah dilakukan tersebut dapat disimpulkan bahwa kombinasi ekstrak etanol kulit markisa dan kulit alpukat memiliki aktivitas untuk melarutkan kristal kalsium oksalat, kombinasi ekstrak yang paling efektif dalam melarutkan adalah kelompok kombinasi IV dengan perbandingan ekstrak kulit markisa dan kulit alpukat 3:1.
SIMPULAN
Hasil penelitian ini dapat ditarik kesimpulan bahwa kombinasi ekstrak etanol kulit alpukat dan kulit markisa memiliki aktivitas untuk melarutkan kristal kalsium oksalat. Kombinasi ekstrak yang paling efektif dalam melarutkan adalah kelompok kombinasi IV dengan perbandingan ekstrak kulit markisa dan kulit alpukat 3:1, mampu melarutkan 14,799 mg/L kalsium.
DAFTAR PUSTAKA
Ali, A. R., Masi, G. N., & Kallo, V. 2017. Perbandingan Kualitas Hidup Pasien Gagal Ginjal Kronik Dengan Comorbid Faktor Diabetes Melitus Dan Hipertensi Di Ruangan Hemodialisa RSUP Prof Dr R.D Kandou Manado. E-Jurnal Keperawatan, 5(2).
BPOM. 2010. Acuan Sediaan Herbal (Vol. 5). Jakarta: Direktorat OAI BPOM RI.
Cahyana, R. D. 2015. Aktivitas Antikalkuli Ekstrak Etanol Tapak Dara (Catharanthus roseus) secara In Vitro dan In Vivo pada Tikus dengan Induksi Etilen Glikol. Skripsi. Institut Pertanian Bogor. Bogor.
Chang, C., Yang, M., Wen, H., & Chern, J. 2002. Estimation of Total Flavonoid Content in Propolis by Two Complementary Colorimetric Methods. Journal of Food and Drug Analysis, 10(3): 178-182.
Dewi, E. K., Walanda, D. K., & Sabang, S. M. 2016. Pengaruh Ekstrak Seledri (Apium graveolens L.) terhadap Kelarutan Kalsium dalam Batu Ginjal. Jurnal Akademika Kimia, 5(3): 127-132.
Harahap, R. (2019). Pengaruh Kecepatan Pengadukan Terhadap Ekstraksi Flavonoid dari Kulit Buah Alpukat (Persea Americana Mill.) dengan
Pelarut Etanol. Skripsi. Universitas Sumatera Utara, Sumatera Utara.
Jagessar, R. (2017). Phytochemical Screening and Chromatographic Profile of The Ethanolic and Aqueous Extract of Passiflora edulis and Vicia faba L. (Fabaceae). Journal of
Pharmacognosy and Phytochemistry, 6(6): 1714-1721.
Kristianingsih, I., & Wiyono, A. S. 2015.
Penggunaan Infusa Daun Alpukat (Persea americana Mill.) dan Ekstrak Daun Pandan (Pandanus
amarryllifolius Roxb) sebagai Peluruh Kalsium Batu Ginjal Secara In Vitro. Jurnal Wiyata, 2(1): 93-101.
Kurniasih, D. 2019. Uji Aktivitas Ekstrak Etanol Rimpang Nampu (Homalomena occulta) terhadap Kelarutan Kalsium Oksalat pada Batu Ginjal dengan Metode Titimetri. Skripsi. Universitas Muhammadiyah Malang, Malang.
Moeloek, N. F. 2018. Air Bagi Kesehatan: Upaya Peningkatan Promotif Preventif Bagi Kesehatan Ginjal di Indonesia. Hari Ginjal Sedunia (World Kidney Day) 2018 dan Ulang Tahun PERSI (pp. 1-34). Jakarta: Menteri Kesehatan Republik Indonesia.
Permata, Y. M., Angkat, L., & Wahyuni, H. S. 2017. Analisis Kadar Kalium dan Daya Larut Kalsium Oksalat Oleh Infusi Selada (Lactuca sativa L.) Secara. Jurnal Farmasi Galenika, 4(2): 38-44.
Prayoga, D., Nocianitri, K., & Puspawati, N. N. 2019. Identifikasi Senyawa Fitokimia dan Aktivitas Antioksidan Ekstrak Kasar Daun Pepe (Gymnema reticulatum Br.) pada Berbagai Jenis Pelarut. Jurnal Ilmu dan Teknologi Pangan, 8(2): 111-121.
Shalaby, M., Abu-Elsaad, N. M., & Ibrahim, T. M. 2020. An Insight Into The Effect Of Persea Americana As A Potassium Rich Diet On Adenine Induced Renal Fibrosis In Mice. Egyptian Journal of Basic and Applied Sciences, 7(1): 281291.
Susanti, N. N., Sukmawardani, Y., & Musfiroh, I. 2016. Analisis Kalium dan Kalsium pada Ikan Kembung dan Ikan Gabus. IJPST, 3(1): 26-30.
Swintari, N. W., Yuliet, & Khaerati, K. 2017. Aktivitas Kombinasi Ekstrak Etanol Daun Sirsak (Annona muricata L.) dan Daun Pegagan (Centella asiatica L. Urb) terhadap Kelarutan Kalsium Batu Ginjal secara In Vitro. Galenika Journal of Pharmacy, 3(1): 34-42.
Syamsul, M., & Zahrah, M. A. 2019. Boiling Increase Antioxidant Activity, Total Phenolic Content And Total Flavonoid Content In Plectranthus amboinicus
Leaves. GSC Biological and Pharmaceutical Sciences, 06(03): 2430.
Vuolo, M. M., Lima, G. C., & Junior, M. R. 2019. Passiflora edulis Peel Flour and Health Effects. Flour and Breads and their Fortification in Health and Disease Prevention, 249-258.
Wahyuni, N. 2019. Pengaruh Suhu Terhadap Ekstraksi Flavonoid dari Kulit Buah Alpukat (Persea Americana MILL.) dengan Pelarut Etanol. Skripsi. Universitas Sumatera Utara, Sumatera Utara.
Winarti, Nuryanti, S., & Said, I. 2014. Pengaruh Konsentrasi Ekstrak Tanaman Meniran (Phillanthus niruri L.) dalam Melarutkan Kalsium. Jurnal
Akademika Kimia, 3(4): 214-221.
World Health Organization. 2012. Indonesia: WHO statistical profile. Mortality and Global Health Estimates, 1-3.
Wulandari, G., Rahman, A. A., & Rubiyanti, R. 2019. Uji Aktivitas Antibakteri Ekstrak Etanol Kulit Buah Alpukat (Persea americana Mill) terhadap
Staphylococcus aureus ATCC 25923. Media Informasi, 15(1): 74-80.
Xiong, F., Li, X., Zheng, L., Hu, N., Cui, M., & Li, H. (2019). Characterization and antioxidant activities of
polysaccharides from Passiflora edulis Sims peel under different degradation methods. Carbohydrate Polymers, 218: 46-52.
130
Discussion and feedback