PENGARUH KONSENTRASI AMMONIUM SULFAT ((NH4)2SO4) OPTIMASI JAMUR JERAMI PADI ILS (ISOLAT LOKAL SINGARAJA) UNTUK BIODEGRADASI ZAT WARNA AZO JENIS REMAZOL RED
on
ISSN 1907-9850
PENGARUH KONSENTRASI AMMONIUM SULFAT ((NH4)2SO4) OPTIMASI JAMUR JERAMI PADI ILS (ISOLAT LOKAL SINGARAJA) UNTUK BIODEGRADASI ZAT WARNA AZO JENIS REMAZOL RED
I Nyoman Sukarta1 dan Putu Sumahandriyani2
-
1Jurusan Analis Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Pendidikan Ganesha
-
2Alumni Jurusan Analis Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Pendidikan Ganesha
Email. inyomansukarta@yahoo.co.id
ABSTRAK
Penelitian ini bertujuan untuk mengetahui konsentrasi, waktu kontak, serta pH optimum yang diperlukan oleh jamur jerami padi ILS (Isolat Lokal Singaraja) untuk mendegradasi zat warna azo jenis remazol red. Subjek dalam penelitian ini adalah jamur jerami padi ILS yang diperoleh dari sawah yang ada di Desa Temukus, Kecamatan Banjar, Kabupaten Buleleng. Sedangkan objeknya adalah konsentrasi, waktu kontak, dan pH optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna tekstil jenis remazol red. Tahap pengumpulan data dimulai dari uji pendahuluan biodegradasi zat warna, penumbuhan jamur pada media PDA (potato dextrosa agar) dan Czapex cair, uji kualitatif enzim lignolitik, dan uji biodegradasi zat warna pada variasi kondisi lingkungan. Konsentrasi zat warna remazol red sebelum dan sesudah didegradasi oleh jamur jerami padi ILS diukur menggunakan spektrofotometer Hach. Hasil penelitian menunjukkan bahwa degradasi zat warna azo jenis remazol red RB menggunakan jamur jerami padi ILS berlangsung optimum pada konsentrasi zat warna 30 ppm, lama waktu kontak 10 hari, dan pH 5 dengan efisiensi masing-masing sebesar 57,77; 71,13; dan 50,88%.
Kata kunci : jamur jerami padi ILS, biodegradasi, remazol red, dan enzim lignolitik
ABSTRACT
This study aims to determine the concentration, contact time, and the optimum pH required by the ILS rice straw mushrooms to degrade azo dyes remazol red type. Subject in this study is ILS rice straware mushroom which is obtained from existing fields in Temukus Village, Banjar District, Buleleng Regency. The objecs are the concentration, contact time, and the optimum pH required by the ILS rice straw mushroom to degrade textile dyes remazol red type. Stage of data collection starts from the preliminary test biodegradability of dyes, mold growing on PDA medium (potato dextrosa agar) and liquid Czapex, qualitative test of lignolitic enzyme, and dye biodegradation test on the variation of environmental conditions. The concentrations of remazol red dye before and after degraded by the ILS rice straw mushroom was measured by using a Hach spectrophotometer. The results showed that the degradation of azo dyes type remazol red RB using the ILS rice straw mushroom was optimum at color concentration of 30 ppm, contact time of 10 days, and pH 5 with the efficiency of each of 57,77; 71,13; and 50,88%.
Keywords : ILS rice straw mushroom, biodegradation, remazol red, and the lignolitic enzyme
PENDAHULUAN
Dewasa ini permasalahan limbah industri menjadi sesuatu yang hangat dibicarakan, salah satunya limbah cair pada industri tekstil. Industri tekstil menghasilkan air limbah sangat banyak dengan kandungan bahan organik yang ekstrim serta intensitas warna tinggi. Kondisi air limbah tersebut dapat menurunkan nilai estetika lingkungan, mengganggu ekosistem akuatik serta mempengaruhi kesehatan manusia (Sastrawidana et al., 2010).
Salah satu limbah industri yang menjadi kontributor utama penyebab pencemaran air adalah limbah zat warna yang dihasilkan dari proses pencelupan pada suatu industri tekstil, seperti zat warna azo. Zat warna azo disintesis untuk tidak mudah rusak oleh perlakuan kimia maupun perlakuan fotolitik. Untuk itu, bila dibuang ke perairan akan mengganggu estetika dan meracuni biota air di dalam badan air tersebut. Hal ini dikarenakan berkurangnya oksigen yang dihasilkan selama proses fotosintesis akibat terhalangnya sinar matahari untuk masuk ke dalam badan air yang disebabkan oleh keberadaan limbah zat warna. Selain itu perombakan zat warna azo secara aerobik pada dasar perairan menghasilkan senyawa amina aromatik yang kemungkinan lebih toksik dibandingkan dengan zat warna azo itu sendiri (Van der Zee, 2002).
Penggunaan jamur untuk pengolahan limbah tekstil sangat menarik untuk diketahui lebih lanjut. Salah satu jenis jamur yang berpotensi untuk digunakan dalam pengolahan limbah tekstil adalah jamur jerami. Jamur jerami yang memiliki enzim lignolitik dapat dimanfaatkan untuk pengolahan limbah tekstil, karena jamur mampu menggunakan bahan organik yang terdapat dalam limbah tekstil sebagai sumber energi. Selain itu jamur juga memiliki gugus fungsi seperi -OH (hidroksil), – NH2 (amino), -SH (sulfidril) dan yang lainnya yang dapat menyerap zat warna tekstil (Sastrawidana at al., 2009).
Pada penelitian ini digunakan jamur jerami padi. Jamur jerami padi merupakan salah satu jamur yang dapat menghasilkan enzim lignolitik ekstraseluler seperti laccase, mangan
peroksidase dan lignin peroksidase. Enzim lignolitik tersebut selain mampu mendegradasi senyawa aromatik polisiklik, senyawa fenolik juga sangat potensial digunakan untuk mendegradasi zat warna sintetik (Sastrawidana et al., 2010). Atas dasar inilah pemanfaatan jamur jerami padi berpotensi sebagai pendegradasi zat warna azo, yang pada penelitan ini menggunakan zat warna azo jenis remazol red RB yang termasuk ke dalam jenis zat warna reaktif, yang banyak digunakan dalam pencelupan tekstil.
Berdasarkan permasalahan di atas, penelitian ini ditujukan untuk mengetahui: 1) konsentrasi optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red; 2) waktu kontak optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red; dan 3) pH optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red.
MATERI DAN METODE
Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah media PDA (Potato Dextrosa Agar), media Czapex cair (dalam 1 liter media Czapex cair mengandung nutrien 3 g NaNO3; 0,5 g KCl; 0,5 g MgSO4.7H2O; 0,01 g FeSO4.7 H2O; 1 g KH2PO4; 1 g chloraamphenicol; dan 30 g sukrosa), jamur jerami padi ILS, zat warna azo jenis remazol red RB, aquades, serbuk gergaji pohon kelapa, aluminium foil, wrapping plastic, alkohol, indikator pH universal, kapas, NaOH, HCl, phenol red, MnSO4, H2O2, n-propanol, asam tartarat, buffer phosphate pH 4, 5, 6, 7, dan 8.
Peralatan
Alat-alat yang digunakan dalam penelitian ini adalah Spektrofotometer UV-Vis, Spektrofotometer Hach, sentrifuge, neraca, kaca arloji, corong, spatula, pipet tetes, batang pengaduk, gelas kimia 50 mL, cawan petri, inkubator, labu ukur 50 mL, water pump, Erlenmeyer 1000 mL, pH meter, oven, pipet volumetri, pipet ukur, hot plate, autoclave, botol.
Cara Kerja
Penumbuhan Jamur Jerami Padi ILS pada Media PDA
Jamur jerami padi ILS dihancurkan dan ditambahkan dengan air steril, kemudian cairannya ditransfer secara aseptik ke media PDA menggunakan cawan petri. Selanjutnya diinkubasi dalam inkubator dengan suhu 35°C selama 3 hari.
Kultivasi (Perbanyakan) Kultur Pada Media Cair
Jamur yang tumbuh pada media PDA ditransfer secara aseptik ke media Czapex cair menggunakan Erlenmeyer 250 mL. Selanjutnya campuran diatur pada pH 5 dan diaerasi selama 7 hari menggunakan water pump.
Uji Kualitatif Enzim Lignolitik
Enzim lignolitik yang dihasilkan oleh jamur jerami padi diuji secara kualitatif dengan cara sebagai berikut. Suspensi jamur disaring kemudian filtratnya disentrifuse pada 4000 rpm selama 30 menit. Selanjutnya supernatannya dibagi menjadi dua bagian untuk uji enzim mangan peroksidase (MnP) dan lignin peroksidase (LiP).
Uji Enzim Mangan Peroksidase
Sebanyak 0,6 mL supernatan ditambahkan 0,3 MnSO4 0,1 mM; 0,3 phenol red 0,1 mM; 0,3 mL buffer fosfat pH 5; dan 0,3 mL H2O2 50 mM. Terbentuknya warna orange
kecokelatan menunjukkan bahwa sampel positif mengandung enzim mangan peroksidase.
Uji Enzim Lignin Peroksidase
Sebanyak 0,6 mL supernatan ditambahkan 0,3 n-propanol 100 mM; 0,3 asam tartarat 250 mM; dan 0,3 mL H2O2 10 mM. Terbentuknya warna kuning menunjukkan bahwa sampel positif mengandung enzim lignin peroksidase.
Pembuatan Kurva Standarisasi
Metode pembuatan kurva standarisasi dilakukan dengan cara larutan standar zat warna remazol red RB dengan konsentrasi 10, 20, 30, 40, dan 50 ppm diukur absorbansinya dengan menggunakan Spektrofometer Hach pada
panjang gelombang 520 nm. Data absorbansi tersebut selanjutnya digunakan untuk membuat kurva standarisasi.
Uji Biodegradasi Zat Warna pada Variasi Kondisi Lingkungan
Sebanyak 22,5 mL media Czapex cair dimasukkan ke dalam botol steril yang telah berisi 1 g serbuk gergaji pohon kelapa dan ditambahkan 2,5 mL remazol red 100 ppm sehingga konsentrasi zat warna remazol red dalam 25 mL campuran adalah 10 ppm, campuran inilah yang digunakan sebagai kontrol. Kemudian untuk sampelnya dibuat perlakuan yang sama dengan kontrol, akan tetapi pada sampel ditambahkan sebanyak 3 mL suspensi jamur jerami padi ke dalamnya, selanjutnya ditutup dengan wrapping plastic dan aluminium foil kemudian diinkubasi selama 1 minggu. Setelah 1 minggu, sampel disaring kemudian disentrifuse pada 4000 rpm selama 30 menit dan diukur konsentrasi warna menggunakan Spektrofotometer Hach pada panjang gelombang 520 nm. Dengan cara yang sama dilakukan perombakan pada variasi konsentrasi 20, 30, 40, dan 50 ppm. Masing-masing perlakuan dibuat sebanyak 2 buah. Untuk variasi lama waktu kontak dan pH, dilakukan dengan cara yang sama seperti pada perlakukan konsentrasi. Pada variasi lama waktu kontak, konsentrasi yang digunakan adalah konsentrasi optimum yang didapat dari perlakukan konsentrasi yaitu 30 ppm, sedangkan pada variasi pH, konsentrasi dan waktu kontak yang digunakan adalah 30 ppm dan 10 hari yang didapat dari perlakuan konsentrasi dan lama waktu kontak.
Dari pengukuran konsentrasi zat warna azo dengan menggunakan Spektrofotometer Hach, akan diperoleh data absorbansi. Dari data absorbansi yang diperoleh dapat diketahui konsentrasi zat warna azo yang terdegradasi dalam sampel dengan menggunakan persamaan garis lurus yang sebelumnya didapat dari pengukuran absorbansi standar. Jika konsentrasi zat warna azo dari masing-masing sampel sudah diketahui, selanjutnya menentukan % efisensi perombakannya. Efisiensi perombakan zat warna remazol red ditentukan dengan cara membandingkan konsentrasi zat warna yang terombak terhadap konsentrasi zat warna kontrol
dan dikalikan 100%. Secara matematis persen efisiensi (% E) dapat dihitung dengan menggunakan rumus di bawah ini.
%E = Ca Cs x100% Ca
Dengan Ca merupakan konsentrasi awal atau kontrol dan Cs merupakan konsentrasi setimbang.
HASIL DAN PEMBAHASAN
Penumbuhan Jamur Jerami Padi ILS pada Media PDA dan Czapex Cair
Jamur jerami padi ILS ditumbuhkan dalam media potato dextrosa agar (PDA) dan diinkubasi selama 3 hari. Setelah tumbuh dalam media PDA, miselium jamur diremajakan kembali pada media Czapex cair kemudian diaerasi selama 7 hari. Hasil penumbuhannya dalam media PDA dan Czapex cair disajikan pada Gambar 1.
Jamur jerami padi ILS ditumbuhkan dalam media PDA dan diinkubasi selama 3 hari bertujuan untuk memperoleh miselium jamur.
Terbentuknya miselium jamur dapat dilihat dengan adanya benang-benang putih pada media PDA seperti ditunjukkan pada Gambar 1 (a). Hasil ini menyatakan bahwa jamur telah tumbuh dengan baik pada media PDA. PDA terbuat dari kentang, dekstrosa, dan agar. Kentang merupakan sumber karbohidrat yang mengandung vitamin dan mineral yang cukup tinggi. Fungsi kentang dalam penyusunan PDA adalah mensuplai karbohidrat yang diperlukan oleh jamur dalam pertumbuhannya. Dekstrosa umumnya menyediakan karbohidrat sebagai sumber energi yang berperan dalam pertumbuhan spora jamur, sedangkan agar berfungsi untuk mengentalkan media sehingga mempermudah dalam menumbuhkan jamur (Kusnadi et al., 2003). Setelah tumbuh dalam media PDA, miselium jamur diremajakan kembali pada media Czapex cair kemudian diaerasi selama 7 hari. Hal ini dilakukan guna memperoleh suspensi jamur yang akan digunakan pada proses perombakan remazol red RB. Adapun perubahan warna pada media Czapex cair dari tidak berwarna (Gambar 1 (b)) menjadi berwarna kuning (Gambar 1 (c)) mengindikasikan bahwa enzim lignolitik telah dihasilkan oleh jamur jerami padi ILS.

(a)

(b)

(c)
Gambar 1. Penumbuhan Jamur Jerami Padi ILS (a) pada Media PDA, (b) pada Media Czapex Cair dan (c) Suspensi Jamur pada Media Czapex Cair

(a)

(b)

(c)
Gambar 2. Uji Kualitatif Enzim Lignolitik (a) Suspensi Jamur Jerami Padi ILS, (b) Hasil Uji Enzim MnP, dan (c) Hasil Uji LiP
Uji Kualitas Enzim Lignolitik
Uji kualitatif enzim dilakukan untuk mengetahui adanya enzim lignolitik yang disekresikan oleh jamur jerami padi ILS. Hasil pengujian enzim lignolitik disajikan pada Gambar 2.
Berdasarkan Gambar 2 (b) dapat diketahui bahwa uji kualitatif enzim lignolitik menunjukkan hasil positif terhadap enzim MnP yang ditandai dengan terbentuknya warna orange kecokelatan setelah penambahan fenol red. Awalnya enzim MnP dioksidasi oleh H2O2 membentuk MnP yang teroksidasi (MnP (I)). MnP (I) akan mengoksidasi Mn2+ yang dihasilkan oleh enzim MnP sendiri membentuk Mn3+ yang merupakan oksidator kuat dan enzim MnP kembali ke bentuk semula. Selanjutnya Mn3+ akan mengoksidasi fenol red menghasilkan radikal fenoksil yang tidak stabil. Radikal fenoksil yang dihasilkan akan mengalami reaksi lebih lanjut dan akhirnya melepaskan CO2. Sedangkan Gambar 2 (c) menunjukkan hasil positif terhadap enzim LiP. Mula-mula enzim LiP dioksidasi oleh H2O2 membentuk LiP yang teroksidasi (LiP (I)). LiP (I) akan mengoksidasi n-propanol menjadi propanaldehid yang diindikasikan dengan terbentuknya warna kuning bening, kemudian LiP kembali ke bentuk
semula. LiP mampu mengoksidasi senyawa non-fenolik karena memiliki potensial oksidasi yang tinggi (Hofrichter, 2002). Enzim lignolitik, yaitu MnP dan LiP yang dihasilkan oleh jamur jerami padi ILS inilah yang akan berperan dalam proses degradasi zat warna remazol red RB.
Uji Biodegradasi Zat Warna pada Variasi Kondisi Lingkungan
Perombakan zat warna azo oleh jamur jerami padi ILS terjadi akibat adanya enzim lignolitik. Secara prinsip, perombakan zat warna oleh enzim lignolitik diawali dari oksidasi enzim lignolitik selanjutnya enzim lignolitik dalam keadaan teroksidasi tersebut mengoksidasi zat warna tekstil (Swamy and Ramsay, 1999). Aktivitas jamur itu sendiri dalam merombak zat warna tekstil dipengaruhi oleh faktor lingkungan (John, 2001). Adapun faktor lingkungan yang dikaji dalam penelitian ini adalah konsentrasi zat warna, lama waktu kontak, dan pH.
Biodegradasi pada Variasi Konsentrasi Zat Warna
Biodegradasi remazol red RB pada variasi konsentrasi dari 10-50 ppm dilakukan untuk mengetahui konsentrasi optimum yang bisa dirombak oleh jamur jerami padi ILS.
Konsentrasi optimum zat warna ditentukan dari nilai efisiensi perombakan yang paling besar. Perombakan zat warna berlangsung optimum pada konsentrasi 30 ppm dengan efisiensi sebesar 57,77%. Adapun hasil perhitungan konsentrasi masing-masing sampel pada variasi konsentrasi zat warna disajikan pada Tabel 1.
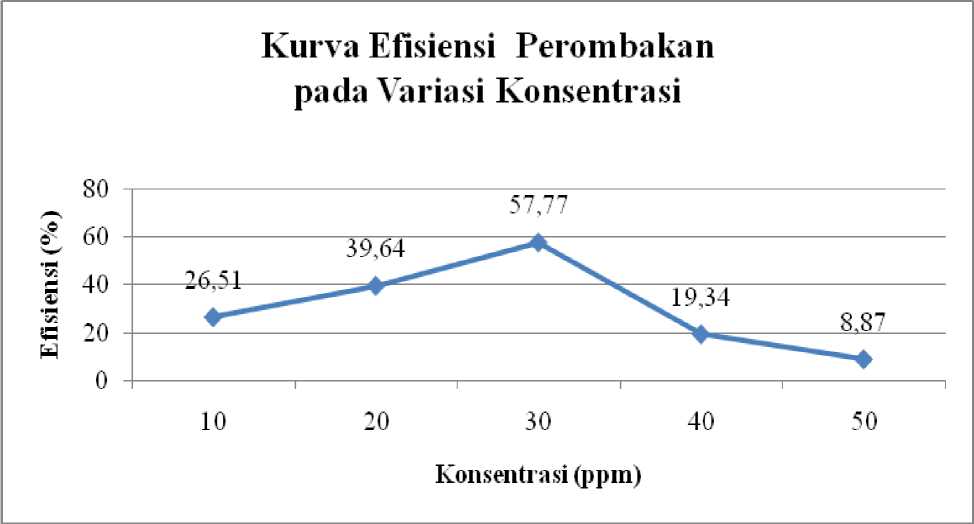
Menurut John (2001) efisiensi perombakan zat warna dipengaruhi oleh besarnya konsentrasi zat warna yang akan dirombak oleh jamur. Efisiensi perombakan pada variasi konsentrasi zat warna disajikan pada Gambar 3.
Table 1. Data Konsentrasi Zat Warna Azo Kontrol, Konsentrasi Zat Warna Azo Setimbang, dan % Efisiensi pada Variasi Konsentrasi
|
Variasi Konsentrasi (ppm) |
Konsentrasi Zat Warna Azo Kontrol (ppm) |
Konsentrasi Zat Warna Azo Setimbang (ppm) |
Konsentrasi Zat Warna Azo Terdegradasi (ppm) |
Efisiensi (%) |
|
10 |
8,7500 |
6,4306 |
2,3194 |
26,51 |
|
20 |
17,8333 |
10,7639 |
7,0694 |
39,64 |
|
30 |
24,8333 |
10,4861 |
14,3472 |
57,77 |
|
40 |
30,1667 |
24,3333 |
5,8334 |
19,34 |
|
50 |
35,8611 |
32,6806 |
3,1805 |
8,87 |
39,64
26.51
19,34
8187
Konsentnisi (ppm)
Kurvn Efisiensi Perombnkiin pιιdιι Variusi Konsentrnsi
Gambar 3. Kurva Efisiensi Perombakan Zat Warna Azo selang Waktu 7 Hari Inkubasi pada berbagai Variasi Konsentrasi
Berdasarkan Gambar 3. diperoleh pola efisiensi perombakan yang meningkat seiring dengan naiknya konsentrasi zat warna dari 10 sampai 30 ppm kemudian menurun pada konsentrasi 40 sampai 50 ppm. Perombakan zat warna remazol red RB yang diinkubasi selama 7 hari berlangsung optimum pada konsentrasi zat warna 30 ppm dengan efisiensi perombakan sebesar 57,77%. Perbedaan efisiensi perombakan pada berbagai konsentrasi zat warna disebabkan oleh beberapa faktor, antara lain laju reaksi enzimatik dan toksisitas zat warna (Pandey et al., 2007).
Toksisitas zat warna azo semakin meningkat seiring dengan meningkatnya konsentrasi (Pandey et al., 2007). Toksisitas zat warna yang tinggi menyebabkan efisiensi perombakan cenderung menurun. Efisiensi perombakan zat warna azo yang tidak toksik atau toksik rendah cenderung meningkat sampai pada konsentrasi tertentu dan selanjutnya menurun sejalan dengan meningkatnya toksisitas zat warna. Remazol red RB tergolong zat warna azo dengan toksisitas rendah, hal inilah yang menyebabkan efisiensi perombakan remazol red RB pada konsentrasi 10 sampai 30 cenderung meningkat kemudian menurun pada konsentrasi 40 sampai 50 ppm. Hasil penelitian ini sejalan dengan kajian Praveen et al. (2009), yang melaporkan bahwa perombakan zat warna azo orange II menggunakan Phanerochaete chrysosporium pada konsentrasi yang rendah yaitu 50 dan 100 ppm memiliki efisiensi masing-
masing sebesar 85,00 dan 88,50%, sedangkan pada konsentrasi 150, 200, dan 250 ppm memiliki efisiensi masing-masing 81,20; 70,00; dan 55,00%.
Biodegradasi pada Variasi Lama Waktu Kontak
Biodegradasi remazol red RB pada variasi lama waktu kontak dari 6-10 hari dilakukan untuk mengetahui waktu kontak yang diperlukan oleh jamur jerami padi ILS dalam merombak zat warna remazol red RB secara optimum. Waktu kontak optimum zat warna ditentukan dari nilai efisiensi perombakan yang paling besar. Perombakan zat warna berlangsung optimum pada waktu kontak 10 hari dengan efisiensi sebesar 71,13%. Adapun hasil perhitungan konsentrasi masing-masing sampel pada variasi lama waktu kontak disajikan pada Tabel 2.
Aktivitas jamur dalam merombak zat warna dipengaruhi oleh lama waktu kontak antara miselium jamur dengan zat warna tersebut (John, 2001). Adapun biodegradasi pada variasi lama waktu kontak dilakukan untuk mengetahui waktu kontak yang diperlukan oleh jamur jerami padi ILS dalam merombak zat warna remazol red RB secara optimum. Waktu kontak optimum zat warna ditentukan dari nilai efisiensi perombakan yang paling besar. Efisiensi perombakan pada variasi lama waktu kontak disajikan pada Gambar 4.
Table 2. Data Konsentrasi Zat Warna Azo Kontrol, Konsentrasi Zat Warna Azo Setimbang, dan % Efisiensi pada Variasi Lama Waktu Kontak
|
Variasi Lama Waktu Kontak (hari) |
Konsentrasi Zat Warna Azo Kontrol (ppm) |
Konsentrasi Zat Warna Azo Setimbang (ppm) |
Konsentrasi Zat Warna Azo Terdegradasi (ppm) |
Efisiensi (%) |
|
6 |
26,6111 |
21,0833 |
5,5278 |
20,77 |
|
7 |
22,1667 |
17,5139 |
4,6528 |
20,99 |
|
8 |
27,7222 |
19,9444 |
7,7778 |
28,06 |
|
9 |
27,0833 |
13,9861 |
13,0972 |
48,36 |
|
10 |
29,2500 |
8,4444 |
20,8056 |
71,13 |
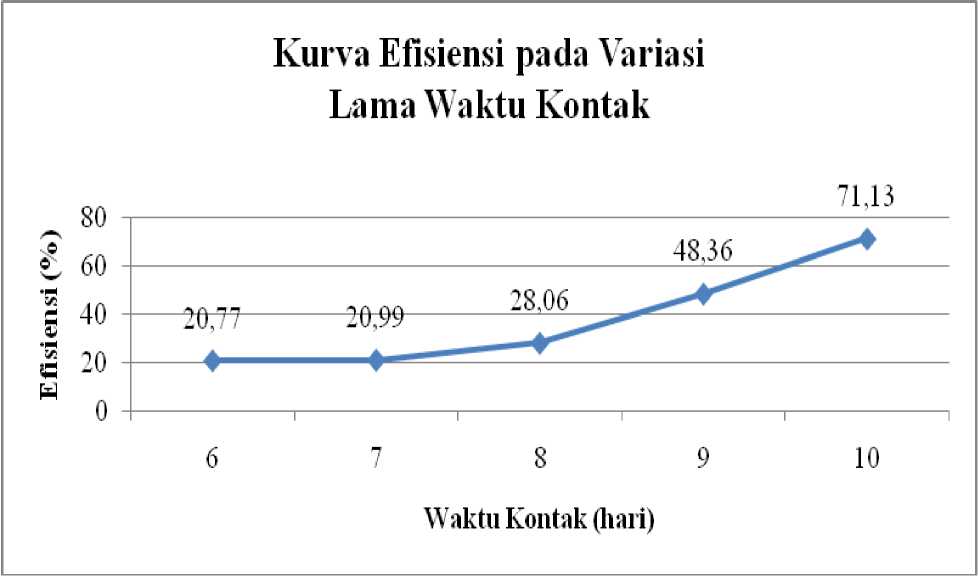
Gambar 4. Kurva Efisiensi Perombakan Zat Warna Azo 30 ppm pada berbagai Variasi Lama Waktu Kontak
Berdasarkan Gambar 4 dapat diketahui bahwa efisiensi perombakan zat warna remazol red RB meningkat seiring dengan lamanya waktu kontak yaitu dari hari ke-6 sampai hari ke-10. Pada tahap awal, yakni dari waktu kontak 6-7 hari, jamur melakukan fase adaptasi dengan lingkungan sehingga menghasilkan efisiensi perombakan yang relatif rendah (20,77-20,99%). Setelah beradaptasi, jamur mengalami fase pertumbuhan hingga waktu kontak 10 hari. Pada fase pertumbuhan inilah jamur mengsekresikan enzim lignolitik yang berperan dalam mendegradasi zat warna, sehingga efisiensinya terus meningkat hingga waktu kontak 10 hari. Meningkatnya efisiensi perombakan hingga waktu kontak 10 hari menunjukkan bahwa jamur belum mencapai waktu kontak optimum pada rentang waktu tersebut, sehingga sampai hari ke-10 jamur masih aktif dalam mendegradasi zat warna yang disebabkan oleh beberapa faktor, antara lain zat warna belum meracuni jamur dan
masih adanya zat makanan yang dapat dipakai nutrisi oleh jamur. Untuk mengetahui waktu kontak optimum, sesungguhnya masih perlu dilakukan penelitian dengan waktu kontak lebih dari 10 hari sampai diperoleh waktu kontak optimum.
Biodegradasi pada Variasi pH
Biodegradasi remazol red RB pada variasi pH dari 4-8 dilakukan untuk mengetahui pH optimum perombakan zat warna menggunakan jamur jerami padi ILS. pH optimum yang diperlukan oleh jamur jerami padi ILS dalam merombak zat warna remazol red RB ditentukan dari nilai efisiensi perombakan yang paling besar. Perombakan zat warna berlangsung optimum pada pH 5 dengan efisiensi sebesar 50,88%. Adapun hasil perhitungan konsentrasi masing-masing sampel pada variasi pH disajikan pada Tabel 3.
Table 3. Data Konsentrasi Zat Warna Azo Kontrol, Konsentrasi Zat Warna Azo Setimbang, dan % Efisiensi pada Variasi pH
|
Variasi pH |
Konsentrasi Zat Warna Azo Kontrol (ppm) |
Konsentrasi Zat Warna Azo Setimbang (ppm) |
Konsentrasi Zat Warna Azo Terdegradasi (ppm) |
Efisiensi (%) |
|
4 |
6,3889 |
4,7222 |
1,6667 |
26,09 |
|
5 |
18,9444 |
9,3056 |
9,6388 |
50,88 |
|
6 |
30,2778 |
20,6250 |
9,6528 |
31,88 |
|
7 |
29,8889 |
27,3611 |
2,5278 |
8,46 |
|
8 |
30,1389 |
28,6806 |
1,4583 |
4,84 |
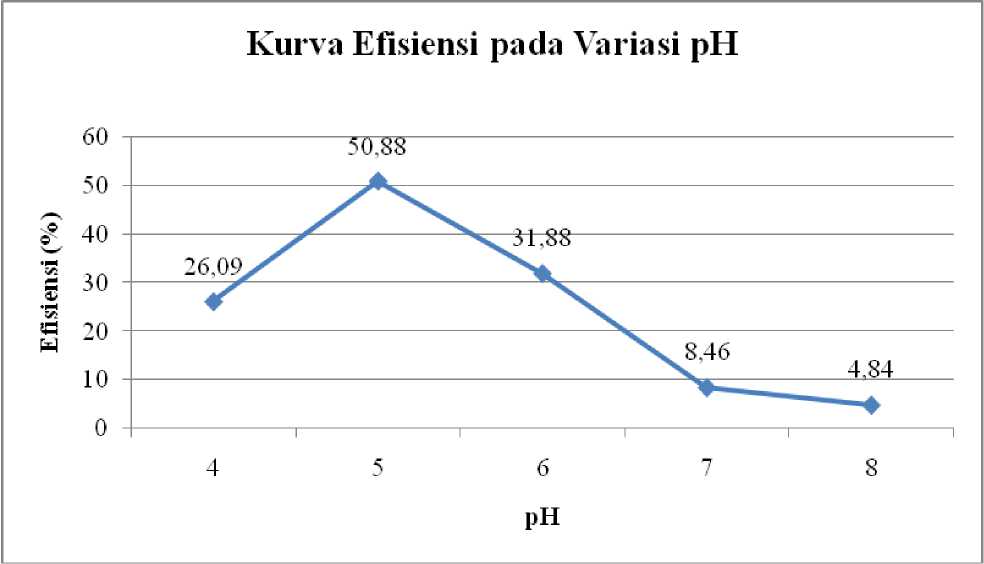
Gambar 5. Kurva Efisiensi Perombakan Zat Warna Azo 30 ppm dengan Lama Waktu Kontak 10 Hari pada Berbagai Variasi pH
Pada pH optimum jamur akan tumbuh dengan baik sehingga enzim yang dihasilkan semakin banyak. Dengan semakin banyaknya enzim yang dihasilkan, maka efisiensi perombakan zat warna semakin besar (Ali and Muhammad, 2008). Efisiensi perombakan pada variasi pH disajikan pada Gambar 5.
Gambar 5 menunjukkan bahwa efisiensi perombakan zat warna remazol red RB menggunakan jamur jerami ILS dipengaruhi oleh pH lingkungan. Efisiensi perombakan meningkat dengan naiknya pH lingkungan dari pH 4 sampai 5 dan menurun dari pH 6 sampai 8. Efisiensi perombakan zat warna remazol red RB 30 ppm yang diinkubasi selama 10 hari pada variasi pH
-
4, 5, 6, 7, dan 8 masing-masing sebesar 26,09; 50,88; 31,88; 8,46; dan 4,84%.
Perbedaan efisiensi perombakan zat warna pada variasi pH disebabkan oleh perubahan aktivitas pertumbuhan jamur. Beberapa jamur dapat tumbuh baik pada pH asam sampai netral, dimana pertumbuhan yang optimum akan dicapai pada pH 4 sampai 5 (Iswanto, 2009). Jika pH meningkat atau menurun melebihi kondisi pH optimum, maka aktivitas katalitik enzim akan menurun dan pada kondisi lingkungan yang tidak menguntungkan inilah pertumbuhan jamur akan terhambat bahkan mati.
Dari hasil penelitian diperoleh bahwa efisiensi paling besar terjadi pada pH 5. Hal ini menandakan bahwa enzim lignolitik yang berperan pada proses perombakan zat warna bekerja dengan baik pada pH 5. Hasil penelitian ini memperkuat simpulan Widiastuti et al. (2007), yang menyatakan bahwa enzim lignolitik baik laccase, LiP, dan MnP dari jamur Omphalina sp. dan Pleurotus ostreatus bekerja secara optimal pada pH 5. Temuan ini juga sejalan dengan kajian Zille (2005), yang menyatakan bahwa enzim lignolitik bekerja secara efektif dan stabil pada pH 5-6.
SIMPULAN DAN SARAN
Simpulan
-
1. Konsentrasi optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red adalah 30 ppm dengan nilai efisiensi sebesar 57,77%.
-
2. Waktu kontak optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red dalam penelitian ini adalah 10 hari dengan nilai efisiensi sebesar 71,13%.
-
3. pH optimum yang diperlukan oleh jamur jerami padi ILS untuk mendegradasi zat warna azo jenis remazol red adalah 5 dengan nilai efisiensi sebesar 50,88%.
Saran
-
1. bagi Peneliti yang tertarik melanjutkan penelitian ini diharapkan untuk lebih berhati-hati dalam melakukan penelitian
sejenis, karena diperlukan kondisi yang steril untuk meminimalisasi kontaminan.
-
2. Perlu dilakukan penelitian lebih lanjut tentang pemanfaatan jamur jerami padi ILS untuk biodegradasi zat warna azo jenis remazol red secara aerob agar dapat dibandingkan daya degradasi optimumnya.
UCAPAN TERIMA KASIH
Terima kasih penulis sampaikan kepada Dr. I Dewa Ketut Sastrawidana, M.Si. yang telah memberikan dorongan, semangat dan saran selama penulisan penelitian ini. Penulis juga mengucapkan terima kasih kepada semua pihak yang telah membantu sehingga tulisan ini dapat terselesaikan.
DAFTAR PUSTAKA
Ali, P. and S. K. Muhammad, 2008, Biodecolorization of Acid Violet 19 by Alternaria solani. African Journal of Biotechnology, 7 : 831-833
Hofrichter, M., 2002, Lignin Conversion by
Manganese Peroxidase (MnP). Enzyme Microbiol. Technol., 30 : 454-466
Iswanto, A. H., 2009, Identifikasi Jamur Perusak Kayu, Fakultas Pertanian Universitas Sumatera Utara, Medan
John, T. N., 2001, Biological Treatment of a Synthetic Dye Water and an Industrial Textile Wastewater Containing Azo Dye Compounds, Thesis_(tidak diterbitkan), Virginia Polytechnic Institute and State University, Blacksburg Virginia
Kusnadi, et al., 2003, Mikrobiologi, Jurusan Pendidikan Biologi UPI Bandung, Bandung
Pandey, A., P., Singh, L., and Iyengar, 2007, Bacterial Decolorization and
Degradation of Azo Dyes,. Int Biodet and Biodeg, 59 : 73-84
Praveen, S., Lakhvinder, S., and Neeraj, D., 2009, Biodegradation of Orange II Dye by Phanerochaete chrysosporium in Simulated Wastewater, Journal of
Scientific & Industrial Research, 68 : 157-161
Sastrawidana, I D. K., I Nyoman Selamat, dan I Nyoman Sukarta, 2009, Penggunaan Enzim Lignolitik dari Jamur Pendegradasi Kayu Teramobil pada Batu Vulkanik untuk Bioremidiasi Limbah Tekstil sebagai Upaya Pelestarian Lingkungan, Laporan Hibah Kompetitif Penelitian Sesuai Prioritas Nasional Batch II DIKTI, Lembaga Penelitian Universitas Pendidikan Ganesha, Singaraja
Sastrawidana, I D. K. dan I Nyoman Sukarta, 2010, Pengolahan Limbah Tekstil Menggunakan Biofilm Konsorsium Bakteri Isolat Lokal Bali pada Reaktor Anaerob-Aerob. Laporan Penelitian Hibah Bersaing DIKTI, Lembaga
Penelitian Universitas Pendidikan Gaesha, Singaraja
Swamy, J. and Ramsay, J. A., 1999, The Evaluation of White Rot Fungi in The Decoloration of Textile Dyes, New York, 24 : 53-62
Van der Zee, 2002, Anaerobic Azo Dye Reduction, Thesis, Wageningen
University, Netherlands
Widiastuti, H., Siswanto, dan Suharyanto, 2007, Optimasi Pertumbuhan dan Aktivitas Enzim Lignolitik Omphalina sp. dan Pleurotus ostreatus pada Fermentasi Padat, Menara Perkebunan, 75 : 93-105
Zille, A., 2005, Laccase Reaction for Textile ApplicationI, Disertasi, Textile
Departement Universidade do Minho
101
Discussion and feedback