SINTESIS SILIKA GEL DARI ABU SEKAM PADI DAN ABU LIMBAH PEMBAKARAN BATU-BATA DENGAN METODE PRESIPITASI
on
Sintesis Silika Gel Dari Abu Sekam Padi dan Abu Limbah Pembakaran Batu-bata Dengan Metode Presipitasi
(Isnawan Hadi, Made Arsa dan I Wayan Sudiarta)
SINTESIS SILIKA GEL DARI ABU SEKAM PADI DAN ABU LIMBAH PEMBAKARAN BATU-BATA DENGAN METODE PRESIPITASI
Isnawan Hadi, Made Arsa, dan I Wayan Sudiarta
Department of Chemistry, Universitas Udayana Jl. Kampus unud jimbaran Bali
Corresponding author, telp/e-mail : 081999905546, Wen.Science@yahoo.com
ABSTRAK
Telah dilakukan penelitian tentang sintesis silika gel dari abu sekam padi dengan metode Presipitasi. Penelitian diawali dengan penentuan suhu optimum pengabuan sekam padi, penentuan konsentrasi NaOH optimum dalam pembuatan Natrium Silikat dari abu sekam padi dan abu pembakaran batu-bata.Sintesis silika gel dilakukan melalui reaksi abu dengan larutan NaOH dan didihkan, sehingga terbentuk natrium silikat. Larutan ini dinetralkan dengan asam sulfat sehingga diperoleh silika gel. Setelah melalui pencucian dan pengeringan silika gel dianalisis dengan spektrofotometer IR dan Difraktometer sinar-X.
Hasil penelitian menujukkan suhu pengabuan sekam padi paling optimum adalah 700 o C, konsentrasi NaOH paling optimum dalam reaksi dengan abu adalah 3M. Berdasarkan karakterisasi dengan IR silika gel telah berhasil dibuat ditandai dengan munculnya serapan gugus fungsi –OH dan silianol pada panjang gelombang 3456,44 – 3487,30 cm-1 dan Si-O-Si atau siloksan pada panjang gelombang 1103,28 – 1087,85 cm-1 dan analisis X-RD menunjukan bahwa silika gel yang terbentuk berbentuk amorf..
Kata kunci : abu sekam padi, abu limbah pembakaran batu-bata, presipitasi, silika gel
ABSTRACT
Studies on synthesis of silica gel from rice hull and waste ofcombustion ash with prepitatian method have been. The studies was with the determination of the optimum temperature incineration of rice husk, the determination of the optimum concentration of NaOH in the manufacture of Sodium Silicate solution from rice hush and brick ash. Synthetic silica gel was obtained by boiling the ash with NaOH solution to create sodium silicate. This solution was neutralized with sulfuric acid and silica gel was produced. After washing and drying the silica gel was analyzed by spectrophotometer IR and X-ray Diffractometer.
The result showed that the optimum incineration temperature of rice husk was 700oC, the optimum concentration of NaOH was 3M. Based on the characterization by IR, silica gel has been successfully created, marked by the absorption indicating and silianol of functional groups –OH at 3456,44-3487,30 cm-1and Si-O-Si or siloxane at 1103,28-1087,85 cm-1and X-RD analysis showed that silica gel formed was amorphous form.
Keywords : Rice husk ash, Waste incineration ash bricks,precipitation, silica gel
PENDAHULUAN
Siliks gel sebagai adsorben telah dikenal luas dalam dunia kimia, karena struktur polimernya yang amorf (tidak tertata), gabungan dari agregat-agregat Si-OH yang membentuk
polimer terarah Si-O-Si, menjadikan senyawa adsorben ini memiliki kestabilan yang cukup baik. Pemanasan tidak mengubah struktur silika gel, bahkan ketika silika gel telah diras jenuh, pemanasan sering dilakukan untuk mengeluarkan atau memutus ikatan H2O dari surface silika
gel.Silika gel banyak diproduksi oleh vendor terkenal selevel merck, Fluca dan sebagainya untuk penelitian. Standar kiesel 60 dan G60 banyak menjadi pilihan alternatif pengambilan silika gel untuk penelitian. Berbeda dengan silika gel konvensional bewarna biru, silika gel kiesel 60 bewarna putih, serbuk halus, dan ringan.Untuk mengetahui karakterisasi silika gel, sering dipergunakan IR Spektroskopy dalam pengenalan gugus fungsinya (Bachrie, 2000).
Silika gel tergolong sebagai silika amorphous yang terdiri dari partikel-partikel dalam bentuk polimer (SiO2)n. Atom Si pada silika gel berikatan kovalen terhadap empat atom O dalam susunan tetrahedral. Setiap atom O tersebut berikatan kovalen dengan atom Si yang lain membentuk gugus fungsional siloksan (-Si-O-Si-) dan silanol (-Si-OH). Pada umumnya panjang ikatan Si-O ± 0,16 nm dan sudut ikatan Si-O-Si sekitar 1480 (Brinker dan Scherer, 1990).
Susunan tetrahedral partikel (SiO2)n pada silika gel berbentuk tidak teratur dan dapat membentuk kerangka tiga dimensi yang lebih besar. Sifat keasaman silika gel sebagai asam bronsted sebanding denga keasaman asam asetat (Ka = 1,75. 10-5) sehingga silika gel juga dapat berperan sebagai basa bronsted yang relatif kuat dengan adanya gugus aktif hidroksil. Pada silika gel terdapat dua jenis gugus aktif hidroksil (-OH) (Sriver,1990:357), yaitu:
-
1. Gugus –OH bebas, jarak antara –OH dengan – OH lainnya 0,50-0,52 nm
-
2. Gugus –OH terikat, dengan jarak –OH dengan –OH yang lain antara 0,25-0,26 nm dan dapat berinteraksi melalui ikatan hidrogen.
Silika gel umumnya disintesis dengan cara presipitasi larutan silikat dan sol silikat. Pada tahun 1998, Ishizaki melakukan sintesis silika gel dari alkoksida tetrametoksisilan (TEOS) yang dikatalisis dengan HCl dengan konsentrasi tinggi pada pelarut alkoholik yang mengandung sedikit air. Dari sintesis tersebut, semakin tinggi konsentrasi HCl yang digunakan saat kondensasi maka akan diperoleh silika gel dengan luas permukaan lebih besar (Ishizaki, 1998:74).
Pori-pori silika gel tergantung pada kondisi preparasinya pada rata-rata berdiameter 7.103-1,8.103 Å sedangkan luas permukaan silika gel antara 450-530 m2/g, dan densitasnya sekitar
0,67-0,75 g/cm2. Luas permukaan silika gel biasanya akan bertambah dengan kenaikan ukuran pori-pori silika gel. Adanya gugus aktif dan sifat-sifat fisik silika gel tersebut maka silika gel secara umum sering digunakan sebagai adsorben, desikan dan pengisi pada kromatografi (sebagai fase diam) (Ishizaki, 1998). Silika gel murni dengan adanya gugus silanol dan siloksan telah dilaporkan dapat mengabsorbsi ion logam keras seperti Na+, Mg2+, Ca2+, dan Fe2+ (Cestari, 2000).
Kelarutan silika gel dalam air pada suhu 250C adalah 20-150 ppm SiO2 (1,2-2,2 mmol/kg). Variasi kelarutan silika gel disebabkan adanya perbedaan ukuran partikel, derajat hidrasi dan kemurnian. Silika gel dalam air larut atau terpolimerisasi dengan persamaan reaksi (Harsono, 2002):
SiO2 (s) + 2H2O (l) -----------► H4SiO4 (aq)
MATERI DAN METODE
Bahan
Sekam padi limbah industri penggilingan padi yang diperoleh dari kabupaten Tabanan Bali, Abu sekam padi limbah industri batu-bata yang diperoleh dari desa keramasan kabupaten Gianyar Bali, Bahan-bahan kimia meliputi : NaOH, H2SO4 , Akuadest, Kertas saring, Plastik klip.
Peralatan
Peralatan yang digunakan pada penelitian ini adalah: Timbangan analitik, kertas saring, bola hisap, pengaduk magnet, buret, desikator, seperangkat alat gelas (meliputi: pipet tetes, pipet volum labu ukur, elenmeyer, gelas beker, tabung reaksi, botol sampel),alat pengerus (mortar dan lumping), corong, cawan porselin, cawan petri, kaca arloji, oven, ayakan 200 mesh, tungku pemanas, pemusing (sentrifuse), pH meter, difraktometer sinar X, spektrofotometer inframerah.
Cara Kerja
Penyiapan sekam padi dan abu limbah serta pengabuan
Sekam padi dan abu sekam padi yang masing-masing diambil dari kabupaten Tabanan
dan desa keramasan kabupaten Gianyar dibersihkan dari batu tanah dan kotoran lainya.Sekam padi dan abu yang sudah bersih dicuci dengan air hingga bersih, kemudian dikeringkan di bawah sinar matahari sampai kering. Selanjutnya sekam padi yang sudah bersih dan kering ditimbang sebanyak 15 gram, selanjutnya di dibakar menggunakan nyala api dengan bantuan bahan bakar spritus sehingga diperoleh arang sekam padiyang bewarna hitam, arang kemudian diabukan dengan variasi suhu yaitu 500, 600, 700, 800, dan 9000C selama 4 jam dalam tungku pemanas(tanur). Setelah pengabuan selesai abu didinginkan, lalu digerus dengan cawan porselin sampai halus dan diayak dengan ayakan 200 mesh, kemudian disimpan dalam desikator. Masing-masing perlakuan dilakukan ulangan sebanyak 3 kali. Abu sekam padi dan abu limbah industri batu-bata yang diperoleh dikarakterisasi dengan difraktometer sinar-X untuk mengetahui tingkat kristalnya (Enymia, 1998).
Sintesis silika gel
Sebanyak 6 gram abu sekam padidari pengabuan 5000C dicampur dengan masing-masing 25 ml larutan NaOH 0,5, 1,0, 2,0, 3,0, dan 4,0 M dalam Erlenmeyer bertutup 250 ml. Masing-masing campuran didihkan sambil diaduk dengan pengaduk magnet(magnetik stirer) pada kecepatan konstan selama 1 jam. Setelah itu disaring dengan kertas saring whatman 42 dan residu dicuci dengan 25 ml air mendidih. Filtrat yang merupakan natrium silikat didinginkan sampai suhu kamar kemudian dititrasi dengan larutan asam sulfat 2 M sampai pH 7. Gel mulai terbentuk dan didiamkan selama 18 jam. Gel yang terbentuk dihancurkan kemudian disentrifugasi dengan kecepatan 2500 rpm. Supernatan yang jernih dibuang kemudian gel dicuci dengan akuadest lalu disentrifugasi lagi dan supernatan yang jernih dibuang lagi. Pencucian ini dilakukan sebanyak 3 kali. Gel kemudian dikeringkan pada 1000C dalam oven selama 12 jam. Silika gel yang diperoleh kemudian digerus dan diayak dengan ayakan 200 mesh. Serbuk silika gel disimpan dalam desikator (Khamat dan Proctor, 1998). Hal yang sama dikerjakan untuk abu sekam padi dari suhu
pengabuan 600,700, 800, 9000C, dan juga untuk abu limbah industri batu bata. Rendemen yang diperoleh dihitung dengan membandingkan berat silika gel yang diperoleh dengan berat abu yang digunakan. Pengulangan percobaan dilakukan sebanyak 3 kali. Silika gel dari hasil sintesis ini dikarakterisasi dengan difraksi sinar –X, dan spektroskopi IR.
HASIL DAN PEMBAHASAN
Penentuan Suhu terbaik pengabuan sekam padi
Variasi suhu dilakukan untuk menentukan suhu terbaik dari pengabuan sekam padi. Penentuan suhu terbaik pengabuan sekam padi dilakukan dengan cara mengabukan sekam padi pada berbagai suhu yaitu 500, 600, 700, 800, dan 900oC. Suhu pengabuan terbaik diketahui dengan cara membuat kurva antara suhu pengabuan sekam dan kadar abu yang dihasilkan. Hasil penelitian pengaruh suhu pengabuan terhadap kadar abu disajikan dalam Gambar 1.
Berdasarkan Gambar 1 dapat dilihat bahwa kadar abu sekam padi dipengaruhi oleh suhu pengabuan. Pada suhu pengabuan 500-700oC kadar abu yang dihasilkan menurun, sedangkan pada suhu 700-900oC kadar abu yang dihasilkan konstan yaitu 21,00%. Dalam hal ini suhu pengabuan terbaik yang digunakan adalah 700oC karena kadar abu yang dihasilkan mulai konstan dengan abu berwarna putih. Pada pengabuan 500 dan 600oC bukan merupakan suhu pengabuan terbaik karena walaupun kadar abunya lebih besar dari kadar abu pengabuan 700oC tetapi masih mengandung pengotor berupa karbon yang berwarna hitam, yang berarti pengabuannya belum sempurna. Pada pengabuan 800 dan 900oC kadar abu yang dihasilkan sama dengan pengabuan pada suhu 700oC tetapi memerlukan energi listrik dan waktu yang lebih banyak.Suhu pengabuan terbaik ini sesuai dengan yang dilaporkan oleh peneliti sebelumnya dimana pengabuan pada 700oC kadar abu yang diperoleh 16-25% dengan abu berwarna putih (Nuryono, 2004)
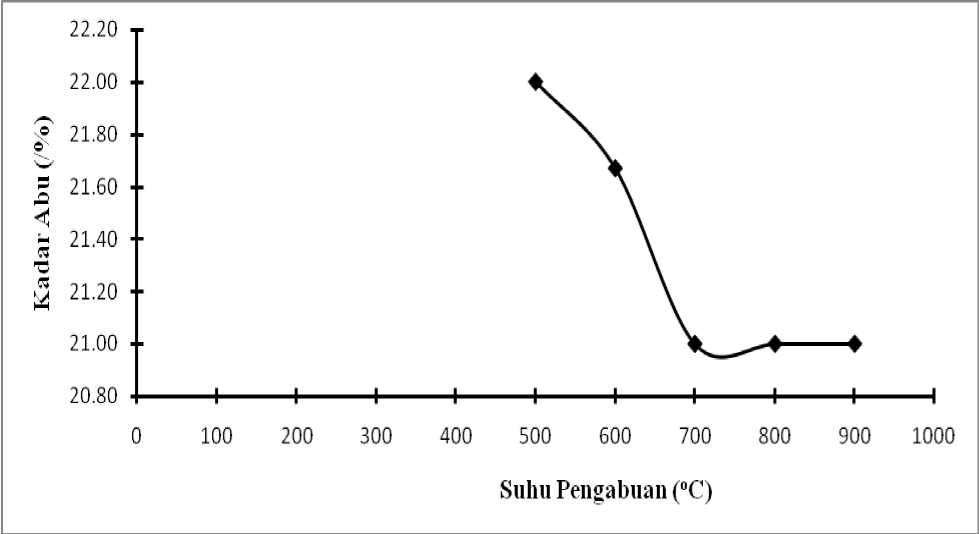
Gambar 1. Kurva pengaruh suhu pengabuan sekam terhadap kadar abu
Perbandingan optimum NaOH dan abu pada sintesis silika gel
Pada penelitian ini juga dilakukan variasi konsentrasi NaOH dalam pembuatan silika gel yang bertujuan untuk mengetahui perbandingan optimum jumlah NaOH dan abu dari masing-masing abu sekam padi limbah industri penggilingan padi dan abu limbah pembakaran batu bata. Adapun konsentrasi masing-masing NaOH adalah dari 0,5, 1, 2, 3, dan 4 M.
Dari penelitian yang telah dilakukan konsentrasi NaOH berpengaruh terhadap jumlah abu yang bereaksi membentuk silika gel untuk setiap jenis abu. Konsentrasi NaOH yang digunakan dalam penelitian ini adalah 0,50; 1,0; 2,0; 3,0; dan 4,0 M (Nuryono, 2004).
Jumlah abu yang bereaksi dihitung dengan cara tidak langsung yaitu dengan menimbang berat abu awal dan berat residu. Selisihnya dianggap telah bereaksi dengan
NaOH membentuk larutan natrium silikat. Larutan ini digunakan sebagai prekursor pembuatan silika gel. Pengaruh konsentrasi NaOH terhadap jumlah abu yang bereaksi dapat dilihat pada Gambar 2.
Gambar 2 menunjukkan bahwa untuk semua jenis abu, dengan kenaikan konsentrasi (mmol) NaOH yang direaksikan, jumlah abu yang bereaksi cenderung naik sampai mendekati titik kesetimbangan. Konsentrasi larutan NaOH yang optimum adalah larutan NaOH 3M. Larutan NaOH dengan konsentrasi lebih kecil dari 3M memberikan persentase abu yang bereaksi juga lebih kecil untuk masing-masing jenis abu. Sedangkan konsentrasi larutan NaOH di atas 3M menyebabkan persentase abu yang bereaksi hampir sama dengan NaOH yang 3M. Rasio jumlah mol NaOH dengan berat (g) abu yang paling optimal adalah 75,0 mmol NaOH : 2 g abu atau 37,5 mmol /g abu (Nittaya and Nuntiya, 2008).
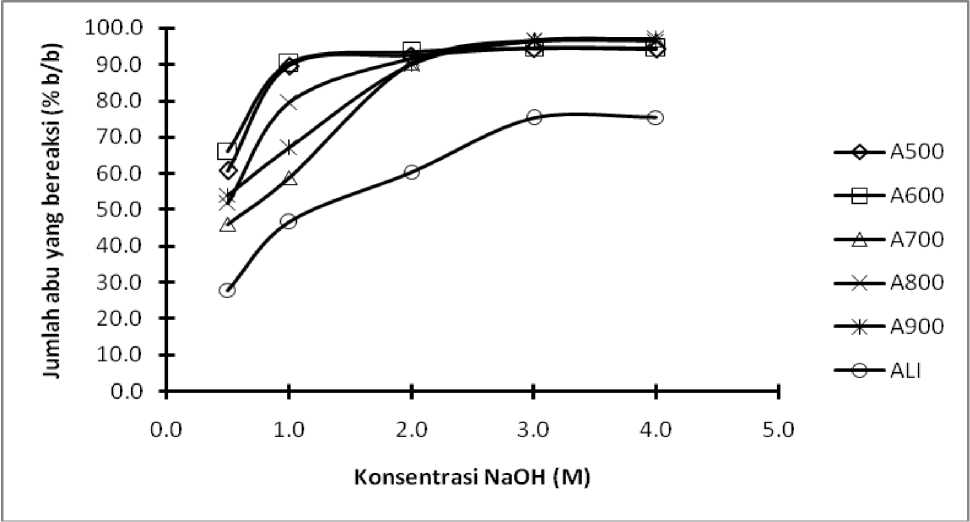
Gambar 2. Kurva pengaruh Konsentrasi NaOH terhadap persen abu yangbereaksi (2,0 g abu direaksikan dengan 25 mL larutan NaOH dididihkan selama 1 jam dengan pengadukan tetap 250 rpm).
Karakterisasi IR
Metode spektroskopi inframerah digunakan untuk mengidentifikasi gugus-gugus fungsionalyang terdapat pada silika gel. Setiap gugus fungsional pada silika gel memiliki serapan yang karakteristik pada bilangan gelombang tertentu sehingga dapat diidentifikasi secara kualitatif menggunakan spektroskopi inframerah. Karakterisasi ini diharapkan dapat digunakan untuk indikasi kualitatif keberhasilan sintesis silika gel. Pola serapan inframerah silika gel dari abu limbah pembakaran batu-bata (SGL4) dan silika gel dari abu sekam padi dengan pengabuan 700oC (SG700) ditunjukkan dalam Gambar 3.
Berdasarkan spektra IR dalam Gambar 3 dapat dilihat bahwa kedua spektra IR mempunyai bentuk yang mirip. Pada silika gel SGL4 dan SG700, pita serapan yang muncul antara bilangan gelombang 3471,87 dan 3456,44 cm-1 mengindikasikan adanya vibrasi ulur dari
gugus fungsi –OH dari silanol (Si-OH). Pelebaran pita terjadi karena gugus fungsi-OH dan air yang terserap pada permukaan silika melalui ikatan hidrogen. Pita serapan pada 3700 cm-1 akibat adanya gugus fungsi –OH terisolasi, yang mana tidak terbentuk ikatan hidrogen dengan silanol-silanol lainnya. Pita serapan pada 1635,64 cm-1 menunjukkan adanya vibrasi bending -OH dari molekul air yang terikat. Pita serapan disekitar 1100 cm-1 menunjukkan vibrasi ulur asimetris Si-O dari siloksan (Si-O-Si) (Sastrohamidjojo, 1992).
Secara umum pita serapan yang muncul pada SGL4 dan SG700 menunjukkan bahwa gugus-gugus fungsional yang terdapat pada kedua silika gel adalah gugus-gugus silanol (Si-OH) dan siloksan (Si-O-Si). Dari interpretasi spektra inframerah terebut dapat disimpulkan bahwa SGLI dan SG700 telah berhasil dibuat.
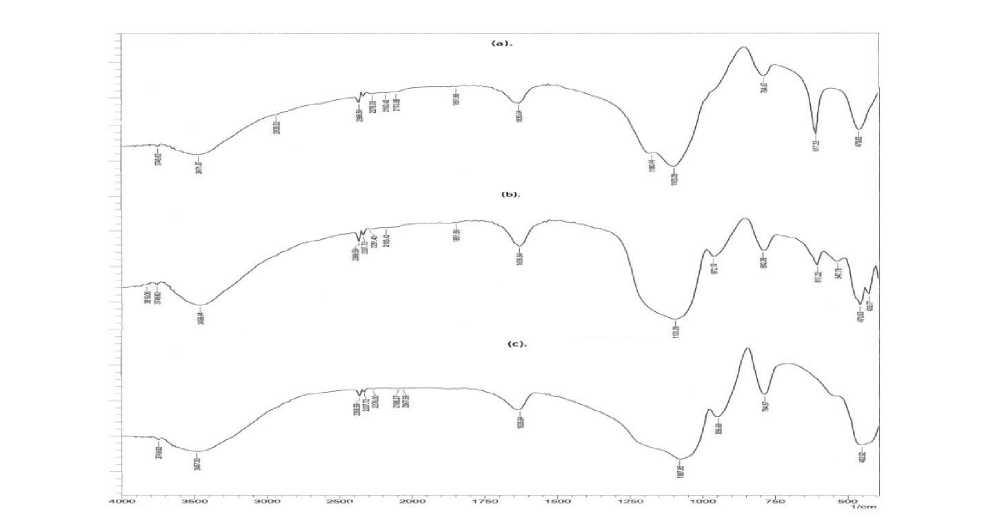
Gambar 3. Spektra Infra merah (a) Silika gel abu limbah industri batu-bata (SGL4), (b)Silika gel abu sekam padi suhu 700 (SG700), dan silika gel pembanding (SG60)
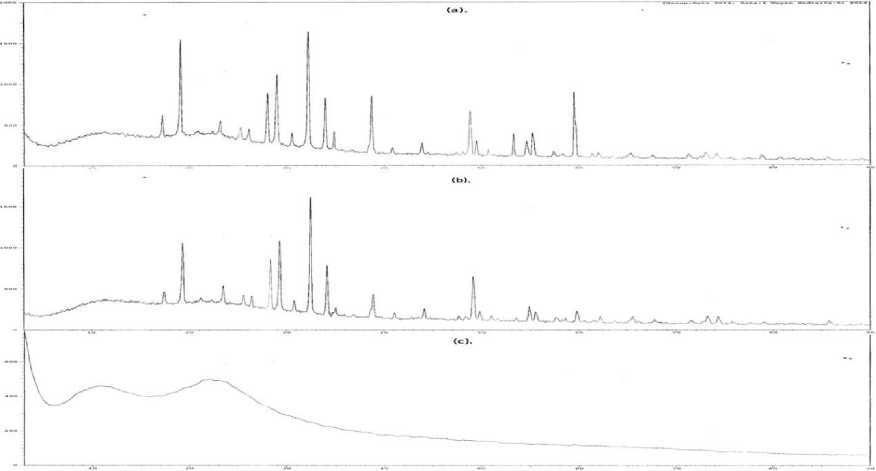
Gambar 4. Difraktogram sinar-X (a) Silika gel abu sekam padi suhu 700, (b) Silika gel abu limbah
industri batu-bata, dan silika gel pembanding (Silika gel tipe 60)
Karakterisasi Difraktometer sinar-X (X-RD)
Karakterisasi dengan metode difraksi sinar-X memberikan informasi mengenai struktur padatan yang dianalisis berupa pola difraksi sesuai dengan tingkat kristalinitasnya. Pola difraksi (SGLI, SG700 dan SG60) ditampilakn pada Gambar 4.
Pada Gambar 4. terlihat bahwa SGL4 dan SG700 menunjukkan pola difraksi dengan puncak yang melebar. SGL4 dan SG700 mempunyai intensitas maksimum pada 2θ antara 15-35o. Melebarnya puncak tersebut menunjukkan bahwa SGLI dan SG700 yang diperoleh mempunyai derajat kekristalan rendah. Kedua silika gel tersebut berbentuk amorftetapi silika gel yang dihasilkan belum begitu maksimal karena masih adanya puncak-puncak yang tajam pada silika gel yang dihasilkan baik dari silika gel dari limbah industri batu-bata maupun silika gel dari hasil sintesis (silika gel suhu 700) ini diduga disebabkan oleh proses pencucian yang kurang maksimal sehingga masih adanya sisa-sisa logam maupun sisa-sisa garam mineral yang masih tertinggal dalam silika gel (Kalapathy, 2000).
SIMPULAN DAN SARAN
Simpulan
-
1. Suhu 700 oC merupakan suhu terbaik dalam pengabuan abu sekam padi sebagai bahan dasar pembuatan silika gel
-
2. Perbandingan optimum jumlah NaOH dan abu diperoleh pada perbandingan 25 mL 3 M NaOH dengan 2 g abu atau 75 mmol NaOH : 2 g abu.
-
3. Kualitas silika gel (a) SGLI, (b) SG700 (c) SG60 dengan karakterisasi menggunakan spektra IR dan XRD memiliki kemiripan sifat dan struktur yang sama ini terlihat dari adanya gugus-gugus silinol (Si-OH) dan siloksan (Si-O-Si) serta struktur yang berbentuk amorf dari masing-masing silika gel yang terlihat pada kisaran 2θ.
Saran
Berdasarkan hasil penelitian dan kesimpulan dapat disarankan perlunya dilakukan penelitian lebih lanjut membuat silika gel menggunakan abu sekam maupun abu pembakaran batubata denganperlakuan asam terlebih dahulu untuk menghilangkan pengotor.
UCAPAN TERIMA KASIH
Melalui kesempatan ini penulis menyampaikan banyak-banyak terimakasih kepada ibu Dra. Ida Ayu Raka Astiti Ash, M.Si., ibu Sri Rahayu Santi, S.Si., M.Si., dan bapak I Nengah Simpen, S.Si., M.Si.
DAFTAR PUSTAKA
Bachrie, S., 2000, Variasi Asam Organik pada Metode Sol-Gel, Laporan Penelitian, Universitas Andalas, Sumatra Barat
Brinker, C.J., dan Scherer, W.J., 1990, Sol-Gel Science : The physics and Chemistry or Sol-Gel, Processing, Academic press, San Diego
Cestari, A.R., 2000 Thermochemical
Investigation on The Adsorption of Some Difalent Cation of Modified Silicas Obtained from Sol-Gel Process, Thermochemical Acta, 348 : 25-31
Enymia, S., amik 1998, Pembuatan Silika Gel Kering dari Sekam Padi Untuk Pengisi Karet Ban, Jurnal Ker dan Gelas Indonesia, 7 (1&2)
Harsono, H., 2002 PembuatanSilika Amorf dari Limbah Sekam Padi, Jurnal Ilmu Dasar, 3 (2) : 98-103
Ishizaki, K., 1998, Porous Material Process
Technology and Application, Kluwer Academic Publisher, Dordrecth.
Kalapathy, U., 2000, A Simple Method for Production of Pure Silika From Rice Hull Ash, Bioresource Technology, 73 : 257-256
Kammath,.S. R. and Proctor, A., 1998, Silica From Rice Hull Ash: Preparation and
Characterization, Cereal Chem., 75 (4) : 484-487
Nittaya, T. and Nuntiya, A., 2008, Synthesis and characterization of nanosilica from rice husk ash preparated by precipitation method, Departmen of Industrial
Chemistry, Faculty of Science, Chiang Mai University, Thailand
Nuryono, 2004, Pengaruh Temperatur Pengabuan Sekam Padi Terhadap Karakter Abu dan Silika Gel Sintetik, Review Kimia, 7 (2) : 67-81
Sastrohamidjojo, H., 1992, spektroskopi
Inframerah, Liberty Jogjakarta
Shriver, D. F., 1990, Inorganic Chemistry,
Oxford University Press, Oxford
38
Discussion and feedback