PENGARUH EKSTRAKSI TERHADAP EFEKTIVITAS SERBUK BIJI SEMANGKA (CURCUBITACEAE) DAN SERBUK BIJI ASEM (FABACEAE) SEBAGAI KOAGULAN ALAMI PENGGANTI TAWAS
on
ISSN 1907-9850
PENGARUH EKSTRAKSI TERHADAP EFEKTIVITAS SERBUK BIJI SEMANGKA (CURCUBITACEAE) DAN SERBUK BIJI ASEM (FABACEAE) SEBAGAI KOAGULAN ALAMI PENGGANTI TAWAS
Yunita1, Anak Agung Istri Agung Mayun Laksmiwati,1* dan Ni Komang Ariati1
1Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran, Bali
*E-mail : laksmiwati546@yahoo.com
ABSTRAK
Koagulan alami adalah koagulan yang berasal dari tanaman biji yang mengandung protein polikationik sehingga dapat menetralisir partikel muatan dalam rantai koloid. Protein yang larut dalam air akan bermuatan positif, dan memiliki sifat polielektrolit yang sama dengan tawas. Penelitian ini menggunakan serbuk biji asem dan semangka sebagai koagulan alami, dengan membandingkan hasil filtrat per hari yang dimaserasi dengan n-heksan, etanol, tanpa maserasi serta residu hasil maserasi. Pengukuran tingkat kekeruhan dilakukan dengan menggunakan metode jar test. Sedangkan penurunan kekeruhan dilakukan dengan alat turbidimeter. Hasil penelitian menunjukkan bahwa penurunan kekeruhan (NTU) filtrat serbuk biji asem yang dimaserasi n-heksan terbaik di hari keenam dan yang dimaserasi etanol terbaik di hari pertama dengan NTU berurutan 72,16% dan 82,16%, sedangkan yang tanpa maserasi NTUnya 60,00%. Pada filtrat serbuk biji semangka yang dimaserasi n-heksan terbaik di hari ketiga dan yang dimaserasi etanol terbaik di hari kelima dengan NTU 69,75% dan 65,50%, sedangkan yang tanpa maserasi NTUnya 52,50%. Nilai tingkat kekeruhan dari residu serbuk biji asem yang dimaserasi dengan n-heksan dan etanol berturut-turut 70,16% dan 62,00%, sedangkan NTU dari residu biji semangka yang dimaserasi dengan n-heksan dan etanol menunjukkan hasil yang sama yaitu 60,00%. Dari hasil penelitian dapat dikatakan bahwa filtrat dari serbuk biji asem yang dimaserasi etanol paling baik sebagai koagulan alami pengganti tawas, dibandingkan filtrat serbuk biji semangka dan residunya.
Kata kunci : Tawas, koagulan, serbuk biji asem, serbuk biji semangka
ABSTRACT
Natural coagulant is a coagulant derived from plant seeds containing polycationic protein that can neutralize charged particles in a colloidal chain. Water-soluble proteins would be positively charged, and have similar polyelectrolyte properties to aluminium sulphate (alum). This research aimed to compare the effectiveness of seed powder, n-hexane and ethanol filtrates at variation time of maceration, as well as residual of tamarind and watermelon seeds as natural coagulants. Measurements of water turbidity level was done using a jar test method while decreasing of turbidity was measured with turbidimeter. The results showed that the best coagulant for n-hexane tamarind filtrate was found at sixth day and ethanol tamarind filtrate at first day of maceration by decreasing turbidity with NTU value of 72.16% and 82.16% respectively. The decreased in turbidity using the residual of n-hexane and ethanol tamarind was 70.16 and 62.0% respectively while tamarind seed powder without maceration decreased turbidity with NTU value of 60.00 %. On the other hand, the best coagulant for n-hexane watermelon filtrate was found at third day and ethanol tamarind filtrate at fifth day of maceration by decreasing turbidity with NTU value of 69.75.16% and 65.50% respectively. The decreased of turbidity by applying the residual of n-hexane and ethanol from watermelon seed was the same with NTU value of 50.0%. From this research, it can concluded that ethanol filtrate of tamarind was found as the best natural coagulant to substitute alum compared to watermelon seed powder filtrate and their residues.
Keywords: Alum, coagulants, tamarind seed powder, watermelon seed powder
PENDAHULUAN
Koagulasi dan flokulasi merupakan proses penting dalam penjernihan air. Metode pengolahan air pada umumnya digunakan pengolahan secara fisika-kimia. Asam amino kationik merupakan asam amino dengan rantai samping yang mengandung gugus amina yang bermuatan positif (Lehninger, 1990). Semakin tinggi protein yang mengandung asam amino kationik maka semakin tinggi pula potensi dari kemampuan biji-bijian tersebut sebagai biokoagulan. Penggunaan bahan alami dapat digunakan untuk mengurangi penggunaan bahan sintetis dengan tujuan “back to nature”. Proses koagulasi dengan biji seperti biji asem dan biji semangka, akan memberikan hasil pengolahan lebih baik di bandingkan dengan pengolahan air yang menggunakan bahan sintetis (Amagloh dkk, 2009). Nilai tingkat kekeruhan (NTU) digunakan sebagai parameter karena menunjukkan tingkat kekeruhan air, dimana semakin tinggi persen penurunan maka sampel yang digunakan itu semakin baik sebagai koagulan alami.
Koagulasi dan flokulasi merupakan proses penting dalam penjernihan air, koagulasi adalah destibilisasi partikel koloid dan partikel tersuspensi termasuk bakteri dan virus melalui penetralan muatan elektrik untuk mengurangi gaya tolak menolak antar partikel sehingga partikel-partikel tersebut dapat saling bergabung. Koagulasi secara kimia dapat dilakukan dengan penambahan elektrolit, pencampuran koloid yang berbeda muatan, dan penambahan koagulan. Flokulasi adalah proses penggabungan partikel-partikel yang tidak stabil setelah proses koagulasi melalui proses pengadukan (stirring) lambat sehingga terbentuk gumpalan atau flok yang dapat diendapkan atau disaring pada proses pengolahan selanjutnya (Hadi,1997). Koagulan sintetik adalah garam logam yang bereaksi dengan air yang bersifat alkali (basa) untuk menghasilkan flok logam hidroksida yang tidak larut, dimana flok yang terbentuk tidak dapat digolongkan sebagai partikel koloid (Karamah dkk, 2008). Koagulan yang paling sering digunakan adalah tawas.
Koagulan alami yang biasa digunakan berasal dari biji tanaman karena mengandung protein polikationik karena mengandung asam amino kationik di dalam rantai polipeptidanya sehingga dapat menetralisir partikel muatan
negatif dalam koloid (Eckenfelde, 2000). Semangka merupakan tanaman buah berupa herba yang tumbuh merambat. Tanaman ini berasal dari Afrika, semangka termasuk kedalam suku curcubitaceae. Tanaman semangka bersifat semusim, tergolong cepat berproduksi karena umurnya hanya sampai 6 bulan (Wiharjo, 1993). Asam Jawa dihasilkan oleh pohon yang bernama ilmiah Tamarindus indica, termasuk kedalam suku fabaceae (Leguminoceae). Spesies ini adalah satu-satunya anggota marga Tamarindus. Asam jawa adalah sebuah tanaman daerah tropis dan termasuk tumbuhan berbuah polong (Rukmana, 2000).
Berdasarkan hal diatas perlu dilakukan kajian pengaruh proses maserasi terhadap perbandingan hasil maserasi antara residu dan filtrat pada serbuk biji asem dan serbuk biji semangka yang dimaserasi dengan pelarut etanol dan n-heksan terhadap efektivitasnya sebagai koagulan alami pengganti tawas. Selain itu, untuk mengetahui persen penurunan tingkat kekeruhan dari serbuk biji asem dan serbuk biji semangka yang di maserasi dengan pelarut etanol, n-heksan serta tanpa maserasi
MATERI DAN METODE
Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah biji semangka, biji asem, alum (tawas), n-heksan, etanol, air keruh, dan aquadest.
Peralatan
Alat-alat yang digunakan pada penelitian ini adalah peralatan gelas, magnetik stirer, turbidimeter, pH meter, saringan ukuran 250 mikron, neraca analitik digital, neraca analitik, pipet volume 10mL, labu ukur 100mL, kertas saring, dan seperangkat alat jar test.
Cara Kerja
Biji semangka dan biji asem yang sudah tua dan kering ditumbuk agar menjadi serbuk halus kemudian diayak dengan ukuran 250 mikron. Sebanyak 30 gram serbuk yang sudah halus dimaserasi dengan pelarut n-heksan untuk mengurangi kandungan lemak selama 6 x 24 jam (6 hari) dimana setiap 24 jam pelarutnya diganti dengan pelarut yang baru. Larutan disaring, kemudian residunya
dikeringkan diudara terbuka hingga beratnya konstan. Filtrat yang diperoleh per hari disimpan didalam botol gelap. Residu yang diperoleh disimpan sebagai sampel rendah lemak. Prosedur yang sama dilakukan untuk maserasi dengan etanol.
Sebanyak 5 gram residu serbuk biji semangka rendah lemak (hasil maserasi dengan n-heksana) dimasukan kedalam labu ukur 100mL dan ditambah akuadest hingga tanda batas. Kemudian dipindahkan kedalam erlenmeyer 250 mL dan diaduk selama 30 menit. Selanjutnya campuran ini disaring, diperoleh filtrat larutan induk koagulan alami. Perlakuan yang sama dilakukan pada residu serbuk biji asem, dan serbuk biji tanpa maserasi.
Sumber air yang masih keruh diambil dan diukur pH awal serta kekeruhan awalnya terhadap setiap pengujian masing-masing jenis koagulan. Disiapkan 6 gelas beaker 1000mL masing-masing diisi sampel air keruh 1000mL dan diukur pHnya sebagai pH awal. Kemudian ditambahkan dengan larutan induk 5% dengan variasi volume 2,5; 5,0; 7,5; 10,0; 12,5; dan 15,0 mL diaduk dengan alat pengaduk jar test. Campuran diaduk dengan pengadukan cepat 120 rpm selama 3 menit, kemudian pengadukan lambat 60 rpm selama 10 menit, dan setelah itu didiamkan selama 2 jam. Sesudah 2 jam sampel air hasil koagulasi
diambil pada daerah permukaan dan diukur pHnya sebagai pH akhir. Pengujian untuk sampel koagulan induk biji asem dan tawas dilakukan dengan cara yang sama seperti pada larutan koagulan biji semangka. Masing-masing pengujian dilakukan 3 x ulangan.
Sampel air hasil koagulasi diuji dengan menggunakan alat turbidimeter untuk mengetahui penurunan tingkat kekeruhan (NTU) dalam air tersebut setelah penambahan koagulan alami. Uji turbidimetri juga dilakukan pada air yang telah ditambah dengan tawas 5% sebagai koagulan pembanding. Persentase penurunan kekeruhan dihitung dengan rumus:
nilai awal—nilaiakhiy
% Penurunan = x 100%
nilai awal
HASIL DAN PEMBAHASAN
Koagulan Serbuk Biji Asem
Filtrat hasil maserasi serbuk biji asem dengan n-heksan menunjukan warna yang berbeda-beda setiap harinya. Pada hari pertama hasil filtrat berwarna sedikit kuning jernih dan hari berikutnya sampai hari keenam warnanya semakin memudar dan menjadi tidak berwarna
Tabel 1 Rerataan Persen Kekeruhan Serbuk Biji Asem yang dimaserasi dengan n-heksan
|
Filtrat |
Air baku (NTU) |
pH Awal |
Volume koagulan (mL) |
Hasil Perlakuan (NTU) |
pH Akhir |
.Penurunan (%) |
|
Hari pertama |
200 |
7,82 |
7,5 |
58,60 |
7,82 |
70,70 |
|
Hari kedua |
200 |
7,84 |
2,5 |
87,70 |
7,74 |
56,15 |
|
Hari ketiga |
200 |
7,74 |
10,0 |
82,00 |
7,59 |
59,00 |
|
Hari keempat |
200 |
7,71 |
12,5 |
63,00 |
7,65 |
68,50 |
|
Hari kelima |
200 |
7,69 |
15,0 |
70,67 |
7,66 |
64,66 |
|
Hari keenam |
200 |
7,69 |
15,0 |
55,67 |
7,62 |
72.16 |
|
Residu asem yang dimaserasi dengan n- |
200 |
7,76 |
5,0 |
59,62 |
7,72 |
70,16 |
heksan
Pada filtrat serbuk biji asem yang di maserasi dengan n-heksan dalam Tabel 1 menunjukan bahwa penurunan NTU paling tinggi sebesar 72,16% ditunjukkan pada hari keenam dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL. Residu hasil maserasi dengan n-heksan menunjukkan
penurunan NTU paling tinggi dengan penambahan volume koagulan induk 5%
sebanyak 5,0 mL yaitu sebesar 70,16%. Perbedaan volume koagulan yang terjadi pada tingkat kekeruhan diakibatkan pengikatan koloid oleh polimer menyebabkan molekul polimer akan mengikat partikel koloid pada satu sisi. Pada bagian dari rantai yang tidak
mengikat koloid dapat berikatan dengan rantai lain yang telah mengikat koloid. Semakin banyak ikatan yang terjadi semakin banyak koloid yang bergabung, membentuk gumpalan (flok) yang dapat mengendap, bagian rantai yang bebas tidak berikatan dengan rantai yang lainnya maka rantai tersebut akan menutupi seluruh permukaan partikel koloid yang diikatnya. Hal ini menyebabkan partikel koloid kembali stabil. Penambahan koagulan yang tidak seimbang dapat menyebabkan kegagalan pembentukan flok, sehingga terjadi perbedaan
|
Tabel 2 Rerataan Persen Kekeruhan Serbuk Biji Asem yang dimaserasi dengan Etanol | ||||||
|
Filtrat |
Air baku (NTU) |
pH Awal |
Volume koagulan (mL) |
Hasil Perlakuan (NTU) |
pH Akhir |
Penurunan (%) |
|
Hari pertama |
200 |
7,94 |
5,0 |
35,67 |
8,03 |
82,16 |
|
Hari kedua |
200 |
7,72 |
7,5 |
45,00 |
7,85 |
77,50 |
|
Hari ketiga |
200 |
7,84 |
15,0 |
88,67 |
7,77 |
55,66 |
|
Hari keempat |
200 |
7,70 |
2,5 |
96,67 |
8,00 |
51,66 |
|
Hari kelima |
200 |
7,85 |
2,5 |
106,00 |
7,83 |
47,00 |
|
Hari keenam |
200 |
7,75 |
15,0 |
83,00 |
7,73 |
58,50 |
|
Residu asem yang dimaserasi dengan |
200 |
7,28 |
15,0 |
76,00 |
6,95 |
62,00 |
|
etanol Asem tanpa maserasi |
200 |
7,37 |
15,0 |
80,00 |
7,39 |
60,00 |
|
Pada filtrat serbuk biji asem yang di |
rantai lain yang telah mengikat koloid. Semakin banyak ikatan yang | |||||
maserasi dengan etanol seperti disarikan pada Tabel 2. menunjukan bahwa penurunan NTU paling tinggi yaitu sebesar 82,16% ditunjukkan pada hari pertama dengan penambahan volume koagulan induk 5% sebanyak 5,0 mL. Nilai residu hasil maserasi dengan etanol menunjukkan penurunan NTU paling tinggi sebesar 62,00% yang diperoleh dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL. Hasil proses koagulasi dengan menggunakan serbuk tanpa proses maserasi menunjukkan hasil penurunan NTU yang tidak jauh berbeda dengan filtrat hasil maserasi. Penurunan angka paling tinggi dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL adalah 62,00%. Adanya perbedaan volume koagulan yang terjadi pada tingkat kekeruhan diakibatkan pengikatan koloid oleh polimer menyebabkan molekul polimer akan mengikat partikel koloid pada satu sisi. Pada bagian dari rantai yang tidak mengikat koloid dapat berikatan dengan
hasil tertinggi pada volume koagulan yang ditambahkan.
Nilai pH pada awal pengukuran dan pH akhir dari hasil penelitian pada Tabel 1 menunjukkan tidak terjadi perubahan nilai pH yang signifikan, karena nilai pH masih berkisar diantara pH 6-8.
Asem yang dimaserasi dengan etanol menunjukan hasil filtrat yang perubahan warnanya berbeda-beda setiap harinya. Pada filtrat hari pertama berwarna coklat pekat, hingga hari kedua filtrat masih berwarna coklat tapi kepekatannya berkurang hingga pada hari ke 6 filtrat berwarna bening.
Terjadi semakin banyak koloid yang bergabung, membentuk gumpalan (flok) yang dapat mengendap, bagian rantai yang bebas tidak berikatan dengan rantai yang lainnya maka rantai tersebut akan menutupi seluruh permukaan partikel koloid yang diikatnya. Hal ini menyebabkan partikel koloid kembali stabil. Penambahan koagulan tidak seimbang dapat menyebabkan kegagalan pembentukan flok, sehingga terjadi perbedaan hasil tertinggi pada volume koagulan.
Nilai pH pada pengukuran pH awal dan pH akhir dari hasil penelitian seperti tertera pada Tabel 2 tidak menunjukkan perubahan nilai pH yang signifikan, karena nilai pH masih berkisar diantara pH 6-8.
Koagulan Serbuk Biji Semangka
Semangka yang dimaserasi dengan n-heksan menunjukan hasil filtrat yang perubahan warnanya berbeda-beda setiap
harinya. Pada filtrat hari pertama berwarna kuning jernih, hingga hari berikutnya pada hari ke 6 filtrat berwarna bening.
Tabel 3 Rerataan Persen Kekeruhan Serbuk Biji Semangka yang dimaserasi dengan n-heksan
|
Filtrat |
Air baku (NTU) |
pH Awal |
Volume koagulan (mL) |
Hasil Perlakuan (NTU) |
pH Akhir |
Penurunan (%) |
|
Hari pertama |
200 |
7,72 |
12,5 |
80,00 |
6,88 |
60,00 |
|
Hari kedua |
200 |
6,99 |
15,0 |
70,50 |
6,83 |
64,75 |
|
Hari ketiga |
200 |
7,50 |
15,0 |
60,50 |
7,34 |
69,75 |
|
Hari keempat |
200 |
7,37 |
15,0 |
62,00 |
7,38 |
69,00 |
|
Hari kelima |
200 |
7,38 |
15,0 |
66,00 |
7,39 |
67,00 |
|
Hari keenam |
200 |
7,23 |
15,0 |
73,00 |
7,29 |
63,50 |
|
Residu semangka yang dimaserasi |
200 |
7,36 |
15,0 |
80,00 |
7,40 |
60,00 |
dengan n-heksan
Pada filtrat serbuk biji semangka yang di maserasi dengan n-heksan seperti disarikan pada Tabel 3. penurunan NTU paling tinggi yaitu sebesar 69,75%. ditunjukkan pada hari ketiga dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL Nilai residu hasil maserasi dengan n-heksan menunjukkan penurunan NTU paling tinggi yaitu 60,00% yang diperoleh dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL. Adanya perbedaan volume yang terjadi pada tingkat kekeruhan diakibatkan pengikatan koloid oleh polimer menyebabkan molekul polimer akan mengikat partikel koloid pada satu sisi. Pada bagian dari rantai yang tidak mengikat koloid dapat berikatan dengan rantai lain yang telah mengikat koloid. Semakin banyak ikatan yang terjadi semakin banyak koloid yang bergabung, membentuk gumpalan (flok) yang dapat mengendap, bagian rantai
yang bebas tidak berikatan dengan rantai yang lainnya maka rantai tersebut akan menutupi seluruh permukaan partikel koloid yang diikatnya. Hal ini menyebabkan partikel koloid kembali stabil. Penambahan koagulan tidak seimbang dapat menyebabkan kegagalan pembentukan flok, sehingga terjadi perbedaan hasil tertinggi pada volume koagulan.
Nilai pH pada pengukuran pH awal dan pH akhir dari hasil penelitian seperti tertera pada Tabel 3. tidak menunjukkan perubahan nilai pH yang signifikan, karena nilai pH masih berkisar diantara pH 6-8.
Semangka yang dimaserasi dengan etanol menunjukkan hasil filtrat yang perubahan warnanya berbeda-beda setiap harinya. Pada filtrat hari pertama berwarna kuning jernih, hingga hari berikutnya dan pada hari ke 6 filtrat berwarna bening.
Tabel 4 Persen Kekeruhan Serbuk Biji Semangka yang dimaserasi dengan Etanol
|
Filtrat |
Air baku (NTU) |
pH Awal |
Volume koagulan (mL) |
Hasil Perlakuan (NTU) |
pH Akhir |
Penurunan (%) |
|
Hari pertama |
200 |
7,20 |
12,5 |
82,00 |
7,23 |
59,00 |
|
Hari kedua |
200 |
7,37 |
15,0 |
76,00 |
7,23 |
62,00 |
|
Hari ketiga |
200 |
7,20 |
15,0 |
77,00 |
7,03 |
61,00 |
|
Hari keempat |
200 |
7,33 |
15,0 |
72,00 |
7,02 |
64,00 |
|
Hari kelima |
200 |
7,22 |
15,0 |
69,00 |
7,20 |
65,50 |
|
Hari keenam |
200 |
7,09 |
15,0 |
70,00 |
7,06 |
65,00 |
|
Residu semangka |
200 |
7,10 |
15,0 |
80,00 |
7,18 |
60,00 |
yang dimaserasi
dengan etanol
Pada filtrat serbuk biji semangka yang di maserasi dengan etanol dalam Tabel 4 menunjukkan bahwa penurunan NTU paling tinggi ditunjukkan pada hari kelima dengan penambahan volume koagulan induk 5% sebanyak 15,0 mL adalah 65,50%. Nilai residu hasil maserasi dengan etanol menunjukkan penurunan NTU paling tinggi dengan penambahan volume koagulan induk 5% sebanyak 15,0 adalah 60,00%. Proses hasil tanpa maserasi menunjukan hasil penurunan yang tidak jauh beda pada hasil filtrat yang dimaserasi. Penurunan angka paling tinggi dengan penambahan volume koagulan induk 5% sebanyak 15,0 adalah 52,50%. Pengujian pada hasil perlakuan dilakukan sebanyak 3 kali pengulangan, setelah dirata-ratakan diperoleh hasil pada Tabel 4. Adanya perbedaan volume yang terjadi pada tingkat kekeruhan diakibatkan pengikatan koloid oleh polimer menyebabkan molekul polimer akan mengikat partikel koloid pada satu sisi. Pada bagian dari rantai yang tidak mengikat koloid dapat berikatan dengan rantai lain yang telah mengikat koloid. Semakin banyak ikatan yang terjadi semakin banyak koloid yang bergabung, membentuk gumpalan (flok) yang dapat mengendap, bagian rantai yang bebas tidak berikatan dengan rantai yang lainnya maka rantai tersebut akan menutupi seluruh permukaan partikel koloid yang diikatnya. Hal ini menyebabkan partikel koloid kembali stabil. Penambahan koagulan tidak seimbang dapat menyebabkan kegagalan pembentukan flok, sehingga terjadi perbedaan hasil tertinggi pada volume koagulan.
Nilai pH pada pengukuran pH awal dan pH akhir dari hasil penelitian pada Tabel 4 tidak terjadi perubahan nilai pH yang signifikan, karena nilai pH masih berkisar diantara pH 6-8.
Koagulan Sintetis
Koagulan sintesis atau yang disebut juga alum (tawas) 5% dengan variasi volume 2,5; 5,0; 7,5; 10,0; 12,5; dan 15,0 mL
Tabel 5 Rerataan Persen Kekeruhan Larutan
Standar Tawas
|
Jenis koagulan |
Air baku (NTU) |
pH awal |
Volume koagulan (mL) |
Hasil perlakuan (NTU) |
|
Koagulan |
200 |
7,48 |
2,5 |
11,00 |
|
sintetis |
200 |
7,40 |
5,0 |
10,00 |
|
200 |
7,32 |
7,5 |
9,00 | |
|
200 |
7,30 |
10,0 |
7,00 | |
|
200 |
7,29 |
12,5 |
5,00 | |
|
200 |
7,25 |
15,0 |
5,00 |
Seperti tertera pada Tabel 5, koagulan sintetik tawas menunjukkan penurunan angka kekeruhan diatas 90,00%. Angka yang menunjukan hasil yang paling tinggi pada penelitian ini pada penambahan volume koagulan sebanyak 12,5 mL dan 15,0 mL adalah 97,50%. Nilai pH pada pengukuran pH awal dan pH akhir seperti tertera padal Tabel 5 tidak menunjukkan perubahan nilai pH yang signifikan, karena nilai pH masih berkisar diantara pH 6-8.
Perbandingan Hasil
Berdasarkan hasil penelitian didapatkan hasil perbandingan antara filtrat
dan residu serbuk biji asem serta serbuk biji semangka yang dimaserasi dengan etanol, n-heksan dan tanpa maserasi, dengan tawas sebagai pembanding diperoleh kemampuan koagulan serbuk biji asem lebih baik dibandingkan dengan serbuk biji semangka. Pada proses maserasi, filtrat yang diperoleh memberikan hasil yang lebih baik dibandingkan residunya. Maserasi serbuk sampel dengan etanol menunjukan hasil yang lebih baik, dibandingkan dengan n-heksan dan serbuk sampel tanpa dimaserasi. Serbuk sampel tanpa maserasi sebagai koagulan menunjukkan hasil yang kurang baik karena protein dari serbuk biji tidak terlarut.
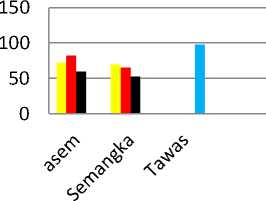
n-heksan
■ Etanol
■ Tanpa maserasi
■ Tawas
Gambar 1 Grafik Perbandingan Persentase
Penurunan Kekeruhan Sampel
Hasil penelitian menunjukan bahwa penurunan kekeruhan optimum, filtrat hari pertama serbuk biji asem yang dimaserasi dengan etanol dengan volume 5,0 mL sebesar 82,16 %. Sedangkan pada serbuk biji semangka filtrat hari ketiga yang dimaserasi dengan n-heksan pada volume 15,0 mL sebesar 69,75 %, dan tawas dengan volume 12,5 atau 15,0 mL sebesar 97,50 %. Hal ini menunjukan bahwa pada suku Fabaceae lebih banyak mengandung asam amino kationik dibandingkan suku Curcubitaceae .
SIMPULAN DAN SARAN
Simpulan
Efektifitas koagulan serbuk biji asem dan semangka yang dimaserasi dengan pelarut etanol lebih tinggi dibandingkan serbuk biji yang dimaserasi dengan pelarut n-heksan. Filtrat hasil maserasi memiliki kemampuan koagulan yang lebih tinggi dibandingkan residunya. Penurunan kekeruhan serbuk biji asem yang dimaserasi dengan n-heksan, etanol, dan tanpa maserasi terjadi pada filtrat hari keenam pada n-heksan dan hari pertama pada etanol berturut-turut adalah sebesar 72,16 %, 82,16 % dan 60,00% pada
penambahan volume koagulan induk masing-masing 15,0mL. Sedangkan penurunan kekeruhan pada serbuk biji semangka yang diperoleh tanpa maserasi, filtrat n-heksana di hari ketiga dan etanol di hari kelima dengan penambahan volume koagulan induk masing-masing 15mL berturut-turut adalah sebesar 52,50 % , 69,75 %, dan 65,50 %. Saran
Perlu dilakukan penelitian lebih lanjut dengan analisis konsetrasi induk yang berbeda pada hasil filtrat maserasi agar menemukan hasil yang optimum, pengujian pada jenis sampel koagulan berbeda dengan variasi pelarut yang lain, serta uji instrument HPLC pada sampel filtrat koagulan untuk mengetahui jenis asam amino kationik pada filtrat koagulan alami.
UCAPAN TERIMA KASIH
Terima kasih penulis sampaikan kepada A.A.I.A Mayun Laksmiwati, Ni Komang Ariati,
Ida Ayu Raka Astiti Asih, I Wayan Gede Gunawan, dan. Ni Wayan Bogoriani.
DAFTAR PUSTAKA
Amagloh, Kweku F., dan Benang A., 2009, Effectiveness of Moringa Oleifera Seed as Coagulant for Water Purification, Full Length Research Paper, African Journal of Agricultural Research Vol. 4 (1), pp.119123, http://www.academicjournals.org/AJAR .ISSN 1991-637X © 2009 Academic
Journals.
Eckenfelde, W., 2000, Industrial Water
Pollution Control, McGrow-Hill Inc
Edition 3: New York.
Hadi, W., 1997, Perencanaan Bangunan
Pengelohan Air Minum. Makalah, FTSP – ITS, Surabaya.
Karamah, Fathul, E., dan Kustiano, F. G., 2008, Perbandingan Perlakuan Koagulasi dengan Mengguanakn Koagulan Fe(SO4).7H2O
dan Al2(SO4)3.18H2O Terhadap Kinerja
Membrane Mikrofiltrasi Polypropilene
Hollow Fiber, Repository Laporan Penelitian. Fakultas Teknik Universitas Indonesia ; Depok.
Lehninger, 1990, Dasar-dasar Biokimia, jilid 1, Penerbit Erlangga, Surabaya.
Rukmana, R., 2000. Budidaya Asam Jawa.
Kanisius: Yogyakarta.
Wihardjo, S., 1993, Bertanam Semangka.
Kanisisus, Yogyakarta.
94
Discussion and feedback