KADAR LOGAM SENG PLASMA DAN ALKOHOL DEHIDROGENASE PADA TIKUS YANG DIBERI ETANOL
on
ISSN 1907-9850
KADAR LOGAM SENG PLASMA DAN ALKOHOL DEHIDROGENASE PADA TIKUS YANG DIBERI ETANOL
Elfrida Magdalena Manurung1*, Ida Bagus Putra Manuaba1, Anak Agung Bawa Putra1 1Jurusan Kimia Fakultas MIPA Universitas Udayana, Bukit Jimbaran, Bali
*E-mail: eιifridamagdalena23@gmail.com
ABSTRAK
Penelitian ini bertujuan mengetahui kadar logam seng plasma alkohol dehidrogenase pada tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL. Rancangan penelitian ini menggunakan Randomized Posttest Only Control Group Desain dengan dua kelompok perlakuan dan satu kelompok kontrol. Rata-rata kadar logam seng plasma pada tikus kontrol (K) dan tikus yang diberi etanol 40 % dengan volume 2 mL (P1) dan 3 mL (P2) adalah 445,83 ± 27,76 mg/L; 928,38 ± 183,13 mg/L; dan 1228,75 ± 80,00 mg/L. Hasil perhitungan rata-rata aktivitas alkohol dehidrogenase plasma pada tikus kontrol dan tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL adalah 21,00 ± 0,34 ng/mL; 18,69 ± 0,31 ng/mL dan 17,05 ± 0,33 ng/mL. Hasil ANOVA menunjukkan p < 0,05 sehingga terdapat perbedaan bermakna kadar logam seng plasma dan aktivitas alkohol dehidrogenase pada tikus kontrol dan tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL. Hasil analisis Tukey/HSD untuk kadar rata-rata logam seng plasma tikus kontrol dan tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL memiliki perbedaan signifikan, yaitu terjadinya peningkatan kadar logam seng plasma dan pada aktivitas alkohol dehidrogenase dengan terjadi penurunan pada kelompok tikus yang diberi etanol 40 % dengan volume 2 mL dan
PENDAHULUAN
Kasus kematian akibat overdosis minuman beralkohol di Indonesia menjadi masalah yang perlu perhatian dari pemerintah dalam penanggulangannya (Panjaitan, 2003). Etanol dari minuman beralkohol di dalam tubuh akan mengalami biotransformasi yang melibatkan tiga jalur, yaitu: (1) jalur lintas alkohol dehidrogenase (sitosol) merupakanm jalur utama metabolisme etanol. Etanol di dalam tubuh dikonversi menjadi asetaldehid dengan alkohol dehidrogenase untuk
mengkatalisir pelepasan ion hidrogen dari etanol dan berikatan dengan kofaktor NAD+ membentuk NADH (Katzung, 2007), (2) Jalur Microsomal Ethanol Oxidizing System (MEOS) yakni proses metabolisme etanol jika konsentrasi etanol dalam darah < 100 mg/dL. Sistem MEOS mengkonversi asetaldehid menjadi asam asetat oleh aldehid dehidrogenase di dalam mitikondria (Wright, 1991), dan (3) Jalur peroksisom atau sistem katalase yakni metabolisme H2O2 yang dapat mengubah keadaan redoks dengan perubahan metabolisme lemak dan karbohidrat ketika kadar etanol
meningkat di dalam tubuh sehingga menghambat sintesis protein dengan menambah jaringan kolagen (Zakhari, 2006).
Konsumsi etanol dapat meningkatkan kadar logam seng plasma dan menurunkan aktivitas alkohol dehidrogenase di dalam tubuh (Aquino, et al., 2011). Overdosis etanol dapat menurunkan kadar logam seng plasma dan meningkatkan aktivitas alkohol dehidrogenase. Penelitian ini diharapkan terjadi peningkatan kadar logam seng plasma dan penurunan aktivitas alkohol dehidrogenase yang diberi etanol. Logam seng adalah situs aktif alkohol
MATERI DAN BAHAN
Bahan
Bahan yang digunakan dalam penelitian ini adalah plasma darah tikus, etanol 96 %, H2O2 pekat, HNO3 70 %, H2SO4 96 %, buffer fospat pH 7, EDTA, NaH2PO4.2H2O, Na2HPO4.2H2O, dan reagen KIT MAK053-1KT Sigma – Aldrich
Peralatan
Alat yang digunakan dalam penelitian ini adalah neraca analitik, pipet tetes, pipet volume, pipet mikro, batang pengaduk, gelas beker, gelas ukur, corong, hot plate, tabung eppendorf, water bath gelmar science, pipet kapiler hemotokrit, spuit injeksi, sentrifugasi clements 2000, spektrofotometer UV-Vis Varint DMS 80, dan Inductivity Coupled Plasma Atomic Emisssion Spectrometry (ICPE) 9000 Series Shimadsu.
Cara Kerja
Penyiapan hewan uji
Hewan uji diadaptasi selama satu minggu sebelum pengambilan sampel darah tikus. Tikus ditempatkan pada kandang yang berukuran 30 x 30 x 20 cm3. Adaptasi dilakukan pada tikus kontrol dan perlakuan dengan penyeragaman makanan dengan pemberian pakan standar dan air minum lalu tikus dialokasi menjadi tiga kelompok. Kelompok kontrol dengan 3 tikus dan kelompok perlakuan dengan 4 ekor tikus dan siap untuk dilakukan pengambilan sampel darah.
dehidrogenase sehingga dilakukan penentuan kadar logam seng untuk mengetahui kerja hati mengkonversi etanol menjadi asetaldehid. Pemberian suplemen yang mengandung logam seng akan dapat menormalkan kembali kadar logam seng plasma darah sehingga kasus keracunan minuman beralkohol dapat diatasi,
Pengambilan sampel plasma darah tikus
Sampel plasma darah tikus diambil di Desa Nyalian, Banjarangkan - Klungkung pada tanggal 23 Maret 2016. Plasma darah diambil sebanyak ± 1 mL lalu dimasukkan ke dalam tabung eppendorff yang berisi EDTA sebagai anti koagulan. Dilakukan analisis kadar logam seng dan aktivitas alkohol dehidrogenase tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL.
Penentuan kurva kalibrasi pada larutan standar ZnSO4.7H2O
ZnSO4.7H2O sebanyak 0,2198 g dilarutkan dengan HNO3 1 M hingga volume 500 mL sehingga didapatkan larutan standar ZnSO4.7H2O 100 ppm. Sebanyak 0 µL, 250 µL, 500 µL dan 750 µL larutan ZnSO4.7H2O 100 ppm diambil untuk membuat larutan standar 0 ppb, 250 ppb, 500 ppb dan 750 ppb diencerkan dengan HNO3 0,1 M. Larutan ini digunakan sebagai penentuan kurva kalibrasi logam seng.
Penentuan kadar logam seng plasma tikus
Plasma darah sebanyak 100 µL dimasukkan ke dalam gelas beker 100 mL ditambahkan dengan larutan HNO3 37 %, H2SO4 96 %, dan H2O2 ( 6 : 2 : 1). Campuran tersebut didestruksi di atas hotplate selama 5 menit pada suhu 100oC. Larutan hasil destruksi dimasukkan dalam labu ukur 25 mL lalu diencerkan dengan akuades. Dianalisis dengan menggunakan ICPE sehingga dihasilkan nilai intensitas sebagai kadar logam seng plasma tikus yang diberi etanol dan juga tikus kontrol.
Penentuan aktivitas alkohol dehidrogenase plasma tikus
Aktivitas alkohol dehidrogenase diukur dengan menggunakan Assay KIT MAK053-1KT Sigma-Aldrich. Sampel plasma darah sebanyak 10 µL diambilkan dan dimasukkan ke dalam plate well lalu ditambahkan 2 µL larutan kontrol positif dan buffer ADH assay hingga volume menjadi 50 µL. Campuran tersebut ditambahkan 100 µL larutan Mix Reaction dan 100 µL larutan Background Control untuk setiap sampel. Setiap sampel pada plate well diinkubasi selama 3 menit pada suhu 37°C dengan pembacaan microplate well dengan menggunakan spektrofotometri UV-Vis untuk mengukur nilai optical density pada λ = 450 (OD 450) dan inkubasi dilakuka selama 30 menit hingga 2 jam pada suhu 37°C. Nilai optical density pada λ = 450 (OD 450) inilah yang digunakan untuk mendapatkan hasil dari aktivitas alkohol dehidrogenase plasma tikus.
Analisis data hasil penelitian
Data hasil penelitian dianalisis secara statistik. Jika distribusi data normal dan homogen dengan p < 0,05 maka analisis dilanjutkan dengan analisis parametrik metode ANOVA menggunakan program SPPS (Statistical Product and Servies Solution) pada tinggal kepercayaan 95 %. Pengambilan keputusan didasarkan pada nilai statistik hitung dan nilai statistik tabel. Jika p > 0,05 mengandung normal kembali dengan maka Ho diterima dan H1 ditolak, sebaliknya jika p < 0,05 maka H1 diterima dan Ho ditolak.
HASIL DAN PEMBAHASAN
Persamaan regresi linear untuk kurva kalibrasi logam seng adalah y = 0,86 x + 117 dengan koefisien regresi (R) sebesar 0,9980. Pengukuran kadar logam seng plasma tikus kontrol dan tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL ditunjukan pada Gambar
-
1. Perbedaan kadar logam seng plasma tikus
kontrol karena darah yang mengalir ke organ hati, jantung, dan lambung untuk setiap tikus berbeda. Jumlah dan kecepatan darah yang mengalir ke hati di dalam tubuh selama proses peredaran darah menyebabkan adanya perbedaan jumlah aliran darah yang mengalir di organ tubuh tikus kontrol. Semakin besar volume dan jumlah darah maka darah yang mengalir ke hati semakin besar (Lienhardt, et al., 2005).
Tikus yang diberi etanol 40 % dengan variasi volume 2 mL dan 3 mL menghasilkan variasi kadar logam seng. Banyaknya volume etanol yang diberikan akan mempengaruhi jumlah kadar logam seng yang dihasilkan. Semakin banyak volume etanol yang diberikan maka etanol yang diserap akan semakin cepat dan banyak sehingga kadar etanol meningkat. Dengan meningkatnya kadar etanol maka kadar logam seng plasma juga meningakat. Peningkatan kadar logam seng plasma sebanding dengan meningkatnya alkohol dehidrogenase di dalam tubuh yang berfungsi dalam metabolisme etanol. Kadar logam seng plasma tikus yang diberi etanol 40 % dapat ditunjukan pada Gambar 1. Kadar logam seng plasma pada tikus yang diberi etanol 40% dengan volume sebanyak 3 mL lebih besar jika dibandingkan dengan tikus yang diberi etanol sebanyak 2 mL.
Pemberian etanol yang semakin banyak menyebabkan terjadinya proses penyerapan dan metabolisme etanol semakin cepat di dalam tubuh tikus sehingga kadar logam seng yang dihasilkan juga semakin banyak (Marchitti, et al., 2008). Semakin besar tubuh tikus maka semakin banyak kandungan air di dalam tubuh tikus karena hampir dua per tiga dari berat badan tikus terdiri dari air. Tingginya kandungan air menyebabkan konsentrasi etanol darah berkurang sehingga proses penyerapan etanol menjadi lebih cepat yang menyebabkan terjadi peningkatan kadar etanol dan kadar logam seng plasma didalam tubuh (Koivisto H., 2007).
|
bθ 1500 e U c2 1000 W) tΛ 500 "1 0 33 |
1292.5 1162.5 1175 1285 1140 762.5 732.5 K/ P0 422.5 487.5 427.5 —P1 I II III IV |
Pengulangan Pengukuran Kadar Logam Seng Plasma
Gambar 1. Kadar Logam Seng Plasma Tikus Kontrol dan Tikus yang diberi Etanol 40 %
Kelompok Tikus Kontrol dan Kelompok Tikus Pemberian Etanol
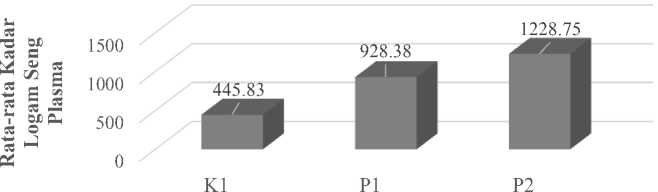
Gambar 2. Rata-rata Kadar Logam Seng Plasma Tikus Kontrol dan Tikus yang diberi Etanol 40 %
Gambar 2 menunjukan rata-rata kadar logam seng tilkus kontrol dan tikus yang diberi etanol. Kadar yang diberi etanol 40 % sebanyak 3 mL (P2) sebesar 1228,75 ± 80,00 mg/L dan standar deviasi 1228,75 ± 85,17 mg/L ; tikus yang diberi etanol 40 % sebanyak 2 mL (P1) sebesar 928,38 ±183,13 mg/L dan standar deviasi sebesar 928,38 ± 260,76 mg/L dan tikus kontrol (K1) sebesar 445,83 ± 27,76 mg/L dan standar deviasi sebesar 445,83 ± 36,1. Metabolisme etanol melibatkan alkohol dehidrogenase pada proses oksidasi menjadi asetaldehid. Alkohol dehidrogenase memiliki situs aktif berupa logam seng. Logam seng di dalam darah akan membentuk kompleks dengan kofaktor NAD+ sehingga logam seng akan berikatan dengan satu kofaktor NAD+ menjadi NADH. Jadi semakin banyak jumlah etanol yang diberikan akan menyebabkan peningkatan pada kadar logam seng plasma di dalam darah (Hoek and Pastorino, 2004)
Analisis Data Hasil Kadar Logam Seng Plasma Tikus
Data dianalisis ANOVA dengan SPSS kadar logam seng plasma pada tikus kontrol dan diberi etanol 40 % dengan volume 2 mL dan 3 mL.Tabel 1 menunjukkan nilai p < 0,05 maka H1 diterima. Hal ini menyatakan adanya perbedaan yang signifikan dengan terjadinya peningkatan kadar logam seng plasma tikus yang diberi etanol 40 % dengan volume etanol 3 mL dan 2 mL terhadap tikus kontrol. Uji Post Hoc Study dengan uji Tukey/HSD menunjukkan bahwa perbedaan yang bermakna pada kadar logam
seng plasma tikus kontrol dan diberi tikus yang diberi etanol memberikan nilai perbedaan yang paling signifikan pada kelompok tikus dengan pemberian etanol 40 %. Hal ini menunjukan terjadi peningkatan kadar logam seng plasma tikus yang diberi etanol dibandingankan pada tikus kontrol.
Penentuan dari aktivitas alkohol dehidrogenase plasma tikus
Gambar 3 menunjukkan aktivitas alkohol dehidrogenase tikus yang diberi etanol 40 % sebanyak 3 mL (P2) sebesar 17,05 ± 0,33 ng/mL dan standar deviasi sebesar 17,05 ± 0,48 ng/mL; kelompok tikus yang diberi etanol 40 % sebanyak 2 mL (P1) sebesar 18,69 ± 0,41 ng/mL dan standar deviasi sebesar 18,69 ± 0,43 ng/mL pada kelompok tikus kontrol (K1) dengan sebesar 21,00 ± 0,34 ng/mL dan standar deviasi sebesar 21,00 ± 0,44 ng/mL sehingga tingkat kesalahan pengerjan penelitian berkisar 0,02 -0,10 ng/mL
Volume etanol yang diberikan semakin banyak pada tikus maka meningkatkan kadar logam seng plasma dan menurunkan aktivitas alkohol dehidrogenase plasma tikus yang diberi etanol karena dalam proses metabolisme etanol terjadi peningkatan kadar ADH. Hal ini mengakibatkan reaksi sempurna etanol menjadi asetaldehid. Pada umumnya hasil pemberian etanol secara akut pada tikus dapat meningkatkan kadar ADH sebagai marker kerusakan awal pada hati tikus (Marchitti, et al., 2008).
Tabel 1. Analisis ANOVA dengan SPSS untuk Kadar Logam Seng Plasma Tikus Kontrol dan Tikus Diberi Etanol 40 % dengan Volume 2 mL dan 3 mL
|
Sum of Squares |
df |
Mean Square |
F |
Sig. | |
|
Between Groups |
1054348,532 |
2 |
527174,266 |
27,548 |
0,000 |
|
Within Groups |
153090,104 |
8 |
19136,263 | ||
|
Total |
1207438,636 |
10 |
25
20
Q
15
• 21.41
18.06
0-----
17.05
20.44
C17.71
18.84
10
5
0
I
II
21.16
■o19.03
18.81
-O
16.86
16.59
—•— P2
—•— Kontrol
P1
III
IV
Pengulangan Pengukuran Aktivitas ADH
Gambar 3. Aktivitas Alkohol Dehidrogenase pada Tikus Kontrol dan Tikus yang diberi Etanol 40 %
Tubuh memproduksi enzim ADH yang mengubah etanol menjadi asetaldehid dan mengubah asetaldehid menjadi asetat (Hoek et al., 2004; Lieber, 2005; Moon et al., 2007). Enzim ADH berperan dalam toleransi dan ketergantungan etanol baik pemecahan etanol menjadi asetaldehid dan asetaldehid menjadi asetat yang tidak beracun ( Seitz, et al.,.2001).
Keadaan mukosa lambung dan usus juga mempengaruhi proses penyerapan etanol di dalam tubuh tikus. Adanya jenis makanan tertentu dalam lambung saat dilakukan pemberian etanol mempengaruhi proses penyerapan etanol di dalam tubuh. Jumlah etanol yang diserap tergantung pada seberapa cepat lambung mampu mengosongkan isinya. Jika tikus yang diberi etanol diberi makan maka kecepatan etanol untuk diserap tubuh menjadi tiga kali lebih lambat daripada saat lambung yang kosong (Hoek and Pastorino, 2004).
Analisis Hasil Aktivitas Alkohol Dehidrogenase Plasma Tikus Wistar
Tabel 2 menunjukkan adanya penurunan aktivitas alkohol dehidrogenase plasma tikus yang diberi etanol. Pemberian etanol pada tikus memberikan pengaruh secara nyata (P < 0,05) maka nilai p < 0,05 maka H1 diterima untuk hasil
one way anova. Dengan nilai H1 yang diterima maka plasma darah tikus kontrol dan perlakuan menyatakan adanya perbedaan yang bermakna pada setiap aktivitas alkohol dehidrogenase plasma tikus dalam menurunkan aktivitas alkohol dehidrogenase plasma tikus yang diberi etanol.
Penurunan aktivitas alkohol dehidrogenase dengan signifikan adalah tikus yang diberi etanol 40 % sebanyak 3 mL (P2) dengan simpangan rata-rata sebesar 17,05 ± 0,33 dan standar deviasi adalah 17,05 ± 0,48; kelompok tikus yang diberi etanol 40 % sebanyak 2 mL (P1) dengan simpangan rata-rata 18,69 ± 0,41 dan standar deviasi sebesar 18,69 ± 0,43 pada kelompok tikus kontrol (K1) dengan simpangan rata-rata sebesar 21,00 ± 0,34 dan standar deviasi sebesar 21,00 ± 0,44. Hasil uji Tukey/HSD menunjukkan bahwa terjadi perbedaan yang bermakna pada aktivitas alkohol dehidrogenase plasma tikus kontrol dan kelompok perlakuan pemberian etanol dengan nilai perbedaan paling signifikan pada kelompok tikus dengan pemberian etanol 40 %. Hal ini menunjukan terjadinya penurunan aktivitas alkohol dehidrogenase plasma tikus yang diberi etanol 40 % dengan volume 2 mL dan 3 mL dibandingkan dengan tikus kontrol.
Tabel 2. Data ANOVA dengan SPSS Untuk Aktivitas Alkohol Dehidrogenase Plasma Tikus Kontrol dan Tikus yang Diberi Etanol 40 % dengan Volume 2 mL dan 3 mL
|
Sum of Squares |
df |
Mean Square |
F |
Sig. | |
|
Between Groups |
26,768 |
2 |
13,384 |
61,541 |
0,000 |
|
Within Groups |
1,740 |
8 |
0,217 | ||
|
Total |
28,508 |
10 |
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil dan pembahasan, maka dapat ditarik simpulan sebagai berikut : 1. Kadar logam seng plasma meningkat dengan pemberian etanol 40 % sebanyak 2 mL dan 3 mL
-
2. Aktivitas alkohol dehidrogenase plasma tikus menurun dengan pemberian etanol 40 % sebanyak volume 2 mL dan 3 mL.
Saran
Dalam penelitian ini perlu dilakukan pengukuran berat badan tikus sebagai satu parameter terkendali dalam penentuan kadar logam seng plasma darah. Pengambilan darah tikus tidak dilakukan pemberian pakan dan air minum dalam penentuan kadar logam seng plasma darah yang diberi etanol 40 % dengan volume 2 mL dan 3 mL
UCAPAN TERIMA KASIH
Pada kesepatan ini penulis mengucapkan terima kasih kepada Bapak Dewa Raka yang telah membantu dalam proses pengambilan sampel plasma darah tikus dan yang telah memberikan pengetahuan dan teknik - teknik dalam pengambilan sampel darah tikus pada aorta tikus.
DAFTAR PUSTAKA
Aquino, N., Forti, C.J., Zucolotto, V.,
Ciancaglini, P., and De Andrade, R.A., 2011, The Kinetic Behavior of Dehydrogenase Enzymes in Solution and Immobilized onto Nanostructured Carbon Platforms, Process
Biochemistry, 46(11) : 2347-2352
Hoek, J.B and Pastorino. J.G., 2004, Cellular Signaling Mechanisms in Alcohol-Induced Liver Damage, Semin. Liv. Dis. 24: 257-272
Katzung,BG., 2007, Basic and Clinical
Pharmacology ed 10th, The McGraw-Hill Companies.Inc, USA
Lienhardt, C., Fielding, K., Silah, JS., Bah, B., Gustafon, P., and Worndorff, D., Invertigation of the Risk Factors for Tubercolosis: A Case - Control Study in Three Countries in West Africa, Int J Epidemiol 2005(34): 914-923
Marchitti, S.A., Brocker, C., Stagos. D., and Vasiliou. V., 2008. Non-P450
Aldehyde Oxidizing Enzymes: The Aldehyde Dehydrogenase Superfamily, Expert Opin, Drug Metab, Toxicol, 4(7): 697-720.
Moon, K., Abdelmegeed. M.A., and Song B., 2007, Inactivation of Cytosolic Aldehid Dehydrogenase via Nitrosylation in Ethanol Exposed Rat Liver, FEBS Lett, 21(5): 3967-3972.
Panjaitan dan Ruqiah Ganda Putri., 2003, Bahaya Gagal Hamil yang diakibat Minuman Beralkohol., Program Pasca Sarjana IPB, Bogor.
Seitz, H.K., Matsuzaki. S., Yokohama. A., Hormann. N., Vakevainen. S., and Wang Xian Dong., 2001, Alcohol and Cancer. Alcoholisme: Clin. Exp. Res. 25: 137-143s.
Wright H., 1991, Effect of Alcohol on the Male Reproductive System, Alcohol Health & Research World Spring.
Zakhari Samir., 2006, Overview: How is Alkohol Metabolized by the Body, National Institute on Alcohol Abuse and Alcoholism (NIAAA) 5635, Fisher Lane, MSC 9304 Be
106
Discussion and feedback