SINTESIS NANOPARTIKEL PERAK (NPAg) MENGGUNAKAN EKSTRAK AIR DAUN KEMANGI (Ocimum Sanctum Linn.) DAN APLIKASINYA DALAM FOTODEGRADASI ZAT WARNA METILEN BIRU
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 7 Nomor 2, Oktober 2019

SINTESIS NANOPARTIKEL PERAK (NPAg) MENGGUNAKAN EKSTRAK AIR DAUN KEMANGI (Ocimum Sanctum Linn.) DAN APLIKASINYA DALAM FOTODEGRADASI ZAT WARNA METILEN
BIRU
Marsela Luruk Bere1, James Sibarani1.2, Manuntun Manurung1.2
-
1) Magister Kimia Terapan, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Denpasar-Bali, Indonesia
-
2) Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana, Jimbaran, Badung-Bali, Indonesia marsela_bere@yahoo.com
ABSTRAK: Penelitian ini bertujuan untuk mensintesis nanopartikel perak (NPAg) menggunakan ekstrak air daun kemangi (Ocimum Sanctum Linn.) yang digunakan sebagai katalis untuk fotodegradasi metilen biru. Ekstrak air daun kemangi mengandung senyawa flavonoid dan tanin yang berfungsi sebagai bioreduktor untuk mereduksi Ag+ menjadi Ag0 dan penstabil nanopartikel perak. Perbandingan volume ekstrak daun kemangi dengan volume larutan AgNO3 1 mM divariasikan sebesar 1:9, 2:8, 3:7, 4:6, 5:5 dan suhu sintesis juga divariasikan pada 25%, 40%, 50%, 60%. Keberhasilan sintesis dikonfirmasi dengan spektroskopi sinar tampak pada panjang gelombang 447 nm. Analisis nanopartikel perak (NPAg) dilakukan dengan Particle Size Analyser (PSA). Perbandingan volume optimum diperoleh pada perbandingan 2:8 dengan ukuran NPAg sebesar 70,19±0,89 nm. Degradasi metilen biru dilakukan pada kondisi optimum dimana volume nanopartikel sebesar 4 mL, pH 10 dan waktu fotodegradasi selama 3 jam. Fotodegradasi metilen biru pada kondisi optimum tersebut adalah sebesar 77,90% dari konsentrasi awal sebesar 200 ppm.
Kata Kunci: Nanopartikel perak, kemangi (Ocimum Sanctum Linn), fotodegradasi, metilen biru, bioreduktor.
ABSTRACK: Synthesis of silver nanoparticles (NPAg) used as catalysts for photodegradation of methylene blue was conducted using water extract of basil leaves (Ocimum Sanctum Linn.). The water extract of basil leaves contains flavonoids and tannins which function as bioreductors of Ag+ to Ago and stabilize silver nanoparticles. The volume ratio of basil leaf extract to solution of AgNO 3 1 mM were varied by 1: 9, 2: 8, 3: 7, 4: 6, 5: 5 and the synthesis temperature was also
varied at 25 %, 40 %, 50 %, 60 %. The success of the synthesis was confirmed by visible light spectroscopy at a wavelength of 447 nm. Analysis of silver nanoparticles (NPAg) was carried out with the Particle Size Analyzer (PSA). The optimum volume ratio was obtained at a ratio of 2: 8 with the NPAg size of 70.19 ± 0.89 nm. The optimum conditions for photodegradation of methylene blue were achieved at nanoparticle volume of 4 mL, pH of 10, and irradiation time of 3 hours. The photodegradation of methylene blue at these optimum conditions was 77.90% out of 200 ppm of mentylene blue solution.
Keywords: Silver nanoparticles, basil (Ocimum Sanctum Linn), photodegradation, methylene blue, bioreductor.
Kegiatan industri tekstil yang semakin berkembang menghasilkan produksi limbah cair berwarna dari
proses pencelupan ikut meningkat. Limbah cair berwarna, apabila dibuang langsung ke badan air penerima tanpa diolah terlebih dahulu dapat memberikan
dampak negatif terhadap ekosistem perairan [1]. Salah satu limbah cair ini yaitu metilen biru. Metililasi klorida atau metilen biru adalah senyawa kimia aromatik heterosiklik dengan rumus kimia [C16H18N3SCl] dan merupakan dye kationik dengan daya adsorpsi yang sangat kuat. Oleh karena itu, untuk mengurangi zat warna tersebut digunakan metode fotodegradasi berbasis “Green Chemistry”. Dalam fotodegradasi ini menggunakan nanopartikel logam sebagai katalis dan sinar UV [2,3].
Nanopartikel logam yang digunakan yaitu perak. Nanopartikel ini memiliki permukaan plasmon penyerapan di wilayah UV-VIS (SPR) [4]. Adanya Surface Plasmon Area (SPR) membuat nanopartikel perak dapat menyerap lebih banyak sinar sehingga menghasilkan banyak hole positif dan elektron. Kemudian membentuk radikal superoksida dan radikal hidroksil yang membantu menguraikan polutan organik menjadi zat yang aman bagi lingkungan [5].
Nanopartikel perak disintesis menggunakan tanaman kemangi [6]. Kemangi mengandung senyawa alkoloid, saponin, flavonoid, triterpenoid, steroid, dan tanin yang diperkirakan membantu proses sintesis nanopartikel perak [7]. Fenolik seperti flavonoid dan tanin memiliki gugus hidroksil (OH), dan karbonil (CO) yang dapat mengikat logam [8]. Gugus fungsi ini bekerja dengan cara mendonorkan elektron ke ion Ag+ untuk menghasilkan Ag partikel-nano [9], dan sebagai agen stabilisasi untuk mencegah aglomerasi dalam media berair [10] (Gambar 1). Oleh karena itu, dilakukan penelitian tentang nanopartikel perak yang disintesis menggunakan daun kemangi dan diaplikasikan sebagai fotokatalis dalam degradasi zat warna metilen biru.
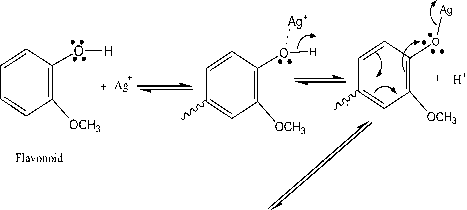
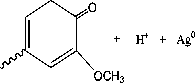
Gambar 1. Mekanisme pembentukan
nanopartikel perak oleh flavonoid [11].
Bahan yang digunakan dalam penelitian ini adalah daun kemangi (Ocimum Sanctum Linn.) diambil dari dusun Toleon desa Umanen Lawalu Nusa Tenggara Timur, padatan FeCl3 analis p.a., serbuk Mg, etanol 70%, padatan KI p.a, padatan I2 teknis, larutan HCl 37%, padatan AgNO3 p.a, padatan NaOH p.a, padatan metilen biru dibeli dari toko zat warna.
Alat yang digunakan dalam penelitian ini adalah neraca analitik, kertas Whatman No.1, pengaduk magnetik, pemanas magnetic, pH meter, sentrifugasi, peralatan gelas kimia, spektrofotometer UV-VIS merk Biochrom dan Particle Size Analyzer (PSA) merk Malvern serial MAL/165275.
Pembuatan serbuk daun kemangi
Daun kemangi segar sebanyak 340,194 gram dikeringkan dengan diangin-anginkan pada suhu kamar. Daun yang telah kering ditimbang lagi untuk mengetahui kadar air akhir. Setelah itu dipotong kecil-kecil kemudian dihaluskan dengan tumbukan tradisional [10].
Pembuatan ekstrak air daun kemangi
Sebanyak 3,2321 gram serbuk daun kemangi, dicampur dengan 400 mL aquades. Campuran ini dipanaskan pada
suhu 60 oC selama 15 menit [12]. Setelah itu didinginkan pada suhu ruang dan disaring dengan kertas Whatman No.1. Ekstrak air daun kemangi digunakan untuk proses sintesis nanopartikel perak (NPAg) dan skrining fitokimia. Apabila ekstrak ini tidak digunakan maka perlu disimpan pada suhu 4C [13].
Skrining fitokimia
Ekstrak air daun kemangi digunakan untuk menguji kandungan senyawa Alkaloid dengan pereaksi Wagner, Flavonoid, Tanin [14].
Sintesis nanopartikel perak
Sintesis NPAg dilakukan dengan variasi perbandingan volume ekstrak daun kemangi dengan larutan AgNO3 1 m yaitu 1:9, 2:8, 3:7, 4:6, 5:5. Variasi ini diberi perlakuan suhu 25 C, 40C, 50C, 60°C dan penyimpanan selama 1-5 hari. Perbandingan volume, suhu dan waktu di analisis dengan spektrofotometer UV-VIS dengan panang gelombang 200-800 nm [10].
Penentuan ukuran nanopartikel perak dengan Particle Size Analyser
Sebanyak 15 mL nanopartikel perak diencerkan dengan menambahkan 10 mL akuabides. Hasil pengenceran dipipet lalu dimasukan ke dalam cell setinggi 2 cm dan diukur ukuran nanopartikel perak menggunakan Particle Size Analyser (PSA) sebanyak 3 kali pengukuran.
Penentuan jumlah optimum Nanopartikel perak
Diambil 11 labu erlemeyer 100 mL masing-masing diisi dengan 50 mL metilen biru 50 ppm dan ditambahkan larutan nanopartikel perak volume dari 010 mL. Suspensi diradiasi dengan lampu UV selama 5 jam sambil diaduk dengan pengaduk magnetik [15]. Setelah di irradiasi, suspensi disaring dan absorbansi filtratnya diukur dengan spektrofotometer UV-VIS pada panjang
gelombang 664 nm. Selanjutnya dihitung nilai persentase degradasi dengan Rumus 1:
Kadar degradasi (%) = (C ° C) x 100% ...(1)
Penentuan pH optimum
Diambil 8 labu erlemyer 100 mL masing-masing diisi dengan 50 mL metilen biru 50 ppm dan sejumlah nanopartikel perak optimum, dan diatur pH-nya yaitu pH 3, 4, 7, 8, 10, 11 dengan menambahkan larutan HCl 0,01 M untuk pH asam dan NaOH 0,5 M untuk pH basa lalu diukur dengan pH meter. Suspensi diradiasi dengan sinar ultraviolet selama 5 jam sambil diaduk dengan pengaduk magnetik. Setelah di irradiasi, suspensi disaring dan absorbansi filtratnya diukur dengan spektrofotometer UV-VIS pada panjang gelombang 664 nm. Selanjutnya dihitung persentase degradasi dengan Rumus 1.
Penentuan waktu optimum
Diambil 6 buah labu erlemeyer 100 mL masing-masing diisi dengan 50 mL metilen biru 50 ppm, sejumlah nanopartikel perak optimum dan diatur pH pada pH optimum. Suspensi diradiasi dengan sinar UV masing-masing selama 1-6 jam sambil diaduk dengan pengaduk magnetik. Setelah di irridiasi, suspensi disaring dan absorbansi filtratnya diukur dengan spektrofotometer UV-VIS pada panjang gelombang 664 nm. Selanjutnya dihitung nilai persentase degradasi dengan Rumus 1.
Fotodegradasi metilen biru
Diambil 4 buah labu erlemeyer 100 mL masing-masing diisi dengan 50 mL metilen biru dengan variasi konsentrasi 50-300ppm, ditambahkan sejumlah nanopartikel perak optimum dan larutan diatur pada pH optimum. Suspensi diradiasi dengan sinar UV selama waktu optimum sambil diaduk dengan pengaduk magnetik. Setelah di irradiasi, suspensi disaring dan absorbansi filtratnya diukur
Tabel 1. Hasil Pemeriksaan Fitokimia Ekstrak Daun Kemangi (Ocimum Sanctum Linn.)
|
Senyawa |
Pereaksi |
Persyaratan |
Hasil |
Keterangan |
|
Alkaloid |
Wagner |
Adanya endapan coklat kemerahan |
Coklat dan tidak terbentuk endapan |
(-) |
|
Tanin |
FeCl3 |
Hijau kehitaman/biru kehitaman/biru |
hijau kehitaman |
(+) |
|
Flavonoid |
Mg + HCl |
Merah bata |
Merah bata |
(+) |
Keterangan : (+) : terkandung senyawa
(-) : tidak terkandung senyawa
A B
3,00
2,50
2,00
1,50
1,00
0,50
0,00
380 420 460 500 540 580 620 660 700 740 7
Panjang Gelombang
3,00
0,00
2,50
2,00
1,50
1,00
380 420 460 500 540 580 620 660 700 74
Panjang Gelombang
D
C
380 420 460 500 540 580 620 660 700 740 78
Panjang Gelombang
3,00
2,50
2,00
1,50
1,00
0,50
0,00
380 420 460 500 540 580 620 660 700 74
Panjang Gelombang
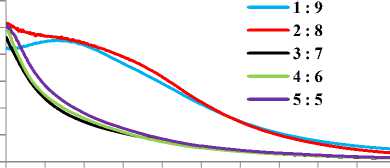
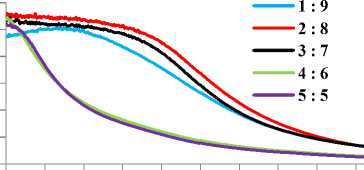
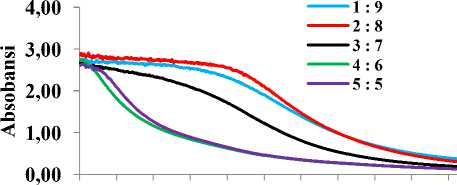
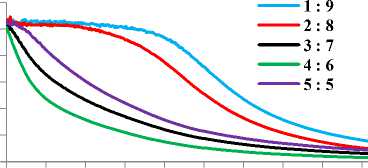
Gambar 2. Spektrum UV-VIS NPAg pada perbandingan volume ekstrak dengan larutan AgNO3
1 mM yang sintesis pada suhu 25oC (A), 40oC (B), 50oC (C) dan 60oC (D).
dengan spektrofotometer UV-VIS pada panjang gelombang 664 nm. Selanjutnya dihitung nilai persentase degradasi dengan Rumus 1.
-
3. HASIL DAN PEMBAHASAN
-
3.1 Skrining fitokimia
-
Uji pendahuluan dilakukan untuk mengetahui kandungan kimia dari ekstrak air daun kemangi (Ocimum Sanctum Linn.). Hasil uji ini dapat dilihat pada Tabel 1.
Nanopartikel perak dengan suhu 25oC, 40oC, 50oC, 60oC pada perbandi-
C
A
380 430 480 530 580 630 680
Panjang Gelombang(nm)
380 430 480 530 580 630 680
Panjang Gelombang (nm)
3,00
2,50
2,00
1,50
1,00
0,50
0,00
380 430 480 530 580 630 680
Panjang Gelombang (nm)
D
Panjang Gelombang (nm)
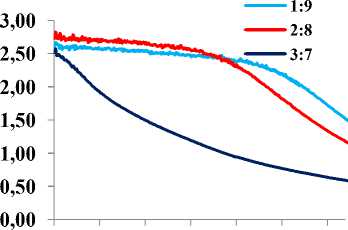
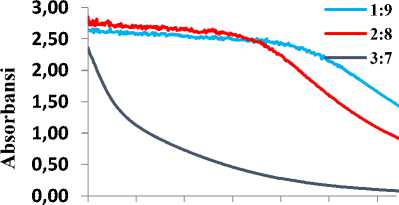
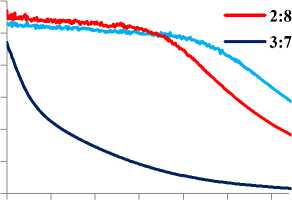
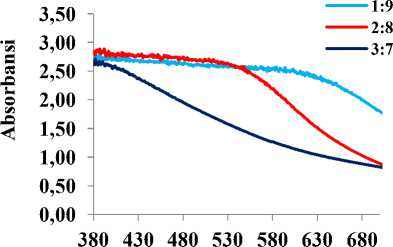
Gambar 3. Spektrum UV-VIS NPAg pada perbandingan volume ekstrak dengan larutan AgNO3 1 mM yang bervariasi diukur pada hari ke-2 (A), ke-3 (B), ke-4 (C), ke-5 (D).
ngan volume 1:9, 2:8 dan suhu 40oC pada perbandingan volume 3:7 warnanya merah kecoklatan selama proses sintesis yang membuktikan terbentuknya nanopartikel perak [16]. Oleh karena itu, dapat dikatakan bahwa perbandingan volume 1:9 dan 2:8 pada suhu 25C, 50oC, 60C dan 3:7 pada suhu 40C terbentuk nanopartikel perak. Indikasi terbentuknya nanopartikel dengan perubahan warna dibuktikan dengan menggunakan spektrofotometer UV-VIS. Hasil analisis dari variasi perbandingan volume ekstrak air daun kemangi dan larutan AgNO3 1 mM memberikan puncak serapan pada kisaran 445-447 nm. Serapan ini merupakan karakteristik yang khas dari nanopartikel perak dengan panjang gelombang 400-450 nm [17] seperti
terlihat pada Gambar 2. Selain itu, nanopartikel perak yang terbentuk ini dapat ditentukan jumlahnya dari nilai absorbansi [3]. Dari data variasi perbandingan volume didapatkan perbandingan 2:8 memiliki nilai absorbansi tertinggi yang menunjukan bahwa banyaknya jumlah nanopartikel perak yang terbentuk.
Kestabilan nanopartikel perak selama 1-5 hari memberikan puncak serapan dengan kisaran 445-447 nm (Gambar 3). Panjang gelombang tersebut masih dalam rentang krakteristik SPR dari nanopartikel perak sehingga dikatakan bahwa nanopartikel tersebut masih stabil karena tidak terjadi pergeseran puncak
serapan ke panjang gelombang yang lebih besar [18], dan panjang gelombang tersebut tidak mengalami penurunan intensitas serapan pada kisaran 380-400 nm sebagai indikasi bahwa nanopartikel perak belum terbentuk dan masih dalam bentuk ion perak [19].
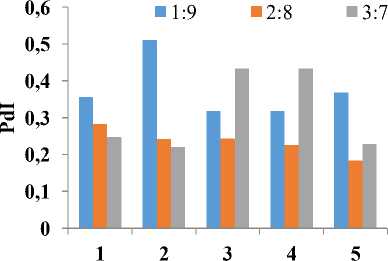
perak pada perbandingan volume 1:9 yang terbentuk tidak seragam karena nilai PdI>0,5. Sedangkan nanopartikel perak pada perbandingan volume 2:8, 3:7, 4:6, 5:5 yang terbentuk lebih seragam. Perbandingan ini walaupun secara ukuran nanopartikel perak lebih besar dibandingkan perbandingan 1:9.
Waktu (Hari)
Perbandingan Volume Ekstrak Terhadap Larutan AgNO3 1 mM
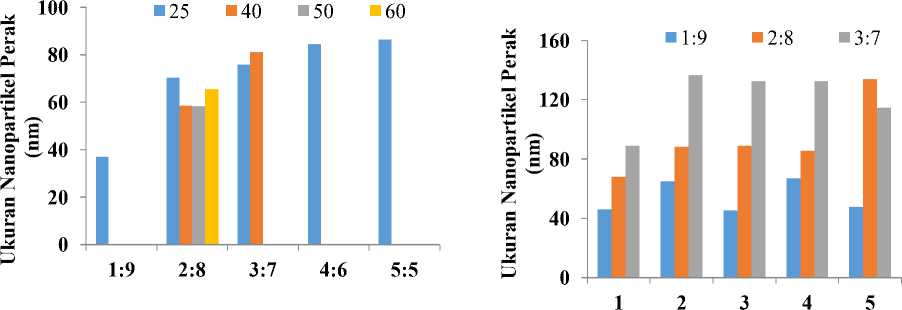
Gambar 4. Pengaruh perbandingan volume terhadap ukuran NPAg pada suhu 25 T, 40C, 50oC, 60T.
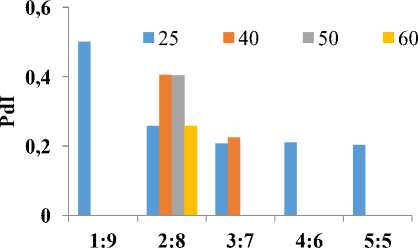
Perbandingan Volume Ekstrak Terhadap Larutan AgNO3 1 mM
Gambar 5. Pengaruh perbandingan volume terhadap PdI pada suhu 250C, 40T, 50oC, 60C.
Nanopartikel perak yang disintesis pada suhu (T) tertentu menghasilkan ukuran dan distribusi ukuran
(Polydispersity Index, PdI) yang berbeda-beda (Gambar 4 dan 5). Nanopartikel
Gambar 6. Pengaruh waktu terhadap ukuran nanopartikel perak pada suhu 25 °C.
Waktu (Hari)
Gambar 7. Pengaruh waktu terhadap PDI pada suhu 25C.
Nanopartikel perak yang dibentuk pada suhu 40oC, 50T, 60T memiliki ukuran lebih kecil dari 100 nm pada perbandingan volume 2:8. Hal yang sama juga dilaporkan oleh Ayu [20] yang mensintesis nanopartikel perak menggunakan ekstrak bungkil biji jarak dimana dengan suhu yang semakin tinggi ukuran nanopartikel perak yang dibentuk makin kecil. Dari hasil penelitian, ukuran
nanopartikel makin kecil seiring bertambahnya suhu namun pada suhu ke 60°C terjadi peningkatan ukuran nanopartikel. Hal ini mungkin disebabkan karena pada suhu ini sebagian dari senyawa penstabil mengalami kerusakan.
Senyawa flavonoid dan tanin selain sebagai reduktor, juga bisa sebagai penstabil karena memiliki gugus fungsi hidroksil (-OH) dan karbonil (-CO) yang berinteraksi dengan partikel perak membentuk lapisan electric double layer. Hasil interaksi ini membentuk lapisan rangkap listrik pada permukaan partikel perak yang menyebabkan partikel yang satu dengan yang lain saling bertolakan dan tidak terbentuk aglomerasi. Kestabilan diukur dari penyimpanan selama 1-5 hari dengan ukuran nanopartikel perak dan PdI dapat dilihat pada Gambar 6 dan Gambar 7. Semakin tinggi konsentrasi dari senyawa penstabil ini akan menghasilkan ukuran partikel yang semakin kecil [6].
Penggunaan NPAg sebagai katalis pada reaksi fotodegradasi metilen biru diawali dengan penyinaran dengan sinar UV terhadap NPAg sehingga elektron pada katalis tersebut tereksitasi dari pita valensi ke pita konduksi dan meninggalkan hole positif pada pita valensi. Elektron pada pita konduksi akan bereaksi dengan oksigen membentuk ion radikal superoksida O2-•, sedangkan hole pada pita valensi bereaksi dengan ion hidroksi (OH-) membentuk radikal hidroksida (OH•) yang akan mendegradasi struktur metilen biru [20]. Pengaruh jumlah volume nanopartikel perak terhadap persen degradasi metilen biru diamati pada Gambar 8. Degradasi metilen biru meningkat seiring bertambahnya volume
nanopartikel perak (NPAg) yang ditambahkan hingga jumlah optimumnya yaitu 4 mL dimana persen degradasinya adalah sebesar 87,72%.
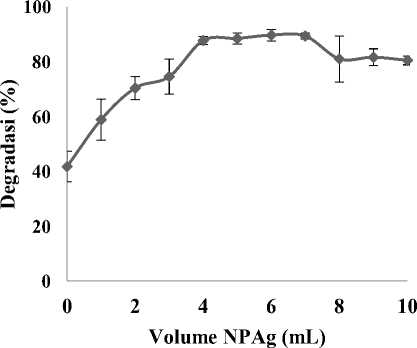
Gambar 8. Pengaruh volume NPAg terhadap persen degradasi MB
100
80
60
40
0

2 4 6 8 10 12
pH
Gambar 9. Pengaruh pH larutan terhadap persen degradasi MB
Optimasi pH
Pengaruh pH terhadap persen degradasi metilen biru diamati pada rentang pH 3 sampai 11 dengan waktu irradiasi selama 5 jam (Gambar 9). Data menunjukkan bahwa pH optimum untuk proses fotodegradasi metilen biru menggunakan NPAg ini adalah pH 10 dengan persen degradasi sebesar
92,38%. Hal ini mengindikasikan bahwa semakin tinggi konsentrasi ion hidroksil (OH-) maka konsentrasi radikal hidroksil (OH *) akan meningkat. Radikal ini yang
akan berperan mendegradasi zat warna metilen biru. Selain itu, elektron juga akan bereaksi dengan oksigen yang terlarut membentuk radikal superoksida yang membantu mendegradasi metilen biru.
Optimasi Waktu Irradiasi
Pengaruh waktu radiasi terhadap persen degradasi metilen biru diamati pada Gambar 10. Hasil ini menunjukan bahwa peningkatan persen degradasi seiring bertambah waktu namun penyinaran di atas 4 jam tidak memberikan peningkatan persen degradasi sebesar peningkatan persen degradasi 2 ke 3 jam sehingga waktu optimum dari penyinaran tersebut adalah 3 jam dengan persen degradasinya 95,77%. Peningkatan tersebut terjadi karena pengaruh radiasi sinar UV yang terus bertambah, sehingga foton yang mengenai nanopartikel perak akan semakin banyak akibatnya pembentukan radikal hidroksida (OH•) makin meningkat.
100
80

ft ■a ft
bi
60
40
20
0
0
2 4 6
Waktu Radiasi (Jam)
Gambar 10. Pengaruh waktu radiasi terhadap persen degradasi MB
Efektivitas nanopartikel perak
Efektifitas fotodegradasi metilen biru dilakukan dengan variasi konsentrasi metilen biru seperti terlihat pada Tabel 2. Efektivitas nanopartikel perak (NPAg) dalam mendegradasi zat warna metilen biru dapat dilihat dari kemampuan menurunkan konsentrasi zat warna metilen biru dalam waktu radiasi optimum 3 jam. Efektifitas nanopartikel perak dalam mendegradasi metilen biru dilakukan pada beberapa variasi konsentrasi metilen biru. Variasi konsentrasi metilen biru yang paling sedikit terdegradasi adalah 50 ppm sebanyak 4,693 mg sedangkan konsentrasi metilen biru yang paling banyak terdegradasi adalah 200 ppm sebanyak 15,580 mg. Sehingga disimpulkan bahwa nanopartikel perak mampu mendegradasi metilen biru pada konsentrasi konsentrasi 200 ppm.
Sintesis nanopartikel perak (NPAg) telah berhasil dilakukan dengan mencampurkan ekstrak air daun kemangi dan larutan AgNO3 1 mM dengan perbandingan volume 2:8. Ukuran nanopartikel yang diperoleh adalah 70,19±0,8855 nm dengan kestabilan yang baik. Penggunaan nanopartikel perak mampu mendegradasi konsentrasi metilen biru sebesar 77,90% dari 200 ppm dengan lama penyinaran selama 3 jam.
Tabel 2. Efektifitas Fotodegradasi dari 50 mL Larutan Metilen Biru dengan Variasi Konsentrasi
|
Konsentasi Awal Metilen Biru (ppm) |
Persen degradasi rata-rata (%) |
SD |
Banyaknya MB yang terdegradasi (mg/1 L sampel) |
|
50 |
93,86 |
1,190 |
4,693 |
|
100 |
83,69 |
1,188 |
8,369 |
|
200 |
77,90 |
6,686 |
15,580 |
|
300 |
44,45 |
8,728 |
13,335 |
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada Ibu Wiji Rahayu, S.Si dari PT. DKSH Jakarta yang memfasilitasi pengukuran ukuran NPAg dengan PSA. Ucapan terima kasih juga diberikan kepada Ni Made Puspawati, M.Phil., PhD, Dr. Ida Ayu Gede Widihati, S.Si., M.Si. dan Dr. I Gusti Ayu Kunti Sri Panca Dewi, M.Si yang telah memberikan masukan serta kritikan demi kesempurnaan penulisan artikel ini.
-
[1] Gustiana, S., Notodarmodjo, S., Syafila, M., Radimah, L.C. 2014. DekolorasiFotokatalik Zat Warna Remazol Black 5 Dengan
Menggunakan Nanopartikel TiO2 dan Ag yang Terimmobilisasi pada Nanofiber Selulosa Bakterial (SB). Arena Tekstil 29(2): 107-114.
-
[2] Wijaya, K., Sugiharto, E., Fatimah, I., Sudiono, S., Kurniaysih, D. 2006. Utilisasi TiO2- Zeolit dan Sinar UV untuk Fotodegradasi Zat Warna Cango Red. Berkala MIPA 3: 27-35.
-
[3] Haryani, Y., Kartika, F.G., Yuharmen, Putri, M.E., Alchalish, T.D., Melanie, Y. 2016. Pemanfaatan Ekstrak Air Rimpang Jahe Merah (Zingiber
Officinale Linn Varrubrum) pada
Biosintesis Sederhana Nanopartikel Perak. Chemica et Natura Acta 4(3): 151-155.
-
[4] Sharma, V.K., Yhgard, R.A., Lin, Y. 2009. Silver Nanoparticles: Green Synthesis and their antimicrobial activities. Advances in Colloid and Interface Science 145(9): 83-96.
-
[5] Tang, C. dan Chen, V. 2004. The Photocatalytic Degradation of Reactive Black 5 Using TiO2/UV in An Annular Photoreactor. Water Research 38: 2775-2781.
-
[6] Mallikarjuna, K., Narasimha, G., Dillip, G.R., Praveen, B., Shreedhar, B., Lakshmi, C.S., Reddy, B.V.S.,
Raju, B.D.P. 2011. Green Synthesis of Silver Nanoparticles Using Ocimum Leaf Extract and Their
Characterization. Digest Journal of Nanomaterials and Biostructures 6(1): 181-186.
-
[7] Angelina, M., Turnip, M., Khotimah, S. 2015. Ujian Aktivitas Antibakteri Ekstrak Etanol Daun
Kemangi(Ocimum Sanctum L.)
Terhadap Pertumbuhan Bakteri Escherichia Coli dan Staphylococcus Aureus. Protobiont 4(1): 184-189.
-
[8] Michalak, A. 2006. Phenolic Compound and Their Antioxidant Activity in Plants Growing under Heavy Metal Stress. Polis Journal of Enviroumental Study 15(4): 523-530.
-
[9] Masakke, Y., Sulfikar, Rasyid, M. 2015. Biosintesis Partikel-nano Perak Menggunakan Ekstrak Metanol Daun Manggis (Garcinia Mangostana L.). Jurnal Sainsmat IV(1): 28-41.
-
[10] Awwad, M.A., Salem, M.N., Abdeen O.A. 2013. Green Synthesis of Silver Nanoparticles Using Carob Leaf Extract and Its Antibacterial Activity. International Journal of Industrial Chemsitry 4: 1-6.
-
[11] Zakir, M., Maming, Lembang, Y.E., Lembang, S.M. 2014. Synthesis of Silver and Gold Nanoparticles
Through Reduction of Ketapang
(Terminalia Catappa). Presents in the International Conference on
Advanced Material and Partical
Nanotechnology: 1-9.
-
[12] Tapa, L.F., Suryanto, E., Momuat, I.L. 2016. Biosintesis Nanopartikel Perak Menggunakan Ekstrak Empelur Batang Sagu Baruk (Arenga
Microcarpha) dan Aktivitas
Antioksidannya. Chem.Prog 9(1): 915.
-
[13] Maryani, D., Firdaus, L.M., Nurhamidah. 2017. Biosintesis Nanopartikel Perak Menggunakan
Ekstrak Buah Markisa
(PassifbraFlavicarva) untuk
Mendeteksi Logam Berat. Jurnal
Pendidikan dan Ilmu Kimia 1(1): 4954.
-
[14] Sopianti, S.D. dan Sary, W.D. 2018. Skrining Fitokimia dan Profil KLT Metabolit Sekunder dari Daun Ruku-ruku (Ocimum Tenolflorum L.) dan Daun Kemangi (Ocimum Sanctum L.). Scientia8(1): 44-52.
-
[15] Diantariani, P.N., Widihati, G.A.I., Megasari, R.A.A.G.I. 2014.
FotodegradasiMetilen Biru dengan Sinar Ultarviolet dan Katalis ZnO. Jurnal Kimia 8(1): 137-143.
-
[16] Bar, H., Bhui, Kr.D., Sahoo, P.G., Sarkar, P., Pyne, S., Misra, A. 2009. Green Synthesis of Silver Nanoparticles Using Seed Extract of JatrophaCurcas. Colloids and
Surfaces a Physicochemical and Engineering Aspects 348: 212-216.
-
[17] Solomon, S.D.M., Bahadory, A.V., Jeyarajasingam, S.A., Rutkowsky, C., Borits. 2007. Synthesis and Study of Silver Nanoparticles. Journal of Chemical Education 84(2): 322-325.
-
[18] Pinto, V.V., Ferreira, M.J., Silva, R., Santus, H.A., Silva, F., Pereira, C.M. 2010. Long Time Effect on the Stability of Silver Nanoparticles in Aqueous Medium: Effect of the Synthesis and Stronge Condition, Colloids Surf. A: Physicochem. Eng. Aspects 364: 19-25.
-
[19] Gunsolus, I.L., Mousavi, M.P.S., Hussein, K., Buhlmann, P., Haynes, C.L. 2015. Effect of Humic and Funic Acids on Silver Nanoparticles Stability, Dissolution and Toxicity. Environ Sci. Technol. 49: 8078-8086.
-
[20] Ayu, H. 2015. “Kinetika Sintesis Nanopartikel Perak dari Larutan AgNO3 dengan Menggunakan Ekstrak Bungkil Biji Jarak Pagar
(JatrophaCuras L.) sebagai Reduktor” (Tesis). Bogor: Institut Pertanian
Bogor.
-
[21] Attia, A.J., Kadhim, S.H., Hussen, F.H. 2007. Photocataliytc Degradation of Textile Dyeing Wastewater Using Titanium Dioxide and Zin Oxide. EJournal of Chemistry 2: 219-223.
164
Discussion and feedback