CANGKANG KERANG DARAH (Anadara granosa) ASAL PULAU LEMBATA-NTT SEBAGAI SUMBER KALSIUM PADA PEMBUATAN BIOMATERIAL HIDROKSIAPATIT (HAp) DENGAN METODE PRESIPITASI
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 11, Nomor 2, Oktober 2023

CANGKANG KERANG DARAH (Anadara granosa) ASAL PULAU LEMBATA-NTT SEBAGAI SUMBER KALSIUM PADA PEMBUATAN
BIOMATERIAL HIDROKSIAPATIT (HAp) DENGAN METODE
PRESIPITASI
Yulius Dala Ngapa1 dan Jumilah Gago2
-
1 Program Studi Pendidikan Fisika, Fakultas Keguruan dan Ilmu Pendidikan, Universitas Flores Jln Sam Ratulangi No. XX Ende – Flores, NTT Kode Pos 86319 ydalangapa@gmail.com
-
2 Program Studi Pendidikan Biologi, Fakultas Keguruan dan Ilmu Pendidikan, Universitas Flores Jln Sam Ratulangi No. XX Ende – Flores, NTT Kode Pos 86319
ABSTRAK: Kerang darah (Anadara granosa) merupakan sumber daya alam potensial di pulau Lembata provinsi Nusa Tenggara Timur. Penangkapan kerang darah yang berlangsung sepanjang tahun menghasilkan dampak negatif berupa limbah cangkang yang belum dikelola secara maksimal. Cangkang kerang darah mengandung kalsium tinggi yang berpotensi untuk dimanfaatkan sebagai prekursor kalsium dalam sintesis hidroksiapatit (HAp). Kandungan kalisum dalam cangkang spesies ini mencapai 44,57%. Metode yang digunakan dalam sintesis HAp ini ialah metode presipitasi, dengan mereaksikan Ca(OH)2 dari sampel cangkang kerang darah dan (NH4)2HPO4 sebagai sumber prekursor fosfat. Berdasarkan hasil spektrum difraksi sinar–X, kristalinitas HAp yang diperoleh sebesar 90,15%. Dari analisis gugus fungsi menggunakan spektrum inframerah transformasi Fourier diperoleh gugus fungsi OH-, PO43-, dan CO32- dalam senyawa HAp. Analisis berdasarkan mikroskop elektron pemayaran menunjukkan bahwa HAp memiliki bentuk bulat yang seragam.
Kata kunci: Biomaterial; hidroksiapatit; kerang darah; presipitasi; pulau Lembata.
ABSTRACT: Blood clam (Anadara granosa) is a potential natural resource on Lembata Island, East Nusa Tenggara province. Catching blood clams that take place throughout the year has a negative impact in the form of shell waste that has not been managed optimally. Blood clam shells contain high calcium which has the potential to be utilized as a calcium precursor in the synthesis of hydroxyapatite (HAp). The calcium content in the shells of this species reaches 44.57%. The method used in the synthesis of HAp is the precipitation method, by reacting Ca(OH)2 from shell samples blood clam and (NH4)2HPO4 as a source of phosphate precursor.Based on the results of the X-ray diffraction spectrum, the crystallinity of the HAp obtained was 90.15%. From the functional group analysis using the Fourier transform infrared spectrum, the functional groups OH-, PO43-, and CO32- were obtained in HAp compounds. Analysis based on scanning electron microscopy showed that HAp has a uniform spherical shape.
Keywords: Biomaterials; hydroxyapatite; blood clams; precipitation; Lembata island.
Perkembangan penelitian biomaterial pengganti tulang telah memberikan manfaat yang besar dalam dunia kesehatan terutama dalam bidang kedokteran gigi dan ortopedi
-
[1] . Hal ini disebabkan pengaplikasian biomaterial bersifat efektif karena mempunyai sifat yang sama dengan materi sintesis yang biokompatibel, tidak mengandung racun, serta sesuai dengan
jaringan tubuh manusia sehingga tidak menimbulkan efek samping terhadap tubuh. Selain itu, bahan utamanya berasal dari pemanfaatan material berbahan dasar alami dan limbah dimana ketersediaannya melimpah di lingkungan sekitar [2]. Biomaterial bermanfaat sebagai material sintesis yang baik digunakan sebagai bahan dalam merangsang proses remodeling dan regenerasi untuk tulang, gigi, dan jaringan kerangka yang rusak dan hilang melalui proses pencangkokan atau implantasi [3].
Hidroksiapatit (HAp) merupakan salah satu biomaterial yang banyak disintesis untuk tujuan tersebut. Hidroksiapatit adalah senyawa kalsium fosfat dengan rumus kimia Ca10(PO4)6(OH)2 yang memiliki kemiripan struktur dengan komponen mineral pembentukan tulang dan gigi Selain itu, hidroksiapatit memiliki fase kristal dari senyawa kalsium fosfat yang bersifat paling stabil [4]. HAp telah banyak dimanfaatkan sebagai bahan regenerasi tulang dan implan biomedik karena keunggulan yang dimilikinya antara lain: biokompatibel, osteokonduktif, dan bioaktif [5]. Biokompatibel artinya mampu bertahan terhadap korosi dan tidak mengalami penolakan oleh jaringan tubuh. Osteokonduktif, yaitu memiliki kemampuan untuk mendukung pertumbuhan dan pembentukan jaringan tulang sedangkan bioaktif artinya mampu merangsang pertumbuhan tulang di sekitar implan [6].
Proses pembuatan hidroksiapatit dapat bersumber dari kalsium sintetik maupun alami [7]. Sintesis HAp dari sumber bahan kimia murni menggunakan biaya yang cukup mahal dan penyediaan bahan yang cukup sulit . Harga hidoksiapatit sekitar Rp 300.000/gram dan menurut data BPPT (Badan Pengkajian dan Penerapan Teknologi) harga hidroksiapatit sintetik merupakan 1 juta rupiah per gram dan diimpor dari Jepang dan ketersediannya bergantung berdasarkan produk luar negeri atau impor [8]. Oleh karena itu, dibutuhkan sumber kalsium dari material alami yang dapat digunakan sebagai bahan dasar
pembuatan hidroksiapatit. Beberapa bahan yang dapat digunakan untuk menyintesis HAp adalah berbagai jenis kerang seperti cangkang keong sawah [9], kerang hijau [10], kerang kepah [11], kerang lokan [12].
Penelitian ini menggunakan cangkang kerang darah (Anadara granosa) yang banyak tersebar di pesisir pantai pulau Lembata, Nusa Tenggara Timur. Selama ini, cangkang kerang darah terbuang percuma sehingga berpotensi sebagai limbah yang dapat mencemari lingkungan. Kandungan kalsium karbonat (CaCO3) pada cangkang kerang darah sekitar 98% sehingga dapat digunakan sebagai sumber kalsium pada sintesis hidroksiapatit. Tingginya kalsium dalam cangkang memberi peluang inovasi untuk menggantikan produksi HAp dari bahan baku yang biayanya relatif tinggi serta upaya untuk mengoptimalkan nilai ekonomis dan manfaat bagi kehidupan. Metode sintesis HAp yang umum digunakan adalah metode presipitasi, metode hidrotermal, metode hidrolisis, dan metode sol-gel [13]. Perbedaan pemilihan metode sintesis yang digunakan akan memengaruhi karakter dan kualitas hidroksiapatit yang dihasilkan [14]. Presipitasi adalah metode yang banyak digunakan karena penggunaannya yang mudah, reaksi yang sederhana, hasil samping berupa air dan penggunaan pelarut yang tidak terlalu mahal.
Berdasarkan pada uraian sebelumnya, maka dilakukan penelitian sintesis HAp dan penciriannya dimana sumber utama kalsium berasal dari cangkang kerang darah yang berasal dari pesisir pantai pulau Lembata menggunakan metode presipitasi. Pencirian dilakukan dengan menggunakan difraktometer sinar-X (XRD) untuk mengetahui fase dan kristalinitas dari senyawa tersebut dan spektrofotometer inframerah transformasi Fourier (FTIR) untuk mengetahui gugus fungsi. Selain itu, digunakan juga mikroskop elektron payaran (SEM) untuk melihat morfologi permukaan HAp. Hasil penelitian ini diharapkan dapat menjadikan cangkang kerang darah pulau
Lembata sebagai salah satu sumber alternatif kalsium untuk pembentukan HAp.
Bahan-bahan yang digunakan cangkang kerang darah yang berasal dari pulau Lembata propinsi Nusa Tenggara Timur, (NH4)2HPO4, akuades, kromat sulfat, stronsium, indikator pH universal, dan kertas saring. Peralatan yang di digunakan adalah peralatan gelas, pengaduk magnetik, oven, sentrifugasi, penyaring vakum, neraca analitik, tanur, sonikator, mesin penggiling, mortar, penangas air, termometer, blender, saringan 100 mesh, SSA (Spektrofotometer Serapan Atom) (Shimazu AA700), XRD (Shimadzu tipe 7000), FTIR (Shimadzu tipe 21), dan SEM Carl-Zeiss Bruker EVO MA10.
Penelitian terdiri dari lima tahap. Tahap pertama yaitu preparasi dan sterilisasi cangkang kerang darah. Tahap kedua adalah kalsinasi cangkang darah supaya didapatkan CaO. Tahap ketiga adalah preparasi bahan. Tahap keempat adalah sintesis HAp dengan metode presipitasi. Tahap kelima uji analisis SSA, XRD, FTIR dan SEM.
Preparasi Cangkang Kerang Darah
Kerang darah dibersihkan menggunakan air lalu direbus selama 1 jam kemudian ditiriskan dan dijemur di bawah sinar matahari sampai kering. Cangkang kemudian digiling menggunakan mesin penggiling sampai berbentuk bubuk lalu diayak dengan ukuran 100 mesh. Selanjutnya serbuk tersebut dicirikan menggunakan XRD.
Kalsinasi Kandungan CaCO3 Cangkang Kerang Darah
Kalsinasi diperlukan sebelum sintesis HAp untuk mengubah kandungan CaCO3 cangkang kerang darah menjadi CaO. Sejumlah serbuk cangkang darah yang
telah kering dimasukkan ke dalam cawan porselen yang sebelumnya telah dibilas dengan HNO3 pekat. Serbuk cangkang kerang darah kemudian dipanaskan di dalam tanur pada suhu 1100 °C selama 3 jam. Setelah itu, Serbuk CaO hasil kalsinasi dicirikan menggunakan XRD.
Konversi CaO Menjadi Ca(OH)2
CaO dapat dikonversi menjadi Ca(OH)2 melalui suatu reaksi eksotermik dengan air. Abu yang didapat dari proses kalsinasi cangkang kerang darah dihidrasi dengan cara dibiarkan kontak dengan udara (mengandung uap air) selama 1 minggu di suhu kamar. Untuk memastikan terbentuknya Ca(OH)2, maka dicirikan menggunakan XRD.
Pengukuran Kadar Kalsium Cangkang Kerang Darah
Sampel hasil kalsinasi ditimbang sebanyak 0.1 g ke dalam labu takar 100 mL. Kemudian, ditambahkan 5 mL HNO3 pekat. Sampel didiamkan kurang lebih 5 menit sampai menjadi larut dan jernih. Sampel kemudian ditera dengan air bebas ion dan dihomogenkan. Selanjutnya dipipet 1 mL larutan yang tadi dan dimasukkan ke dalam labu ukur 100 mL. Sampel ditera dengan air bebas ion dan dihomogenkan. Lalu ditambahkan sedikit strontium agar stabil dalam pengukuran. Kemudian, diukur dengan SSA pada λ = 422.7 nm.
Sintesis Hidroksiapatit Metode Presipitasi
Larutan Ca(OH)2 0.5 M disiapkan sebagai prekursor kalsium (Ca) dan larutan (NH4)2HPO4 0.3 M sebagai prekursor fosfat (P). Hidroksiapatit disintesis melalui reaksi suspensi Ca(OH)2 dan larutan (NH4)2HPO4. Larutan (NH4)2HPO4 0.3 M diteteskan pada suspensi larutan Ca(OH)2 0.5 M dengan kondisi suhu dijaga agar tetap (40±2) oC sambil diaduk menggunakan pengaduk magnetik.
Sintesis dilakukan dengan pH 10 lalu diaduk lagi kemudian hasil sintesis didekantasi selama 24 jam. Setelah
didekantasi kemudian disonikasi selama 4 jam kemudian dioven lalu disentrifugasi selama 5 menit dengan kecepatan 4500 rpm. Setelah endapan terpisah, larutan disaring untuk mendapatkan endapan lalu dicuci tiga kali dengan air suling dan endapan dikeringkan dalam oven pada suhu 105 oC selama 4 jam. Serbuk HAp yang telah kering kemudian dipanaskan pada suhu 1000 oC. Sampel HAp dicirikan menggunakan XRD untuk mengetahui fase HAp yang terbaik. Setelah diperoleh suhu sintering terbaik kemudian dilakukan pengujian dengan dilakukan sintesis dengan pH 9 dan pH 11 lalu dicirikan menggunakan XRD, FTIR dan SEM.
Tahap preparasi, Cangkang kerang darah dibersihkan dengan cara disikat dan dicuci dengan tujuan untuk menghilangkan pengotor. Hasil penentuan kalsium dengan SSA diperoleh data cangkang kerang darah memiliki kadar kalsium sebesar 44,57%. Hasil ini menunjukan bahwa cangkang kerang darah mengandung kadar kalsium yang cukup tinggi dan berpotensi sebagai prekursor dalam sintesis HAp. Pola difraksi XRD memberikan informasi keberadaan CaCO3 pada tahap preparasi seperti pada Gambar 1.
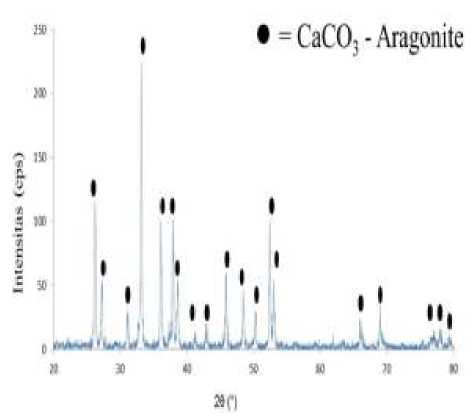
Gambar 1. Difraktogram serbuk cangkang kerang darah sebelum kalsinasi.
Cangkang kerang darah dikalsinasi dalam tanur pada suhu 1000 oC selama 5 jam untuk mengubah fase CaCO3 menjadi fase CaO melalui proses pelepasan gas–gas dalam bentuk karbonat ataupun hidroksida sehingga menghasilkan bahan dalam bentuk oksida [15]. Kalsinasi sendiri juga dapat menghilangkan zat–zat yang tidak dibutuhkan seperti H2O, air kristal, gas (CO2), dengan persamaan reaksi:
CaCO3(s) → CaO(s) + CO2(g).
Kalsinasi pada suhu rendah dapat menyebabkan senyawa CaO yang dihasilkan berubah kembali menjadi CaCO3 dan dekomposisi CO2 yang dihasilkan akan cukup rendah, oleh sebab itu kalsinasi dalam proses ini dilakukan pada suhu 1000 °C. Kalsinasi juga dapat menghilangkan senyawa organik dan pengotor yang mengganggu dalam proses pembentukan HAp [16].
Proses konversi CaO menjadi Ca(OH)2 dilakukan dengan cara dihidrasi pada ruang terbuka selama satu minggu. Hal ini dilakukan agar uap air kontak langsung dengan CaO membentuk Ca(OH)2 melalui suatu reaksi eksotermik dengan air [17]. Persamaan reaksi:
CaO(s) + H2O(g) → Ca(OH)2 (s).
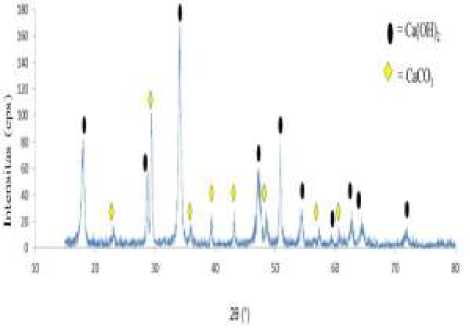
Gambar 2. Difraktogram sinar-x serbuk cangkang kerang darah setelah kalsinasi dan dihidrasi.
Setelah dihidrasi, serbuk Ca(OH)2 diuji menggunakan XRD dan menghasilkan pola difraksi seperti pada Gambar 2.
Hasilnya menunjukan bahwa kalsium yang terkandung pada serbuk cangkang kerang darah yang telah dikalsinasi adalah Ca(OH)2. Puncak puncak XRD disesuaikan dengan Joint Committee on Powder Diffraction Standards (JCPDS) untuk Ca(OH)2 dan CaCO3. Puncak puncak untuk Ca(OH)2 dicirikan keberadaannya pada sudut 2θ = 18.04°, 28.71°, 34.13°, 47.29°, 50.84°, 54.39°, 59.44°, 62.68°, 64.43°, dan 71.86°. Adanya puncak lain pada sudut 2θ = 23.11°, 29.42°, 35.95°, 39.41°, 43.15°, 48.52°, 57.30°, dan 60.60° menunjukkan bahwa masih ada sedikit pengotor dari CaCO3 yang belum berubah fasa menjadi Ca(OH)2. Terbentuknya fase CaCO3 dikarenakan selama proses hidrasi terdapat CO2 sehingga CaO berubah menjadi CaCO3. Fase CaCO3 juga terjadi karena proses kalsinasi yang tidak sempurna. Namun, hal ini tidak signifikan mengganggu untuk memperoleh fasa tunggal HAp. Senyawa Ca(OH)2 yang diperoleh ini merupakan starting material yang digunakan dalam tahap sintesis HAp.
Hasil Sintesis HAp
Serbuk HAp disintesis dengan mereaksikan Ca(OH)2 dari hasil kalsinasi dengan (NH4)2HPO4 berdasarkan
perbandingan mol 10:6 sesuai dengan rasio mol Ca/P 1,67 dan pH 10, persamaan reaksi:
10Ca(OH)2+ 6(NH4)2HPO4 -----►
Ca10(PO4)6(OH)2 + 6H2O + 12NH4OH.
Serbuk HAp yang telah disintesis diidentifikasi menggunakan XRD untuk mengetahui fase yang terkandung.
Hidroksiapatit dengan pH kurang dari 10 atau melebihi 10 akan menyebabkan terbentuknya senyawa kalsium fosfat lain yang tidak diinginkan [18]. Oleh karena itu pemantauan pH terus dilakukan selama proses sintesis HAp. Suhu sintering sangat penting dalam proses
menghasilkan HAp murni karena fasa selain HAp dapat terbentuk apabila suhu sintering terlampau tinggi maupun terlampau rendah. Jika suhu sintering terlampau tinggi maka akan terbentuk senyawa apatit karbonat tipe A Ca10(PO4)6CO3 dan jika suhu sintering terlampau rendah maka akan terbentuk senyawa apatit karbonat tipe B Ca10(PO4)3CO3(OH)2[19].
Hasil Karakterisasi Fasa HAp menggunakan XRD
Identifikasi fasa HAp dianalisis dengan XRD yang dicirikan oleh puncak difraksi yang khas antara sudut 2θ 20-80° (gambar 3). Pola XRD menunjukkan bahwa serbuk hasil sintesis merupakan murni fasa tunggal HAp berdasarkan data JCPDS No. 090432. Hal ini dibuktikan dari puncak ciri khas yang kuat pada 2θ = 31.83°, 32.24°, dan 32.96° tanpa adanya puncak asing.
Sintering dalam proses sintesis HAp diperlukan untuk memperoleh fasa murni HAp. Derajat kristalinitas HAp hasil sintesis yang diperoleh yaitu 90,15%.
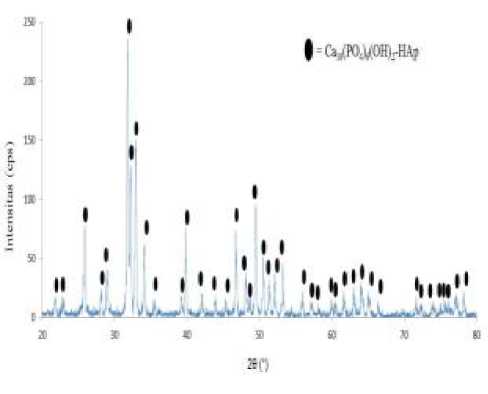
Gambar 3. Difraktogram sinar-X HAp
Hasil Karakterisasi FTIR pada HAp
Keberhasilan sintesis HAp pada penelitian ini dapat ditinjau dengan menggunakan XRD. Hidroksiapatit disintesis dengan metode presipitasi melalui reaksi antara serbuk Ca(OH)2
sebagai sumber kalsium dan (NH4)2HPO4 sebagai sumber fosfat.
Analisis spektrum FTIR dilakukan untuk menegaskan informasi gugus fungsi dari senyawa HAp yang dihasilkan yaitu gugus fungsi PO43- dan OH- dalam HAp. Spektrum FTIR HAp yang telah disintesis dapat dilihat pada Gambar 4. Berdasarkan pita spektrum FTIR dari HAp yang telah disintesis terdapat gugus fungsi penyusun HAp, yaitu gugus OH- dan PO43-. Adanya serapan pada bilangan gelombang 1092.02, 1038.29, 962.45, 602.30, dan 571.71 cm-1 merupakan vibrasi dari gugus PO43-.
3-Penelitian [20] melaporkan serapan PO43-muncul pada bilangan gelombang di sekitar 1085-1092, 1033-1035, 1000, 933-962, dan 500-611 cm-1. Adanya gugus OH-
ditunjukkan dengan munculnya serapan pada bilangan gelombang 3572.28 dan 632.18 cm-1. Serapan dan puncak OH-sesuai dengan yang dilaporkan oleh [21] bahwa gugus OH- muncul pada bilangan gelombang 3575 dan 628 cm-1.
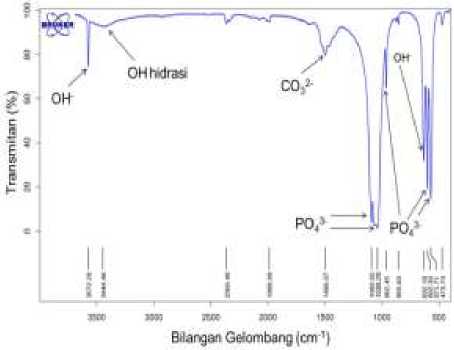
Gambar 4. Spektrum gugus fungsi HAp.
Keberadaan gugus CO32- menunjukan masih adanya pengotor. Hasil ini sesuai dengan analisis XRD yang menunjukan adanya CaCO3. Menurut [22] bahwa adanya substitusi karbonat pada gugus hidroksil atau fosfat dapat disebabkan oleh kelarutan CO2 di lingkungan sekitar terkait dengan pengadukan yang kuat selama sintesis
HAp. Hasil FTIR ini telah menegaskan akan keberadaan senyawa murni HAp.


Gambar 5. Foto SEM HAp perbesaran (a) 3000X ; (b) 10.000X
Hasil Karakterisasi SEM pada HAp
Analisis SEM pada HAp bertujuan untuk melihat morfologi kristal HAp. Gambar 5 menunjukkan morfologi HAp Foto SEM Gambar 5. HAp yang diperoleh memiliki bentuk bulat yang seragam. Keseragaman bentuk tersebut karena pada suhu sintering 1000 °C hanya dihasilkan Hap
Porositas HAp berfungsi menyediakan lingkungan biologi yang baik pada adhesi sel, interaksi selular, proliferasi, dan migrasi. Dengan demikian, pori HAp yang terdapat di antara butiran HAp diharapkan memiliki kemampuan sebagai media pertumbuhan tulang baru setelah implantasi. Tampak partikel HAp berbentuk bola dan terjadi aglomerasi. Penelitian [23] juga melaporkan hal yang sama bahwa pada SEM partikel HAp membentuk partikel aglomerasi.
-
1. KESIMPULAN
Kandungan kalsium dari limbah cangkang kerang darah dapat dimanfaatkan [4]
sebagai starting material dalam sintesis hidroksiapatit. Kadar kalsium dalam bahan baku yang diukur menggunakan SSA adalah sebesar 44,57%. Hasil analisis XRD, puncak HAp dengan intensitas tertingi diperoleh pada variasi rasio Ca/P yaitu [5]
-
1,67. Hasil analisis FTIR, pada sampel terdapat gugus PO43- dan OH- yang mengindikasikankan adanya kandungan hidroksiapatit pada cangkang kerang darah. Dari hasil analisa SEM menunjukkan struktur HAp berbentuk bola dan terjadi [6]
aglomerasi. Hasil sintesis dengan metode presipitasi menunjukkan hidroksiapatit yang diperoleh merupakan fasa tunggal HAp.
-
2. UCAPAN TERIMA KASIH [7]
Penulis mengucapkan terima
kasih kepada Direktorat Riset, Teknologi, dan Pengabdian Masyarakat Kementerian Pendidikan, Kebudayaan Riset dan Teknologi yang telah mendanai penelitian [8]
ini melalui hibah Penelitian Dosen Pemula tahun 2023 serta Lembaga Penelitian dan Pengabdian pada Masyarakat Universitas Flores yang memberikan dukungan dan kesempatan sehingga penelitian ini dapat [9]
terlaksana.
-
3. DAFTAR PUSTAKA
-
[1] Komala D., Amin M.N., Rahayu Y.C.
Uji sitotoksitas hidroksiapatit cangkang telur ayam ras (Gallus gallus) terhadap sel fibroblas ligamen periodontal manusia. Stomatognatic: Jurnal Kedokteran Gigi. 2022, 19(1), 49-54.
-
[2] Suci I.A., Ngapa Y.D. Sintesis dan karakterisasi hidroksiapatit (HAp) dari cangkang kerang ale-ale
menggunakan metode resipitasi [10]
double stirring. Cakra Kimia. 2020, 8(2), 73-81.
-
[3] Akbar F., Kusumaningrum R., Jamil M.S., Noviyanto A., Widayatno W.B., Wismogroho A.S., Rochman N.T.
Sintesis Ca2P2O7 dari limbah kerang [11]
dengan metode solvotherma. Jurnal
Fisika dan Aplikasinya. 2019, 15(3), 110-113.
Charlena, Suparto I.H., Putri D.K. Synthesis of hydroxyapatite from rice fields snail shell (Bellamya javanica), through wet method and pore podification using chitosan. Procedia Chemistry, 2015.17(1), 27-35.
Suprianto K., Hidayati., Nilam C., Khairiyah N., Amelia R, Rahmadita S. Hidroksiapatit dari cangkang telur sebagai bone graft yang potensial dalam terapi periodontal. Clinical Dental Journal. 2019, 5(3), 76-87.
Poernomo H. Teknik bone tissue engineering (BTE) untuk regenerasi jaringan periodontal dan estetik pada edentulous ridge. Interdental Jurnal Kedokteran Gigi. 2019, 15(2), 56-59. Perwiranegara S.A., Bayuseno P.B., Ismail R. Pengaruh daya microwave terhadap karakterisasi hidroksiapatit berbahan cangkang rajungan. Jurnal Teknik Mesin. 2021, 9(4), 559-564.
Rachmantio C. Pengaruh suhu dan waktu kalsinasi terhadap kemurnian hidroksiapatit berbasis cangkang kerang hijau untuk aplikasi pada bone tissue engineering. 2023, 11(1), 1-6. Karisma A.D., Kriswanto O.N., Rachmaningtrias R. Sintesis
nanohidroksiapatit berbahan
cangkang keong sawah (Pila
ampullacea) dengan variasi
konsentrasi H3PO4 menggunakan
metode ultrasound assisted
precipitation. Prosiding Seminar Nasional Teknik Kimia “Kejuangan” Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia Yogyakarta, 25 Mei 2023. 1-5
Sari M., Yusuf Y. Synthesis and characterization of hydroxyapatite based on green mussel shells (Perna viridis) with calcination temperature variation using the precipitation method. 2018, 11(3), 357-370.
Ningsih R.P., Wahyuni N., Destiarti L. Sintesis hidroksiapatit dari
cangkang kerang kepah (Polymesoda erosa) dengan variasi waktu
pengadukan. Jurnal Kimia
Khatu;istiwa. 2014. 3(1), 22-26.
-
[12] Charlena, Suparto I.H., Laia D.P.O., Synthesis and characterization of hydroxyapatite from polymesoda placans shell using wet precipitation method. Jurnal Bios Logos. 2023, 13(1), 85-96.
-
[13] Kadir L.A., Permana D., Aziz T. Sintesis dan karakterisasi bionano hidroksiapatit (HAp) secara insitu dengan metode hidrotermal.
Cokroaminoto Journal of Chemical Science. 2022, 4(2), 1-4.
-
[14] Akbar A.F., Qurrota‘Aini F., Nugroho B, Cahyaningrum S.E., sintesis dan karakterisasi
hidroksiapatit tulang ikan baung (Hemibagrus nemurus) sebagai kandidat implan tulang. Jurnal Kimia Riset. 2021, 6(2), 93-101.
-
[15] Anggresani L., Perawati S., Rahayu I.J. Limbah tulang ikan tenggiri (Scomberomorus guttatus) sebagai sumber kalsium pada pembuatan hidroksiapatit. Jurnal Katalisator. 2019, 4(2), 133-140.
-
[16] Wahdah I., Wardhani S., Darjito. Sintesis hidroksiapatit dari tulang sapi dengan metode basah pengendapan. Kimia Student Journal 2014, 1(1), 92-97.
-
[17] Ningsih P., Rini N., Wahyuni, Destiarti L. Sintesis hidroksiapatit dari cangkang kerang kepah (Polymesoda erosa) dengan variasi waktu pengadukan. Jurnal Kimia Khatulistiwa. 2014, 3(1), 22-26.
-
[18] Fadli D.F., Azis Y., Yusnimar. Pengaruh suhu dan pH terhadap bentuk partikel hidroksiapatit dari precipitated calcium carbonate (PCC) kulit telur itik melalui metode presipitasi. Jurnal Online Mahasiswa Fakultas Teknik. 2019, 6(1), 1-8.
-
[19] Pratiwi D.I., Fadli A., Zultiniar. Pengaruh Suhu Reaksi dan Kecepatan Pengadukan pada Sintesa
Hidroksiapatit dari Kulit Kerang Darah (Anadara granosa) dengan Menggunakan Metode Hidrotermal Suhu Rendah. Jurnal Online
Mahasiswa Fakultas Teknik. 2015.
2(2). 1-10.
-
[20] Bano N., Jikan S.S., Basri H., Adzila S., Zago D.M. XRD and FTIR study of A&B type carbonated hydroxyapatite extracted from bovine bone, AIP Conference Proceedings. 2019, 2068(1), 143-150.
-
[21] Dedourkova T., Zelenka J., Zelenkova M., Benes L., Svoboda L. Synthesis of sphere-like nanoparticles of hydroxyapatite, Procedia
Engineering. 2012, 42, 1816–1821.
-
[22] Purwasasmita B.S., Gultom R.S.
Sintesis dan karakterisasi serbuk
hidroksiapatit skala lab sub-mikron menggunakan metode presipitasi, Bionatura: Jurnal Ilmu Hayati dan Fisik. 2008, 10(2), 155-167.
-
[23] Poinern G., Brundavanam R.,
Fawcett D. Nanometre scale
hydroxyapatite ceramics for bone tissue engineering, American Journal of Biomedical Engineering. 2013,
3(6), 148-168.
85
Discussion and feedback