Studi Komparasi Jenis Pelarut Ekstraksi terhadap Kandungan Fitokimia Daun Tanaman Kubis Ungu
on
Nandur
Vol. 1, No. 4, Oktober 2021 https://ojs.unud.ac.id/index.php/nandur
EISSN: 2746-6957 | Halaman 159-167 Fakultas Pertanian, Universitas Udayana
Studi Komparasi Jenis Pelarut Ekstraksi terhadap Kandungan Fitokimia Daun Tanaman Kubis Ungu
Hengky Surya Bhuana, Made Sritamin*), I Gede Putu Wirawan
Program Studi Agroekoteknologi Fakultas Pertanian Universitas Udayana
Jl. PB. Sudirman Denpasar, Bali 80232 *)Email: madesritamin@gmail.com
Abstract
Red cabbage is a plant that is rich in antioxidant, one of its secondary metabolites, antosianin that gave the purple color on red cabbage has multiple health effects for human such as preventing cancer, tumor, and many more. The use of this secondary metabolites in plants nowadays is very popular, not only for its pharmacological effects, but also as an antibacterial, coloring agent, flavoring agent, natural pesticide, etc. Therefore, this study is needed to look for another potentially benefical compound in the plant, such as red cabbage, a plant that is more than just a salad. The aim of this study was to determine the effect of the types of extraction solvents on phytochemical compound of red cabbage plant leaves. The dried off plant macerated with two kinds of solvents, aquades, and ethanol. After about +3 days, both of the extract got evaporated with rotary evaporator. The yields of evaporating will be tested with GCMS analysis. The result showed that kind of extraction solvents do affect the yield from evaporating, and GC-MS analysis. Aquades showed to have a better capability in both of extraction, or on the analysis with GC-MS.
Keywords: Red Cabbage, Phytochemical, Solvents, GC-MS, Indole-3-acetonitrile
Bahan alam (natural products) dapat diartikan sebagai segala sesuatu yang dihasilkan oleh alam, yang secara ilmiah maupun tradisional terbukti memiliki beragam manfaat dalam berbagai bidang kehidupan. Seiring majunya peradaban istilah back to nature kerap kali muncul sebagai salah satu hal yang diunggulkan dalam berbagai bidang, istilah ini muncul sebagai ajakan untuk kembali memanfaatkan, memberdayakan, serta melestarikan potensi alam. Dan tidak dapat dipungkiri lagi pemanfaatan bahan alam dalam bidang kesehatan, kosmetik, bahan makanan, dan lain sebagainya semakin nyata adanya. Popularitas penggunaan bahan alam pada berbagai bidang kehidupan sebagai pilihan semakin meningkat karena dinilai lebih aman, sehingga dapat menekan kemungkinan efek negatif yang timbul. Berbagai penelitian pun dilakukan untuk mengembangkan produk-produk yang berbasis pada bahan alam, yang juga ikut meningkatkan nilai ekonomis dari beberapa bahan alam.
Bahan alam dapat didefinisikan sebagai komponen atau substansi kimia yang merupakan metabolit sekunder (secondary metabolites) yang dapat berupa komponen tunggal/murni hasil isolasi maupun yang masih berupa campuran komponen dalam bentuk ekstrak, sediaan kering dari bagian tertentu atau keseluruhan dari suatu organisme baik tumbuhan, mikroba, ataupun hewan yang dieksplorasi dan dimanfaatkan karena efek farmakologis (pharmacological effect), efek terapi (therapeutic effect), antioksidan (antioxidative effect), antibakteri (antibacterial), atau kemampuannya sebagai bahan pewarna (coloring agent), penyedap (flavoring agent), pengharum (parfuming agent), pengikat (fixative agent), serta karena aktivitas biologis (biological activity) lainnya seperti kemampuan sebagai pestisida alami (natural pesticide) (Nugroho, 2017).
Proses pengujian metabolit sekunder suatu tanaman umumnya dimulai dengan pengeringan sampel, penghalusan, ekstraksi, kemudian diikuti dengan uji masing-masing metabolit sekunder yang terkandung di dalamnya. Tidak jarang dalam pengujiannya sendiri pun digunakan berbagai macam cara, atau metode yang digunakan untuk memperoleh hasil yang paling memuaskan. Seperti metode pengeringannya, jenis pelarutnya, lama pengeringan, ataupun metode ekstraksi tanaman yang digunakan. Tentu saja, hasil yang diperoleh untuk setiap faktor pembanding tidak selalu memberikan hasil yang sama pada semua jenis tanaman, sehingga perlu dilakukan penelitian untuk menemukan cara terbaik dalam memperoleh kandungan fitokimia pada setiap jenis tanaman.
Tanaman yang digunakan dalam penelitian ini adalah kubis ungu. Kubis ungu merupakan tanaman herbal dengan daun berwarna ungu biasanya dikonsumsi sebagai salad, dan minuman (el-Mowafy et al., 2012). Warna ungu pada tanaman kubis ungu disebabkan oleh salah satu senyawa metabolit sekunder yakni antosianin yang dimiliki oleh tanaman kubis ungu. Antosianin juga memiliki manfaat sebagai antioksidan. Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya dengan cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali dan dapat memutus reaksi berantai dari radikal bebas (Putri et al., 2018). Antioksidan yang bermanfaat dalam mencegah beberapa penyakit seperti kolesterol, diabetes, jantung, dan kanker. Dalam kubis ungu terdapat banyak komponen bioaktif yaitu isotiosianat, vitamin A, B, C, dan antosianin (Singh et al., 2006).
Saat ini belum terdapat banyak penelitian yang mengkaji kandungan fitokimia daun tanaman kubis ungu, oleh karena itu penulis melakukan penelitian dengan judul “Studi Komparasi Jenis Pelarut Ekstraksi Terhadap Kandungan Fitokimia Daun Tanaman Kubis Ungu” dengan harapan ke depannya dapat menjadi pedoman, atau tambahan informasi mengenai kandungan fitokimia daun tanaman kubis ungu, sekaligus dapat menentukan jenis pelarut terbaik yang dapat menghasilkan jumlah ekstrak tertinggi.
Penelitian ini akan dilaksanakan di Laboratorium Sumber Daya Genetika dan Biologi Molekuler Universitas Udayana, juga di Laboratorium Forensik Polresta Denpasar, mulai dari bulan Mei 2021 sampai dengan bulan Juni 2021.
Bahan yang digunakan dalam penelitian ini adalah aquades, etanol 96%, alkohol 95%, kubis ungu, selotip, aluminium foil, plastic wrap, dan tisu. Alat yang digunakan dalam penelitian ini adalah toples, tampah, pisau, talenan, corong, saringan, botol, timbangan digital, rotary evaporator, labu alas bulat, sendok, blender, batang pengaduk, wadah kecil, gas chromatography-mass spectrometry (GCMS), centrifuge, lipoclear tubes, injection syringe, mikropipet, dan rak test tube.
Sampel tanaman pertama-tama dicuci bersih terlebih dahulu, kemudian dipotong menjadi bagian-bagian yang lebih kecil. Sampel berikutnya dikering anginkan selama +7 hari. Secara umum simplisia harus dikeringkan pada suhu di bawah 30oC, untuk menghidari terurainya komponen kimia yang terdapat dalam tumbuhan akibat dari pengaruh suhu (Marjoni, 2019). Setelah itu sampel diblender.
Sampel tanaman selanjutnya akan diekstrak dengan metode maserasi. Sebanyak 100 gram sampel dimaserasi menggunakan dua liter pelarut. Maserasi dilakukan dengan merendam sampel yang telah disiapkan ke dalam pelarut pada wadah yang telah disiapkan. Proses maserasi berlangsung selama +3x24 jam. Pengadukan secara berkala dilakukan untuk memaksimalkan proses ekstraksi. Larutan ekstrak kemudian disaring untuk dipisahkan dengan bahan asalnya. Selanjutnya larutan hasil ekstraksi diuapkan dengan rotary evaporator (RE) sehingga diperoleh ekstrak kental yang berikutnya siap untuk diujikan kandungan fitokimianya.
Kegiatan maserasi dilakukan menggunakan dua jenis pelarut ekstraksi yakni aquades, dan etanol. Selanjutnya ekstrak total dari masing-masing pelarut ditimbang untuk mengetahui seberapa banyak ekstrak kental yang diperoleh setelah melalui serangkaian tahap di atas untuk masing-masing jenis pelarut.
Ekstrak kental hasil penguapan RE selanjutnya digunakan dalam pengujian kandungan fitokimia tanaman melalui uji GC-MS. Sebelum itu dilakukan pengaturan pada alat GC-MS yang akan digunakan. Pertama-tama ekstrak kental akan diambil sebanyak 1 mikro, dan akan diencerkan 10x, kemudian disentrifugasi dengan kecepatan 3000 rpm selama 3 menit. Sampel yang sudah disentrifugasi selanjutnya diambil sebanyak 1 mikro dengan injection syringe, kemudian akan diinjeksikan pada alat GC-
MS untuk mengetahui kandungan senyawa fitokimia yang terkandung dalam sampel. Hal ini dilakukan untuk ekstrak dari kedua jenis pelarut.
Sampel berupa tanaman kubis ungu (Gambar 1) diperoleh dari Desa Pancasari, Kabupaten Buleleng. Kubis ungu yang diambil sebagai sampel adalah kubis ungu yang berumur +4 bulan dari varietas Takii.

Gambar 1. Kubis Ungu (Sumber: Dokumentasi Pribadi)
Berdasarkan penelitian yang telah dilakukan, hasil akhir berupa ekstrak kental diperoleh dari masing-masing maserat dari ke dua jenis pelarut. Sebesar 21,66 gram ekstrak kental aquades daun tanaman kubis ungu berhasil diperoleh melalui penguapan dengan alat rotary evaporator, dan 13,32 gram ekstrak kental etanol daun tanaman kubis ungu.
Tabel 1. Perbandingan total rendemen ekstrak dari kedua jenis pelarut
|
Jenis Pelarut |
Rendemen (gram) |
Rendemen (persen) |
|
Aquades |
21,66 |
21,66 |
|
Etanol |
13,32 |
13,32 |
Seperti yang terlihat pada Tabel 1, dapat dikatakan bahwa aquades lebih baik untuk digunakan sebagai pelarut dalam mengekstrak daun tanaman kubis ungu dibandingkan dengan etanol dilihat dari total rendemen yang dihasilkan. Tingginya rendemen ekstrak daun tanaman kubis ungu dengan pelarut aquades menunjukkan bahwa ekstraksi yang dilakukan menggunakan pelarut aquades pada daun tanaman kubis ungu memiliki kemampuan yang lebih baik dalam mengekstrak daun tanaman kubis ungu, karena jumlah ekstrak kental yang diperoleh lebih banyak daripada ekstrak
kental yang diperoleh dari ekstraksi yang dilakukan dengan menggunakan jenis pelarut etanol.
Adanya perbedaan jumlah rendemen yang dihasilkan dari ekstraksi yang dilakukan menggunakan kedua jenis pelarut berhubungan dengan perbedaan nilai polaritas yang dimiliki dari masing-masing jenis pelarut yang digunakan. Efektivitas ekstraksi suatu senyawa oleh pelarut sangat tergantung kepada kelarutan senyawa tersebut dalam pelarut, sesuai dengan prinsip like dissolve like yaitu suatu senyawa akan terlarut pada pelarut dengan sifat yang sama (Kemit et al., 2015).
Gas Chromatography-Mass Spectrometry (GC-MS) merupakan instrumen yang digunakan untuk mengidentifikasi senyawa yang terkandung dari suatu sampel, yang mengkombinasikan kromatografi gas, dan spektrometri massa sebagai peralatan yang digunakan secara berpaduan. Sampel yang diinjeksikan akan berjalan sepanjang kolom. Sebanyak 1 μl sampel yang sudah diencerkan 10x diinjeksikan akan berjalan dalam kolom yang memiliki panjang kolom 30 meter, diameter 0,25 mm, dan ketebalan 0,25 μm (HP-5MS UI). Suhu yang digunakan selama pengoperasian instrumen adalah 70oC – 290oC. Lima menit awal suhu yang digunakan adalah 70oC, kemudian seiring dengan berjalannya waktu suhu dinaikkan 10oC/menit, dan pada tiga menit terakhir suhu yang digunakan adalah 290oC. Proses ini berlangsung selama 30 menit yang terhitung sejak penginjeksian sampel ke dalam inlet instrumen (disajikan dalam Tabel 2).
Tabel 2. Metode GC 7809B (SN US17213016), MSD 5977B (SN G7078B
US1721D0001)
|
Metode |
Awal |
Suhu Oven Kenaikan |
Akhir |
Total (menit) |
Flow (mL/menit) |
Split |
Kolom |
|
Bahan |
70oC, |
10oC |
290oC, |
30 |
2,9 |
1 |
HP-5MS |
|
Alam |
lima |
/menit |
tiga |
IOO |
UI | ||
|
menit |
menit |
30 m, |
0,25 mm, 0,25 μm
Terdapat beberapa jenis senyawa yang berhasil teridentifikasi melalui uji GCMS dari kedua jenis ekstrak yang diujikan. Pada ekstrak etanol daun tanaman kubis ungu terdapat empat jenis senyawa yang berhasil teridentifikasi, sedangkan pada ekstrak aquades daun tanaman kubis ungu terdapat tujuh jenis senyawa yang berhasil teridentifikasi.

Gambar 2. Grafik hasil uji GC-MS ekstrak etanol daun tanaman kubis ungu
|
Tabel 3. Hasil analisa uji GC-MS ekstrak etanol daun tanaman kubis ungu | ||||
|
No |
RT |
Area (%) |
Nama Senyawa |
Qual |
|
1 |
3.689 |
22.22 |
2-Mercaptopraponoic acid |
45 |
|
2 |
9.855 |
8.09 |
4-Mercaptophenol |
83 |
|
3 |
13.092 |
61.65 |
1’,1’-Dicarboethoxy-1.beta.,2.beta.-dihydro-3’H-cycloprop[1,2]cholesta-1,4,6-trien-3-one |
11 |
|
4 |
17.351 |
8.03 |
1H-Indole-3-acetonitrile |
81 |
Pada pengujian ekstrak etanol daun tanaman kubis ungu terdapat empat puncak yang masing-masing teridentifikasi pada waktu retensi 3.689, 9.855, 13.092, dan 17.351 seperti yang terlihat pada kromatogram Gambar 2, namun tidak ditemukan adanya senyawa yang memiliki nilai “qual” >90. Artinya, dari keempat jenis senyawa yang ditemukan, sejatinya tidak dapat dibenarkan bahwa senyawa yang berhasil ditemukan adalah senyawa yang serupa seperti yang tertera pada Tabel 3. Dalam pengujian GC-MS senyawa dapat dikatakan serupa, atau benar senyawa yang teridentifikasi sesuai dengan database yang digunakan apabila memiliki nilai qual >90.
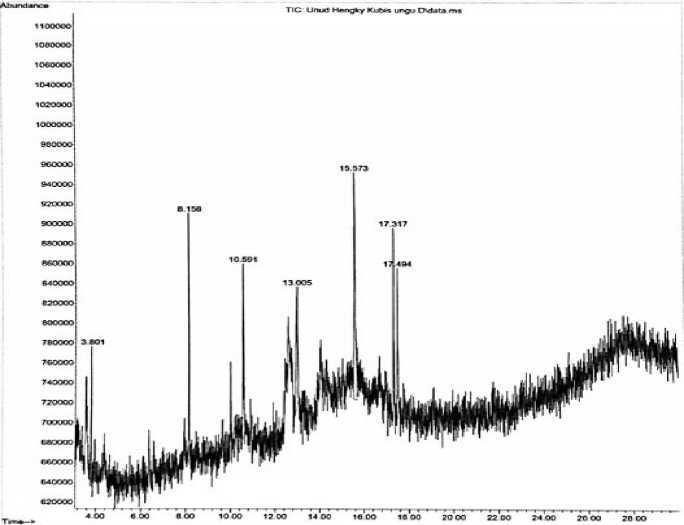
Gambar 3. Grafik hasil uji GC-MS ekstrak aquades daun tanaman kubis ungu
|
Tabel 4. Hasil analisa uji GC-MS ekstrak aquades daun tanaman kubis ungu | ||||
|
No |
RT |
Area (%) |
Nama Senyawa |
Qual |
|
1 |
3.801 |
8.75 |
Diethyl 1-(8-azido-1-naphthyl)-1H-1,2,3-triazole-4,5-dicarboxylate |
83 |
|
2 |
8.156 |
12.92 |
4H-Pyran-4-one, 2,3-dihydro-3,5-dihydroxy-6-methyl- |
86 |
|
3 |
10.591 |
14.01 |
N’-(2-Bromobenzylidene)-2-(1-bromo-2-naphthyloxy)butyrohydrazide |
59 |
|
4 |
13.005 |
15.68 |
1,5-Methano-1H,7H,11H-furo[3,4- |
11 |
g]pyrano[3,2-b]xanthene-7,15-dione,3,3a,4,5-tetrahydro-8-hydoxy-1-(4-hydroxy-3-methyl-2-butenyl)-3,3,11,11-tetramethyl-13-(3-methyl-2-butenyl)-, [1R-[1.alpha.,1(Z),3a.beta.,5.alpha.,14as*]]-
|
5 |
15.573 |
30.63 |
N-(Trifluoroacetyl)-o,o’ ,o’ ‘-tris(trimethylsilyl)norepineohrine |
46 |
|
6 |
17.317 |
6.74 |
1H-Indole-3-acetonitrile |
94 |
|
7 |
17.494 |
11.26 |
Octasiloxane, 1,1,3,3,5,5,7,7,9,9,11,11,13,13,15,15-hexadecamethyl |
49 |
Pada kromatogram ekstrak aquades daun tanaman kubis ungu (Gambar 3), terdapat tujuh puncak yang masing-masing teridentifikasi pada waktu retensi 3.801, 8.156, 10.591, 13.005, 15.573, 17.317, dan 17.494. Berbeda dengan hasil analisa uji GC-MS ekstrak etanol daun tanaman kubis ungu, pada hasil analisa uji GC-MS ekstrak aquades daun tanaman kubis ungu terdapat senyawa yang berhasil teridentifikasi yang memiliki nilai qual 94. Artinya senyawa dari sampel yang diujikan dapat dikatakan adalah senyawa yang benar, atau serupa dengan senyawa yang terdaftar pada database. Seperti yang terlihat pada Tabel 4, senyawa tersebut adalah senyawa yang berada pada nomor urut enam, yang bernama 1H-Indole-3- acetonitrile.
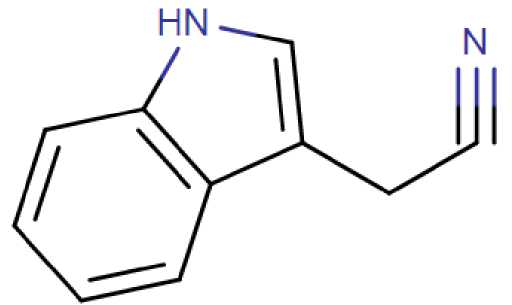
Gambar 4. Struktur molekul 1H-Indole-3-acetonitrile
1H-Indole-3-acetonitrile, dikenal juga sebagai 3-(cyanomethyl) indole, atau IAN, termasuk ke dalam kelas senyawa organik yang dikenal dengan sebutan 3- alkylindoles merupakan senyawa yang mengandung bagian indole yang membawa rantai alkyl pada posisi 3 (FooDB, 2010).
3-Indoleacetonitrile juga merupakan fitoaleksin (HMDB, 2007). Fitoaleksin adalah antibiotik yang diproduksi oleh tanaman yang sedang diserang. Fitoaleksin yang diproduksi dalam tanaman bertindak sebagai racun bagi organisme yang menyerang dengan merusak dinding sel, menunda pematangan, mengganggu metabolisme, atau mencegah reproduksi patogen. 3-Indoleacetonitrile umum terdapat dalam sayuran seperti kubis, kembang kol, dan brokoli.
Menurut FooDB (2010), senyawa ini memiliki kemampuan sebagai anti kanker, anti tumor, dan juga fitohormon. Dalam peranannya sebagai anti kanker, dan anti tumor, senyawa ini mampu menghambat, atau mencegah proliferasi neoplasma. Sebagai fitohormon, lebih tepatnya zat pengatur tumbuh (ZPT) senyawa ini dapat mengatur pembentukan batang, daun dan bunga, serta perkembangan, dan pematangan buah. Senyawa ini memiliki peran sebagai auksin, hormon tanaman, metabolit tanaman, dan metabolit xenobiotik manusia (PubChem, 2004).
Dilihat dari selisih berat rendemen antara ekstrak daun tanaman kubis ungu yang dimaserasi menggunakan pelarut aquades (21,66 gram), dan pelarut etanol (13,32 gram), menunjukkan bahwa pelarut aquades memiliki kemampuan lebih baik dalam mengekstrak daun tanaman kubis ungu. Hasil uji GC-MS menunjukkan bahwa jenis pelarut yang digunakan untuk ekstraksi berpengaruh terhadap kandungan fitokimia daun tanaman kubis ungu, hal ini ditunjukkan dengan jumlah senyawa yang berhasil teridentifikasi pada ekstrak etanol daun tanaman kubis ungu (empat jenis senyawa), dan ekstrak aquades daun tanaman kubis ungu (tujuh jenis senyawa).
Daftar Pustaka
el-Mowafy, M. A., El-Motaleb. (2012). Treatment Effect of Red Cabbage and Cysteine
Against Paracetamol Induced Hepatotoxicity In Experimental Rats. Journal of Applied Sciences Research, 8(12): 5852-5859, 2012 ISSN 1819- 544X.
FooDB. (2010). Compound 1H-Indole-3-acetonitrile (FDB001365).
https://foodb.ca/compounds/FDB001365. (diakses pada 03 Juli 2021).
HMDB. (2007). Metabocard for 3-Indoleacetonitrile (HMDB0006524).
https://hmdb.ca/metabolites/HMDB0006524. (diakses pada 03 Juli 2021).
Kemit, N., I W. R. Widarta, K. A. Nocianitri. (2015). Pengaruh Jenis Pelarut Dan Waktu Maserasiterhadap Kandungan Senyawa Flavonoid Dan Aktivitas Antioksidan Ekstrak Daun Alpukat (Persea Americana Mill). Jurnal. Fakultas Teknologi Pertanian, Universitas Udayana, Denpasar.
Nugroho, A. (2017). Buku Ajar Teknologi Bahan Alam. Lambung Mangkurat University Press, Banjarmasin.
PubChem. (2004). 3-Indoleacetonitrile. https : // pubchem. ncbi. nlm. nih. Gov / compound / 3-Indoleacetonitrile. (diakses pada 03 Juli 2021).
Putri, A. S., E. Bekti, dan S. Hayati. (2018). Kajian Pemanfaatan Kubis Merah (Brassica oleracea L.) Sebagai Antioksidan dan Aplikasinya Pada Kerupuk Kubis Merah. Laporan Penelitian Dosen. Fakultas Teknologi Pertanian, Universitas Semarang, Semarang.
Singh, J., A. K. Upadhyay, A. Bahadur, B. Singh, K. P. Singh, Mathura Rai. (2006).
Antioxidant Phytochemicals In Cabbage (Brassica oleracea L. var. capitata). Scientia Horticulturae 108 (2006) 233–237.
167
Discussion and feedback