Seroprevalensi Leptospirosis pada Anjing Kintamani di Bali
on
Jurnal Ilmu dan Kesehatan Hewan, Agustus 2015
Vol 3 No 2: 41-44
Seroprevalensi Leptospirosis pada Anjing Kintamani di Bali
Seroprevalence of Leptospirosis in Kintamani Dog in Bali
Mutawadiah1, I Ketut Puja Puja2, Nyoman Sadra Dharmawan3*
1Balai Besar Veteriner, Denpasar, Bali
-
2Laboratorium Genetika dan Teknologi Reproduksi Fakultas kedokteran hewan, Universitas Udayana, Denpasar, Bali
-
3Laboratorium Patologi Klinik Veteriner Fakultas Kdokteran Hewan, Universitas Udayana, Denpasar, Bali
*corresponding author: nsdharmawan@unud.ac.id
ABSTRACT
The aim of this study was to determine the seroprevalence of leptospirosis in Kintamani dogs in Bali. Blood samples were collected from 55 Kintamani dogs. The sera examination was conducted in the Veterinary Research Centre, Bogor. Microscopic Agglutination Test was performed to detect the presence of antibodies against 14 leptospira antigens. The results showed that the prevalence of leptospirosis in Kintamani dogs in Bali was 18.18% (10/55). Two out of 10 positive sera samples (3.64%) reacted with three serovar; 5 (9.09%) reacted with two serovar; and 3 (3.64%) reacted with one serovar. There were four types of serovars detected in this study, namely: Leptospira interrorgans serovar Celledoni, Leptospira interrorgans serovar Canicola, Leptospira interrorgans serovar Cynopteri dan Leptospira interrorgans serovar Ichterohemorrhagiae. The research found that Leptospira interrorgans serovar Cellodini was very common in Kintamani dog.
Key words: seroprevalence, leptospirosis, Kintamani dog, MAT
ABSTRAK
Penelitian ini bertujuan untuk mengetahui seroprevalensi leptospirosis pada anjing kintamani di Bali. Sampel yang digunakan berupa serum anjing kintamani yang berasal dari Bali sebanyak 55 sampel. Pemeriksaan dilakukan dengan menggunakan Uji MAT (Microscopic Agglutination Test) yang dilakukan di Balai Besar Penelitian Veteriner Bogor. Hasil penelitian menunjukkan bahwa prevalensi leptospirosis pada anjing kintamani di Bali sebesar 18,18% (10/55). Dari 10 sampel serum yang positif, 2 sampel (3,64%) bereaksi positif terhadap tiga serovar; 5 sampel (9,09%) bereaksi positif terhadap dua serovar; dan 3 sampel (3,64%) bereaksi positif terhadap satu serovar. Ada empat tipe serovar yang terdeteksi pada penelitian ini, yaitu: Leptospira interrorgans serovar Celledoni, Leptospira interrorgans serovar Canicola, Leptospira interrorgans serovar Cynopteri dan Leptospira interrorgans serovar Ichterohemorrhagiae. Hasil penelitian menunjukkan bawa Leptospira interrorgans serovar Celledoni paling umum ditemukan pada ajning Kintamani.
Kata kunci: seroprevalensi, leptospirosis, anjing Kintamani, uji MAT
PENDAHULUAN
Leptospirosis adalah penyakit zoonosis yang disebabkan oleh patogen Leptospira spp. (Etish et al., 2014). Leptospirosis merupakan penyakit zoonosis penting (Etish et al., 2014), ditemukan hampir di seluruh dunia dan dikenal sebagai penyakit yang menimbulkan masalah kesehatan masyarakat global karena angka kejadiannya yang meningkat, baik di
negara berkembang maupun di negara maju (Vijayachari et al., 2008).
Leptospirosis pada ternak dapat menyebabkan kerugian ekonomi pada industri peternakan akibat gangguan reproduksi yang ditimbulkannya. Gangguan reproduksi yang ditimbulkan leptospirosis seperti abortus, anak lahir mati, atau lemah. Hal ini sangat berpengaruh terhadap peningkatan produksi ternak di dalam suatu peternakan.
Leptospirosis pada anjing dapat disebabkan oleh infeksi dari berbagai serovar leptospira interrogans antara lain L. australis, L. autumnalis, L. ballum, L. batislava, L. bataviae, L. canicola, L. grippotyphosa, L. hardjo, L. pomona, L. tarassovi, L. icterohaemorrhagica. Perpindahan leptospira ke hewan atau individu lainnya dapat melalui kontak langsung dan tidak langsung. Pada anjing, tanda klinis akan muncul setelah masa inkubasi yang berlangsung selama 5-15 hari (rata-rata 1 minggu). Hewan yang menderita per-akut akan menunjukkan gejala berupa anoreksia (hilangnya nafsu makan), lesu, hiperestesi otot-otot perifer, pernafasan yang dangkal, muntah, demam, mukosa pucat dan detak jantung cepat. Kerusakan sel-sel trombosit akan mengakibatkan koagulasi perivaskuler yang luas sehingga terjadi ptechie dan acchymoses di kulit, epistaksis dan melena. Tanda klinis lain yang cukup khas adalah jaundice (kekuningan) pada membran mukosa.
Diagnosa terhadap leptospirosis tidak cukup hanya berdasarkan tanda klinis, hematologi, dan kimiawi darah. Ada dua uji serologi yang biasa digunakan yaitu Microscopic Aglutination Test (MAT) dan Enzyme-Linked Immunosorbent Assay (ELISA). MAT merupakan uji serologi yang paling banyak digunakan pada anjing (Sykes et al., 2011; Senthil et al., 2013). Uji MAT dianggap sebagai baku emas untuk mendiagnosis leptospirosis (Dutta et al., 2005). Uji ini juga digunakan pada seroinvestigasi leptospirosis pada sapi (Rocha, 1998; Ebrahimi et al, 2004) dan pengujian sera manusia (Darodjat dan Ronohardjo, 1989) serta menentukan seroprevalensi sera manusia dan hewan (Ratnam et al, 1994). Pada uji MAT digunakan antigen hidup dan diperlukan banyak serogrup sebagai antigen untuk hasil yang optimum.
Penelitian ini bertujuan memperoleh data tentang kejadian leptospirosis pada anjing kintamani di Bali. Secara khusus bertujuan untuk mengetahui seroprevalensi leptospirosis pada anjing kintamani di Bali.
MATERI DAN METODE
Sampel Serum
Sampel yang diambil berasal dari 55 ekor anjing kintamani di Bali yaitu di Kota Denpasar, Kabupaten Tabanan, Kabupaten Gianyar, dan Kabupaten Bangli. Serum dipisahkan dari darah yang sebelumnya diambil. Selanjutnya pengujian serologi MAT (Microscopic Agglutination Test) dilakukan di Balai Besar Penelitian Veteriner Bogor.
Pemeriksaan secara microscopic
agglutination test (MAT)
Pemeriksaan pendahuluan sebanyak 0,05 ml enceran serum 1:50 diisikan pada lubang microtiter plate, kemudian tambahkan 0,05 ml antigen, dan diinkubasi pada suhu 30ºC selama 2 jam.
Dengan menggunakan deluter campuran serum dan antigen dipindahkan ke kaca objek (tidak ditutup dengan kaca penutup) dibaca dengan mikroskop medan gelap pada pembesaran 100x. Serum yang menunjukkan reaksi 50% aglutinasi atau lebih dilakukan titrasi. Titrasi sebanyak 0,05 ml enceran serum 1:100, 1:200, 1:400 dan 1:1600
masing-masing diteteskan dalam lubang-lubang microtiter plate, dan kemudian masing-masing enceran tersebut ditambahkan 0,05 ml antigen yang menunjukkan reaksi positif pada pemeriksaan pendahuluan, dan diinkubasi pada suhu 30ºC selama 2 jam. Pembacaan dilakukan seperti pada pemeriksaan pendahuluan. Titik akhir pembacaan adalah 50% aglutinasi (atau 50% leptospira yang tidak teraglutinasi) dan titer didefinisikan sebagai “enceran akhir tertinggi serum dalam campuran serum dan antigen yang menunjukkan 50% aglutinasi atau lebih”
HASIL DAN PEMBAHASAN
Hasil
Hasil pemeriksaan menunjukkan bahwa 10 dari 55 sempel serum (18,18%) bereaksi positif terhadap satu atau lebih serovar (Tabel 1). Dari 10 sampel serum yang positif tersebut, 2 sampel (3,64%) bereaksi positif
terhadap tiga serovar; 5 sampel (9,09%) bereaksi positif terhadap dua serovar; dan 3 sampel (3,64%) bereaksi positif terhadap satu serovar.
Tabel 1. Hasil Uji Serologi MAT Terhadap Leptospirosis pada Anjing Kintamani Asal Bali
|
Hasil Pemeriksaan |
Jumlah sampel |
% |
Serovar |
|
Positif terinfeksi |
10 |
18,18 | |
|
1 serovar |
3 |
5,45 |
2 (cel) 1 (can) |
|
2 serovar |
5 |
9,09 |
4 (cel + can) 1 (cel + ict) |
|
3 serovar |
2 |
3,64 |
1 (cel + can + ict) 1 (cel + can + cyn) |
|
Negatif Total |
45 55 |
81,82 100 |
- |
Keterangan: cel = serovar celledoni; can = serovar canicola; cyn = serovar cynopteri; ict = serovar ichterohemorrhagiae
10
8
6
4
2
0
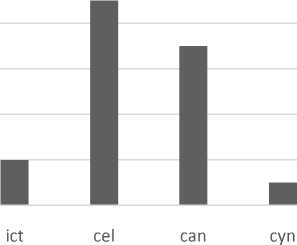
Gambar 1. Jumlah Serovar Pengujian Serologi MAT Terhadap Leptospirosis pada Anjing Kintamani Asal Bali. (ict = serovar ichterohemorrhagiae; cel = serovar celledoni; can = serovar canicola; cyn = serovar cynopteri).
Dari hasil penelitian ini, terdeteksi 4 serovar dari 14 serovar standar yang digunakan untuk pengujian leptospirosis di Indonesia (Gambar 1). Keempat serovar tersebut berasal dari Leptospira interrorgans serovar Celledoni, Leptospira interrorgans
serovar Canicola, Leptospira interrorgans serovar Cynopteri dan Leptospira interrorgans serovar Ichterohemorrhagiae. Jumlah terbanyak ditemukan pada Leptospira interrorgans serovar Celledoni. Dari sepuluh sampel serum yang bereaksi positif terhadap leptospira, sembilan di antaranya adalah Leptospira interrorgans serovar Celledoni.
Pembahasan
Hasil pemeriksaan serologi MAT terhadap 55 serum anjing kintamani menunjukkan bahwa 10 serum bereaksi positif terhadap satu atau lebih serovar. Hasil ini memberikan gambaran bahwa seroprevalensi kasus leptospirosis pada anjing kintamani di Bali yaitu 18,18%. Hasil penelitian ini merupakan laporan pertama seroprvalensi leptospirosis pada anjing kintamani yang ada di Bali.
Di antara kejadian leptospirosis pada hewan di Indonesia, seroprevalensi leptospirosis pada anjing kintamani cukup rendah. Jika dibandingkan dengan seroprevalensi leptospirosis pada anjing di negara-negara lain, seroprevalensi leptospirosis pada anjing kintamani di Indonesia, khususnya di Bali, juga tergolong rendah. Seroprevalensi leptospirosis pada anjing di Kerala India adalah 36,36% (Soman et al., 2014). Publikasi lain menyebutkan bahwa seroprevalensi leptospirosis pada anjing di United States pada tahun 2002-2004 adalah lebih dari 20% (George et al., 2006).
Seroprevalensi leptospirosis pada anjing kintamani asal Bali ini didominasi oleh Leptospira interrorgans serovar Celledoni, dimana serovar ini banyak ditemukan di Australia. Di Australia, serovar yang pertama kali diisolasi adalah Leptospira weili serovar Celledoni yang diisolasi di Ingham pada tahun 1952 dan di Queensland yang diisolasi pada tahun 1995, menggunakan Random Ampilified Polymorphic DNA (RAPD) (Henry et al., 2002).
KESIMPULAN
Seroprevalensi leptospirosis pada anjing kintamani di Bali adalah 18,18%. Leptospira
interrorgans serovar Celledoni paling umum ditemukan pada anjng Kintamani.
DAFTAR PUSTAKA
Darodjat M, Ronohardjo P. 1989. Diagnosa
serologic microscopic agglutination test
(MAT) untuk leptospirosis pada serum manusia. Penyakit Hewan XXI (37).
Semester I: 1-8.
Dutta TK, Chistopher M. 2005. Leptospirosis – An overview. J Assoc Physicians India 2005. 53: 545-551.
Ebrahimi A, Nasar Z, Kojouri GHA. 2004.
Seroinvestigation of bovine leptospirosis in shahrekord district, central Iran. Iranian J. Vet. Res. University of Shiraz. 5 (2) Ser. (10). 1383: 110-113.
Etish JL, Chapman PS, Klag AR. 2014. Acquired nephrogenic diabetes insipidus in a dog with leptospirosis. Irish Vet J. 67: 7.
George EM, Lynn FG, Nita WG, Richard JC. 2006. Canine Leptospirosis, United States, 2002-2004. Emerging Infectious Diseases.
Henry R, Barnett L, Dohnt M, Smythe L, Greene T. 2002. Proffered Papper 18. Molecular Analysis of Veterinari Pathogens. School of
Biomolecularand Biomedical Science, Griffith University Logan, Queensland, Australia.
Ratnam S, Everard COR, Alex C. 1994. A pilot study on the prevalence of leptospirosis in Tamilmadu State. Indian Vet. J. 71: 10591063.
Rocha T. 1998. A review of leptospirosis in farm animals in Portugal. Rev. Sci. Tech. Off. In. Epiz. 17(3): 699-712.
Senthil NR, Palanivel KM, Rishikesavan R. 2013. Sereoprevalence of leptospiral antibodies in canine population in and around Namakkal. J Vet Med. Article ID 971810 : 4.
Soman M, Jayaprakasan V, Mini M. 2014. Epidemiological Study on Human and Canine Leptospirosis in Central and North Kerala, India.
Sykes JE, Hartmann K, Lunn KF, Moore GE, Stoddard RA, Goldstein RE. 2011. ACVIM small animal consensus statement on leptospirosis: diagnosis, epidemiology,
treatment, and prevention. J Vet Intern Med. 25: 1-13.
Vijayachari PAP, Sugunan AN, Shriram. 2008. Leptospirosis: an emerging global public health problems, J Biosci 33(4): 557-569.
44
Discussion and feedback