PROFIL KANDUNGAN KIMIA EKSTRAK ETANOL 80% KULIT BATANG Michelia champaca L. DENGAN KROMATOGRAFI LAPIS TIPIS DAN PEREAKSI PENDETEKSI
on
Profil Kandungan Kimia Ekstrak Etanol 80% Kulit Batang Michelia champaca L. dengan Kromatografi
Lapis Tipis dan Pereaksi Pendeteksi Normansyah, A., Ariantari, N. P., Astuti, K. W.
PROFIL KANDUNGAN KIMIA EKSTRAK ETANOL 80% KULIT BATANG Michelia champaca L. DENGAN KROMATOGRAFI LAPIS TIPIS DAN PEREAKSI PENDETEKSI
Normansyah, A 1, Ariantari, N.P 1, Astuti, K.W 1
1Jurusan Farmasi Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Udayana
Korespondensi: Normansyah, A
Jurusan Farmasi – Fakultas Matematika Dan Ilmu Pengetahuan Alam – Universitas Udayana
Jalan Kampus Unud-Jimbaran, Jimbaran-Bali, Indonesia 80364 Telp/Fax: 0361-703837
Email : normansyah.andri19@gmail.com
ABSTRAK
Michelia champaca L. (Magnoliaceae) merupakan tanaman yang secara tradisional telah digunakan oleh masyarakat untuk mengobati demam. Penelitian sebelumnya menunjukan bahwa ekstrak n-heksan, kloroform dan metanol kulit batang cempaka kuning diketahui mengandung minyak atsiri dan terpenoid, selain itu pada ekstrak kloroform terdapat flavonoid dan ekstrak metanol mengandung tanin. Penelitian ini bertujuan untuk mengetahui kandungan kimia yang terdapat dalam ekstrak etanol 80% kulit batang M. champaca L dengan menggunakan metode KLT dan pereaksi pendeteksi.
Identifikasi kandungan kimia ekstrak etanol 80% kulit batang M. champaca L dengan metode KLT dilakukan dengan menggunakan fase diam silika gel GF254 dan fase gerak kloroform:metanol (95:5 v/v). Bercak diamati pada sinar UV dengan panjang gelombang 254 nm, 366 nm serta disemprot dengan pereaksi pendeteksi H2SO4 dan uap ammonia. Hasil yang didapatkan menunjukkan bahwa bercak nomor 1, 4, 5 dan 9 dengan Rf berturut-turut sebesar 0,08; 0,28; 0,35 dan 0,89 diduga termasuk ke dalam golongan terpenoid, karena setelah disemprot dengan H2SO4 10% dan dipanaskan, terjadi perubahan warna menjadi merah muda, magenta dan ungu. Sedangkan pada bercak nomor 3 dan 8 dengan Rf berturut-turut sebesar 0,21 dan 0,77 diduga termasuk ke dalam golongan flavonoid, karena berwarna hijau pada UV 366 nm dan tidak mengalami perubahan warna setelah diuapi dengan ammonia. Berdasarkan hasil tersebut, dapat disimpulkan bahwa ekstrak etanol 80% M. champaca L. mengandung senyawa flavonoid dan terpenoid.
Kata Kunci : Ekstrak Etanol 80%, Kandungan Kimia, KLT, Michelia champaca L., Pereaksi Pendeteksi
-
1. PENDAHULUAN
Cempaka kuning (Michelia champaca L.) merupakan salah satu tanaman yang termasuk dalam suku Magnoliaceae dan sering digunakan untuk pengobatan oleh masyarakat Bali. Umumnya masyarakat sering menggunakan rebusan kulit batang M. champaca L. untuk mengobati demam (Widyaningrum, 2011).
Penelitian yang dilakukan oleh Ariantari dan Rustini (2013) melaporkan bahwa ekstrak metanol kulit batang cempaka kuning diketahui memiliki kandungan kimia minyak atsiri, terpenoid, glikosida, tanin dan flavonoid.
KLT merupakan metode pemisahan yang dapat digunakan untuk memisahkan senyawa campuran menjadi komponen-komponen tunggalnya. Metode ini masih banyak digunakan karena mampu memisahkan campuran senyawa dengan cukup baik, pelaksanaannya mudah juga pemilihan fase diam dan fase gerak dapat
disesuaikan dengan komponen yang ingin dipisahkan (Gandjar dan Rohman, 2007). Penelitian untuk menentukan kandungan kimia dalam suatu tanaman obat, perlu dilakukan untuk mengetahui kandungan yang memiliki aktivitas farmakologis. Hal tersebut dilakukan sebagai standarisasi bahan baku obat tradisional sehingga dapat dikembangkan menjadi fitofarmaka (Wijono, 2003).
Pada penelitian ini, akan ditentukan profil kandungan kimia ekstrak etanol 80% kulit batang M. champaca L. dengan menggunakan metode KLT dan pereaksi pendeteksi.
-
2. BAHAN DAN METODE
-
2.1 Bahan Penelitian
-
Kulit batang cempaka kuning (M. champaca L.) didapatkan dari daerah Pupuan, Tabanan. Determinasi tanaman dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Kebun Raya Eka
Karya Bedugul. Pelarut yang digunakan yaitu etanol 96% (teknis) dan akuades. Pada KLT bahan-bahan yang digunakan yaitu Lempeng silika GF254 (Merck 0,25 mm), kloroform pa, metanol pa, amoniak pa akuades dan asam sulfat 10%.
-
2.2 Alat Penelitian
Alat yang digunakan pada penelitian ini adalah vaccum rotary evaporator, alat-alat gelas, lampu UV (CAMAG), timbangan analitik dan pipet kapiler.
-
2.3 Prosedur Penelitian
-
2.3.1 Pembuatan Ekstrak Etanol Kulit Batang
-
M. champaca L.
Serbuk kulit batang M. champaca L. yang telah kering, didigesti dengan etanol 80% selama 2 jam pada suhu 500C menggunakan rotary evaporator lalu maserat yang dihasilkan disaring. Maserat yang dihasilkan disaring, ditampung dan diendapkan semalam. Maserat diuapkan kembali dengan vaccum rotary evaporator lalu dioven untuk mendapatkan ekstrak kental. Setelah
didapatkan ekstrak kental, kemudian ditimbang menggunakan timbangan analitik.
-
2.3.3 Kromatografi Lapis Tipis Ekstrak Etanol
Kulit Batang M. champaca L.
Sepuluh miligram ekstrak kulit batang M. champaca L. dilarutkan dalam 1 mL etanol 80%. Sebanyak 10 μL kemudian ditotolkan pada plat KLT silika gel GF254 yang telah diaktifkan. Plat KLT dimasukkan ke dalam chamber yang telah dijenuhkan dan dielusi. Plat dikeringkan dalam oven pada suhu 50oC, lalu diamati di bawah sinar UV 254 nm dan 366 nm. Selanjutnya, plat KLT disemprot dengan pereaksi pendeteksi H2SO4 10%v/v dan ammonia serta diamati reaksi warna yang terjadi.
-
3. HASIL
Profil kromatogram hasil KLT fase normal ekstrak etanol 80% kulit batang M. champaca L. ditampilkan pada gambar 3.1. Hasil uji menunjukkan bahwa ekstrak tesebut mengandung senyawa golongan flavonoid dan triterpenoid.
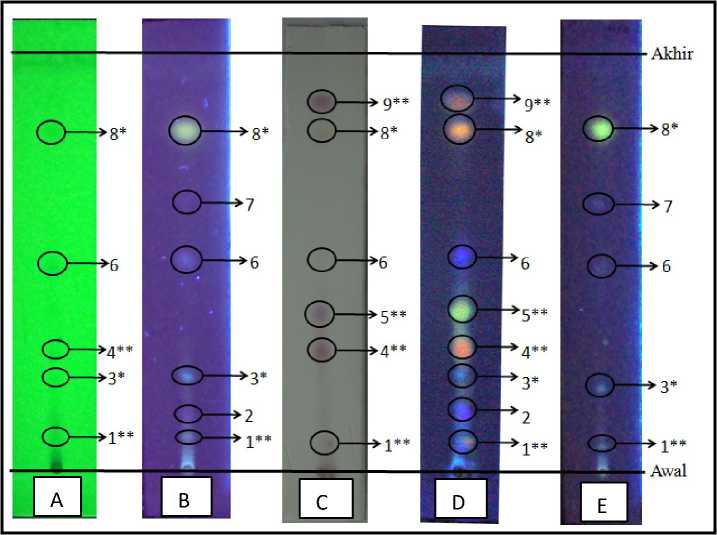
Gambar 3.1 Profil kromatogram ekstrak etanol 80% kulit batang M. champaca L. dengan fase diam silika gel GF254 , pada pengamatan (A) Sinar UV 254 nm, (B) Sinar UV 366 nm, (C)
setelah disemprot H2SO4 10%, (D) setelah disemprot H2SO4 10% kemudian diamati pada UV 366 nm dan (E) diuapi dengan ammonia dan diamati pada UV 366 nm
Keterangan:
-
- * = Diduga mengandung senyawa golongan flavonoid
-
- ** = Diduga mengandung senyawa golongan terpenoid
-
4. PEMBAHASAN
Pembuatan ekstrak etanol kulit batang M. champaca L. dilakukan dengan metode digesti menggunakan pemanasan lemah, yaitu pada suhu 40o-50o C. Untuk meningkatkan kecepatan difusi zat aktif ke dalam pelarut sehingga mempercepat proses penyarian (Departemen Kesehatan RI, 1986). Proses digesti dilakukan dengan pelarut etanol 80% karena etanol merupakan pelarut yang bersifat universal dengan indeks polaritas 5,2 (Poeloengan, 2007) sehingga senyawa polar maupun nonpolar dapat terekstraksi secara maksimal.
Ekstak yang diperoleh dipisahkan dengan metode KLT. Berdasarkan data pada gambar 3.1, terdapat 9 bercak hasil pemisahan yang teramati pada KLT ekstrak etanol 80% kulit batang M. champaca L. Bercak nomor 1, 4, 5 dan 9 dengan Rf berturut-turut sebesar 0,08; 0,28; 0,35 dan 0,89 diduga termasuk ke dalam golongan terpenoid, karena setelah disemprot dengan H2SO4 10% dan dipanaskan, terjadi perubahan warna menjadi merah muda, magenta dan ungu. Menurut Sharifa et al. (2012), senyawa terpenoid akan membentuk warna merah muda hingga ungu atau violet setelah disemprot dengan H2SO4 10% dan dipanaskan. Sedangkan pada bercak nomor 3 dan 8 dengan Rf berturut-turut sebesar 0,21 dan 0,77 diduga termasuk ke dalam golongan flavonoid. Berdasarkan Markham (1988), bercak nomor 3 dengan nilai Rf sebesar 0,21 termasuk dalam golongan flavonoid auron yang tidak mengandung 4’-OH bebas atau flavanon tanpa 5-OH bebas atau flavonol yang mengandung 3-OH bebas dan disertai atau tanpa 5-OH bebas, karena berwarna hijau pada UV 366 nm dan tidak mengalami perubahan warna setelah diuapi dengan ammonia. Sedangkan bercak nomor 8 dengan Rf sebesar 0,77, termasuk dalam golongan flavonoid yaitu flavonol yang mengandung 3-OH bebas dan mempunyai atau tidak mempunyai 5-OH bebas karena berflouresensi kuning pada pengamatan dibawah sinar UV 366 nm dan tidak mengalami perubahan warna setelah diuapi dengan ammonia. Senyawa terpenoid merupakan senyawa yang tersusun atas isopren. Senyawa terpenoid dilaporkan memiki berbagai aktivitas biologis seperti antimalaria (Graziose et al., 2012), antibakteri (Gupta, 2011) dan antioksidan (Hashem et al., 2012). Flavonoid merupakan senyawa polifenol dengan susunan C6-C3-C6 sebagai kerangka dasar. Senyawa flavonoid dilaporkan memiliki berbagai aktivitas biologis
seperti antibakteri (Saravanakumar, 2009), antimalaria (Fotie, 2008), antifungal (Kanwal et al., 2010), dan antivirus (Zandi et al., 2011).
-
5. KESIMPULAN
Hasil penelitian menunjukkan bahwa ekstrak etanol 80% Michelia champaca L. mengandung senyawa terpenoid dan flavonoid. Perlu dilakukan penelitian lanjutan untuk melihat aktivitas farmakologis serta pemisahan kandungan kimia dari kulit batang M. champaca L.
UCAPAN TERIMA KASIH
Staf Laboratorium Farmakognosi dan Fitofarmasi Jurusan Farmasi Fakultas MIPA Universitas Udayana atas bantuan dan dukungannya.
DAFTAR PUSTAKA
Ariantari, N. P., Rustini, N. L., Tumewu L., Hafid A. F., Widyawaruyanti A. 2013. Aktivitas Antimalaria Ekstrak Kulit Batang Cempaka Kuning Terhadap Plasmodium Falciparum 3D7. Jurnal Ilmu Kefarmarsian Indonesia Vol. 11(1): 66-69
Departemen Kesehatan RI. 1986. Sediaan Galenik. Jakarta: Direktorat Jendral Badan Pengawas Obat dan Makanan. P. 143-145
Fotie, J. 2008. The Antiprotozoan Potential of Flavonoids. Pharmacognosy Review, Vol. 2(3): 6-19
Gandjar, I. G. dan A. Rohman. 2007. Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal: 86-94
Graziose, R., Rathinasabapathy T., Lategan C., Poulev A., Smith P.J., Grace M., Lila M.A., and Raskin I. 2011. Antiplasmodial Activity of Aporphine Alkaloids and Sesquiterpene Lactones from Liriodendron tulipifera L. Journal Ethnopharmacol, Vol. 133(1):26-30.
Gupta, N., 2011. Antimicrobial ActivityPattern of Certain Terpenoids. International Journal of Pharma and Bio Sciences, Vol. 2(1): 8791
Hashem, F. A., Sengab, A. E., Shabana, M. H., and Khaled S. 2012. Antioxidant Activity of Mayodendron igneum of Isolated Terpenoids. Journal of Medicinally Active Plants, Vol: 1(3): 88-97
Kanwal, Q., Hussain, I., Hamid, L. S., and Javaid, A., 2010. Antifungal Activity of Flavonoids Isolated from Mango (Mangifera indica L.)
Leaves. Natural Product Research, Vol. 24(20):1907-1914
Markham, K.R. 1988. Cara Mengidentifikasi Flavonoid. Bandung: Penerbit ITB. Hal: 20-25
Poeloengan, M., Andriani, Susan, M. N., Komala, I., dan Hasnita M., 2007. Uji Daya Antibakteri Ekstrak Etanol Kulit Batang Bungur (Largerstoremia speciosa Pers) Terhadap Staphylococcus aureus dan Eschericia coli Secara In vitro. Seminar Nasional Teknologi Peternakan dan Veteriner, Hal: 776-782
Saravanakumar, A., Venkateshwaran, K., Vanitha, J., Ganesh, M., Vasudevan, M., and Sivakumar, T., 2009. Evaluation of Antibacterial Activity, Phenol and Flavonoid Contents of Thespesia populnea Flower Extracts. Pak. J. Pharm. Sci., Vol. 22(3): 282-286
Sharifa, A. A., Jamaludin, J., Kiong, L. S., Chia, L. A., dan Osman, K. 2012. Anti-Urolithiatic Terpenoid Compound from Plantago major Linn. (Ekor Anjing). Sains Malaysiana, Vol. 41(1): 33–39.
Widyaningrum H. 2011. Kitab Tanaman Obat Nusantara. Yogyakarta: MedPress: 620622
Wijono, S. H. S. 2003. Isolasi dan Identifikasi Flavonoid pada Daun Katu (Sauropus androgynus (L.) Merr). Makara, Sains, Vol 7 (2): 2
Zandi, K., Teoh, B. T., Sam, S. S., Wong, P. F., Mustafa, M. R., and AbuBakar, S., 2011. Antiviral Activity of Four Types of Bioflavonoid Againt Dengue Virus Type-2. Virology Journal, Vol. 8(1):560

JURNAL FARMASI UDAYANA
jurusan Farmasi-Fakultas mipa-universitas udayana
bukπ Jimbaran - bau
• (0361)703837 ‘Email: j Urnalfarmasiudavanafa gmail.com
SURAT PERNYATAAN
PERSETUJUAN PEMBIMBING
Yang bertandatangan di bawah ini, menyatakan bahwa :
|
Artikei dengan judul |
: Profd Ifonclungan Krmifo BKstrati ttααol 80% Kultt BotfotiQ Michfoio ⅛∣pc<a. L. dengan KrowotOQffoF' lapis IlpU dan ⅛∣⅛aκsi PwdeteKP |
|
Disusun oleh |
: Andri Norwansyoh |
|
NIM |
: OQcescsoog |
|
Email mahasiswa |
: WxnicWfoh. aodcdQ^gvnad com ■ |
Telah kami setujui untuk dipublikasi pada “Jurnal Farmasi Udayana”.
Demikian surat pernyataan ini kami buat, agar dapat dipergunakan sebagaimana mestinya.
Bukit Jimbaran, .÷1.. .⅛'.r!'.^ 20.. Pembimbing Tugas Akhir
Ni Puw Ariomvxi Λ ⅞w ,M ⅛ro >⅜f⅛
NIP. l⅛⅛U70÷ZCθS∞2Ct½
157
Discussion and feedback