Molecular Docking Sianidin dan Peonidin sebagai Antiinflamasi pada Aterosklerosis Secara In Silico
on
Susanti dkk.
pISSN: 2301-7716; eISSN: 2622-4607 Jurnal Farmasi Udayana, Vol 7, No.1, Tahun 2018, 28-33
Molecular Docking Sianidin dan Peonidin Sebagai Antiinflamasi pada Aterosklerosis Secara In Silico
Susanti, N. M. P.1*, D. P. D. Saputra1, P. L. Hendrayati1, I. P. D. N. Parahyangan1, I. A. D. G. Swandari1
1Program Studi Farmasi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana, Bukit Jimbaran, Badung, 80361
*Penulis korespondensi:: dekpitsusanti@unud.ac.id
Received June 27, 2018; Accepted July 5, 2018
ABSTRAK
Aterosklerosis merupakan penyakit inflamasi kronis yang diawali oleh disfungsi endotel sehingga terjadi pertumbuhan plak pada dinding dalam arteri. Disfungsi endotel menyebabkan endotel mengaktifkan NF-ĸB sehingga terjadi proses transkripsi gen proinflamasi yang mendukung pertumbuhan plak aterosklerosis. Antosianin ubi jalar ungu merupakan senyawa yang diketahui memiliki aktivitas menghambat proses inflamasi. Antosianin mayor yang terdapat dalam ubi jalar ungu adalah sianidin dan peonidin. Dilakukan uji aktivitas sianidin dan peonidin sebagai antiinflamasi pada aterosklerosis berdasarkan interaksinya pada protein NF-ĸB menggunakan metode molecular docking secara in silico. Tahapan penelitian yang dilakukan adalah penyiapan database struktur protein NF-ĸB, preparasi protein menggunakan aplikasi Chimera1.10.1, preparasi dan optimasi struktur 3D sianidin dan peonidin menggunakan aplikasi HyperChem8, serta validasi metode molecular docking dan docking sianidin dan peonidin pada protein NF-ĸB menggunakan aplikasi Autodock4.2. Hasil penelitian menunjukkan bahwa sianidin dan peonidin memiliki afinitas dan membentuk ikatan hidrogen dengan protein NF-ĸB. Energi ikatan antara sianidin dan peonidin dengan protein NF-ĸB berturut-turut sebesar -7,92 kkal/mol dan -7,86 kkal/mol yang sama-sama membentuk ikatan hidrogen dengan asam amino LEU472 pada binding site yang sama dengan native ligand. Sianidin dan peonidin memiliki potensi aktivitas sebagai antiaterosklerosis karena memiliki afinitas dengan protein NF-ĸB sehingga mempu mencegah proses inflamasi dalam pembentukan plak aterosklerosis.
Kata Kunci : Antiaterosklerosis, sianidin, peonidin, molecular docking, in silico
ABSTRACT
Atherosclerosis is a chronic inflammatory disease that begins with endothelial dysfunction resulting in plaque growth in the inner walls of the arteries. Endothelial dysfunction causes endothelial activates NF-ĸB resulting in a transcription of proinflammatory gene supporting the growth of atherosclerotic plaque. The purple sweet potato anthocyanin is a compound known to have activity inhibiting the inflammatory process. The major anthocyanins contained in purple sweetpotato are cyanidine and peonidine. The cyanidine and peonidin activity test was performed as antiinflammatory at atherosclerosis based on their interaction on NF-ĸB protein using molecular docking method in silico. The stages of this research are preparation of protein structure database of NF-ĸB, protein preparation using Chimera1.10.1 application, preparation and optimization of cyanidin and peonidin 3D structure using HyperChem8 application, and validation of molecular docking and docking method of cyanidin and peonidin on NF-ĸB protein using application Autodock4.2. The results showed that cyanidine and peonidine had affinity and formed a hydrogen bond with the NF-ĸB protein. The bond energy between cyanidine and peonidine with the NF-ĸB protein is -7.92 kcal/mol and -7.86 kcal/mol which together form the hydrogen bond with the LEU472 amino acid on the binding site equal to the native ligand. Cyanidin and peonidine have the potential of activity as antiatherosklerosis because it has an affinity with the NF-ĸB protein so that it prevents the inflammatory process in the formation of atherosclerotic plaque.
Keywords: Antiaterosklerosis, cyanidine, peonidine, molecular docking, in silico
Penyakit kardiovaskular merupakan penyakit akibat gangguan fungsi jantung dan pembuluh darah yang menyebabkan 31% atau sekitar 17,5 juta jiwa dari jumlah kematian dunia pada tahun 2012. Dari jumlah kematian tersebut, 7,4 juta disebabkan oleh penyakit jantung koroner (PJK) dan 6,7 juta oleh stroke (Kemenkes RI, 2017). PJK terjadi akibat penyempitan arteri koroner sehingga tidak ada aliran darah ke otot jantung. Hal yang mendasari terjadinya PJK adalah aterosklerosis yang merupakan inflamasi kronis pada dinding dalam arteri sehingga terjadi penebalan dan penurunan elastisitas (Srividya, 2017).
Hiperkolesterolemia kronik merupakan salah satu hal utama penyebab disfungsi endotel. Hiperkolesterolemia kronik akan menyebabkan terjadinya penimbunan LDL di daerah intima. Adanya radikal bebas akan menyebabkan teroksidasinya LDL yang disebut ox-LDL yang mampu mengaktifkan sel endotel sehingga menghasilkan sitokin proinflamasi dan molekul adhesi yang merangsang infiltrasi monosit dan limfosit T ke daerah intima. (Lintong, 2009; Hansson, 2005). Sitokin akan memicu diferensiasi monosit menjadi makrofag yang akan memfagositosis ox-LDL sehingga membentuk sel busa yang berkontribusi dalam terjadinya plak aterosklerosis (Ingersoll et al., 2011; Francis and Pierce, 2011). Selain itu, sitokin proinflamasi mampu menyebabkan fosforilasi IĸB sehingga NF-ĸB terlepas dari kompleks NF-ĸB-IĸB menuju nukleus untuk mendukung proses transkripsi gen proinflamasi (Ayukarningsih, 2014). Berdasarkan mekanisme terbentuknya plak tersebut, maka dilakukan penelitian guna pengembangan obat aterosklerosis salah satunya melalui mekanisme pencegahan pembentukan plak dengan penghambatan proses terjadinya infllamasi.
Antosianin merupakan senyawa yang diketahui memiliki aktivtas farmakologi sebagai antiinflamasi serta memiliki aktivitas dalam proteksi penyakit kardiovaskular. Dalam usus halus, antosianin akan dihidrolisis menjadi bentuk aglikon (antosianidin) yang lebih hidrofobik. Bentuk ini akan lebih mudah diabsorpsi secara difusi pasif dan
bioavailabilitasnya akan lebih baik dibandingkan dengan antosianin sehingga potensi efek yang dihasilkan juga semakin besar (Pojer et al., 2013; Speciale et al., 2014).
Beberapa penelitian mengenai aktivitas antiinflamasi antosianin dari ubi jalar ungu dalam menghambat proses inflamasi telah dilaporkan, dimana antosianin mayor yang terdapat dalam ubi ungu adalah sianidin dan peonidin (Lim et al., 2013). Maka dari itu, perlu dilakukan penelitian untuk mengetahui aktivitas sianidin dan peonidin sebagai antiinflamasi pada aterosklerosis berdasarkan interaksinya pada protein NF-ĸB menggunakan metode molecular docking secara in silico. Dengan metode ini dapat diketahui afinitas ikatan ligand uji serta interaksi yang terjadi sehingga dapat diprediksi potensi sianidin dan peonidin sebagai antiinflamasi pada aterosklerosis.
Bahan yang digunakan adalah protein NF-ĸB (pdb id: 4IDV) yang diunduh dari https://www.rcsb.org/ pdb/home/home.do dan struktur tiga dimensi sianidin dan peonidin dibuat dan dipreparasi menggunakan program HyperChem 8.
Seperangkat komputer dengan spesifikasi Windows 7 64 bit dan program Autodock 4.2 pada OS Windows, Chimera 1.10.1, dan HyperChem 8.
Preparasi protein NF-ĸB diawali dengan memilih protein dalam bentuk aktif yang berikatan dengan native ligand. Selanjutnya protein NF-ĸB dan native ligand dipisahkan dengan program Chimera 1.10.1 untuk menyediakan ruang (pocket/cavity) sehingga diketahui bentuk pocket dan koordinat pocket sebagai bahan docking.
Validasi metode molecular docking dilakukan dengan men-docking-kan kembali native ligand pada protein target yang sudah dihilangkan native ligand-nya menggunakan
program Autodock 4.2. Metode dikatakan
valid apabila nilai RMSD yang diperoleh ≤ 3Å
sehingga dapat dilakukan docking senyawa uji dengan protein target (Jain and Nicholls., 2008). Untuk memperoleh metode yang valid, maka dilakukan pengaturan pada grid box sehingga diperoleh nilai RMSD ≤ 3Å.
Struktur tiga dimensi senyawa uji sianidin dan peonidin dibuat dan dioptimasi menggunakan program HyperChem 8. Optimasi struktur dilakukan pada struktur tiga dimensi sianidin dan peonidin dengan metode komputasi semi-empiris AM1 dan dilakukan kalkulasi dengan single point serta optimasi geometri.
Senyawa uji sianidin dan peonidin yang telah dioptimasi di-docking-kan dengan protein NF-ĸB yang telah dihilangkan native ligand-nya menggunakan program Autodock 4.2 dengan grid box hasil validasi. Hasil analisis akan menunjukkan senyawa dengan konformasi dan energi ikatan terendah untuk berikatan dengan protein target.
Analisis data dilakukan berdasarkan hasil energi ikatan yang dihasilkan dari hasil molecular docking. Nilai energi ikatan menunjukkan kekuatan ikatan antara senyawa uji dengan reseptor. Semakin rendah energi ikatan, maka semakin kuat ikatan antara senyawa dengan reseptor. Interaksi yang terjadi antara sianidin dan peonidin dengan protein NF-ĸB dapat dilihat dari jenis ikatan yang terbentuk antara sianidin dan peonidin dengan protein target
Protein NF-ĸB memiliki 4 rantai, yaitu A, B, C, dan D. Native ligand inhibitor dari protein NF-ĸB, yaitu 4-{3-[2- amino-5-(2-methoxyethoxy) pyrimidin-4- yl]-1H- indol-5-yl}-2-methylbut-3-yn-2-ol (13V) terletak pada semua rantai protein NF-ĸB dan preparasi protein NF-ĸB pada penelitian ini menggunakan rantai A. Struktur protein NF-ĸB dan native ligand
yang sudah terpisah dapat dilihat pada gambar 1.
Validasi metode molecular docking dilakukan dengan men-docking-kan kembali protein NF-ĸB tanpa ligand dengan native ligand yang telah dipisahkan sebelumnya menggunakan program Autodock 4.2. Hasil dan visualisasi interaksi validasi metode molecular docking dapat dilihat pada tabel 1 dan gambar 2.
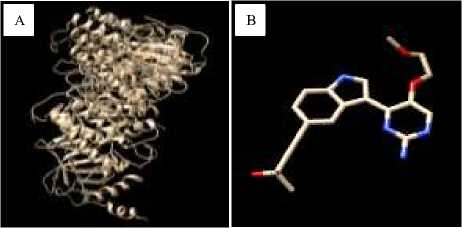
Gambar 1. Struktur Protein NF-ĸB (A) dan native ligand (B) yang telah terpisah dari proteinnya.
Tabel 1. Hasil Validasi Metode Molecular Docking
|
Ligan |
Energi Ikatan (Kkal/mol) |
RMSD (Å) |
Ikatan Hidrogen |
Gugus |
|
Native |
-9,84 |
1,80 |
PHE535 |
HN1- |
|
Ligand |
O1 |
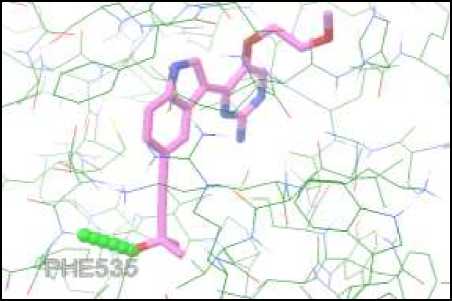
Gambar 2. Visualisasi Interaksi antara Native Ligand dengan Protein NF-ĸB. Interaksi berupa ikatan hidrogen ditandai dengan deretan bola berwarna hijau. Native ligand digambarkan dengan struktur berwarna ungu.
Kompleks protein digambarkan berupa struktur di sekitar native ligand.
Struktur 3D sianidin dan peonidin digambar dan dioptimasi menggunakan program HyperChem 8. Hasil dari optimasi struktur sianidin dan peonidin ditunjukkan pada gambar 3.
Docking sianidin dan peonidin dilakukan menggunakan program Autodock 4.2 dengan pengaturan koordinat tempat interaksi yang sama dengan koordinat tempat interaksi native ligand pada protein NF-ĸB. Hasil yang diperoleh dari proses docking antara sianidin dan peonidin dengan protein NF-ĸB berupa energi ikatan dan ikatan hidrogen yang terbentuk. Hasil dan visualisasi interaksi docking yang terjadi antara sianidin dan peonidin dengan protein NF-ĸB dapat dilihat pada tabel 2 dan gambar 4.
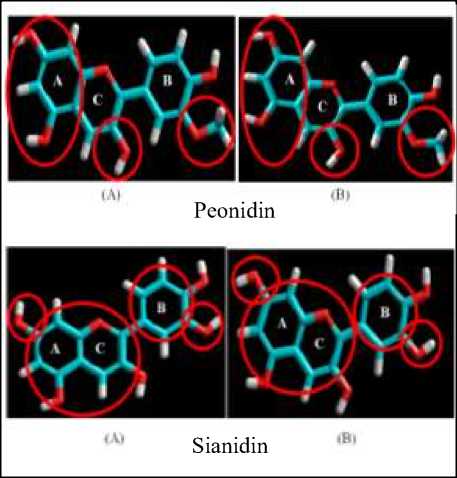
Gambar 3. Struktur 3D Sianidin dan Peonidin dengan Kalkulasi Single Point (A) dan Optimasi Geometri (B). Gugus yang mengalami pergeseran geometri ditunjukkan oleh lingkaran berwarna merah.
Preparasi protein NF-ĸB dilakukan dengan memisahkan protein dengan native ligand sehingga tersedia ruang (pocket/cavity) yang nantinya digunakan saat proses docking sianidin dan peonidin pada protein tersebut. Preparasi protein NF-ĸB menggunakan rantai A yang mengandung native ligand inhibitor 4-{3-[2-amino-5-(2-methoxyethoxy) pyrimidin-4-yl]-1H-indol-5-yl}-2-methylbut-3-yn-2-ol (13V). Hasil dari proses preparasi protein ini adalah struktur protein tanpa native ligand dan native ligand yang disimpan dalam bentuk file pdb.
Validasi metode molecular docking dilakukan dengan men-docking-kan kembali protein NF-ĸB tanpa ligand dengan native ligand yang telah dipisahkan sebelumnya menggunakan program Autodock 4.2. Parameter validasi metode yang digunakan adalah nilai RMSD (Root Mean Square Deviation) yang merupakan pengukuran dua pose dengan membandingkan posisi atom antara struktur eksperimental dengan struktur yang di-docking-kan pada protein (Lestari, 2015). Metode dikatakan valid apabila diperoleh nilai RMSD ≤ 3 Å, sehingga dari hasil validasi yang didapatkan menunjukkan bahwa metode yang
|
Tabel 2. Hasil Docking antara sianidin dan peonidin dengan protein NF-ĸB | |||
|
Ligan |
Energi Ikatan (Kkal/mol) |
Ikatan Hidrogen |
Gugus |
|
Sianidin |
-7,92 |
LEU472 |
HN-O3 |
|
Peonidin |
-7,86 |
LEU472 |
HN-O3 |
digunakan telah valid (Jain and Nicholls., 2008). Semakin kecil nilai RMSD yang diperoleh menunjukkan bahwa pose ligand yang diprediksi semakin baik karena semakin mendekati konformasi native ligand (Agistia dkk., 2013).Optimasi struktur 3D sianidin dan peonidin diawali dengan menggambar struktur sianidin dan peonidin, kemudian dilanjutkan dengan kalkulasi single point untuk mengetahui energi awal dari struktur 3D sianidin dan peonidin. Energi yang diperoleh saat dilakukan kalkulasi single point sianidin sebesar -3611,698392 kkal/mol dan peonidin sebesar -3857,658802 kkal/mol. Selanjutnya dilakukan optimasi geometri yang bertujuan untuk meminimalisasi energi agar diperoleh struktur sianidin dan peonidin yang paling stabil ditandai dengan penurunan nilai energi total
struktur 3D sianidin dan peonidin secara berturut-turut menjadi -3653,787721 kkal/mol dan -3920,027926 kkal/mol (Fitriasari, 2008). Docking sianidin dan peonidin pada active site dari protein NF-ĸB dilakukan menggunakan program Autodock 4.2 dengan pengaturan koordinat tempat interaksi yang sama dengan koordinat tempat interaksi native ligand pada protein tersebut. Hasil yang diperoleh dari proses docking antara sianidin dan peonidin dengan protein NF-ĸB berupa data energi ikatan dan ikatan hidrogen pada 10 konformasi terbaik. Energi ikatan menunjukkan afinitas antara sianidin dan peonidin dengan protein tersebut, semakin kecil energi ikatan yang diperoleh maka semakin stabil ikatan yang terbentuk (Laksmiani et al., 2016). Energi ikatan antara sianidin dan peonidin dengan protein NF-ĸB berturut-turut sebesar -7,92 kkal/mol dan -7,86 kkal/mol yang sama-sama membentuk ikatan hidrogen dengan asam amino LEU472.
Berdasarkan nilai energi ikatan yang diperoleh menunjukkan bahwa senyawa sianidin dan peonidin memiliki potensi aktivitas sebagai antiaterosklerosis karena memiliki afinitas dan membentuk ikatan hidrogen dengan protein NF-ĸB. Ikatan yang terjadi antara sianidin dan peonidin dengan protein NF-ĸB mampu menghambat transkripsi gen proinflamasi dan migrasi otot polos sehingga terbentuknya plak aterosklerosis pada dinding pembuluh darah dapat dihambat.
Sianidin dan peonidin memiliki potensi aktivitas sebagai antiaterosklerosis karena memiliki afinitas dan membentuk ikatan hidrogen dengan protein NF-ĸB sehingga mempu mencegah proses inflamasi dalam pembentukan plak aterosklerosis secara in silico.
Penulis mengucapkan terimakasih kepada semua pihak yang telah membantu penelitian ini.
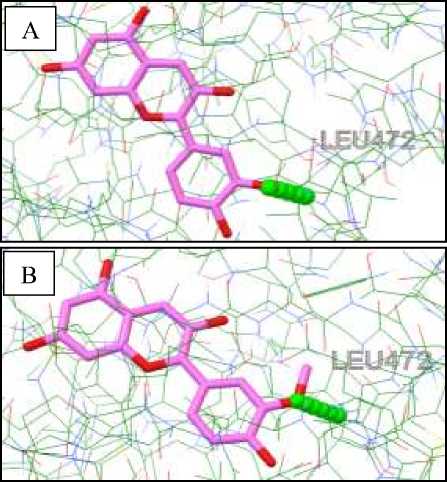
Gambar 4. Visualisasi Interaksi antara protein NF-ĸB dengan sianidin (A) dan peonidin (B).
Interaksi berupa ikatan hidrogen ditandai dengan deretan bola berwarna hijau. Sianidin dan peonidin digambarkan dengan struktur berwarna ungu. Kompleks protein digambarkan berupa struktur di sekitar sianidin dan peonidin.
DAFTAR PUSTAKA
Agistia, D. D., H. Purnomo, M. Tegar, A. E.
Nugroho. 2013. Interaksi Senyawa Aktif dari Aegle marmelos Correa sebagai Anti Inflamasi dengan Reseptor COX-1 dan COX-2. Traditional Medicine Journal. Vol.18:80-87
Ayukarningsih, Y. 2014. Efek α-Mangostin terhadap Aktivitas NF-ĸB, dan Kaspase-3 Enterosit pada Bayi Tikus Model Enterokolitis Nekrotikans. International Journal of Agriculture System. Vol.4:162-168
Fitriasari, A., N. K. Wijayanti, N. Ismiyati, D. Dewi. W. Kundarto, B. S. A. Sudarmanto, dan E. Meiyanto. 2008. Studi Potensi Kurkumin dan Analognya sebagai Selective Estrogen Receptor Modulator (SERMs): Docking pada Reseptor Estrogen β. Pharmacon. Vol.9:27-32
Francis, A. A. and G. N. Pierce. 2011. An Integrated Approach dor The Mecanism Responsible for
Atherosclerotic Plaque Regression. Experimental and Clinical Cardiology. Vol.16:77-86
Ingersoll, M. A., A. M. Platt, S. Potteaux, and G. J. Randolph. 2011. Monocyte Trafficking in Acute and Chronic Inflammation. Trends in Immunology. Vol.32:470-477
Jain, A. N. and A. Nicholls. 2008. Recommendation for Evaluation of Computational Methods. Journal of Computer-Aided Molecular Design. Vol.22:133-139.
Kemenkes RI. 2017. Penyakit Jantung Penyebab Kematian Tertinggi, Kemenkes Ingatkan Cerdik. Available at
go.id/pdf.php?id=17073100005 (Diakses pada 25 Juni 2018).
Laksmiani, N. P. L., N. L. P. V. Paramita, and I. M. A. G. Wirasuta. 2016. In Vitro and In Silico Antioxidant Activity of Purified Fractions from Purple Sweet Potato Ethanolic Extract. International Journal of Pharmacy and Pharmaceutical Sciences. Vol.8:177-181
Lestari, T. 2015. Studi Interaksi Senyawa Turunan 1,3-Dibenzoiltiourea sebagai
Ribonukleotida Reduktase Inhibitor. Jurnal Farmasi Indonesia. Vol.7:163-169
Lim, S., J. Xu, J. Kim, T. Chen, X. Su. J. Standard, E. Carey, J. Griffin, B. Herndon, B. Katz, J. Tomich, and W. Wang. 2013. Role of Anthocyanin-enriched Purple-fleshed Sweet Potato P40 in Colorectal Cancer Prevention. Molecular Nutrition and Food Research. Vol. 57:1908-1917.
Lintong, P. M. 2009. Perkembangan Konsep Patogenesis Aterosklerosis. Jurnal Biomedik. Vol.1:12-22
Pojer, E., F. Mattizi, D. Johnson, and C. S. Stockley. 2013. The Case for Anthocyanin Consumption to Promote Human Health: A Review. Comprehensive Reviews in Food Science and Food Safety. Vol.12:483-508
Speciale, A., F. Cimino, A. Saija, R. Canali, and F. Virgili. 2014. Bioavailability and Molecular Activities of Anthocyanins as Modulators of Endothelial Function. Genes and Nutrition. Vol.9:1-19
Srividya. 2017. Atherosclerosis-Coronary Heart Disease and The Recent Advancements in The Treatment of Aterosclerosis. Journal of Medical and Health Sciences. Vol. 6:1-9
33
Discussion and feedback