BIOSORPSI Cr(III) OLEH BIOSORBEN KULIT KAPUK (Ceiba pentandra (L.) Gaertn) TERAKTIVASI ASAM NITRAT
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 16 (1), JANUARI 2022 DOI: https://doi.org/10.24843/JCHEM.2022.v16.i01.p12
p-ISSN 1907-9850
e-ISSN 2599-2740
BIOSORPSI Cr(III) OLEH BIOSORBEN KULIT KAPUK (Ceiba pentandra (L.) Gaertn) TERAKTIVASI ASAM NITRAT
I W. Sudiarta*, A. A. S. D. Prameswari dan I M. S. Negara
Program Studi Kimia, Fakultas MIPA, Universitas Udayana, Bukit Jimbaran, Bali *Email: wayansudiarta@unud.ac.id
ABSTRAK
Kulit buah kapuk (Ceiba pentandra (L.) Gaertn) merupakan limbah pertanian yang kurang dimanfaatkan. Kulit buah kapuk mengandung senyawa organik seperti selulosa, hemiselulosa, dan lignin yang cukup tinggi. Komponen tersebut mengandung gugus hidroksil (-OH), karbonil (-C=O), dan karboksil (-COOH) yang dapat digunakan dalam proses biosorpsi. Penelitian ini bertujuan untuk mengetahui karakteristik biosorben kulit kapuk teraktivasi HNO3, kondisi optimum biosorpsi ion logam Cr (III), dan kapasitas biosorpsi biosorben kulit kapuk. Parameter yang dipelajari dalam penentuan karakteristik biosorben meliputi keasaman permukaan, jumlah situs akif, luas permukaan, dan gugus fungsi yang berperan dalam biosorpsi. Optimasi kondisi biosorpsi ion logam Cr (III) dilakukan dengan menentukan pH, waktu kontak, dan konsentrasi awal larutan Cr (III). Hasil penelitian menunjukkan bahwa biosorben teraktivasi HNO3 0,02 M (BAN3) memiliki karakteristik keasaman permukaan, jumlah situs aktif, dan luas permukaan berturut-turut sebesar 17,7949+0,5999 mmol/g, 1,0716+0,0361×1022 molekul/gram, dan 36,94147+0,00158 m2/g. Kondisi optimum biosorpsi ion logam Cr (III) pada pH 5, waktu kontak 90 menit, konsentrasi awal larutan Cr (III) 1800 mg/L. Proses biosorpsi mengikuti pola isoterm Langmuir dengan nilai R2 sebesar 0,975 dan kapasitas biosorpsi sebesar 59,28 mg/g. Karakterisasi menggunakan FTIR menunjukkan bahwa biosorben mengandung gugus fungsi seperti –OH, C=O, C-O-H, dan C-O-C yang berperan dalam proses biosorpsi.
Kata kunci: Biosorpsi,biosorben, Cr (III), kulit buah kapuk.
ABSTRACT
Kapok husk (Ceiba pentandra (L.) Gaertn) is an under-utilized agricultural waste. Kapok husk contains quite high percentage of organic compounds such as cellulose, hemicellulose, and lignin. Those compounds contain hydroxyl groups (-OH), carbonyl group (-C=O), and carboxyl group (-COOH) that can be used in the biosorptions process. This study aimed to determine the characteristic of the biosorbent activated by HNO3, the optimum conditions of the Cr (III) biosorption, and the biosorption capacity of the biosorbent. The parameters studied for determining characteristics of the biosorbent were surface acidity, number of active sites, surface specific area, and functional groups that play a role in the biosorption. Optimation condition of the Cr (III) biosorption was carried out by determining the pH, contact time, and initial concentration of Cr (III). The result showed that the activated kapok husk powder with HNO3 0,02 M (BAN3) has characteristics of surface acidity, the number of active site and surface specific area of 17,7949±0,5999 mmol/g, 1,0716±0,0361×1022 molecule/gram and 36,94147 ÷0,00158 m2/g respectively. The optimum conditions of the Cr (III) biosorption were obtained at pH 5, contact time 90 minutes, and initial concentration of Cr (III) at 1800 mg/L. Isotherm biosorption followed the Langmuir isotherm model with R2 value of 0,975 and biosorption capacity of 59,28 mg/g. Characterization using FTIR showed that biosorbent contained -OH, C=O, C-O-H, dan C-O-C functional groups which played a role in the biosorption process.
Keywords: Biosorption, biosorbent, Cr (III), kapok husk.
PENDAHULUAN
Kemajuan industri memberikan dampak negatif pada lingkungan berupa pencemaran. Pencemaran tersebut disebabkan oleh limbah industri yang mengandung logam berat yang dibuang begitu saja ke badan air tanpa melalui pengolahan terlebih dahulu, sehingga
menimbulkan pencemaran perairan. Keberadaan logam berat dalam konsentrasi tinggi pada lingkungan sangatlah berbahaya karena sifat toksik dan persistensinya di dalam lingkungan (Edelynna dkk., 2012).
Logam kromium merupakan salah satu logam yang banyak digunakan dalam industri seperti penyamakan kulit, elektroplating, tekstil,
dan cat. Logam kromium memiliki sifat toksik jika terakumulasi dalam tubuh dalam jangka panjang dan dapat menyebabkan gangguan kesehatan berupa iritasi paru-paru hingga kanker (ATSDR., 2012).
Berbagai metode pengolahan limbanh logam berat telah dikembangkan untuk mengurangi kadar logam berat dalam limbah diantaranya koagulasi, elektroanalisis, dan pemisahan membrane. Metode alternatif yang dapat digunakan untuk menangani pencemaran logam berat yaitu dengan metode biosorpsi menggunakan material biologis sebagai adsorben (biosorben). Penggunaan biosorben saat ini banyak dikembangkan dan digunakan secara luas karena harganya murah, memiliki kapasitas penyerapan yang tinggi dan ramah lingkungan (Ramalingam et al., 2014).
Mulyawan dkk. (2015) melaporkan bahwa daun ketapang dapat digunakan sebagai biosorben logam timbal.Biosorben dari kulit kopi terxanthasi telah dilaporkan oleh Adriansyahdkk. (2018) untuk biosorpsi logam berat Cu (II) dan Cr (VI). Sudiarta dan Sulihingtyas (2012) melaporkan pemanfaatan sabut kelapa hijau teramobilisasi EDTA untuk biosorpsi Cr (III). Selain beberapa jenis biosorben di atas, kulit kapuk sangat berpotensi dimanfaatkan sebagai biosorben karena memiliki kandungan selulosa, hemiselulosa, dan lignin yang cukup tinggi.
Putra (2014) melaporkan bahwa kandungan dan komponen kimia dalam kulit buah kapuk dari tiga daerah berbeda yaitu alfa-selulosa berkisar 23,82%-36,3%, hemiselulosa pada kulit buah kapuk berkisar 27,12%-33,25%, dan lignin berkisar 10,54%-26,02%. Komponen tersebut mengandung gugus aktif seperti hidroksil, karbonil, dan karboksil yang memiliki peran dalam penyerapan logam berat (Zein dkk., 2019).
Kapasitas biosorpsi suatu biosorben dapat ditingkatkan dengan aktivasi maupun modifikasi baik secara fisika maupun kimia. Pemakaian zat aktivator juga bertujuan memperluas permukaan adsorben sehingga pori-pori adsorben semakin membesar (Mufrodi dkk., 2008). Dalam penelitian ini asam nitrat (HNO3) digunakan sebagai aktivator untuk mengaktivasi biosorben, karena asam nitrat mempunyai ion H+ yang dapat melarutkan mineral pengotor dengan cara menukar ion logam atau mineral yang terikat pada biosorben dan melarutkan pengotor organik yang terdapat pada biosorben sehingga
situs aktif yang terbentuk semakin banyak (Sudiarta, 2012).
Berdasarkan latar belakang tersebut pemanfaatan kulit kapuk teraktivasi HNO3 sebagai biosorben logam Cr (III) menarik untuk diteliti sehingga dapat diketahui bagaimana kemampuan kulit kapuk dalam menyerap logam berat Cr (III). Kondisi yang mempengaruhi besarnya kapasitas biosorpsi seperti aktivasi, pH, waktu kontak, dan konsentrasi awal larutan Cr (III) dipelajari lebih lajut dalam penelitian ini.
MATERI DAN METODE
Bahan
Bahan-bahan kimia yang digunakan dalam penelitian ini antara lain HCl, HNO3, NaOH, phenolphthalein, CrCl3.6H2O, H2C2O4, K2Cr2O7, NaN3, H2SO4, KMnO4, NH4OH, aseton, difenil karbasida, metilen biru, aquadest, dan sampel kulit kapuk (Ceiba pentandra (L.) Gaertn) kering yang diperoleh dari wilayah kampus Universitas Udayana, Jimbaran.
Alat
Alat-alat yang digunakan dalam penelitian ini antara lain seperangkat alat gelas laboratorium, bola hisap, neraca analitik, magnetic stirer, kertas saring, pH meter, oven, ayakan ukuran 80 mesh dan 100 mesh, Spektrofotometer UV-Vis Shimadzu UV-1800, dan Spektrofotometer FTIR Shimadzu IR Prestige-2.
Prosedur Kerja
Penyiapan Biosorben Kulit Kapuk
Kulit kapuk yang sudah bersih dan kering dipotong kecil-kecil kemudian dihaluskan dengan blender lalu diayak dengan ayakan 80 mesh dan 100 mesh (ukuran partikel 150 µm – 180 µm). Serbuk dicuci kembali dengan aquades sampai bersih dan dikeringkan dalam oven bersuhu 70°C dan diberi kode BOO.
Aktivasi Biosorben Kulit Kapuk
Sebanyak 1 g biosorben BOO dimasukkan ke dalam erlenmeyer dan ditambahkan 25 mL larutan HNO3 0,005 M. Campuran diaduk selama 1,5 jam, kemudian residunya disaring dan dicuci dengan aquades hingga pH netral (pH 7) dan dikeringkan dalam oven bersuhu 70°C. Perlakuan yang sama dilakukan untuk aktivasi menggunakan larutan HNO3 0,01 dan 0,02 M. Biosorben dengan perlakuan ini berturut-turut diberi kode BAN1, BAN2, dan BAN3.
Penentuan Keasaman Permukaan Biosorben
Sebanyak 0,25 g BAN1, BAN2, dan BAN3 masing-masing dimasukkan ke dalam erlenmeyer dan ditambahkan 25,0 mL larutan NaOH 1 mol/L yang telah dibakukan, kemudian campuran diaduk selama 1,5 jam. Setelah 1,5 jam campuran disaring dan residunya dibilas dengan aquades. Filtrat bersama bilasan ditambah indikator phenolphthalein lalu dititrasi dengan larutan HCl 1 mol/L yang telah dibakukan. Titrasi juga dilakukan terhadap larutan blanko yang hanya mengandung larutan NaOH. Pengulangan dilakukan sebanyak tiga kali. Keasaman permukaan total dapat ditentukan dengan persamaan berikut:
„ 1 1 i (mmolλ [(V1-V2)×Mhc1 Keasamantotal ^-j = ——1^(1)
dimana V1 merupakan volume HCl titrasi blanko (mL), V2 merupakan volume HCl titrasi biosorben (mL), dan Bmassa biosorben (g)
Karakterisasi Luas Permukaan Biosorben
Sebanyak 0,10 g BAN1, BAN2, dan BAN3 masing-masing dimasukkan ke dalam erlenmeyer yang berisi 20,0 mL larutan metilen biru 50 mg/L. Campuran diaduk dengan variasi waktu 10, 20, 30, 40, 50, dan 60 menit. Campuran disaring dan metilen biru yang tersisa dalam filtrat dianalisis dengan Spektrofotometer UV-Vis. Percobaan diulangi sebanyak tiga kali (Dwipayana dkk., 2017). Luas permukaan dihitung dengan persamaan berikut:
xm .n . A s = --------.
Mr
.
(2)
dimana S merupakan luas permukaan adsorben (m2/g), N merupakan bilangan avogadro (6,022 x 1023 mol-1), Xm merupakan berat adsorbat teradsorpsi (g/g), Amerupakan luas penutupan oleh 1 molekul metilen biru (197 x 10-20 m2), dan Mr adalah massa molekul relatif metilen biru (320,5 g/mol).
Analisis Cr (III) sebagai Cr (VI)
Sebanyak 0,5 mL filtrat dimasukkan ke dalam erlenmeyer, selanjutnya ditambahkan 5 tetes NH4OH 1 mol/L, 1,0 mL H2SO4 1 mol/L, dan 20 mL aquades. Larutan dipanaskan selama 10 menit kemudian ditambahkan 2 tetes KMnO4 0,10 mol/L dan pemanasan dilanjutkan selama 2 menit. Larutan ditambah NaN3 0,08 mol/L
sampai larutan menjadi bening. Pemanasan dihentikan dan larutan didinginkan. Setelah dingin larutan dipindahkan ke dalam labu ukur 50 mLsecara kuantitatif, kemudian ditambahkan 1,0 mL H2SO4 1 mol/L dan 1 mL difenil karbasida 0,5% dan ditepatkan dengan aquades sampai tanda batas lalu dihomogenkan. Sampel dianalisis menggunakan Spektrofotometer UV-Vis pada panjang gelombang maksimumnya (APHA et al., 1998).
Penentuan pH Optimum Biosorpsi Cr (III)
Sebanyak 0,25 g biosorben BAN optimum masing-masing dimasukkan ke dalam erlenmeyer lalu ditambahkan sebanyak 10,0 mL larutan Cr (III) 200 mg/L dan pH larutan diatur masing-masing pada pH 1, 2, 3, 4, dan 5. Campuran diaduk selama 1,5 jam. Campuran disaring dan Cr (III) yang tersisa pada filtrat dianalisis dengan Spektrofotometer UV-Vis sebagai kompleks Cr (VI)-Difenilkarbasida.
Percobaan diulangi sebanyak tiga kali. Jumlah ion logam Cr (III) yang terserap oleh setiap gram sampel dapat dihitung dengan persamaan berikut:
Wads =
Ci-C2 IOOO
× v×⅛
(3)
dimana Wads merupakan massa Cr (III) yang terserap oleh 1 gram sampel (mg/g), B merupakan massa sampel yang digunakan (g), C1 merupakan konsentrasiawal larutan Cr (III) (mg/L), C2 merupakan konsentrasi akhir larutan Cr (III) (mg/L), dan V adalah volume larutan Cr (III) (mL).
pH optimum dapat diketahui dengan membuat kurva antara banyaknya Cr (III) yang terserap oleh 1 gram sampel (mg/g) terhadap pH.
Penentuan Waktu Optimum Biosorpsi Cr (III)
Sebanyak 0,25 g BAN optimum dimasukkan ke dalam erlenmeyer dan masing-masing ditambah 10,0 mL larutan Cr (III) 200 mg/L dan diatur pada pH optimumnya. Campuran diaduk dengan variasi waktu 5, 10, 20, 30, 45, 60, 90, dan 120 menit. Selanjutnya campuran disaring dan Cr (III) yang tersisa pada filtrat dianalisis dengan Spektrofotometer UV-Vis sebagai kompleks Cr (VI)-Difenilkarbasida.
Percobaan diulangi sebanyak tiga kali. Jumlah ion logam Cr (III) yang terserap oleh setiap gram sampel dapat dihitung dengan
Persamaan 3. Waktu kontak optimum dapat diketahui dengan membuat kurva antara jumlah Cr(III) yang diserap oleh 1 gram sampel (mg/g) terhadap waktu kontak (menit).
Penentuan Konsentrasi Awal Larutan, Isoterm dan Kapasitas Biosorpsi Cr (III)
Sebanyak 0,25 g BAN optimum dimasukkan ke dalam erlenmeyer dan ditambahkan 10,0 mL larutan Cr (III) dengan konsentrasi 50, 100, 200, 300, 400, 500, 750, 1000, 1200, 1500, 1800, dan 2100 mg/L. Campuran diinteraksikan pada pH dan waktu kontak optimumnya. Campuran disaring dan Cr (III) yang tersisa pada filtrat dianalisis dengan Spektrofotometer UV-Vis sebagai kompleks Cr (VI)-Difenilkarbasida. Percobaan diulangi sebanyak tiga kali. Jumlah ion logam Cr (III) yang terserap oleh setiap gram sampel dapat dihitung dengan Persamaan 3.
Konsentrasi awal larutan dapat diketahui dengan membuat kurva antara jumlah ion logam Cr (III) yang diserap oleh 1 g sampel (mg/g) terhadap konsentrasi larutan (mg/L).
Pola isoterm dan kapasitas biosorpsi diketahui dengan melakukan uji linieritas dan perhitungan menggunakan Persamaan 4 dan Persamaan 5.
Pola Isoterm Langmuir:
- = - + —..................................................(4)
m b bK
dimana C merupakan konsentrasi Cr(III) dalam kesetimbangan (mol/L), m merupakan jumlah Cr(III) yang terserap per gram absorben (mg/gram), dan b adalah kapasitas biosorpsi.
Pola Isoterm Freundlich:
log m = log K + 1 log C.............................(5)
dimana m merupakan massa adsorbat terjerapper gram adsorben (mg/g), C merupakan konsentrasi kesetimbangan adsorbat setelah adsorpsi (mg/L).
Identifikasi Gugus Fungsi Biosorben dengan Spektrofotometer FTIR
Biosorben kulit kapuk tanpa aktivasi (BOO), dengan aktivasi HNO3 (BAN), dan biosorben yang sudah menyerap Cr (BAN-Cr) diuji dengan menggunakan Spektrofotometer Fourir Transform Infra Red. Spektra hasil analisis dibandingkan untuk mengetahui apakah terdapat perbedaan nilai bilangan gelombang dari gugus fungsi pada biosorben tanpa aktivasi
(BOO), dengan aktivasi HNO3 (BAN) dan yang sudah menyerap Cr (BAN-Cr).
HASIL DAN PEMBAHASAN
Keasaman Permukaan Biosorben
Penentuan keasaman permukaan biosorben BAN1, BAN2 dan BAN3 dilakukan dengan metode titrasi asam basa. Hasil keasaman permukaan dan jumlah situs aktif bisorben dapat dilihat pada Tabel 1.
|
Tabel 1. |
Keasaman dan biosorben |
jumlah situs aktif |
|
Biosorben |
Keasaman permukaan rata-rata SD (mmol/g) |
Jumlah situs aktif rata-rata SD (1022) (molekul/gram) |
|
BAN1 |
17,5460 0,6729 |
1,05662 0,0405 |
|
BAN2 |
16,9861 0,1865 |
1,02290 0,0112 |
|
BAN3 |
17,7949 0,5999 |
1,07161 0,0361 |
Berdasarkan uji statistik One Way Anova variasi konsentrasi aktivator tidak memberikan pengaruh yang signifikan terhadap nilai keasaman permukaan dan jumlah situs aktif, tetapi biosorben teraktivasi HNO3 0,02 M (BAN3) memberikan nilai keasaman permukaan dan jumlah situs aktif tertinggi yaitu sebesar 17,7949 0,5999 mmol/g dan 1,07161 0,0361×1022
molekul/g. Hal ini menunjukkan bahwa pada kondisi tersebut aktivator lebih mampu membersihkan pengotor yang terikat pada biosorben dan meningkatkan pembentukan situs asamBronsted yaitu gugus karboksil (-COOH) dan hidroksi (-OH) dari biosorben yang berperan mendonorkan proton/H+ (Sudiarta, 2009). Saat proses biosorpsi proton akan digantikan oleh ion logam sehingga semakin banyak situs asam yang terbentuk maka semakin banyak ion logam yang dapat teradsorpsi (Wogo dkk., 2014).
Karakterisasi Luas Permukaan Biosorben
Luas permukaan biosorben ditentukan dengan metode metilen biru, dimana banyaknya metilen biru yang terserap sebanding dengan luas permukaan biosorben. Hasil penentuan luas permukaan biosorben dapat dilihat pada Tabel 2.
Hasil uji statistik One Way Anova pada penentuan luas permukaan biosorben diperoleh hasil dimana variasi konsentrasi aktivator tidak memberikan pengaruh yang signifikan terhadap
nilai luas permukaan biosorben, tetapi biosorben teraktivasi HNO3 0,02 M (BAN3) memberikan nilai luas permukaan spesifik tertinggi yaitu sebesar 36,94147-0,00158m2∕g. Hal ini menunjukkan bahwa pada kondisi tersebut aktivator selain dapat meningkatkan pembentukan situs aktif pada biosorben juga dapat mengurangi pengotor berupa mineral dan senyawa organik yang terikat pada biosorben sehingga membuka pori dan memperluas permukaan biosorben sehingga lebih banyak biosorben yang teradsorpsi (Krismayanti dkk., 2019).
Tabel 2. Luas permukaan spesifik biosorben
kulit kapuk
|
Biosorben |
Xm rata-rata SD (10^3) (g/g) |
S rata-rata SD (m2/g) |
|
BAN1 |
9,9776 |
36,93223 0,00778 |
|
0,0021 | ||
|
BAN2 |
9,97710 |
36,93051 |
|
0,001 |
0,00359 | |
|
BAN3 |
9,9801 |
36,94147 |
|
0,0004 |
0,00158 |
Berdasarkan hasil karakterisasi penentuan keasaman permukaan dan luas permukaan maka biosorben yang memiliki keasaman dan luas permukaan tertinggi dimiliki oleh biosorben BAN3 yang selanjutnya ditentukan kondisi optimum penyerapan ion logam Cr (III).
Penentuan pH Optimum Biosorpsi Cr (III)
Penentuan pH optimum biosorpsi biosorben BAN3 dilakukan variasi pH pada larutan awal yaitu pada pH 1-5. Hasil penelitian menunjukkanjumlah ion logam Cr (III) terserap secara maksimal oleh biosorben pada pH 5dengan daya serap rata-rata sebesar 7,7291 0,0013 mg/g. Kurva jumlah ion logam Cr (III) yang terserap terhadap waktu interaksi dapat dilihat pada Gambar 1.
Pada pH 1 dan 2 jumlah ion logam Cr (III) yang terserap lebih sedikit, hal ini disebabkan karena adanya kompetisi antara ion H+ yang lebih banyak dalam larutan, sehingga kation logam Cr (III) sulit berikatan dengan situs-situs aktif pada biosorben. Pada pH 3 hingga 5 terjadi peningkatan jumlah ion logam Cr (III) yang terserap, karena pada kondisi ini jumlah ion H+ pada larutan mulai berkurang sehingga kompetisi antara kation logam Cr3+ dengan ion H+ berikatan pada biosorben juga berkurang. Sedangkan pada
pH di atas 5 menurut Nurafriyanti dkk. (2017) cenderung terjadi presipitasi ion Cr3+ karena bereaksi dengan ion OH- sehingga membentuk endapan Cr(OH)3 yang dapat menghalangi proses biosorpsi yang berlangsung. pH berperan dalam proses biosorpsi karena mempengaruhi muatan pada situs aktif dan muatan ion logam dalam larutan.
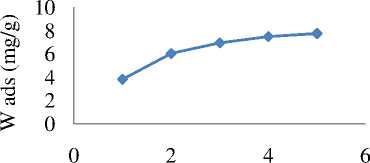
pH awal larutan Cr (III)
Gambar 1. Kurva jumlah ion logam Cr (III) yang terserap terhadap pH awal larutan.
Penentuan Waktu Kontak Optimum Biosorpsi Cr (III)
Waktu kontak optimum biosorpsi ditentukan pada pH optimum 5 dengan variasi waktu interaksi 5, 10, 20, 30, 45, 60, 90, dan 120 menit. Penentuan waktu kontak bisorpsi dilakukan untuk mengetahui pada waktu berapakah ion logam Cr (III) dapat terserap secara maksimal. Kurva jumlah ion logam Cr (III) yang terserap terhadap waktu interaksi dapat dilihat pada Gambar 2.
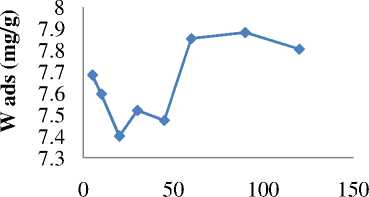
Waktu kontak (menit)
Gambar 2. Kurva jumlah ion logam Cr (III) yang terserap terhadap waktu kontak.
Berdasarkan Gambar 2. dapat dilihat pada awalnya serapan ion logam Cr (III) cenderung fluktuatif karena persaingan untuk berikatan dengan sisi aktif dan lemahnya ikatan ion logam Cr (III) pada biosorben sehingga ion logam Cr (III) yang terserap dapat terlepas dan terikat kembali pada sisi aktif biosorben. Pada menit ke 90 ion logam Cr (III) terserap secara maksimum oleh biosorben kulit kapuk dengan
daya serap rata-rata 7,8824+0,0098 mg/g. Kemudian pada menit ke 120 jumlah ion logam Cr (III) yang terserap mengalami penurunan. Pada kondisi tersebut biosorben sudah dalam keadaan jenuh berikatan dengan adsorbat sehingga apabila ditambahkan waktu biosorpsinya akan menyebabkan terjadinya proses desorpsi atau pelepasan kembali adsorbat dai biosorben.
Penentuan Konsentrasi Awal Larutan Cr (III)
Penentuan konsentrasi awal larutan bertujuan untuk mengetahui pada konsentrasi berapakah ion logam Cr (III) dapat terserap secara maksimal oleh biosorben. Penentuan konsentrasi awal dilakukan pada pH 5, waktu kontak 90 menit dan variasi konsentrasi larutan 50, 100, 200, 300, 400, 500, 750, 1000, 1200, 1500, 1800, dan 2100mg/L. Kurva jumlah ion logam Cr (III) yang terserap terhadap konsentrasi awal larutan dapat dilihat pada Gambar 3.

Konsentrasi larutan (mg/L)
Gambar 3. Kurva jumlah ion logam Cr (III) yang terserap teradap konsentrasi awal.
Berdasarkan Gambar 3. dapat dilihat bahwa dengan bertambahnya konsentrasi adsorbat yang diinteraksikan maka jumlah ion logam Cr (III) yang terserap juga mengalami peningkatan hingga titik optimumnya. Pada konsentrasi 50 mg/L hingga 1800 mg/L jumlah ion logam Cr (III) yang terserap terus mengalami peningkatan. Peningkatan ini terjadi karena situs aktif dan jumlah pori pada permukaan biosorben masih dapat menyerap adsorbat. Pada konsentrasi 1800 mg/L, ion logam Cr (III) terserap secara maksimal dengan daya serap rata-rata 58,8675 +0,0058 mg/g. Kemudian pada konsentrasi diatas 1800 mg/L jumlah ion logam Cr (III) yang terserap mengalami penurunan, karena konsentrasi ion logam Cr (III) yang berinteraksi semakin banyak, sedangkan situs aktif dan jumlah pori pada biosorben sudah
dalam keadaan jenuh dan tidak mampu menyerap adsorbat (Zein dkk., 2019)
Penentuan Pola Isoterm dan Kapasitas Biosorpsi
Pola isoterm biosorpsi pada biosorben kulit kapuk terhadap ion logam Cr (III) dapat diketahui dari persamaan regresi linier isoterm Langmuir dan persamaan regresi linier isoterm Freundlich. Pola isoterm yang dapat mewakili reaksi yang terjadi ditentukan dari nilai R2 yang paling mendekati nilai 1. Pola isoterm Langmuir dan Freundlich pada biosorben kulit kapuk dapat di lihat pada Gambar 4 dan Gambar 5.
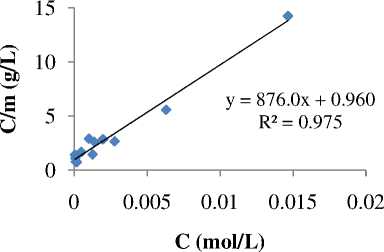
Gambar 4. Pola isoterm biosorpsi Langmuir pada biosorben kulit kapuk
-0.5
Log C (µg/mL)
0 0.5 1 1.5 2 2.5 3 3.5
0
M
-1
S
M
-1.5
-2
-2.5
y = 0.585x - 2.672 R² = 0.870
-3
Gambar 5. Pola isoterm biosorpsi Freundlich pada biosorben kulit kapuk
Pada Gambar 4 dapat diketahui persamaan isoterm Langmuir memiliki nilai R2 sebesar 0,975 dan pada Gambar 5 dapat diketahui bahwa persamaan isoterm Freundlich memiliki nilai R2 sebesar 0,870. Pola isoterm biosorpsi yang terjadi pada biosorpsi ion logam Cr (III) oleh biosorben kulit kapuk merujuk pada pola isoterm Langmuir karena memiliki nilai R2 paling mendekati 1. Pola isoterm Langmuir menandakan biosorpsi berlangsung satu lapis
(monolayer) dari molekul-molekul adsorbat dengan permukaan biosorben yang bersifat homogen karena masing-masing situs aktif hanya menyerap satu molekul.
Berdasarkan persamaan isoterm Langmuir selanjutnya dapat ditentukan kapasitas biosorpsi optimum ion logam Cr (III) yaitu sebesar 59,28 mg/g.
Identifikasi Gugus Fungsi Biosorben dengan Spektrofotometer FTIR
Identifikasi gugus fungsi bertujuan untuk mengetahui gugus fungsi yang terkandung pada biosorben kulit kapuk yang berperan dalam proses biosorpsi. Spektra hasil karakterisasi disajikan pada Gambar 6.
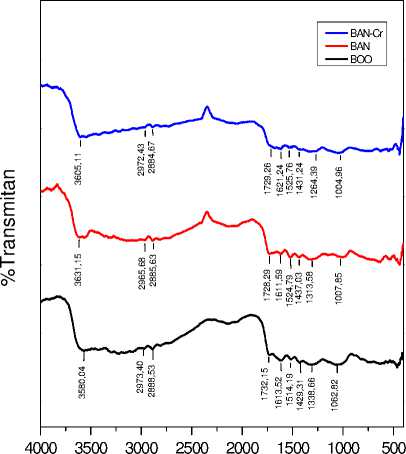
Bilangan gelombang (cm-1)
Gambar 6. Spektrum FTIR dari biosorben kulit kapuk
Gugus fungsi yang teridentifikasi yaitu – OH, C=O, -CH, C-O-H, C-O-C dan C=C. Analisis spektra FTIR dari biosorben kulit kapuk tanpa aktivasi menunjukan vibrasi gugus –OH (hidroksil) dari senyawa-senyawa organik seperti selulosa, hemiselulosa dan lignin (Chun et al, 2015) pada panjang gelombang 3580,04 cm-1 dengan intensitas 54,12. Setelah dilakukan aktivasi puncak ini bergeser ke 3631,15 cm-1 dengan intensitas meningkat menjadi 60,71. Hal ini dikarenakan larutan HNO3 telah mendekomposisikan pengotor yang berupa garam-garam mineral dan senyawa organik yang berikatan dengan biosorben. Setelah menyerap
Cr (III) puncak bergeser ke 3605,11 cm-1 dengan intensitas 33,71.
Pada spektrum juga terlihat pergeseran bilangan gelombang dengan intensitas tertentu pada gugus fungsi setelah proses biosorpsi Cr (III). Bilangan gelombang pada gugus C=O (karboksil) bergeser menjadi 1729,26 cm-1, bilangan gelombang pada gugus C-O-H bergeser menjadi 1264,39 cm-1, dan bilangan gelombang gugus C-O-C bergeser menjadi 1004,96 cm-1.
Berdasarkan hasil FTIR, gugus fungsi yang diperkirakan terjadi interaksi dengan ion logam yaitu -OH, C=O, C-O-H, dan C-O-C. Bergesernya bilangan gelombang mengindikasikan adanya interaksi antara gugus fungsi biosorben dengan ion Cr (III) (Bijang dkk., 2018). Intensitas serapan yang berbeda antara biosorben sebelum dengan setelah biosorpsi membuktikan telah terjadinya penyerapan ion logam oleh biosorben kulit buah kapuk (Zein dkk, 2019).
Mekanisme biosorpsi yang dapat terjadi antara gugus fungsi dengan biosorben yaitu mekanisme pertukaran ion dan pembentukan kompleks koordinasi antara bisorben dengan ion logam Cr (III) dimana elektron bebas dari atom oksigen pada biosorben menempati orbital kosong yang dimiliki oleh ion logam Cr (III) (Kusumawardani dkk., 2018).
SIMPULAN DAN SARAN
Simpulan
Luas permukaan biosorben BAN1, BAN2, dan BAN3 masing-masing yaitu sebesar 36,93223, 36,93051, dan 36,94147 m2/g. Jumlah situs aktif secara berurut-turut 1,0566 ×1022, 1,0229×1022, dan 1,0716×1022 molekul/g. Gugus fungsi yang diperkirakan berinteraksi dengan ion logam yaitu -OH, C=O, C-O-H, dan C-O-C. Kondisi optimum biosorpsi ion logam Cr (III) pada pH 5, waktu kontak 90 menit, dan konsentrasi awal larutan 1800 mg/L. Kapasitas biosopsi sebesar 59,28 mg/g dan pola isoterm bisorpsi merunjuk pada pola isoterm Langmuir.
Saran
Berdasarkan penelitian yang diperoleh maka perlu dilakukan penelitian mengenai kemampuan biosorpsi dari biosorben kulit kapuk terhadap kulit kapuk jenis lain, logam-logam berat pencemar lainnya, zat warna pencemar atau diaplikasikan secara langsung pada limbah yang mengandung logam kromium.
DAFTAR PUSTAKA
Agency for Toxic Subtances and Disease Registry (ATSDR). 2012. Toxycological Profile for Chromium. U.S Department of Health and Human Sevices. Atlanta.
APHA, AWWA, and WEF. 1999. Standard Methods for the Examination of Water and Wastewater, 20th ed. American Public Health Association. WashingtonD.C.
Bijang, C. M., Latupeirissa, J., dan Ratuhanrasa, M. 2018. Biosorpsi Ion Logam Tembaga (Cu2+) Pada Biosorben Rumput Laut Coklat (Padina australis). Indo. J. Chem. 6(1): 26-37.
Chun, K. S., Husseinsyah, S. and Yeng, C. M. 2015. Green Composites from Kapok Husk and Recycled Polypropylene: Processing torque, tensile, thermal, and morphological properties. Journal of Thermoplastic Composite Materials. 29(11): 1517-1535.
Dwipayana, A.A.G.A. S, Sudiarta, I. W, dan Budiarsa, S.I.W. 2017. Karakteristik dan Kapasitas Biosorben Kulit Jeruk Siam Lumanjang (Citrus nobilis Tan.) Teraktivasi H2SO4 dalam Menurunkan Kadar Ca dan Mg dalam Air. Jurnal Kimia. 11(1): 30-35.
Edelynna, A.M.O., Wirespathi, Raharjo, dan Widowati, B. 2012. Pengaruh Kromium Heksavalen (VI) terhadap Tingkat Kelangsungan Hidup Ikan Nila (Oreochromis niloticus). Jurnal
LenteraBio.1(2): 75-79.
Krismayanti, N.P., Manurung, M., dan Suastuti, N.G.A.M.D.A. 2019. Sintesis Arang Aktif Dari Limbah Batang Bambu Dengan Aktivator NaOH Sebagai Adsorben Ion Krom (III) dan Timbal (II). Cakra Kimia. 7(2): 189-197.
Kusumawardani, R., Zaharah, T. A., dan Destiarti, L. 2018. Adsorpsi Kadmium (II) Menggunakan Adsorben Selulosa Ampas Tebu Teraktivasi Asam Nitrat. Jurnal Kimia Khatulistiwa.7(3): 75-83.
Mufrodi, Z., Nur, W., dan Ranny, C. K. 2008. Adsorpsi Zat warna Tekstil dengan Menggunakan Abu Terbang (Fly Ash) untuk Variasi Massa Adsorben dan Suhu Operasi. Prosiding: Seminar Teknoin, Bidang Teknik Kimia dan Tekstil. Yogyakarta.
Nurafriyanti, Prihatini, N.S., dan Syauqiah, I. 2017. Pengaruh Variasi pH dan Berat Adsorben Dalam Pengurangan Konsentrasi Cr Total pada Limbah Artifisial Menggunakan Adsorben Ampas Daun Teh. Jukung Jurnal Teknik Lingkungan. 3(1): 56-65.
Putra, I. T. 2014. Karakteristik Kimia Kulit Kapuk Randu Sebagai Bahan Energi Biomassa. Skripsi. Institut Pertanian Bogor. Bogor.
Ramalingam, S., Parthiban, L., and Rangasamy, P. 2014. Biosorption Modeling with Multilayer Percepton for Removal of Lead and Zinc Ions Using Crab Shell Particles. Arab J Sci Eng.39: 8465-8475.
Sudiarta, I.W. 2009. Biosorpsi Ion Cr (III) Pada Rumput Laut Eucheuma spinosum Teraktivasi Asam Sulfat. Jurnal Kimia. 3(2): 93-100.
Sudiarta, I.W., Diantariani, N.P., dan Yulihastuti, D.A. 2012. Biosorpsi Cr (III) Pada Biosorbent Serat Sabut Kelapa Hijau Teraktivasi Asam Nitrat. Chem. Prog. 5(1): 25-30.
Sudiarta, I.W. dan Sulihingtyas, D.W. 2012. Biosorpsi Cr (III) Pada Biosorben Serat Sabut Kelapa Hijau Teramobilisasi EDTA. Jurnal Kimia.6(1): 29-36
Wogo, H.E., Kadang, L., dan Mir, M.A. 2014. Termodinamika Adsorpsi Ca (II) dan Cd (II) Pada Adsorben Ampas Tahu. Sains dan Terapan Kimia. 8(2): 120-128.
Zein, R., Nofita, D., Refilda, dan Aziz., H. 2019. Penyerapan Timbal (II) dan Cadmium (II) di dalam Larutan Menggunakan Kulit Buah Kapuk. Jurnal Chimica et Natura Acta. 7(1): 37-45.
100
Discussion and feedback