FOTODEGRADASI RHODAMIN B OLEH KATALIS ZEOLIT ALAM-TiO2/ZnO dan IRRADIASI SINAR TAMPAK
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 15 (1), JANUARI 2021 DOI: https://doi.org/10.24843/JCHEM.2021.v15.i01.p13
p-ISSN 1907-9850
e-ISSN 2599-2740
FOTODEGRADASI RHODAMIN B OLEH KATALIS ZEOLIT ALAM-TiO2/ZnO DAN IRRADIASI SINAR TAMPAK
N. K. A. Oktapiani, I N. Simpen*, dan I M. S. Negara
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Jimbaran, Bali, Indonesia.
*Email: nengahsimpen@unud.ac.id
ABSTRAK
Penelitian tentang pembuatan komposit zeolit alam-TiO2/ZnO yang digunakan dalam proses fotodegradasi zat warna rhodamin B dan irradiasi sinar tampak telah dilakukan. Komposit yang terbentuk dikarakterisasi menggunakan metode BET (Bruneau, Emmet, dan Teller) untuk mengamati luas permukaan spesifik komposit, Fourier Tranform Infrared (FTIR) untuk menentukan gugus fungsi yang terkandung, dan metode titrasi asam-basa untuk mengetahui sifat asam-basa permukaan dan jumlah situs aktifnya. Karakteristik optimum diperoleh pada luas permukaan spesifik zeolit alam-TiO2/ZnO (3:1) sebesar 49.349 m2/g, dengan keasaman permukaan zeolit alam-TiO2/ZnO (3:1) adalah 2,9561±0,0586 mmol/g dengan jumlah situs aktif 1,7796 x 1021 atom/g. Uji fotodegradasi dari komposit zeolit alam-TiO2/ZnO (3:1) terhadap rhodamin B dengan irradiasi sinar tampak, optimum diperoleh pada konsentrasi awal 400 mg/L, waktu irradiasi 10 menit dan pH larutan 1, dengan persentase degradasi sebesar 99,30%.
Kata kunci: fotodegradasi, irradiasi sinar tampak, rhodamin B, zeolit alam-TiO2/ZnO
ABSTRACT
The synthesis of natural zeolite-TiO2/ZnO composite which is used in the photodegradation process of rhodamine B dyes and visible light irradiation has been conducted. The composite was characterized using BET (Bruneau, Emmet, and Teller) method to observe its specific surface area, Fourier Tranform Infrared (FTIR) to determine the functional groups, and acid-base titration methods to determine the acid-base properties of composite surfaces. The optimum characteritics were obtained that the specific surface area of natural zeolite-TiO2/ZnO (3:1) was 49.349 m2/g, surface acidity of natural zeolite-TiO2/ZnO (3:1) of 2,9561±0,0586 mmoles/g with the amount of surface active sites was 1.7796 x 1021 atoms/g. The photodegradation testing of natural zeolite-TiO2/ZnO (3:1) composite with visible light irradiation showed that the optimum conditions obtained at initial concentration of rhodamine B dyes was 400 mg/L, at 10 minutes irradiation time and pH of 1, with the percentage of degradation was 99.30%.
Keywords: photodegradation, visible light irradiation, rhodamine B, natural zeolite-TiO2/ZnO
PENDAHULUAN
Dalam proses pewarnaan kain, sekitar 250% pewarna tekstil dilepaskan ke lingkungan karena molekul pewarna tidak terikat pada kain, khususnya zat pewarna sintetik, seperti halnya rhodamin B (Suteu dan Bilba, 2005). Rhodamin B merupakan salah satu zat warna organik sintetik yang cukup dominan terkandung dalam limbah tekstil. Senyawa ini mengandung gugus inti benzena dan gugus amino yang bersifat basa, sehingga secara alami sulit didegradasi oleh mikroorganisme (Purnawati. 2015). Peraturan pemerintah RI No. 82 tahun 2001 tentang Pengolahan Kualitas Air dan Pengendalian Pencemaran Air, menyatakan bahwa kandungan klorin dalam rhodamin B bila masuk dalam
tubuh manusia dapat memicu gangguan kesehatan, karena sifatnya yang reaktif. Akibatnya, akumulasi rhodamin B dalam tubuh dapat menyebabkan gangguan fungsi hati, ginjal dan menyebabkan kanker. Dengan adanya masalah yang ditimbulkan, maka perlu dilakukan pengolahan limbah zat warna rhodamin B.
Metode alternatif yang saat ini cocok dikembangkan untuk mengolah limbah zat warna tekstil adalah fotodegradasi. Fotodegradasi merupakan metode penguraian senyawa menjadi yang lebih sederhana dengan bantuan foton. Prinsip metode fotodegradasi adalah menguraikan polutan menjadi komponen yang lebih sederhana seperti CO2, H2O, asam atau basa mineral serta senyawa lain yang lebih
sederhana, sehingga tidak membahayakan lingkungan (Fatimah dkk., 2009). Fotodegradasi dapat berlangsung lebih cepat dengan bantuan katalis yang bersifat semikonduktor.
Katalis semikonduktor yang sering digunakan adalah titanium dioksida (TiO2) dan zink oksida (ZnO), karena memiliki energi celah pita (band gap energy) sebesar 3,2 eV. Energi celah pita semikonduktor merupakan energi yang diperlukan oleh elektron untuk mengalami eksitasi dari pita valensi ke pita konduksi (Wijaya dkk., 2005; Ali and Siew, 2006; Attia, 2008). Salah satu, cara yang dapat dilakukan untuk memperkuat kemampuan fotokatalitik yaitu melalui pengembanan material semikonduktor pada material pendukung, seperti halnya zeolit alam (Mackay et al., 2002). Beberapa keuntungan menggunakan pengemban zeolit alam adalah potensi zeolit alam yang melimpah di Indonesia, stabilitas yang tinggi pada kondisi asam dan basa, serta luas permukaan yang besar.
Penelitian Diantariani dkk. (2014) telah menggunakan katalis ZnO dan sinar UV untuk fotodegradasi metilen biru, dengan persentase degradasi 94,67%. Adesia dkk. (2015), menggunakan ZnO-arang aktif dan sinar UV untuk mendegradasi zat warna tekstil congo red dengan persentase degradasi 91,81%. Fauzi dkk. (2019) telah melakukan sintesis dan karakterisasi zeolit alam-TiO2 serta pemanfaatannya sebagai fotokatalis untuk mendegradasi rhodamin B, dengan persentase degradasi sebesar 97,39%. Berdasarkan hal tersebut, belum ditemukan penggabungan dari dua material semikonduktor TiO2/ZnO pada pengemban zeolit alam dan memanfaatkan irradiasi sinar tampak untuk fotodegradasi Rhodamin B, sehingga perlu dilakukan penelitian ini.
MATERI DAN METODE
Bahan
Zeolit alam, TiO2 anatas, ZnO, rhodamin B (C28H31N2O3Cl), akuades, etanol 96%, HCl, NaOH, H2SO4 dan indikator PP (phenolpthalein).
Alat
Lampu 30W HPL (High Power LED-Light Emitting Diode), spektrofotometer UV-vis Shimadzu UV 1800, Spectroscopy Fourier Transform Infrared (FTIR), Surface Area Analyzer (SAA) Quantachrome Autosorb iQ.
Cara Kerja
Preparasi Zeolit
Seratus (100) g zeolit alam ditambahkan 1000 mL H2SO4 2 M, lalu dilakukan pengadukan dengan pengaduk magnet selama 14-16 jam, kemudian dicuci beberapa kali sampai terbebas dari ion sulfat (ditunjukan dengan tes negatif oleh larutan 0,1 M BaCl2). Selanjutnya, dikeringkan dalam oven pada temperatur 120oC, kemudian diayak dengan ayakan ukuran lubang 200 mesh.
Sintesis Komposit
Zeolit alam dan TiO2 dicampur secara padat-padat dengan perbandingan (100:5), lalu dihomogenkan kemudian dipanaskan dalam tanur pada temperatur 350oC selama 12 jam, selanjutnya diayak dengan ayakan ukuran lubang 200 mesh (Fauzi dkk., 2018). Zeolit alam-TiO2 yang terbentuk, ditambahan ZnO dengan perbandingan 1:3, 1:1, 3:1 dan etanol 96%
sebanyak 10 mL. Diaduk menggunakan pengaduk magnet sampai campuran homogen. Campuran kemudian dioven selama 5 jam pada temperatur 120oC dan diayak menggunakan ayakan ukuran lubang 200 mesh. Komposit yang telah halus kemudian dipanaskan dalam tanur pada temperatur 400oC selama 1 jam. Komposit zeolit alam-TiO2/ZnO yang diperoleh ditentukan asam-basa permukaannya dengan cara titrasi asam-basa, analisis gugus fungsi dengan FTIR, dan luas permukaan spesifik BET dengan SAA.
Karakterisasi Situs Asam-Basa Permukaan
Komposit zeolit alam-TiO2/ZnO
dikarakterisasi situs asam dan basa permukaannya secara kuantitatif dengan titrasi asam-basa. Untuk menentukan situs basa ditimbang teliti sebanyak 0,50 g sampel zeolit alam-TiO2/ZnO, kemudian dimasukkan ke dalam Erlenmeyer 250 mL dan ditambahkan 10,0 mL larutan HCl 0,5 M sambil diaduk dengan pengaduk magnet selama 15 menit. Setelah campuran diaduk, ke dalam larutan tersebut ditambahkan 3-4 tetes indikator PP. Campuran dititrasi dengan larutan NaOH 0,5 M sampai terjadi perubahan warna dari tidak berwarna menjadi merah muda. Volume NaOH yang digunakan dalam titrasi dicatat dengan teliti. Untuk menghitung situs basa katalis digunakan Persamaan 1 berikut ini.
, (mmol HCl awal—mmol HCl bebas)
Kebasaan = ------------------------ (1)
M assa k o mp osi t
(Kumar et al., 1995)
Untuk menentukan situs asam ditimbang dengan teliti sebanyak 0,50 g sampel zeolit alam-TiO2/ZnO, dimasukkan ke dalam Erlenmeyer 250 mL dan ditambah 10,0 mL NaOH kemudian ditambah 3-4 tetes indikator PP. Campuran dititrasi dengan larutan HCl 0,5 M sampai terjadi perubahan warna dari merah muda menjadi tidak berwarna. Volume HCl yang digunakan dalam titrasi dicatat dengan teliti. Untuk menghitung situs asam katalis digunakan Persamaan 2 berikut.
(mmol NaOH awal - mmol NaOH bebas)
Keasaman = --------------:---------------- Massakomposit (2)
(Kumar et al., 1995)
Penentuan Konsentrasi Optimum
Gelas Baeker 250 mL diisi dengan larutan rhodamin B 25,0 mL dengan variasi konsentrasi 75, 100, 125, 150, 200, 250, 300, 400, 500, dan 600 mg/L. Ke dalam masing-masing gelas Beaker, dimasukan sebanyak 0,5 g katalis zeolit alam-TiO2/ZnO diaduk sampai homogen dan dimasukkan ke dalam kotak penyinaran dengan sinar lampu LED (30W HPL, 445 nm) selama 2 jam sambil diaduk dengan magnetik stirer. Filtrat ditentukan dengan mengukur absorbansi pada panjang gelombang 553,60 nm. Nilai konsentrasi kemudian dimasukkan ke dalam persamaan persentase degradasi (%D) (Persamaan 3) berikut.
RhB 1 - IRhB 1
%D = —Wl—xl00% (3)
Persentase degradasi yang digunakan menentukan konsentrasi optimum untuk larutan rhodamin B.
Penentuan Waktu Penyinaran Optimum
Dimasukkan 25,0 mL larutan rhodamin B dengan konsentrasi optimum yang telah didapatkan pada prosedur penentuan konsentrasi optimum ditambahkan 0,5 g zeolit alam-TiO2/ZnO dimasukan ke dalam kotak penyinaran dengan sinar lampu LED (30W HPL, 445 nm) masing-masing selama 5, 10, 20, 40, 80, 100, dan 120 menit. Nilai waktu penyinaran kemudian dimasukan ke dalam Persamaan (3).
Penentuan pH Optimum
Larutan rhodamin B 25,0 mL dengan pH 1, 2, 3, 4, 5, 6, dan 7 dengan menambahkan HCl 0,5 M atau NaOH 0,5 M ke dalam larutan. Dimasukkan sebanyak 0,5 g katalis zeolit alam-TiO2/ZnO dengan konsentrasi optimum yang telah didapat pada prosedur sebelumnya kemudian dimasukkan ke dalam kotak penyinaran dengan sinar lampu LED (30W HPL, 445 nm) dengan waktu optimum yang didapat pada prosedur sebelumnya. Nilai pH optimum kemudian dimasukan ke dalam Persamaan (3).
Efektivitas Fotodegradasi pada Kondisi Optimum
Enam buah gelas Beaker 250 mL masing-masing diisi dengan larutan rhodamin B 25,0 mL dan 0,5 g zeolit alam-TiO2/ZnO dengan konsentrasi dan pH optimum. Tiga Beaker gelas dimasukkan kedalam kotak penyinaran dan disinari dengan sinar lampu LED ( 30W HPL, 445 nm ) dengan waktu optimum, sedangkan tiga Beaker gelas tanpa penyinaran. Nilai kondisi optimum kemudian dimasukkan ke dalam Persamaan (3).
HASIL DAN PEMBAHASAN
Gugus Fungsi Katalis
Spekktrometer FTIR sigunakan untuk menentukan gugus fungsi katalis. Hasil analisis disajikan pada Gambar 1.

Bilangan gelombang(cm-1)
Gambar 1. Spektra FTIR (a). ZA-TiO2, (b). ZA-TiO2/ZnO (1:3), (c). ZA-TiO2/ZnO (1:1), dan (d). ZA-TiO2/ZnO (3:1)
Pita serapan tajam pada daerah 16001650 cm-1 merupakan pita dari regangan O-H asimetris bentuk deformasi dari air. Pita serapan yang muncul pada daerah 1250-1190 cm-1 dihasilkan oleh vibrasi SiO4 tetrahedral. Secara umum tidak terjadi perubahan signifikan pada spektra FTIR setelah ditambah ZnO selain perubahan karakteristik ikatan Si-O-Si yang muncul pada bilangan gelombang 1900-1170 cm-1. Pergeseran bilangan gelombang pada pita serapan Si-O-Si menunjukkan pembentukan ikatan hidrogen antara ZnO dan TiO2 dengan gugus hidroksil pada lapisan tetrahedral (Park et al., 2005).
Luas Permukaan Spesifik Katalis
Luas permukaan spesifik merupakan karakter fisik yang penting. Luas permukaan dinyatakan dalam jumlah total luas permukaan zeolit yang berbentuk serbuk dalam setiap massa zeolit (Busca et al., 2014). Hasil penentuan luas permukaan spesifik BET katalis zeolit alam-TiO2/ZnO dengan SAA ditunjukkan dalam Tabel 1.
Tabel 1. Hasil analisis luas permukaan spesifik
katalis zeolit alam-TiO2/ZnO
|
Komposit |
Luas Permukaan (m2/g) |
|
ZA-TiO2 |
84,837 |
|
ZA-TiO2/ZnO (1:3) |
36,172 |
|
ZA-TiO2/ZnO (1:1) |
31,396 |
|
ZA-TiO2/ZnO (3:1) |
49,349 |
Luas permukaan spesifik tertinggi dimiliki oleh katalis ZA-TiO2 sebesar 84,837 m2/g. ZnO yang ditambahkan ke dalam ZA-TiO2 telah menyebabkan penurunan luas permukaan spesifik. Luas permukaan spesifik menurun secara signifikan. Penurunan luas permukaan spesifik disebabkan oleh terperangkapnya molekul ZnO di permukaan zeolit alam yang teraktivasi sehingga pori-pori zeolit alam menjadi tertutupi (Wu et al., 2013). Dalam penelitian Maria et al., (2013), diperoleh luas permukaan spesifik zeolit alam sebesar 63,031 m2/g.
Luas permukaan yang tinggi akan memperbesar kemampuan katalis untuk mengadsorpsi zat warna, sehingga peluang untuk
mendegradasi zat warna juga akan semakin tinggi.
Karakteristik Asam-Basa Permukaan Katalis
Keasaman atau kebasaan permukaan katalis merupakan nilai yang menyatakan jumlah situs aktif asam atau basa Bronsted maupun Lewis yang terdapat di permukaan katalis, yang dinyatakan sebagai jumlah milimol asam atau basa dalam tiap gram katalis. Hasil penentuan asam-basa permukaan serta jumlah situs aktif ditunjukkan pada Tabel 2.
Tabel 2. Nilai keasaman permukaan dan jumlah
situs aktif asam katalis
|
Komposit |
Keasaman permukaan rata-rata (mmol/g) |
Jumlah Situs Aktif Asam (atom/gram) |
|
ZA-TiO2 |
2,0900±0,0774 |
1,4276 x 1021 |
|
ZA-TiO2/ZnO |
2,7515±0,0291 |
1,6564 x 1021 |
|
(1:3) | ||
|
ZA-TiO2/ZnO |
2,8912±0,0001 |
1,7405 x 1021 |
|
(1:1) | ||
|
ZA-TiO2/ZnO |
2,9561±0,0586 |
1,7796 x 1021 |
|
(3:1) |
Hasil penentuan keasaman-kebasaan permukaan katalis zeolit alam-TiO2/ZnO atau ZA-TiO2/ZnO (Tabel 2), menunjukkan bahwa situs asam-basa tertinggi dimiliki oleh katalis zeolit alam-TiO2/ZnO (3:1) dengan keasaman permukaan sebesar 2,9561±0,0586 mmol/g dengan jumlah situs aktif asam sebanyak 1,7796 x 1021 atom/gram. Jumlah situs aktif permukaan yang tinggi menyebabkan peningkatan pembentukan •OH radikal, yang berperan dalam proses fotodegradasi (He et al., 2009). Hal ini berarti, tingginya jumlah situs aktif baik asam maupun basa pada permukaan katalis mampu meningkatkan kemampuan degradasi katalis terhadap rhodamin B. Berdasarkan pertimbangan tersebut, maka katalis ZA-TiO2/ZnO (3:1) dipilih sebagai komposisi yang digunakan dalam penentuan kondisi optimum fotodegradasi rhodamin B.
Konsentrasi Optimum Fotodegradasi
Konsentrasi optimum adalah konsentrasi larutan tertinggi yang dibutuhkan untuk memberikan persentase degradasi larutan
rhodamin B tertinggi. Massa katalis zeolit alam-TiO2/ZnO (3:1) optimum untuk fotodegradasi rhodamin B ditunjukkan pada Gambar 2.
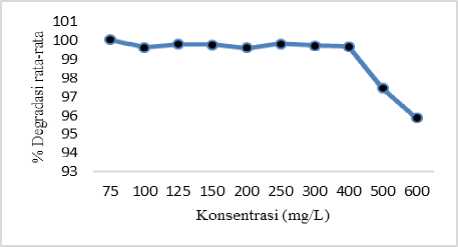
Gambar 2. Kurva hubungan konsentrasi dengan persentase degradasi.
Hasil optimasi konsentrasi menunjukkan terjadinya penurunan persentase degradasi mungkin karena komposit zeolit alam-TiO2/ZnO (3:1) yang digunakan sebagai adsorben mengalami kejenuhan dalam mengadsorpsi larutan rhodamin B pada konsentrasi 500 dan 600 mg/L. Berdasarkan data hasil optimasi konsentrasi, konsentrasi 400 mg/L dengan degradasi 99,67% dipilih sebagai konsentrasi optimum karena persentase degradasi rhodamin B telah relatif konstan.
Waktu Penyinaran Optimum Fotodegradasi
Waktu penyinaran optimum adalah waktu terendah yang dibutuhkan oleh katalis zeolit alam-TiO2/ZnO (3:1) untuk memberikan persentase degradasi rhodamin B tertinggi. Gambar 3 menunjukkan waktu penyinaran optimum untuk fotodegradasi rhodamin B oleh katalis zeolit alam-TiO2/ZnO (3:1).
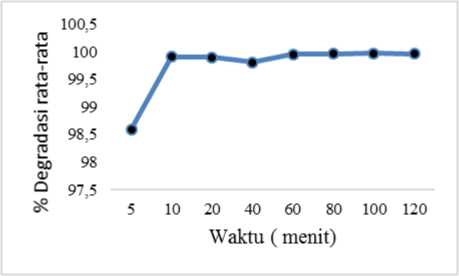
Gambar 3. Kurva hubungan waktu penyinaran dengan persentase degradasi.
Hasil optimasi waktu degradasi menunjukkan bahwa dari menit ke-5 menuju menit ke-10 terjadi kenaikan degradasi rhodamin B. Setelah mencapai menit ke-10, proses
degradasi tidak meningkat secara signifikan, yaitu pada menit ke-20, 40, 60, 80, 100, dan 120 menit persentase degradasi relatif stabil. Hal ini mungkin terjadi karena kemampuan komposit zeolit alam-TiO2/ZnO (3:1) dalam mendegradasi rhodamin B sudah mencapai titik maksimal. Oleh karena itu, menit ke-10 dipilih sebagai waktu yang optimum degradasi rhodamin B dengan presentase degradasi sebesar 99,91%.
pH Optimum Fotodegradasi
Nilai pH optimum suatu larutan mampu memberikan pengaruh terhadap larutan yang dibutuhkan untuk memberikan persentase degradasi terbaik pada reaksi fotodegradasi rhodamin B oleh katalis zeolit alam-TiO2/ZnO. Perbedaan kondisi pH larutan dapat menyebabkan perubahan muatan permukaan dan pergeseran potensial reaksi katalis sehingga mempengaruhi proses degradasi zat warna kekuatan ionik, dan mempengaruhi proses adsorbsi. Hasil percobaan pH kerja dapat dilihat pada Gambar 4.
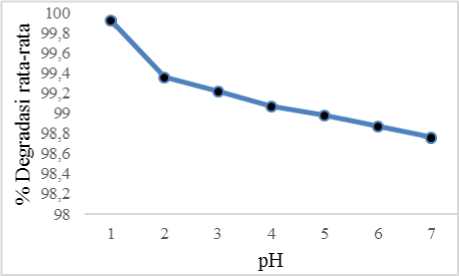
Gambar 4. Kurva hubungan nilai pH dengan
persentase degradasi.
Rhodamin B lebih mudah terdegradasi pada pH asam dari pada pH basa (Gambar 4). Presentase degradasi terus mengalami kenaikan dari pH 7 sampai pH 1. Hal ini dapat dijelaskan menggunakan teori muatan permukaan. Titanium oksida dapat mengalami protonasi ataupun deprotonasi pada kondisi asam atau basa. Reaksi protonasi dan deprotonasi tersebut terjadi menurut persamaan reaksi berikut:
Ti–OH + H+ → TiOH2+
Ti–OH + OH- → TiO- + H2O
Dalam pelarut air, rhodamin B termasuk dalam zat warna bermuatan negatif. Hal ini menyababkan rhodamin B tidak efektif terdegradasi dalam pH basa (Sibarani. 2016). Adanya interaksi elektrostatis antara permukaan titanium dioksida yang bermuatan positif dengan
anion dari rhodamin B yang bermuatan negatif menghasilkan adsorpsi yang kuat dari zeolit. Sebaliknya pada pH basa TiO2 akan bermuatan negatif sehingga akan terjadi gaya tolak-menolak dengan anion rhodamin B. Hal ini menyebabkan rhodamin B terdegradasi lebih efektif pada pH asam dibanding pH basa. Berdasarkan analisis tersebut, maka pH 1 dipilih sebagai pH kerja optimum untuk fotodegradasi rhodamin B oleh katalis zeolit alam-TiO2/ZnO (3:1) dengan persentase degradasi sebesar 99,96%.
Efektivitas Fotodegradasi pada Kondisi Optimum
Larutan rhodamin B 400 mg/L didegradasi menggunakan katalis zeolit alam-TiO2/ZnO (3:1) pada kondisi optimum, dengan maupun tanpa irradiasi cahaya tampak. Kondisi optimum yang dimaksud adalah untuk tiap 25 mL larutan rhodamin B 400 mg/L digunakan 500 mg katalis dan diiradiasi selama 10 menit pada pH 1. Lampu yang digunakan adalah 30W HPL (High Power LED-Light Emitting Diode) dengan panjang gelombang 445 nm dan intensitas cahaya pada saat penyinaran sebesar 14,28 mW/cm2. Hasil fotodegradasi pada kondisi optimum ditunjukkan oleh Gambar 5.
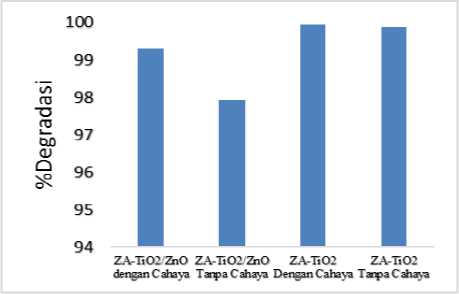
Gambar 5. Persentase fotodegradasi pada kondisi optimum dengan dan tanpa penambahan ZnO
Gambar 5 menunjukkan bahwa persentase degradasi rhodamine B oleh zeolit alam-TiO2/ZnO sebesar 99,30% dengan irradiasi cahaya tampak dan 97,92% tanpa irradiasi cahaya tampak. Selisih antara persentase degradasi dengan dan tanpa irradiasi (penyinaran) relatif kecil, yaitu 1,38%. Sementara, persentase degradasi zeolit alam-TiO2 sebesar 99,94% diperoleh dengan irradiasi cahaya tampak dan 99,90% tanpa irradiasi
cahaya tampak, dengan selisih persentase yang relatif sangat kecil, yaitu 0,04%. Adanya ZnO dalam komposit ZA-TiO2 relatif sama perannya dengan ZA-TiO2. Ini berarti bahwa adanya 25% ZnO memberikan pengaruh yang sama terhadap 25% TiO2 dalam 100% ZA-TiO2.
SIMPULAN
Katalis dengan karakteristik optimum diperoleh pada komposit zeolit alam-TiO2/ZnO (3:1), dengan luas permukaan spesifik 49.349 m2/g, keasaman permukaan 2,9561±0,0586 mmol/g dengan jumlah situs aktif 1,7796 x 1021 atom/g. Uji fotodegradasi dari komposit zeolit alam-TiO2/ZnO (3:1) terhadap zat warna rhodamin B dengan irradiasi sinar tampak, optimum diperoleh pada konsentrasi awal 400 mg/L pada waktu irradiasi 10 menit dan pH larutan 1, dengan persentase degradasi mencapai 99,30%.
UCAPAN TERIMA KASIH
Diucapkan terima kasih kepada bapak Dr. Drs. I Made Sukadana, M.Si., ibu Dra. Emmy Sahara, M.Sc.(Hons), dan ibu A.A.I.A. Mayun Laksmiwati, S.Si., M.Si. atas saran dan masukannya yang telah diberikan.
DAFTAR PUSTAKA
Adesia, S., Diantariani, N. P., dan Suarya, P. 2015. Fotodegradasi zat warna tekstil congo red dengan Fotokatalis ZnO-arang aktif dan Sinar UV. J. Kimia. 9(2): 175182.
Ali, R. and Siew, O. B. 2006. Photodegradation of New Methylen Blue N in Aqueous Solution Using Zinc Oxide and Titanium Dioxide as Catalyst. Jurnal Teknologi. 45(F). 31-42.
Attia, A.J., Kadhim, S. H., and Hussen, F. H.
2008. Photocataliytc Degradation of Textile Dyeing Wastewater Using Titanium Dioxide and Zinc Oxide. EJournal of Chemistry. (5)2: 219-223.
Busca, G., Berardinelli, S., Resini, C., and Arrighi, L. 2014. Technologies for the removal of phenol from fluid streams : A short review of recent development. J. Hazard. Mater.160: 265-288.
Diantariani N. P., Widihati, I. A. G., dan Megasari, I G. A. A. R. 2014.
Fotodegradasi Metilen Biru dengan Sinar Ultra Violet dan Katalis ZnO. J. Kimia. 8(1): 137-143.
Fauzi W. A., Simpen I N., dan Sudiarta I W. 2019. Sintesis dan Karakterisasi Zeolit-TiO2 serta Pemanfaatannya sebagai Fotokatalis dalam Mendegradasi Zat Warna Rhodamin B. J. Kimia 13(1): 74 – 81.
Fatimah, I., Sugiharto, E., Wijaya, K., Tahir, I., dan Kamalia. 2009. Titan Dioksida
Terdispersi pada Zeolit Alam (TiO2/Zeolit) dan Aplikasinya untuk Fotodegradasi Congo Red. Indonesian Journal of Chemistry. 6(1): 38-42.
He, Z., Sun, C., Yang, S., Ding, Y., He, H., and Wang, Z. 2009. Photocatalytic Degradation of Rhodamine B by Bi2WO6 with Electron Accepting Agent Under Microwave Irradiation:
Mechanism and Pathway. Journal of Hazardous Material. 162. 1477-1486.
Kumar, P., Jasra, R. V., and Bhat, T. S. G. 1995. Evolution of Porosity and Surface Acidity in Montmorillonite Clay on Acid Activation. Ind. Eng. Chem. Res. 34: 1440-1448.
Maria, D. C., Cotto-Maldonado, Teresa, C., Eduardo, E., Arancha, G.M., and Francisco, M., 2013, Photocatalytic
Degradation of Rhodamine-B Under UV-Visible Light Irradiation Using Different Nanostructured Catalysts, American Science Journal, 3: 178-202.
MacKay, K. M., MacKay, R. A., and Henderson, W. 2002. Introduction to Inorganic
Chemistry. 6th edition. Nelson Thornes Ltd. United Kingdom.
Park, H. and Choi, W. 2005. Photocatalytic Reactivities of Nation-Coated TiO2 for the Degradation Changed Organic Compounds under UV or Visible Light. Journal Phys. Chem. B. 109(23): 1166711674.
Purnawati, K. Y., Suyasa, I W. B., dan Mahardika, I G. 2015. Penurunan Kadar Rhodamin B dalam Air Limbah dengan Biofiltrasi Sistem Tanaman. J. Ecotropic. 9(2): 486-492.
Peraturan Pemerintah RI No. 82 tahun 2001 tentang Pengolahan Kualitas Air dan Pengendalian Pencemaran Air.
Sibarani, J., Purba, D. L., Suprihatin, I. E., dan Manurung, M. 2016. Fotodegradasi Rhodamin B Menggunakan
ZnO/UV/Reagen Fenton. Jurnal Cakra Kimia. 4(1): 84-94.
Suteu, D. and Bilba, D. 2005. Equilibrium and Kinetic Study of Reactive Dye Brilliant Red HE-3B Adsorption by Activated Charcoal. Scientific Paper. 52: 73-79.
Wijaya, K., Tahir, I., dan Haryati, N. 2005.
Sintesis Fe2O3-Montmorilonit dan
Aplikasinya sebagai Fotokatalis untuk Degradasi Zat Pewarna Congo Red. Indo. J. Chem. 5(1): 41-47.
Wu, H., Zhang, J., Wei, Q., Zheng, J., and Zhang, J. 2013. Transesterification of Soybean oil to Biodiesel Using Zeolit Supported CaO as Strong Base Catalysts. J. Fuel Processing Technology. 109: 1318.
100
Discussion and feedback