ANALISIS KADAR ASAM ASKORBAT (VITAMIN C ) PADA MINUMAN SUPLEMEN DALAM KEMASAN DENGAN METODE SPEKTROFOTOMETRI SECARA LANGSUNG DAN TIDAK LANGSUNG
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 15 (2), JULI 2021 DOI: https://doi.org/10.24843/JCHEM.2021.v15.i02.p03
p-ISSN 1907-9850
e-ISSN 2599-2740
ANALISIS KADAR ASAM ASKORBAT (VITAMIN C ) PADA MINUMAN SUPLEMEN DALAM KEMASAN DENGAN METODE SPEKTROFOTOMETRI SECARA LANGSUNG DAN TIDAK LANGSUNG
I W. Sudiarta, A. Suandi*, dan A. A. I. A. M. Laksmiwati
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana Jalan Kampus Unud-Jimbaran, Jimbaran-Bali, Indonesia
*Email: arisuandi21@gmail.com
ABSTRAK
Asam askorbat atau vitamin C banyak terdapat pada minuman suplemen kemasan yang mudah ditemukan dimanapun dan penggunaanya yang relatif lebih praktis. Untuk mengetahui kadar vitamin C yang tepat dalam minuman suplemen dilakukan pengukuran dengan metode spektrofotometri UV-Vis secara langsung dan tidak langsung. Penelitian ini bertujuan untuk mengetahui metode manakah yang lebih baik untuk analisis vitamin C dan mengetahui apakah kadar vitamin C yang tercantum pada label minuman suplemen kemasan sesuai dengan hasil metode langsung dan tidak langsung. Sampel dipreparasi menggunakan metode spektrofotometri secara langsung dan tidak langsung menggunakan logam pereduksi Cr6+ yang direaksikan dengan vitamin C pada sampel dan dianalisis menggunakan spektrofotometer UV-Vis. Hasilnya menunjukkan bahwa analisis vitamin C dengan metode spektrofotometri lebih baik secara tidak langsung daripada secara langsung. Kadar vitamin C pada sampel minuman suplemen dalam kemasan A, B, dan C yang dianalisis dengan metode spektrofotometri secara langsung diperoleh masing-masing sebesar 1074,34 mg/L ; 5956,44 mg/L dan 6646,28 mg/L dengan nilai %kesesuaian kadar 88,91%, 89,35%, dan 89,66%. Sedangkan kadar vitamin C pada sampel minuman suplemen dalam kemasan A, B, dan C yang dianalisis dengan metode spektrofotometri secara tidak langsung diperoleh masing-masing 1178,17 mg/L ; 6162,41 mg/L dan 6718,58 mg/L dengan % kesesuaian kadar 97,50%, 92,44% dan 90,63%. Hasil uji -t menyatakan tidak ada perbedaan secara signifikan antara kadar vitamin C sampel A yang dianalisis dengan metode tidak langsung dengan kadar yang tertera di label kemasan. Sedangkan kadar vitamin C pada sampel B tidak berbeda secara signifikan baik ditentukan dengan metode langsung maupun tidak langsung.
Kata kunci: Cr6+, minuman suplemen dalam kemasan, spektrofotometer UV-Vis, Vitamin C.
ABSTRACT
Ascorbic acid or vitamin C contained in many supplement drinks are easily found anywhere and its use is relatively more practical. To find out the exact content of vitamin C in supplement drinks, measurements were carried out directly and indirectly using UV-Vis spectrophotometry method. This study aims to find out which spectrophotometric method is better for vitamin C analysis and whether the vitamin C content listed on the supplement drink packaging label is in accordance with the results of the direct and indirect methods. Samples were prepared directly and indirectly using Cr6+ reducing metals reacted with the vitamin C in the samples and analyzed by using a UV-Vis spectrophotometer methods. The results showed that the analysis of vitamin C by indirect spectrophotometric method was better than the direct one. Vitamin C contents in the supplement beverage samples of packaging A, B, and C analyzed using direct spectrophotometric method were 1074.34 mg/L; 5956.44 mg/L and 6646.28 mg/L with percentage of conformity of 88% 91.91%, 89.35% and 89.66%, respectively. Meanwhile, the vitamin C contents in the supplement drink samples of packaging A, B, and C analyzed by indirect spectrophotometric method were 1178.17 mg/L; 6162.41 mg/L and 6718.58 mg/L with percentage of conformity of 97.50%, 92.44% and 90.63%. The -t test results indicated that there was no significant difference of vitamin C content in the sample A analyzed by indirect methods from the content listed on the packaging label. The -t test results also stated that there is no significant difference of vitamin C content in the sample B analyzed either by direct or indirect method.
Keywords: bottled supplement drinks, Cr6+, UV-Vis Spectrophotometer, vitamin C.
PENDAHULUAN
Asam askorbat (AA) atau vitamin C adalah salah satu vitamin penting yang berperan dalam berbagai macam proses biologis menyangkut reaksi transport elektron, hidroksilasi, dan katabolisme oksidatif dari asam amino aromatik. Asam askorbat penting untuk pengembangan dan regenerasi otot, tulang, gigi, dan kulit (Sulistyoningsih, 2011).
Asam askorbat dapat sebagai penetral radikal bebas dalam tubuh mahkluk hidup dengan cara mendonorkan elektron pada radikal bebas tersebut. Asam askorbat biasanya berada dalam 2 bentuk yang tidak stabil, yaitu bentuk tereduksi berupa L-Ascorbic Acid (AA), dan bentuk teroksidasi Dehydroascorbic Acid (DAA), (Akhilender, 2003).
Asam askorbat atau vitamin C banyak terdapat pada buah-buahan, sayuran, makanan olahan dan sediaan farmasi (Sweetman, 2005). Minuman suplemen merupakan salah satu sediaan farmasi yang mengandung berbagai macam vitamin, termasuk vitamin C. Minuman suplemen kemasan memiliki keunggulan mudah ditemukan dimanapun dan penggunaanya yang relatif lebih praktis. Kadar vitamin C dalam minuman suplemen tersebut tertera dalam label kemasan. Untuk mengetahui kebenaran kadar vitamin C dalam minuman suplemen perlu dilakukan pengukuran dengan metode tertentu.
Banyaknya penggunaan asam askorbat telah mendorong banyak peneliti untuk mengembangkan metode penentuannya. Jadi, sangat penting untuk memilih metode yang sederhana dan selektif. Penentuan kadar vitamin C biasanya menggunakan metode titrasi dan metode spektrofotometri (Jiang, et al, 2001).
Mereaksikan asam askorbat dengan ion logam Fe(III), dimana Fe(II) hasil reduksi Fe(III) oleh asam askorbat diabsorbsi oleh resin penukar kation Amberlit IR 200 kemudian dilarutkan dalam asam nitrat dan diukur absorbansinya menggunakan spektrofotometer serapan atom. Logam selain Fe juga dapat digunakan sebagai oksidator, beberapa penelitian menggunakan logam seperti Cu, Cr, Se dan Te sebagai oksidator dalam penentuan kadar vitamin C secara tidak langsung (Jiang, et al, 2001).
Asam askorbat dapat dianalisis pada limit deteksi 1.5μg/mL dengan menggunakan metode spektrofotometri serapan atom ketika bereaksi dengan Cu (II) dengan pembentukan
endapan Cu (I)-tiosianat (Masoomeh et al 2014).
Penentuan asam askorbat juga dapat dilakukan menggunakan oksidator logam kromium (Cr). asam askorbat dapat mereduksi logam Cr (VI) dalam medium asam sulfat dan dikompleksasi dengan difenilkarbazida (DPC), senyawa kompleks yang terbentuk pada reaksi antara Cr (VI) dan DPC berwarna merah violet yang stabil hingga 90 menit. logam selenium (Se) dan asam askorbat dapat ditentukan dengan mereduksi logam Se (IV) yang diasamkan menggunakan asam klorida. (Revanasiddappa dan Venna 2007)
Logam Telenium (Te) juga dapat digunakan untuk analisis asam askorbat. Larutan logam Te (IV) diasamkan dengan asam klorida serta penambahan pereaksi pati beserta iodium. Konsentrasi asam askorbat diperoleh dengan mengurangi absorbansi dari larutan Te (IV) yang sudah direduksi oleh asam askorbat dengan absorbansi blanko (Pojaa, 2015).
Metode tidak langsung dilakukan dengan mengukur kadar logam yang telah direduksi oleh vitamin C, diharapkan akan mengurangi kemungkinan rusaknya vitamin C dalam proses analisis karena vitamin C yang dikenal mudah terpengaruh oleh paparan oksigen dan sinar matahari. Besar penurunan kadar vitamin C pada rantang 6,3 s/d 51,06 % untuk paparan sinar matahari dan 3,34 s/d 14,46% untuk paparan oksigen. Penuruan kadar vitamin C tersebut terjadi setelah sampel minuman bervitamin C terpapar sinar matahari dan oksigen selama 1, 2, dan 3 jam (Lila, 2017).
Penetapan kadar vitamin C menggunakan spektrofotometer UV-Vis dengan pelarut aquades terjadi pergerseran panjang gelombang maksimum dari 243 nm (pada konsentrasi tinggi 30 ppm s/d 100 ppm) sedangkan panjang gelombang 265 nm (pada konsentrasi rendah 0,607 ppm s/d 30 ppm). Pergeseran ini disebut pergeseran batokromik (Laras, 2012).
Pada penelitian ini akan dilakukan penentuan kadar asam askorbat pada mnuman suplemen dalam kemasan secara langsung dan tidak langsung dengan metode spektrofotometri. Sebelumnya metode analisis vitamin C secara langsung dan tidak langsung akan divalidasi serta dibandingkan hasilnya untuk menentukan metode analisis vitamin C terbaik.
MATERI DAN METODE
Bahan
Bahan yang digunakan pada penelitian ini yaitu : Sampel minuman suplemen A, B dan C, vitamin C (asam askorbat) p.a; K2Cr2O7 p.a; asam sulfat 0,1 M; DPC (difenilkarbazida) 0,25%; aseton; dan aquades.
Peralatan
Alat yang digunakan pada penelitian ini yaitu : seperangkat alat gelas, Spektrofotometer UV-Vis, dan pengaduk magnetik.
Cara Kerja
Pembuatan Larutan Standar Analisis Vitamin C Secara Langsung
Sebanyak 100 mg vitamin C dilarutkan dengan aquades sampai 1000 mL. Dari larutan 100mg/L kemudian dibuat variasi konsentrasi vitamin C 0 mg/L, 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L.
Pembuatan Larutan Cr (VI) 10 mg/L
Sebanyak 28,3 mg K2Cr2O7 dimasukan kedalam labu ukur 1000 mL ditambahkan aquades sampai tanda batas dan dihomogenkan sehingga didapatkan konsentrasi Cr(VI) 10 mg/L.
Pembuatan Larutan DPC 0,25%
Sebanyak 0,25 mg DPC dilarutkan dengan aseton dalam labu ukur 100 mL.
Membuat Larutan Standar Analisis Vitamin C Secara Tidak Langsung
Dipipet sebanyak 1 mL dari masing masing larutan baku yang mengandung vitamin C 0 mg/L, 1 mg/L, 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 10 mg/L diikuti dengan pengasaman dengan 1 mL asam sulfat 1,0 mol/L, setelah 10 menit ditambahkan 1 mL 0,25% DPC, ditambahkan aquades sampai tanda batas. Semua larutan diukur absorbansinya dengan spektrofotometer UV-Vis.
Validasi Metode Analisis Kadar Vitamin C Secara Langsung
Uji linearitas
Larutan standar vitamin C dibaca absorbansinya dengan spektrofotometer UV-Vis, pada panjang gelombang 265 nm.
Dilakukan pengulangan sebanyak 3 kali sehingga didapatkan nilai R2 (regresi linearnya) dan kurva kalibrasi dengan persamaan y = a + bx.
Uji Akurasi
Larutan yang mengandung vitamin C 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L. Semua larutan diukur absorbansinya dengan spektrofotometer UV-Vis dengan pengulangan sebanyak 3 kali. Didapatkan nilai absorbansi dari tiap larutan dan dihitung persentase perolehan kembalinya (recovery) dengan rumus berikut ini.
n, n Konsentrasi vitamin C hasil analisis/i\
% Recovery =----------------------x 100%
Konsentrasi vitamin C sebenarnya
Uji Presisi
Larutan vitamin C dengan konsentrasi 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L diukur masing masing absorbansinya dengan spektrofotometer UV-Vis dengan pengulangan 5 kali. Sehingga dapat dihitung SD (Standar Deviasi) dan %RSD (persentase standar deviasi relatif) dari masing masing konsentrasi larutan baku dengan rumus berikut ini,
∑n
. ι (X1- X
SD =—1---
(2)
n-1
%RSD = SDx 100% (3) X
_
dimana X adalah nilai absorbansi, X adalah adalah nilai absorbansi rata rata dan n adalah ulangan.
Uji Limit Deteksi (LOD) dan Limit Kuantitasi (LOQ)
Larutan baku kerja vitamin C 0 mg/L, 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L. diukur masing masing absorbansinya dengan spektrofotometer UV-Vis dan dihitung persamaan kurva kalibrasinya y = a + bx. Sehingga dapat dihitung nilai LOD dan LOQ dengan rumus berikut ini,
LOD = 3^SlyZx) (4) b 7
LOQ = 10 χ SS (y∕x) (5)
dimana S (y⁄x) adalah variasi variabel respon dari nilai (y), b adalah slope absorbansi hasil pengukuran dengan spektrofotometer UV-Vis, Yi adalah nilai absorbansi hasil subtitusi nilai konsentrasi (X) pada persamaan linear dan n adalah jumlah larutan yang diukur absorbansinya.
Validasi Metode Analisis Kadar Vitamin C Secara Tidak Langsung
Uji Linearitas
Dipipet sebanyak 1 mL dari masing masing larutan baku yang mengandung vitamin C 0 mg/L, 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 10 mg/L diikuti dengan pengasaman dengan 1 mL asam sulfat 1,0 mol/L, setelah 10 menit ditambahkan 1 mL 0,25% DPC, ditambahkan aquades sampai tanda batas. Semua larutan diukur absorbansinya dengan spektrofotometer UV-Vis pada panjang gelombang 551 nm, dilakukan pengulangan sebanyak 3 kali. Dihitung nilai penurunan kadar Cr (VI) dan didapatkan nilai R2 (regresi linearnya).
Uji Akurasi
Dipipet sebanyak 1 mL dari masing masing larutan baku yang mengandung vitamin C 2 mg/L, 4 mg/L, 6 mg/L, dan 8 mg/L dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 25 mg/L diikuti dengan pengasaman dengan 1 mL asam sulfat 1,0 mol/L, setelah 10 menit ditambahkan 1 mL 0,25% DPC, ditambahkan aquades sampai tanda batas. Semua larutan diukur absorbansinya dengan spektrofotometer UV-Vis dilakukan pengulangan sebanyak 3 kali. Didapatkan nilai absorbansi dari tiap larutan dan dihitung persentase perolehan kembalinya (recovery) menggunakan rumus persamaan (1).
Uji Presisi
Dipipet sebanyak 1 mL dari masing masing larutan baku yang mengandung vitamin C 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L. dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 10 mg/L diikuti dengan pengasaman dengan 1 mL asam sulfat 1,0 mol/L, setelah 10 menit ditambahkan 1 mL 0,25% DPC, ditambahkan aquades sampai tanda batas. Semua larutan diukur absorbansinya dengan spektrofotometer UV-Vis serta dilakukan pengulangan sebanyak 5 kali. Sehingga dapat dihitung SD (Standar Deviasi) dan %RSD (persentase standar deviasi relatif) dari masing masing konsentrasi larutan baku dengan rumus pada persamaan (2) dan (3).
Uji Limit Deteksi (LOD) dan Limit Kuantitasi (LOQ)
Dipipet sebanyak 1 mL dari masing masing larutan baku yang mengandung vitamin C 0 mg/L, 2 mg/L, 4 mg/L, 6 mg/L dan 8 mg/L dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 10 mg/L diikuti dengan pengasaman dengan 1 mL asam sulfat 1,0 mol/L, setelah 10 menit ditambahkan 1 mL 0,25% DPC, ditambahkan aquades sampai tanda batas. Semua larutan diukur masing masing absorbansinya dengan spektrofotometer UV-Vis agar didapatkan persamaan kurva kalibrasinya y = a + bx. Sehingga dapat dihitung nilai LOD dan LOQ dengan rumus pada persamaan (4) dan (5).
Pengukuran Kadar Vitamin C Pada Sampel Minuman Suplemen Secara Langsung
Masing masing sampel minuman suplemen dalam kemasan A, B dan C yang sudah diencerkan diukur absorbansinya dengan Spektrofotometer UV-Vis.
Pengukuran Kadar Vitamin C Pada Sampel Minuman Suplemen Secara Tidak Langsung
Dipipet sebanyak 1 mL dari masing masing larutan sempel minuman suplemen dalam kemasan A, B dan C yang sudah diencerkan dimasukan ke dalam tiap labu ukur 10 mL, masing masing labu ukur ditambahkan 1 mL larutan Cr (VI) 10 mg/L diikuti dengan pengasaman dengan 1,0 mL asam sulfat 1,0 mol/L, setelah 10 menit 1,0 mL 0,25% DPC ditambahkan dan aquades sampai tanda batas. Semua larutan diukur absorbansinya dengan Spektrofotometer UV-Vis.
HASIL DAN PEMBAHASAN
Validasi Metode Analisis Uji Linearitas
Nilai koefisien korelasi (R2) dan presentase kemiripan metode langsung dan tidak langsung yang dihasilkan dalam penelitian ini dapat dilihat pada Tabel 1.
Nilai koefisien korelasi (R2) yang diperoleh dalam hasil penelitian ini telah memenuhi syarat linearitas yaitu lebih besar dari 0,99 (Miller dan Miller, 2005), sehingga dapat disimpulkan bahwa berdasarkan linearitas metode langsung dan tidak langsung dapat diterima untuk analisis kadar asam askorbat dalam sampel minuman suplemen dalam kemasan. Nilai uji -t
antara metode langsung dan tidak langsung yaitu 0,0718 untuk thitung dan 4,303 untuk ttabel. Dari uji -t antara metode langsung dan tidak langsung disimpulkan bahwa thitung < ttabel maka kedua metode tidak berbeda secara signifikan.
Tabel 1. Koefisien Korelasi (R2) dan Uji Hipotesis (Uji -t).
|
Metode |
Koefesien Kolerasi (R2) |
Uji -t | |
|
t hitung |
t tabel | ||
|
Langsung |
0,9989 ± 0,0003 | ||
|
0,0718 |
4,303 | ||
|
Tidak |
0,9988 ± 0,0017 | ||
|
Langsung | |||
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Uji Akurasi
Uji akurasi digunakan untuk mengetahui kadar asam askorbat yang diperoleh kembali (recovery) dari metode langsung dan tidak langsung serta dibandingkan dengan kadar asam askorbat sebenarnya. (AOAC, 2012). Hasil uji akurasi dalam penelitian ini dapat dilihat pada Tabel 2.
Tabel 2. % Recovery serta Uji -t Analisis
Vitamin C dengan Metode Langsung dan Tidak Langsung
|
Kadar Vit C (mg/L) |
Metode Langsung |
Metode Tidak Langsu ng |
Uji -t |
|
% Recovery ± SD |
% Recover y ± SD |
t hitung t tabel | |
|
2 |
97,977 ± |
99,006 | |
|
0,561 |
± 0,983 | ||
|
4 |
97,397 ± |
99,191 | |
|
0,584 |
± 0,426 | ||
|
6 |
96,326 ± |
97,075 | |
|
0,187 |
± 0,283 |
-4,164 3,182 | |
|
8 |
99,026 ± |
99,709 | |
|
0,081 |
± 0,123 | ||
|
Rata - rata |
97,682 ± |
98,763 | |
|
% Recovery ± SD |
1,381 |
± 1,436 |
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Berdasarkan Tabel 2 dapat dilihat bahwa rata-rata nilai % recovery yang dihasilkan
dalam penelitian ini telah memenuhi syarat akurasi yaitu 80-120% (Ermer, J dan Miller, 2005).
Uji -t untuk parameter akurasi antara metode langsung dan tidak langsung disimpulkan bahwa thitung < -ttabel maka dari parameter akurasi yang dihasilkan dari metode langsung berbeda secara signifikan bila dibandingkan dengan metode tidak langsung.
Sampel yang dipreparasi menggunakan metode tidak langsung memiliki nilai % recovery sebesar 98,763 %, lebih mendekati 100% bila dibandingkan dengan sampel yang dipreparasi menggunakan metode langsung dengan nilai % recovery sebesar 97,682 % sehingga dari
parameter akurasi metode tidak langsung lebih baik digunakan dalam analisis kadar vitamin C.
Uji Presisi
Uji presisi dilakukan dengan cara mengukur serapan sampel dalam kondisi yang sama sebanyak tiga kali pengulangan (Sumardi, 2002). Hasil uji presisi metode langsung dan tidak langsung dapat dilihat pada Tabel 3.
Tabel 3. Hasil Uji Presisi serta Uji -t dari Metode
Langsung dan Metode Tidak
Langsung
|
Kadar Vit C (mg/L) |
Metode Langsung % RSD |
Metode Tidak Langsung % RSD |
Uji -t t hitung t tabel |
|
2 |
1,198 |
1,161 | |
|
4 |
0,627 |
0,359 | |
|
6 |
0,194 |
0,244 |
1,478 3,182 |
|
8 |
0,333 |
0,178 | |
|
Rata - rata |
0,588 |
0,485 | |
|
% RSD |
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Hasil uji presisi pada Tabel 3 menunjukkan bahwa sampel yang dipreparasi menggunakan metode tidak langsung memiliki nilai presisi yang lebih kecil yaitu 0,485% bila dibandingkan dengan sampel yang dipreparasi menggunakan metode langsung dengan nilai presisi sebesar 0,588%. Apabila nilai rata-rata RSD yang dihasilkan dalam analisis ˂ 1%, berarti tingkat
ketelitian yang dimiliki oleh metode tersebut tergolong sangat tinggi. Nilai RSD yang berada pada rentang 1-2% menunjukkan bahwa metode yang diterapkan memiliki tingkat ketelitian yang tergolong cukup teliti (Sumardi, 2002).
Hasil dari uji -t disimpulkan bahwa t hitung < t tabel maka dari parameter presisi, metode langsung dan tidak langsung tidak memiliki perbedaan secara signifikan. Sehingga dari parameter presisi metode langsung dan tidak langsung dapat digunakan untuk analisis vitamin C.
Uji Batas Deteksi (LoD) dan Batas Kuantitasi (LoQ)
Batas deteksi adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Batas kuantitasi merupakan parameter pada analisis yang diartikan sebagai kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Riyanto, 2014).
Hasil uji LoD dan LoQ metode langsung dan tidak langsung dapat dilihat pada Tabel 4.
Tabel 4. Hasil Uji LoD, LoQ serta Uji -t dari Metode Langsung dan Metode Tidak Langsung
|
Parameter |
Metode |
Uji -t | ||
|
Langsung |
Tidak Langsung |
t hitung |
t tabel | |
|
LoD |
0,359 ± 0,057 |
0,288 ± 0,292 |
0,466 |
4,303 |
|
LoQ |
1,197 ± 0,190 |
0,960 ± 0,973 |
0,466 |
4,303 |
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Berdasarkan perhitungan dari kurva metode tidak langsung memiliki nilai LoD 0,288 mg/L dan nilai LoQ 0,960 mg/L yanglebih kecil bila dibandingkan dengan metode langsung dengan nilai LoD 0,359 mg/L dan nilai LoQ 1,197 mg/L.
Hasil uji -t parameter LoD dan LoQ dapat disimpulkan bahwa nilai t hitung < t tabel maka darihasil uji parameter LoD dan LoQ antara metode langsung dan tidak langsung tidak memiliki perberbedaan secara signifikan. Sehingga dari parameter LoD dan LoQ metode
langsung dan tidak langsung dapat digunakan untuk analisis vitamin C.
Penentuan Metode Terbaik dalam Analisis Vitamin C
Berdasarkan hasil uji parameter dalam validasi metode analisis yang meliputi uji linearitas, uji akurasi, uji presisi, LoD dan LoQ disimpulkan bahwa semua metode analisis vitamin C dapat diterima karena telah memenuhi kriteria parameter yang telah ditetapkan dalam validasi metode analisis. Namun, metode terbaik untuk analisis vitamin C adalah metode tidak langsung karena memiliki nilai % recovery yang lebih mendekati 100%.
Penentuan Konsentrasi Vitamin C dalam Sampel Minuman Suplemen Dalam Kemasan
Persamaan regresi linear pada penentuan konsentrasi vitamin C dengan metode langsung didapatkan y = 0,089x – 0,0024 dengan nilai R2 sebesar 0,9989. Persamaan regresi linear pada metode tidak langsung didapatkan persamaan regresi linear y = -0,0587x + 0,8889 dengan nilai R2 sebesar 0,9988. Berdasarkan hasil persamaan regresi kurva kalibrasi vitamin C dengan metode langsung dan tidak langsung yang telah diperoleh, maka kadar vitamin C pada masing-masing sampel minuman suplemen dalam kemasan ditunjukkan pada Gambar 1.
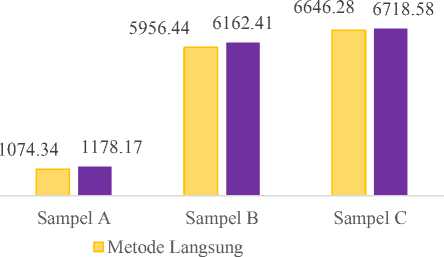
■ Metode Tidak Langsung
Gambar 1. Diagram konsentrasi vitamin C (mg/L) pada sampel minuman suplemen dalam kemasan dengan metode langsung dan tidak langsung.
Untuk mengetahui adanya perbedaan hasil analisis vitamin C dengan metode langsung dan metode tidak langsung maka dilakukan perhitungan persentase kesesuaian kadar vitamin
C hasil analisis dengan metode langsung dan metode tidak langsung serta uji -t yang dibandingkan dengan kadar vitamin C yang tercantum pada label kemasan minuman suplemen yang disajikan dalam Tabel . 5
Tabel 5. Perbandingan kadar vitamin C hasil analisis dengan kadar pada label kemasan minuman suplemen dalam kemasan.
|
Sampel |
Metode Langsung |
Uji -t | ||
|
Kadar (mg/L) |
% kesesuaian kadar |
t hitung |
t tabel | |
|
A 145 mg/120 mL |
1074,34 ± |
88,91 |
-8,116 | |
|
1208,33 mg/L B 1000 mg/150 mL |
14,296 5956,44 ± |
89,35 |
-4,556 |
4,303 |
|
6666,67 mg/L C 1000 mg/140 mL |
135,005 6646,28 ± |
93,05 |
- 26,951 | |
|
7142,86 mg/L |
15,597 | |||
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Hasil uji -t pada metode langsung sampel A , B, C dan hasil uji -t pada metode tidak langsung sampel B dan C berturut turut yaitu nilai t hitung < -t tabel maka kadar vitamin C yang diperoleh dari sampel minuman suplemen A, B dan C yang dianalisis dengan metode langsung dan kadar vitamin C yang diperoleh dari sampel minuman suplemen B dan C yang dianalisis dengan metode tidak langsung berbeda secara signifikan dibandingkan dengan kadar vitamin C yang tertera pada label sampel minuman suplemen dalam kemasan. Hasil uji -t pada sampel A metode tidak langsung didapatkan nilai t hitung > -t tabel maka kadar vitamin C yang diperoleh dari sampel minuman suplemen A yang dianalisis dengan metode tidak langsung tidak berbeda secara signifikan dengan kadar yang tertera pada label kemasan. Untuk mengetahui adanya perbedaan hasil analisis vitamin C dengan metode langsung dan metode tidak langsung maka dilakukan Uji -t yang membandingkan nilai konsentrasi vitamin C dalam minuman suplemen yang disajikan dalam Tabel 6.
Tabel 6 menunjukan hasil uji -t perbandingan antara kadar vitamin C pada sampel minuman suplemen A dan C yang dianalisis dengan metode langsung dan metode
tidak langsung dapat disimpulkan bahwa nilai t hitung < -t tabel maka pada sampel minuman suplemen A dan C konsentrasi vitamin C hasil analisis metode langsung dan tidak langsung, berbeda secara signifikan. Hasil uji -t untuk sampel minuman suplemen B disimpulkan bahwa nilai t hitung > -t tabel maka konsentrasi vitamin C pada sampel minuman suplemen B hasil analisis metode langsung dan tidak langsung, tidak berbeda secara signifikan.
Tabel 6. Perbandingan kadar vitamin C
antara hasil analisis secara langsung dan tidak langsung
|
Sampel |
Metode Langsung |
Metode Tidak Langsung |
Uji -t | |
|
Kadar (mg/L) |
Kadar (mg/L) |
t hitung |
t tabel | |
|
A |
1074,34 ± 14,296 |
1178,17 ± 12,636 |
-16,931 |
4,303 |
|
B |
5956,44 ± 135,005 |
6162,41 ± 27,257 |
-2,204 |
4,303 |
|
C |
6646,28 ± 15,597 |
6718,58 ± 9,836 |
-6,144 |
4,303 |
Keterangan :
Jika nilai t hitung > t tabel, atau -t hitung < -t tabel maka kedua metode berbeda secara signifikan. Jika nilai -t tabel ≤ t hitung ≤ t tabel maka kedua metode tidak berbeda secara signifikan.
Pengukuran kadar vitamin C secara tidak langsung pada sampel minuman suplemen dalam kemasan dapat memberikan hasil yang lebih tinggi karena vitamin C pada sampel direaksikan dengan logam Cr6+ dari K2Cr2O7 sehingga logam Cr6+ tereduksi membentuk logam Cr3+. Logam Cr6+ sisa yang tidak bereaksi dengan vitamin C tersebut dikompleksasi dengan senyawa difenilkarbazida (DPC) dan membentuk larutan berwarna violet pada larutan sampel, penurunan kadar Cr6+ pada sampel berbanding lurus dengan meningkatnya kadar vitamin C pada sampel.
Analisis vitamin C dengan metode tidak langsung memperkecil kemungkinan rusaknya vitamin C pada sampel oleh oksigen, sinar matahari dan suhu karena, vitamin C langsung bereaksi dengan Cr6+ berlebih sehingga paparan oksigen, sinar matahari dan pengaruh suhu dapat diminimalisir. Berbeda dengan metode langsung yang masih memungkinkan rusaknya vitamin C pada sampel oleh oksigen, sinar matahari dan suhu karena, pada proses preparasi dan pengukuran sampel.
Persentase kesesuaian kadar vitamin C pada sampel minuman A, B dan C hasil analisis
dengan metode langsung dan tidak langsung dengan nilai vitamin C yang tercantum pada label kemasan sampel tidak kurang dari 85% berarti perbedaan kadar hasil analisis dengan metode langsung dan tidak langsung dengan nilai vitamin C yang tercantum pada label kemasan sampel tidak lebih dari 15% sehingga masih bisa diterima untuk diedarkan di masyarakat (Perka BPOM, 2016).
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bahwa analisis vitamin C dengan metode spektrofotometri lebih baik menggunakan metode tidak langsung. Kadar vitamin C pada sampel minuman suplemen dalam kemasan A, B, dan C yang dianalisis dengan metode spektrofotometri secara langsung diperoleh sebesar 1074,34 mg/L ; 5956,44 mg/L dan 6646,28 mg/L dengan nilai %kesesuaian kadar 88,91%, 89,35%, dan
89,66%. Sedangkan kadar vitamin C pada sampel minuman suplemen dalam kemasan A, B, dan C yang dianalisis dengan metode spektrofotometri secara tidak langsung diperoleh 1178,17 mg/L ; 6162,41 mg/L dan 6718,58 mg/L dengan %kesesuaian kadar 97,50%, 92,44% dan 90,63%.
Saran
Untuk metode analisis vitamin C secara tidak langsung lebih baik menggunakan lebih banyak jenis logam untuk divalidasi dan dibandingkan hasilnya, sehingga didapatkan logam terbaik yang dapat digunakan untuk analisis vitamin C secara tidak langsung.
DAFTAR PUSTAKA
Akhilender. 2003. Vitamin C In Human Health And Disease Is Still A Mystery? An Overview. Department of
Biochemistry and Nutrition, Central Food Technological Research Institute. Mysore, India.
AOAC. 2012. Official Methods of Analysis of The Association Agricultural
Chemists. 10th ed. Washington DC.
BPOM. 2016. Peraturan Kepala Badan
Pengawas Obat dan Makanan No. 13
Tahun 2016 tentang Pengawasan Klaim Pada Label dan Iklan Pangan Olahan. Kepala Badan Pengawas Obat dan Makanan Republik Indonesia.
Emadi, M., Zare, M. A., Moradlou, O., Iranpour, M. 2014. Indirect Determination of Ascorbic Acid by Atomic Absorption Spectroscopy, Journal of Physical Chemistry and Electrochemistry, Islamic Azad University Marvdasht Branch. Iran. 2(2), 87-92.
Ermer, J. dan Miller, J. H. McB. 2005. Method Validation in Pharmaceutical Analysis, A Guide to Best Practice. Weinheim: Wiley-VchVerlag GmbH dan Co. KGaA.
Jagasia, P. V. 2015. Sensitive Spectrophotometric Determination Of Vitamin C In Herbal Products And Plant Samples. World Journal of Pharmaceutical Research. 4(6): 1762-1769.
Jiang, Q. Zhang and Zhang, J. 2001. Analitica Chimica Acta. Elsevier.
Laras. 2012. Validasi Metode Analisis dan Penentuan Kadar Vitamin C Pada
Minuman Buah Kemasan Dengan
Spektrofotometri UV-Visible. FMIPA UI. Depok.
Miller, J. C. and Miller, J. N. 2005. Statistics and Chemometrics for Analytical Chemistry. 5th ed. Pearson Education Limited. Edinburgh Gate. England. 111.
Sofriani, L. 2017. Pengaruh Paparan SInar Matahari dan Oksigen Terhadap Kandungan Asam Askorbat pada
Minuman Bervitamin. Universitas Sebelas Maret. Surakarta.
Revanasiddappa dan Veena. 2007. Sensitive Spectrophotometric Methods for the Determination of Ascorbic Acid. EJournal of Chemistry. 5(1): 10-15.
Riyanto. 2014. Validasi & Verifikasi Metode Uji: Sesuai dengan ISO/IEC 17025 Laboratorium Pengujian dan Kalibrasi. Yogyakarta: Deepublish.
Sulistyoningsih. 2011. Gizi Untuk Kesehatan Ibu dan Anak., Yogyakarta: Graha Ilmu.
Sumardi. 2002. Validasi Metode Pengujian. Pusat Standardisasi dan Akreditasi Sekretariat Jendral Depertemen Pertanian. Jakarta.
Sweetman SC. 2005. Martindale The Complete Drug Reference. 34th ed. London: Pharmaceutical Press.
147
Discussion and feedback