SENYAWA AKTIF ANTIMAKANDARI UMBI GADUNG (Dioscorea hispida Dennst)
on
ISSN 1907-9850
SENYAWA AKTIF ANTIMAKANDARI UMBI GADUNG (Dioscorea hispida Dennst)
Sri Rahayu Santi
Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran
ABSTRAK
Telah dilakukan penelitian tentang isolasi dan identifikasi senyawa aktif antimakan dari umbi gadung (Dioscorea hispida Dennst). Ekstraksi sekitar 5,0 Kg serbuk kering umbi gadung dengan menggunakan pelarut metanol menghasilkan 12,03 g ekstrak kental. Ekstrak tersebut kemudian dipartisi dengan n-heksana. Kedua ekstrak diuji aktivitas antimakannya dan ekstrak metanol menunjukkan aktivitas yang lebih tinggi dibandingkan ekstrak n-heksana.
Pemisahan ekstrak metanol dilakukan dengan kromatografi kolom menggunakan fase diam silika gel 60 dan fase gerak metanol-kloroform (6:5) menghasilkan 4 fraksi dimana fraksi FA memiliki aktivitas antimakan paling tinggi. Uji kemurnian fraksi FA dengan kromatografi lapis tipis (KLT) didapatkan 2 noda, karena itu dilanjutkan dengan kromatografi lapis tipis preparatif sehingga didapatkan 2 fraksi (FA.1 dan FA.2). Fraksi FA.1 memberikan aktivitas antimakan yang lebih baik dari fraksi FA.2 dan setelah diuji kemurnian fraksi FA.1 memberikan noda tunggal.
Uji fitokimia dan analisis spektrofotometer menunjukkan bahwa isolat aktif (FA.1) kemungkinan adalah senyawa golongan alkaloid yang mempunyai serapan maksimum pada daerah panjang gelombang 277,1 nm dan diduga memiliki gugus fungsi N-H (3425,3 cm-1), C-H alifatik (2927,7 dan 2854,5 cm-1), C=O (1735,8 cm-1), C-N (1110,9 cm-1) dan N-C=O (621,9 cm-1
Kata Kunci : Dioscorea hispida Dennst, antimakan, isolasi, identifikasi
ABSTRACT
Isolation and identification of active antifeedant compounds from gadung tuber (Dioscorea hispida Dennst) has been carried out. As much as 12.03 g of concentrated methanol extract was resulted from 5.0 kg dry gadung tuber that was macerated using methanol. Further, this extract was partitioned with n-hexane to obtain 2 concentrated extracts in n-hexane and methanol. The result of antifeedant test showed that the methanol extract was more active than the n-hexane extract.
Separations of the methanol extract using column chromatography (stationary phase : silica gel 60, mobile phase : methanol-chloroform 6:5) resulted four fractions. The most active fraction, FA , showed 2 spots on the TLC, so it was separated using preparative TLC which resulted in 2 fractions (FA.1 and FA.2). The antifeedant activity of FA.1 fraction was higher than FA.2 fraction and it gave only 1 spot on the TLC
The result of identification using phytochemical test and spectrophotometer analysis suggested that FA.1 fraction was alkaloid compound whose maximum wave length was 277.1 nm and it contained N-H (3425.3 cm-1), CH aliphatic (2927.7 and 2854.5 cm-1), C=O (1735.8 cm-1), C-N (1110.9 cm-1) and N-C=O (621.9 cm-1).
Keywords : Dioscorea hispida Dennst., antifeedant, isolation, identification
PENDAHULUAN
Penelusuran tumbuh-tumbuhan yang dapat menghasilkan senyawa antimakan untuk mengendalikan hama serangga sangat menarik untuk diteliti. Hal ini karena dalam perlindungan tumbuhan, senyawa antimakan tidak membunuh, mengusir atau menjerat serangga hama, bersifat spesifik terhadap serangga sasaran, tidak mengganggu serangga lain, tetapi hanya menghambat selera makan serangga sehingga tumbuhan dan kelangsungan hidup organisme lainnya terlindungi (Tjokronegoro, 1987).
Tumbuhan Dioscorea hispida Dennst di Bali dikenal dengan nama gadung. Umbi tumbuhan ini oleh masyarakat digunakan untuk mengobati kusta, borok, kencing manis, penurun panas, anti rematik, pengencer dahak, menghilangkan nyeri haid, dan racun binatang, sedangkan getahnya digunakan untuk mengobati gigitan ular serta sisa pengolahan tepungnya digunakan sebagai insektisida (Heyne, 1987; Sastroamidjojo, 1997; Hariana, 2004; Harini dkk., 2000; Patcharaporn et al., 2010). Sifat racun umbi gadung disebabkan oleh kandungan dioskorin, rasanya yang menggigit disebabkan oleh kandungan taninnya.Tumbuhan dari genus yang sama yaitu Dioscorea bulbifera linn juga bersifat toksik terhadap Artemia salina Leach dengan LC50 sebesar 0,7460 ppm (Puspawati, 1997). Oleh karena senyawa metabolit sekunder yang terbentuk pada bagian tertentu tumbuhan terdistribusi ke seluruh bagian tumbuhan, maka diduga umbi gadung juga mengandung senyawa yang bersifat toksik. Melalui pendekatan etnobotani bahwa umbi gadung dapat digunakan sebagai insektisida, dan pendekatan kemotaksonomi bahwa tumbuhan dari genus atau famili yang sama kemungkinan juga mempunyai senyawa dengan struktur yang mirip, serta didukung oleh hasil uji pendahuluan ekstrak metanol umbi gadung terhadap Epilachna sparsa, yang menunjukkan aktivitas antimakan 100% pada konsentrasi 5% dan 10% b/v, maka dalam penelitian ini akan dilakukan penelusuran senyawa yang berpotensi sebagai biopestisida khususnya aktivitas antimakan dengan mempergunakan Epilachna sparsa sebagai bioindikator.
MATERI DAN METODE
Bahan
Bahan yang digunakan dalam penelitian adalah umbi gadung (Dioscorea hispida Dennst) diperoleh dari Desa Abiantuwung Tabanan. Identifikasi tentang taksonomi tumbuhan dilakukan di LIPI-UPT. Balai Konservasi Tumbuhan Kebun Raya “Eka Karya” Bali. Bahan kimia yang digunakan adalah metanol, n-heksana, akuades, asam klorida, natrium hidroksida, amonium hidroksida, serbuk magnesium, asam sulfat, kalium bromida, silika gel 60, silika gel GF254 , pereaksi feri klorida, Meyer, Wagner, Willstater, dan pereaksi Lieberman-Burchad. yang berderajat pro analisis (p.a) dan teknis.
Peralatan
Peralatan yang digunakan meliputi: seperangkat alat gelas, neraca analitik, blender, pisau, penguap putar vakum, lampu UV, seperangkat alat kromatografi lapis tipis dan kolom, desikator, tabung reaksi, plat tetes, cawan petri, pipet tetes, pipet ukur dengan berbagai ukuran, spektrofotometer UV-Vis Secoman S 1000 PC dan spektrofotometer Jasco FTIR-5300.
Cara Kerja
Sekitar 5 kg serbuk kering umbi gadung dimaserasi berulang kali dengan 15 L metanol (MeOH) sampai semua komponen terekstraksi. Ekstrak MeOH disaring dan dipekatkan dengan penguap putar vakum sampai diperoleh ekstrak kental MeOH, kemudian dipartisi dengan 240 mL n-heksana. Kedua ekstrak yang diperoleh diuapkan sampai kental, kemudian diuji aktivitasnya terhadap Epilachna sparsa. Ekstrak yang paling toksik dilanjutkan untuk dipisahkan dan dimurnikan dengan teknik kromatografi kolom menggunakan silika gel GF254 dan fase gerak metanol-kloroform (6:5), dan KLT preparatif dengan fase gerak metanol-kloroform (3:2) Tiap fraksi hasil pemisahan kromatografi kolom maupun KLT preparatif diuji aktivitas antimakan dan fraksi yang paling aktif diidentifikasi golongan senyawanya menggunakan uji fitokimia dan analisis fisikokimia menggunakan alat spektrofotometer UV-vis dan Inframerah.
HASIL DAN PEMBAHASAN
Isolasi Senyawa Aktif Antimakan dari Umbi Gadung
Hasil maserasi dari 5 Kg serbuk kering umbi gadung menggunakan 1500 mL pelarut metanol (MeOH) menghasilkan sekitar 12,03 g ekstrak kental metanol yang berwarna coklat. Ekstrak kental metanol yang diperoleh selanjutnya dilarutkan dengan metanol kemudian
dipartisi dengan 240 mL n-heksana. Kedua ekstrak yang diperoleh diuapkan menghasilkan 4,02 g ekstrak n-heksana yang berwarna coklat, dan 5,12 g ekstrak metanol yang berwarna kuning kecoklatan. Hasil uji aktivitas antimakan kedua ekstrak kental yang diperoleh terhadap Epilachna sparsa (E. sparsa) menunjukkan bahwa ekstrak metanol mempunyai aktivitas antimakan yang paling besar yaitu sebesar 95,65 % pada konsentrasi 10%b/v seperti dipaparkan pada Tabel 1 berikut :
Tabel 1. Hasil uji aktivitas antimakan ekstrak metanol dan ekstrak n-heksana
|
No |
Konsentrasi (% (b/v)) |
Aktivitas Antimakan (%) | ||
|
Percobaan 1 |
Percobaan 2 |
Rata-rata | ||
|
1 |
Ekstrak kental metanol 0,1 |
-93,10 |
-93,55 |
-93,33 |
|
5 |
88,24 |
100 |
94,12 | |
|
10 |
91,30 |
100 |
95,65 | |
|
2 |
Ekstrak kental n-heksana 0,1 |
-77,78 |
-60 |
-68,89 |
|
5 |
11,11 |
88,24 |
49,68 | |
|
10 |
93,94 |
92 |
92,97 | |
Pemisahan ekstrak metanol dengan kromatografi kolom menghasilkan empat kelompok fraksi yang selanjutnya diuji aktivitas antimakannya terhadap E. sparsa. Hasil uji
aktivitas antimakan menunjukkan bahwa fraksi FA mempunyai aktivitas yang lebih tinggi dibandingkan fraksi-fraksi lainnya seperti ditunjukkkan pada Tabel 2 berikut :
Tabel 2. Hasil uji aktivitas antimakan fraksi penggabungan
|
No |
Fraksi |
Konsentrasi (ppm)) |
Aktivitas Antimakan (%) | ||
|
Percobaan 1 |
Percobaan 2 |
Rata-rata | |||
|
1 |
FA |
100 |
40 |
66,67 |
53,34 |
|
200 |
66,67 |
41,18 |
53,93 | ||
|
400 |
71,43 |
86,67 |
79,05 | ||
|
800 |
76,47 |
100 |
88,24 | ||
|
1600 |
89,47 |
100 |
94,74 | ||
|
2 |
FB |
100 |
28,57 |
33,33 |
30,95 |
|
200 |
42,86 |
33,33 |
38,10 | ||
|
400 |
64,71 |
40 |
52,05 | ||
|
800 |
96,23 |
52,38 |
74,31 | ||
|
1600 |
71,43 |
95,92 |
83,68 | ||
|
3 |
FC |
100 |
-20 |
-25 |
-22,5 |
|
200 |
-11,11 |
-42,86 |
-26,99 | ||
|
400 |
-20 |
-20 |
-20 | ||
|
800 |
20 |
44,44 |
32,22 | ||
|
1600 |
40 |
33,33 |
36,67 | ||
|
4 |
FD |
100 |
-40 |
-11,11 |
-25,56 |
|
200 |
-33,33 |
-42,86 |
-38,10 | ||
|
400 |
-25 |
-11,11 |
-18,06 | ||
|
800 |
20 |
25 |
22,5 | ||
|
1600 |
16,67 |
33,33 |
25 | ||
Oleh karena itu fraksi FA kemudian diuji kemurniannya pada plat KLT dengan berbagai fase gerak. Hasil uji kemurnian menunjukkkan fraksi FA belum murni sehingga dipisahkan lagi dengan KLT preparatif yang menghasilkan 2 fraksi yaitu FA.1 dan FA.2 kemudian masing-
masing dilanjutkan dengan uji aktivitas. Hasil uji aktivitas antimakan menunjukkan bahwa fraksi FA.1 mempunyai aktivitas yang lebih tinggi dibandingkan fraksi lainnya seperti ditunjukkan pada Tabel 3 berikut :
Tabel 3. Hasil uji aktivitas antimakan fraksi hasil KLT preparatif
|
No |
Fraksi |
Berat (mg) |
Konsentrasi (ppm)) |
Aktivitas Antimakan (%) | ||
|
Percobaan 1 |
Percobaan 2 |
Rata-rata | ||||
|
1 |
FA.1 |
21,5 |
100 |
14,29 |
27,27 |
20,78 |
|
200 |
33,33 |
20 |
26,67 | |||
|
400 |
60 |
45,45 |
52,73 | |||
|
800 |
66,67 |
63,64 |
65,15 | |||
|
1600 |
71,43 |
62,25 |
66,97 | |||
|
2 |
FA.2 |
17,2 |
100 |
20 |
20 |
20 |
|
200 |
33,33 |
27,27 |
30,3 | |||
|
400 |
27,27 |
42,86 |
35,1 | |||
|
800 |
33,33 |
42,86 |
38,8 | |||
|
1600 |
52,94 |
60 |
56,47 | |||
Fraksi FA.1 ini relatif murni secara KLT dengan tetap memberikan satu noda pada berbagai fase gerak yang digunakan seperti: kloroform-metanol (2:3) kloroform-etil asetat (1: 2); metanol-kloroform (6:5). Fraksi FA.1 kemudian diidentifikasi dengan pereaksi fitokimia untuk mengetahui golongan senyawanya, serta dianalisis dengan spektrofotometer UV-Vis dan inframerah.
Identifikasi Isolat (Fraksi A1)
Hasil uji fitokimia menunjukkan bahwa isolat merupakan senyawa golongan alkaloid yang ditunjukkan dengan terbentuknya endapan coklat dan putih dengan pereaksi Wagner dan Meyer. Hasil spektrum inframerah menunjukkan bahwa isolat kemungkinan mengandung beberapa gugus fungsi seperti –N-H (3425,3 cm-1) yang didukung juga oleh munculnya serapan pada daerah bilangan gelombang 1562,2 cm-1
dan 1110,9 cm-1 menunjukkan adanya gugus N-H bending. Gugus C-H alifatik muncul pada daerah bilangan gelombang 2927,7 dan 2854,5 cm-1 dan diperkuat dengan munculnya serapan pada daerah bilangan gelombang 1423,4 cm-1. Adanya pita tajam dengan intesitas sedang di daerah bilangan gelombang 1735,8 cm-1menunjukkan adanya gugus C=O stretcing yang dikenal dengan nama pita I amida. Dugaan ini diperkuat dengan munculnya serapan dari gugus N=C=O pada bilangan gelombang 621,9 cm-1. Pada isolat selain muncul pita I, juga muncul serapan dengan intensitas sedang dari gugus N-H bending pada bilangan gelombang 1562,2 cm-1 yang dikenal dengan nama pita II amida. Serapan melebar dengan intensitas sedang muncul di daerah bilangan gelombang 1110,9 cm-1diduga karena adanya gugus C-N bending yang diperkuat dengan munculnya serapan di daerah 621,9 cm-1, seperti ditunjukkan pada Gambar 1 dan Tabel 4 berikut :
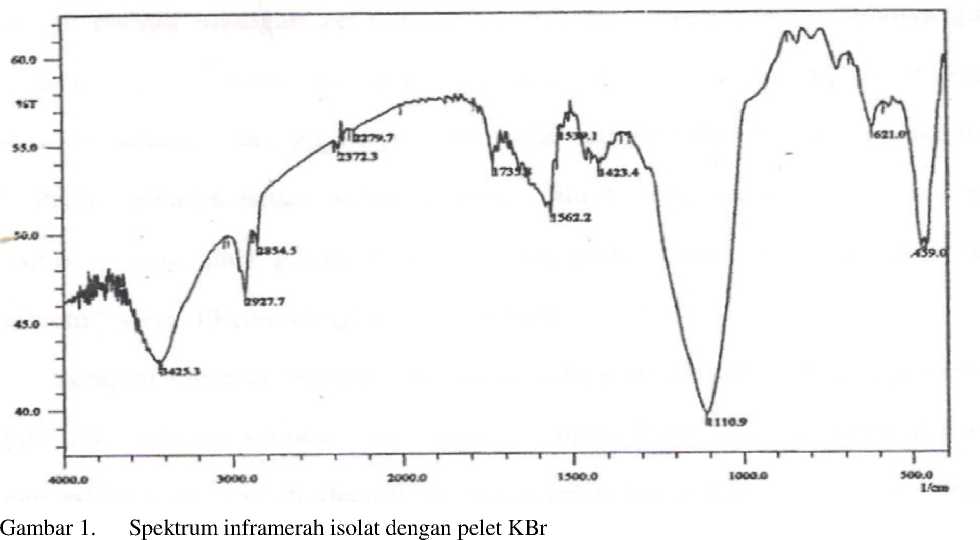
Tabel 4. Analisis spektrum inframerah senyawa hasil isolasi (isolat)
|
No |
Bilangan Gelombang (cm-1) |
Bentuk Pita |
Kemungkinan Gugus Fungsi | |
|
Pada Spektra |
Pada Pustaka (Sastrohamidjojo, 1997; Silverstein et al., 1991) | |||
|
1 |
3425,3 |
3450-3400 |
tajam |
-N-H streching |
|
2 |
2927,7; 2854,5 |
3000-2800 |
Tajam |
-CH alifatik |
|
3 |
2360 |
2000-2400 |
Tajam |
-C≡C- |
|
4 |
1735,8 |
1850-1730 |
Tajam |
-C=O- |
|
5 |
1562,2 |
1565-1475 |
tajam |
-N-H bending |
|
6 |
621,9 |
630-570 |
tajam |
N-C=O |
Hasil analisis menggunakan spektrofotometri UV-vis isolat memberikan serapan pada panjang gelombang 277,1 nm.
Spektrum UV-vis dipaparkan pada Gambar 2 berikut :
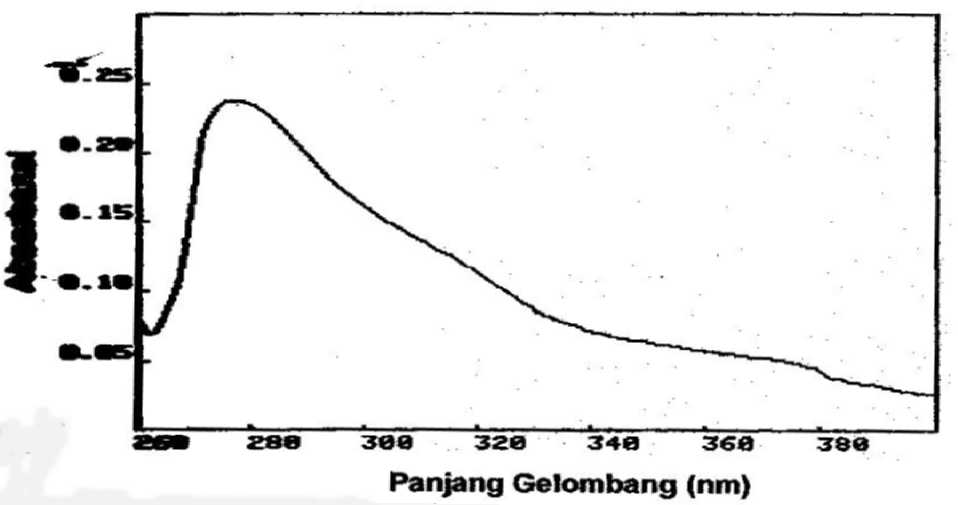
Gambar 2. Spektrum spektrofotometri UV-vis isolat (UV Secoman S 1000 PC)
Serapan yang dihasilkan isolat pada panjang gelombang 277,1 nm kemungkinan akibat terjadinya transisi berturut-turut dari n-π*, dan n-σ*. Dugaan ini diperkuat dari data hasil analisis IR dengan munculnya gugus C=O dan N-H.
SIMPULAN DAN SARAN
Simpulan
Simpulan yang dapat diambil dari penelitian yang telah dilakukan adalah sebagai berikut:
-
1. Isolat aktif antimakan (fraksi FA.1) relatif murni yang diperoleh dari KLT preparatif ekstrak kental metanol, berupa padatan berwarna putih kekuningan sebanyak 21,5 mg berpotensi aktif antimakan.
-
2. Hasil uji fitokimia dan analisis spektrofotometri diduga isolat merupakan senyawa golongan alkaloid dan kemungkinan mengandung gugus fungsi: N-
H, CH alifatik, C=O,C-N, dan N-C=O serta menyerap radiasi UV pada panjang gelombang 277,1 nm akibat dari terjadinya transisi elektronik berturut-tururt dari n-π*dan n-σ*.
Saran
Perlu dilakukan penelitian lebih lanjut untuk mengidentifikasi isolat aktif dengan menggunakan analisis NMR, dan GC-MS sehingga dapat ditetapkan suatu struktur usulan dari isolat aktif tersebut. Perlu dilakukan penelitian dengan menggunakan bioindikator lain selain larva E. sparsa dalam uji hayati antimakan.
UCAPAN TERIMA KASIH
Pada kesempatan ini penulis mengucapkan terimakasih kepada Drs. I Made Sukadana, M.Si dan Ni Wayan Kuwisnahati, S.Si serta kepada semua pihak yang telah membantu kelancaran penelitian ini.
DAFTAR PUSTAKA
Hariana, A., 2004, Tumbuhan Obat dan Khasiatnya, Seri I, Penebar Swadaya, Jakarta
Harini, M. S., 2000, Kamus Penyakit dan Tumbuhan Obat Indonesia (Etnofitomedika), Yayasan Obor
Indonesia, Jakarta
Heyne, K., 1987, Tumbuhan Berguna Indonesia II, a.b. Anonimous, Yayasan Sarana Warna Jaya, Jakarta
Patcharaporn Vanichpakorn, Wei Ding, and Xiao-Xi Cen, 2010, Insecticidal Activity of Five Chinese Medicinal Plants against Plutella xylostella L. Larvae, Journal of Asia-Pacific Entomology
Puspawati, N. M., 1997, Extraction, Isolation, and Characterisation of Biologicaly Active Compounds from Balinse Plants Use in Traditional Medicines, IAEUP-Ditjen Dikti-University of Udayana
Sastrohamidjojo, H., 1997, Spektroskopi,
Liberty, Yogyakarta
Sastrohamidjojo, H., 1997, Obat Asli Indonesia, Dian Rakyat, Jakarta Timur
Silverstin, R. M., Bassler, G. C., and Morrill, T. C., 1991, Spectrometric Identification of Organic Coumpounds, Fifth edition, Jhon Wiley &Sons, Inc., New York
Tjokronegoro, R. K., 1987, Penelusuran
Senyawa Kandungan Tumbuhan
Indonesia, Bioaktif Terhadap Serangga, Disertasi, Universitas Padjadjaran,
Bandung
78
Discussion and feedback