EKSTRAKSI DAN KARAKTERISASI HIDROKSIAPATIT DARI LIMBAH KERAJINAN TULANG SAPI MENGGUNAKAN METODE KOMBINASI ALKALI HIDROTERMAL DENGAN DEKOMPOSISI TERMAL
on
ISSN 1907-9850
EKSTRAKSI DAN KARAKTERISASI HIDROKSIAPATIT DARI LIMBAH KERAJINAN TULANG SAPI MENGGUNAKAN METODE KOMBINASI ALKALI HIDROTERMAL DENGAN DEKOMPOSISI TERMAL
I Gede Andy Andika Parahita*, I Nengah Simpen, dan Ni Gusti Ayu Made Dwi Adhi Suastuti
Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran, Bali
*E-mail : andika.parahita@gmail.com
ABSTRAK
Penelitian ini bertujuan untuk mengekstraksi hidroksiapatit dari limbah kerajinan tulang dan mengkarakterisasinya. Metode yang digunakan adalah metode kombinasi alkali hidrotermal dengan dekomposisi termal, yang dilakukan dengan cara menginteraksikan serbuk tulang dengan NaOH 5% dan dikalsinasi pada suhu 400, 750, 950 dan 1100oC (TB1, TB2, TB3 dan TB4). Nilai yield hidroksiapatit rata-rata yang dihasilkan adalah 68,82%. Karakterisasi kebasaan permukaan tertinggi dimiliki TB1 adalah 2,8345 ± 1,5166 x 10-2 mmol/gram. Karakterisasi FTIR menghasilkan gugus fungsi yang sesuai dengan senyawa hidroksiapatit. Luas permukaan tertinggi dimiliki TB1 adalah 34,4811 m2/gram. Perbandingan Ca/P rata-rata yang didapatkan adalah 1,6838. Karakterisasi XRD menunjukkan penambahan suhu mengakibatkan puncak difraksi yang dihasilkan semakin tajam yang menunjukkan struktur kristal yang dihasilkan semakin tajam.
Kata kunci : hidroksiapatit, ekstraksi, karakterisasi, alkali hidrotermal, dekomposisi termal
ABSTRACT
The aims of this research were to extract and characterize hydroxyapatite from cow bone that got from biowaste. The combination of alkaline hydrothermal with thermal decomposition method was used in this research. The raw cow bone was interacted with 5% NaOH and then calcinated at 400, 750, 950 and 1100oC (TB1, TB2, TB3 dan TB4). The yield average of the hydroxyapatite was 68,82%. Surface basisity characterization showed that the highest surface base was 2,8345 ± 1,5166 x 10-2 mmol/gram in TB1. Characterization of FTIR result showed the fuctional groups indicate hydroxyapatite molecule. The highest surface area was 34,4811 m2/gram in TB1. Average Ca/P ratio was 1,6838. XRD characterization result suggested that increasing temperature in calsination caused the difraction peak sharper.
Keywords : hydroxyapatite, extraction, characterization, alkaly hydrothermal, thermal decomposition
PENDAHULUAN
Tulang merupakan jaringan hidup yang terdiri atas 20-30% fase organik, 60-70% fase anorganik dan sekitar 5% air. Tulang mengandung bahan organik berupa kolagen dan terdapat senyawa lain dalam konsentrasi kecil seperti lipid dan protein non-kolagen, dan bahan anorganik berupa hidroksiapatit (HAp) dengan rumus kimia Ca10(PO4)6(OH)2 sebagai komponen utama serta
kandungan ion lain seperti magnesium, flourida dan natrium (Samuel et al., 1985).
Hidroksiapatit (HAp) adalah sebuah molekul kristalin yang intinya tersusun dari fosfor dan kalsium dengan rumus molekul Ca10(PO4)6(OH)2 yang termasuk di dalam keluarga senyawa kalsium fosfat. Hidroksiapatit yang berasal dari tulang sapi telah secara luas dipergunakan untuk mencangkok, memperbaiki, mengisi atau mengganti tulang, dan dalam pemeliharaan jaringan gigi karena sifat biokompatibel
yang sangat baik dengan jaringan keras, bioakti-vitas dalam membangun kembali jaringan tulang yang telah rusak dan juga di dalam jaringan lunak (Kusrini and Sontang, 2012). Selain itu, hidroksi-apatit juga telah banyak diaplikasikan sebagai katalis, pendukung katalis dan adsorben, karena struktur penyusunnya yang berpori, inert, awet dan dapat berfungsi sebagai penukar kation (Wahl dan Czernuszka, 2006). Hidroksiapatit dapat dibuat dengan cara sintesis menggunakan beberapa metode diantaranya iradiasi ultrasonik (Liu et al., 2004), emulsi membran cair (Jarudilokkul et al., 2007), radiasi metatesis gelombang mikro (Parhia et al., 2004), iradiasi cepat gelombang mikro (Sarig dan Kahana, 2002), RF plasma termal (Xu et al., 2004), presipitasi kimia (Pang dan Bao, 2003), mikroemulsi (Guo et al., 2005) dan hidrolisis (Shih et al., 2004). Namun, proses sintesis ini relatif rumit dan tidak aman secara biologis. Hidroksiapatit alami berasal dari limbah tulang sapi menggunakan beberapa metode telah dipelajari sebelumnya melalui beberapa penelitian, diantaranya teknik kalsinasi (Sobczak et al., 2009), waktu sintering dan temperatur (Kusrini dan Sontang, 2011) serta proses subkritis air, hidrolisis alkali hidrotermal dan dekomposisi termal (Barakat et al., 2009).
Berdasarkan metode sintesis dan ekstraksi hidroksiapatit yang sudah dipelajari sebelumnya menimbulkan upaya untuk mencari metode alternatif lain yang lebih ekonomis, ramah lingkungan, aman dari sisi biologi dan menyederhanakan rumitnya produksi hidroksi-apatit dengan cara sintesis yaitu ekstraksi hidroksiapatit dari limbah kerajinan tulang menggunakan metode kombinasi alkali hidroter-mal dengan dekomposisi termal dan karakterisasinya. Karakterisasi hidroksiapatit menggunakan metode titrasi asam basa, metode adsorpsi metilen biru, FTIR (Fourier Transform Infra Red), LIBS (Laser Induced Breakdown Spectroscopy) dan XRD (X-ray Diffraction). Titrasi asam basa digunakan untuk menentukan kebasaan permukaan secara kuantitatif, sedangkan secara kualitatif dilakukan dengan menggunakan FTIR. Metode metilen biru digunakan untuk mengetahui luas permukaan spesifik senyawa hidroksiapatit hasil ekstraksi. LIBS digunakan untuk mengetahui seberapa besar rasio kelimpahan atom Ca dan P senyawa hasil ekstraksi dan XRD digunakan untuk
mengidentifikasi jenis senyawa serta derajat kristalinitas senyawa hasil ekstraksi.
MATERI DAN METODE
Bahan
Bahan yang digunakan dalam penelitian ini adalah limbah serbuk kerajinan tulang sapi yang berasal dari pengerajin ukiran tulang sapi di Banjar Tegal Suci, Desa Tampaksiring, Gianyar. Bahan-bahan kimia yang digunakan dalam penelitian ini meliputi aseton, phenolphtalein (pp), NaOH, HCl, asam oksalat, metilen biru dan akuades.
Peralatan
Alat-alat yang digunakan adalah pipet volume, gelas ukur, gelas beker, erlenmeyer, labu ukur, mortar, ayakan 400 µm, oven (furnace), desikator, pengaduk magnetik, cawan porselin, bola hisap, timbangan analitik dan pencatat waktu. Peralatan instrumentasi meliputi spektrofotometer UV-Vis, spektrofotometer infra merah (FTIR), LIBS dan difraksi sinar-X (XRD).
Cara Kerja
Preparasi Serbuk Tulang
Serbuk limbah tulang sapi dicuci menggunakan aseton dan akuades untuk menghilangkan kandungan lemak serta kotoran seperti tanah dan pasir yang tercampur pada serbuk tulang. Serbuk tulang dikeringkan pada suhu 160oC selama 12 jam dengan menggunakan oven (Barakat et al., 2009). Serbuk tulang yang sudah kering diayak dengan menggunakan ayakan 400 µm, selanjutnya serbuk tulang diletakkan dalam wadah botol kaca dan diberi kode T0 serta disimpan dalam desikator. Ekstraksi Hidroksiapatit Menggunakan Metode Kombinasi Alkali Hidrotermal dengan Dekomposisi Termal
Sebanyak 500 gram serbuk tulang T0 dicampur NaOH 5% sebanyak 750 mL. Campuran kemudian direfluks selama 3 jam pada suhu 70oC. Selanjutnya, masing – masing sebanyak 100 gram sampel serbuk tulang hasil alkali hidrotermal didekomposisi termal dengan variasi suhu 400oC, 750oC, 900oC dan 1100oC selama 6 jam. Masing-masing serbuk tulang hasil dekomposisi termal diberi kode TB1, TB2, TB3 dan TB4. Hasil dekompoisi termal selanjutnya dikarakterisasi
(Barakat et al., 2009; Wahl and Czernuszka, 2006).
Karakterisasi Kebasaan Permukaan
Hidroksiapatit
Kebasaan permukaan hidroksiapatit dilakukan menggunakan sampel serbuk tulang hasil ekstraksi menggunakan kombinasi alkali hidrotermal dengan dekomposisi termal (TB1, TB2, TB3 dan TB4). Sebanyak 1,0 gram sampel serbuk tulang dari masing-masing perlakuan dimasukkan ke dalam masing-masing erlenmeyer 250 mL dan ditambahkan 10,0 mL larutan HCl 0,3 M sambil diaduk menggunakan pengaduk magnetik selama 15 menit. Campuran ditambahkan 3-4 tetes phenolphtalein (pp). Campuran dititrasi dengan larutan NaOH 0,3 M hingga terjadi perubahan warna dari awalnya tidak berwarna menjadi berwarna merah muda. Untuk menghitung kebasaan permukaan hidroksiapatit digunakan persamaan sebagai berikut :
__mmol HClawaι~ mmol HC⅛gbag H“ P b e rat samp el
(Kumar et al., 1995). Karakterisasi Gugus Fungsi Hidroksiapatit Menggunakan FTIR
Sebanyak 0,3 gram masing-masing sampel hidroksiapatit kombinasi alkali hidrotermal dengan dekomposisi termal (TB1, TB2, TB3 dan TB4), ditambahkan serbuk KBr kemudian diidentifikasi menggunakan FTIR Shimadzu IR Prestige-21 dengan rentang bilangan gelombang 4000-400 cm-1. Hasil analisis yang didapatkan berupa spektra dan data puncak karakteristik serta intensitas dari spektra yang diperoleh (Shaltout et al., 2011). Karakterisasi Luas Permukaan Hidroksiapatit Menggunakan Metode Metilen Biru
Sampel hidroksiapatit kombinasi alkali hidrotermal dengan dekomposisi termal (TB1, TB2, TB3 dan TB4) masing-masing sebanyak 0,1 gram dimasukkan ke dalam Erlenmeyer yang berisi larutan metilen biru 50 ppm sebanyak 20,0 mL, diaduk menggunakan magnetic stirrer dengan variasi waktu 5, 10, 15, 20, 30, 40, 50, dan 60 menit untuk mengetahui waktu kontak maksimum metilen biru dengan sampel. Larutan hasil pengadukan disaring menggunakan kertas saring, dan nilai absorbansinya diukur dengan spektrofotometer UV-Vis pada 664,1 nm untuk
mendapatkan berat penyerapan maksimum (mg/g). Luas permukaan ditentukan menggunakan persamaan sebagai berikut:
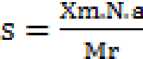
Dimana :
s = luas permukaan hidroksiapatit (m2/g) N = bilangan avogadro (6,022 x 1023 mol-1) Xm = berat metilen biru yang terserap (mg/g) a = luas penutupan 1 molekul metilen biru (197 x 10-20 m2)
Mr = berat molekul metilen biru (320,5 g/mol) (Lowell and Shields, 1984).
Karakterisasi Kelimpahan Atom Ca/P Hidroksiapatit Menggunakan LIBS
Sampel hidroksiapatit kombinasi alkali hidrotermal dengan dekomposisi termal (TB1, TB2, TB3 dan TB4) dianalis menggunakan instrumen LIBS (Laser Induced Breakdown Spectroscopy) Ocean Optics untuk mengetahui perbandingan kelimpahan unsur Ca/P dalam sampel hidroksiapatit (Kasem et al., 2013).
Karakterisasi Kristalinitas Hidroksiapatit Menggunakan XRD
Sampel hidroksiapatit kombinasi alkali hidrotermal dengan dekomposisi termal (TB1, TB2, TB3 dan TB4) dianalisis menggunakan XRD Shimadzu ZD 610 diffraktometer dengan CuKα sebagai sumber radiasinya. Komposisi fase kristalin diidentifikasi dan dicocokkan berdasarkan referensi yang terdapat pada standar data JCPDS. (JCPDS, 1996).
HASIL DAN PEMBAHASAN
Tahap preparasi dilakukan dengan merendam sampel serbuk tulang menggunakan aseton untuk menghilangkan zat organik seperti lemak dan perotein kemudian dibilas dengan akuades untuk menghilangkan debu dan kotoran yang masih tercampur pada serbuk tulang. Serbuk tulang kemudian dikeringkan pada oven 160oC selama 12 jam untuk menghilangkan molekul air yang masih terperangkap pada serbuk tulang. Selanjutnya 500 gram serbuk tulang direfluks menggunakan NaOH 5% sebanyak 750 mL pada suhu 70oC selama 6 jam dan dikeringkan pada suhu 250oC. Serbuk tulang yang dihasilkan
berwarna putih keabuan. Serbuk tulang kemudian dikalsinasi menggunakan variasi suhu 400, 750, 950 dan 1100oC selama masing-masing 6 jam (TB1, TB2, TB3 dan TB4). Variasi suhu digunakan untuk mengetahui perbedaan karakter fisik hidoksiapatit yang dihasilkan. Perbedaan warna hidroksiapatit dapat dilihat dari sampel hidroksiapatit TB1 yang menghasilkan sampel berwarna putih keabuan dan pada sampel TB2 hingga TB4 menghasilkan warna sampel berwarna putih. Perubahan warna menunjukkan adanya proses dekomposisi unsur pengisi tulang yaitu zat organik diantaranya lemak dan protein pada saat kalsinasi. (Kusrini and Sontang, 2012).
Nilai Yield Hidroksiapatit
Nilai yield hidroksiapatit merupakan persentase berat hidroksiapatit yang dihasilkan setelah melalui proses kalsinasi yang dibandingkan dengan berat serbuk tulang sebelum kalsinasi. Nilai yield yang dihasilkan ditampilkan pada Tabel 1.
Tabel 1. Nilai Yield Hidroksiapatit Menggunakan Metode Kombinasi Alkali Hidrotermal Dengan Dekomposisi Termal
|
Sampel |
Yield (%) |
|
TB1 |
71,71 |
|
TB2 |
68,21 |
|
TB3 |
68,03 |
|
TB4 |
67,34 |
Berdasarkan Tabel 1, nilai yield hidroksi-apatit rata-rata yang dihasilkan sebesar 68,82% atau terjadi penurunan massa sebesar 31,18%, sesuai dengan penelitian Ooi et al (2007) yang menunjukkan penurunan massa sampel hingga 33% yang disebabkan hilangnya molekul air dan zat organik dalam sampel serbuk tulang. Nilai yield pada Tabel 1 juga menunjukkan bahwa persentase berat hidroksiapatit menurun seiring dengan kenaikan suhu kalsinasi. Hal ini menunjukkan bahwa terjadi perubahan komposisi penyusun hidroksiapatit yang disebabkan karena pada suhu tinggi zat organik yang terurai sempurna, sehingga hidroksiapatit yang dihasilkan men-jadi lebih murni (Pang dan Bao, 2003).
Karakterisasi Hidroksiapatit
Kebasaan Permukaan Hidroksiapatit
Karakterisasi kebasaan permukaan hidrok-siapatit dilakukan untuk mengetahui jumlah situs basa yang terdapat pada sampel hidroksiapatit. Jumlah situs basa yang terdapat pada sampel hidroksiapatit dianalisis menggunakan metode titrasi asam basa. Nilai kebasaan permukaan dan jumlah situs aktif hidroksiapatit ditampilkan pada Tabel 2.
|
Tabel 2. |
Nilai Kebasaan Permukaan dan Jumlah Situs Aktif Hidroksiapatit | |
|
Sampel |
Kebasaan permukaan (mmol/gram) |
Jumlah situs aktif (situs/gram) |
|
TB1 |
2,8345±1,5166x10-2 |
17,0694 x 1020 |
|
TB2 |
2,2750±1,4832x10-2 |
13,7001 x 1020 |
|
TB3 |
2,1535±1,5166x10-2 |
12,9684 x 1020 |
|
TB4 |
2,1030±1,4491x10-2 |
12,6643 x 1020 |
NaOH yang digunakan dalam hal ini melarutkan senyawa organik seperti sisa lemak dan protein yang masih terikat dalam tulang, sehingga situs basa yang terbentuk menjadi bertambah, dimana lemak dan protein dengan kandungan awal yang cukup tinggi pada tulang dapat diminimalisir dan situs basa yang tertutupi menjadi terbuka. Namun nilai kebasaan permukaan hidroksiapatit menurun siring dengan kenaikan suhu kalsinasi. Adanya penurunan kebasaan permukaan hidroksi-apatit ini disebabkan oleh penutupan situs aktif karena terjadi perubahan struktur hidroksiapatit seiring dengan kenaikan suhu. Hal ini menunjukkan bahwa kristalinitas hidroksiapatit semakin kompak pada suhu tinggi sehingga pori yang awalnya berbentuk makropori menjadi mikropori dan nanopori yang mengakibatkan menurunnya situs basa yang didapatkan. (Han et al., 2007).
Gugus Fungsi Hidroksiapatit
Gugus fungsi hidroksiapatit diidentifikasi menggunakan FTIR dan menghasilkan data berupa spektra FTIR yang ditampilkan pada Gambar 1.
Berdasarkan Gambar 1 mengenai spektra FTIR hidroksiapatit kombinasi alkali hidrotermal dengan dekomposisi termal pada penelitian dan bilangan gelombang yang terdeteksi dirangkum pada Tabel 3.
Tabel 3 menunjukkan gugus fungsi yang Gambar 1. muncul pada spektra FTIR yang ditunjukkan oleh
Tabel 3. Bilangan Gelombang Spektra FTIR Hidroksiapatit Kombinasi Alkali Hidrotermal dengan Dekomposisi Termal
|
Dugaan gugus fungsi (Ooi et al. 2007; Laghzizil et al. 2001) |
Bilangan Gelombang (cm-1) | |||
|
TB1 |
TB2 |
TB3 |
TB4 | |
|
O-H |
636,51; |
651,94; |
650,01; |
655,8; 3495,01; |
|
3572,17; |
3568,31; | |||
|
3570,24 |
3570,24; | |||
|
3643,53 |
3655,11 |
3643,53 | ||
|
Ca-O |
1419,61; |
1409,96; |
1438,9 |
1408,04 |
|
1469,76 |
1458,18 | |||
|
PO43- |
624,94; |
960,55; |
960,55; |
960,55; |
|
960,55; |
1012,63; | |||
|
1008,77 |
1074,35 | |||
|
1010,7 |
1082,07 | |||
|
CO32- |
873,75 |
896,90 |
- |
- |
Gugus fungsi yang muncul merupakan gugus fungsi O-H, Ca-O, dan PO43- yang sesuai dengan struktur hidroksiapatit. Puncak dari gugus-gugus yang terbentuk semakin tajam berbanding lurus dengan kenaikan suhu kalsinasi, yang menunjukkan bahwa peningkatan suhu kalsinasi mengakibatkan penyempitan lebar puncak, intensitas meningkat sehingga gugus – gugus fungsi senyawa hidroksiapatit yang terkandung dalam sampel semakin jelas diidentifikasi sesuai dengan penelitian yang dilakukan oleh Ooi et al. (2007) dan Laghzizil et al. (2001).
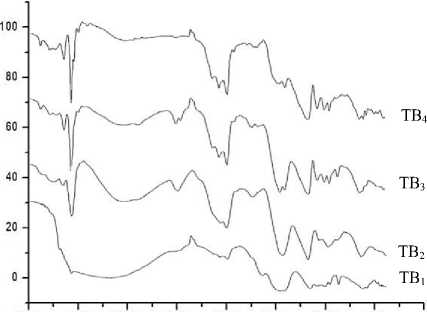
4000 3500 3000 2500 2000 1500 1000 500 0
Bilangan Gelombang (Cm-1)
Gambar 1. Spektra FTIR Hidroksiapatit Kombinasi Alkali Hidrotermal dengan Dekomposisi Termal
Selain itu, muncul pula gugus CO32- yang hanya ditemui pada sampel TA1 dan TA2. Hal ini disebabkan peningkatan suhu mengakibatkan unsur CO32- dalam sampel semakin berkurang hingga akhirnya menghilang pada sampel TA3 yang dikalsinasi pada suhu 950oC karena penggunaan suhu lebih dari 800oC terjadi reaksi dekarboksilasi pada struktur hidroksiapatit (Shaltout et al., 2011).
Luas Permukaan Hidroksiapatit
Luas permukaan hidroksiapatit diidentifikasi dengan metode adsorpsi metilen biru. Panjang gelombang yang digunakan untuk analisis filtrat metilen biru adalah 664,1 nm sesuai dengan panjang gelombang maksimum larutan metilen biru. Luas permukaan hidroksiapatit ditampilkan pada Tabel 4.
Tabel 4. Luas Permukaan Serbuk Tulang, Dekomposisi Termal dan Modifikasi Alkali Hidrotermal dengan Dekomposisi Termal
|
Sampel |
S (m2/g) |
|
TB1 |
34,4811 |
|
TB2 |
32,8413 |
|
TB3 |
30,5238 |
|
TB4 |
29,9323 |
Luas permukaan tertinggi dimiliki sampel TB1 yaitu sebesar 34,4811 m2/g dan luas permukaan menurun seiring dengan bertambahnya suhu kalsinasi. Hal ini dapat disebabkan karena pada saat proses alkali hidrotermal, NaOH yang digunakan dapat melarutkan pengotor sehingga mulut pori menjadi lebih terbuka. Selain itu, OH-yang terikat pada situs dapat mengikat metilen biru lebih banyak, namun dengan bertambahnya suhu, situs yang terbentuk terlepas kembali sehingga mengurangi luas permukaan hidroksiapatit (Shaltout et al., 2011).
Perbandingan Unsur Ca/P Hidroksiapatit
Perbandingan unsur Ca/P diidentifikasi menggunakan LIBS (Laser Induced Breakdown Spectroscopy) yang menghasilkan data berupa intensitas unsur yang dinyatakn dalam satuan atomic unit (a.u.). Perbandingan unsur Ca/P ditampilkan pada Tabel 5.
Tabel 5. Data Perbandingan Ca/P Hidroksiapatit Sampel Perbandingan Ca/P
|
TB1 |
1,6828 |
|
TB2 |
1,6849 |
|
TB3 |
1,6798 |
|
TB4 |
1,6877 |
Berdasarkan Tabel 5 dapat diketahui bahwa perbandingan unsur Ca/P hidroksiapatit rata-rata adalah sebesar 1,68. Hal ini mendekati nilai perbandingan unsur Ca/P pada penelitin yang dilakukan oleh Ooi et al (2007) yang menunjukkan bahwa hidroksiapatit yang diperoleh mendekati murni. Hidroksiapatit yang mendekati murni diduga didapatkan karena pada saat pencucian menggunakan basa panas pada proses alkali hidrotermal menghilangkan zat organik seperti protein dan lemak (Samuel et al., 1985)
Kristalinitas Hidroksiapatit
Kristalinitas hidroksiapatit diidentifikasi menggunakan XRD dengan cara membandingkan nilai puncak-puncak difraktogram yang diperoleh dengan nilai puncak-puncak difraktogram pada database JCPDS no 9-432 (XRD JCPDS file no.9-432, 1996). Puncak-puncak difraktogram hidroksi-apatit yang dihasilkan ditampilkan pada Gambar 2.
Pola difraktogram pada Gambar 2 menunjukkan bahwa hidroksiapatit kombinasi alkali
hidrotermal dengan dekomposisi termal menunjukkan puncak menyempit (tajam) seiring dengan kenaikan suhu pemanasan. Hal ini terjadi karena kristalinitas yang terbentuk semakin baik dan kompak. Puncak tertinggi pada masing-masing sampel kombinasi alkali hidrotermal dengan dekomposisi termal adalah pada sampel TB1 dengan intensitas 100 memiliki sudut 2θ 31,927 serta d-spacing 0,280 nm. Sampel TB2 dengan intensitas 100 memiliki sudut 2θ 31,571 serta d-spacing 0,283 nm. Sampel TB3 dengan intensitas 100 memiliki sudut 2θ 31,582 serta d-spacing 0,283 nm. Sampel TB4 dengan intensitas 100 memiliki sudut 2θ 31,559 serta d-spacing 0,283 nm. Puncak tersebut mendekati database JCPDS no 9-432 dimana puncak tertinggi hidroksiapatit murni dengan intensitas 100 memiliki sudut 2θ 31,77 dan d-spacing 0,281 nm.
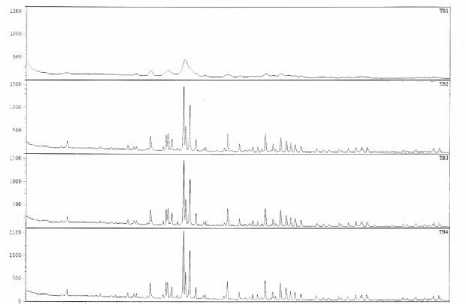
Gambar 2. Pola Difraktogram Hidroksiapatit Kombinasi Alkali Hidrotermal dengan Dekomposisi Termal
Data difraktogram yang dihasilkan menunjukkan bahwa semakin tinggi suhu yang digunakan untuk pemanasan semakin tajam pula puncak-puncak difraksi yang terbentuk sesuai dengan penelitian yang dilakukan oleh Ooi et al (2007), dimana kenaikan suhu mengakibatkan kenaikan intensitas puncak dan berkurangnya lebar puncak yang menunjukkan semakin tinggi kristalinitas dari hidroksiapatit yang dihasilkan. Kalsinasi hidroksi-apatit pada rentang suhu 750-1100oC memiliki kristalinitas yang serupa, walaupun kenaikan suhu menaikkan intensitas puncak dan menurunkan lebar puncak difraksi (Koutsopoulos, 2002). Adanya kalsinasi pada proses ekstraksi mengakibatkan adanya karbon dioksida dari
karbonat dalam hidroksiapatit dari tulang sapi yang terbebas sehingga hidroksiapatit yang dihasilkan menjadi lebih murni. Kalsinasi juga menyebabkan adanya penyusutan serta pemadatan sampel yang diakibatkan adanya perubahan komposisi unsur pengisi (zat organik) pada saat proses pemanasan yang menghasilkan tajamnya puncak difraksi (Venkateswarlu et al., 2010).
SIMPULAN DAN SARAN
Simpulan
Metode kombinasi alkali hidrotermal dengan dekomposisi termal yang digunakan untuk mengektraksi hidroksiapatit menghasilkan hidroksiapatit yang baik dan sesuai dengan standar hidroksiapatit yang ditunjukkan oleh persentase yield hidroksiapatit rata-rata yang dihasilkan adalah 68,82% dan karakterisasi kebasaan permukaan terendah dimiliki sampel TB4 dan kebasaan permukaan tertinggi dimiliki sampel TB1. FTIR menghasilkan gugus fungsi yang sesuai dengan molekul hidroksiapatit. Luas permukaan terendah dimiliki oleh sampel TB4 dan tertinggi dimiliki oleh sampel TB1. Kelimpahan atom Ca/P rata-rata yang diperoleh adalah 1,6838. Karakterisasi dengan XRD menghasilkan semakin tinggi suhu yang digunakan untuk pemanasan semakin sempit pula puncak-puncak difraksi yang terbentuk.
Saran
Mengingat pentingnya karakteristik porositas spesifik pada material padatan, maka perlu dilakukan penelitian lebih lanjut mengenai pengukuran luas permukaan dan porositas hidroksiapatit menggunakan metode BET gasorpsi N2.
UCAPAN TERIMA KASIH
Penulis sampaikan ucapan terima kasih kepada Ida Ayu Gede Widihati, Putu Suarya dan Ni Komang Ariati. Penulis juga menyampaikan ucapan terima kasih kepada tim Laboratorium Penelitian Jurusan Kimia FMIPA Universitas Udayana, Laboratorium Bersama FMIPA Universitas Udayana dan Laboratorium Kimia
FMIPA Universitas Gadjah Mada yang telah memberikan bantuan dan dukungan fasilitas hingga penelitian ini selesai.
DAFTAR PUSTAKA
Barakat, N.A.M., Khil, M.S., Omran, A.M., Sheikhh, F.A., and Kim, H.Y., 2009,
Extraction of Pure Natural Hydroxyapatite from the Bovine Bones Bio Waste by Three Different Methods, Journal of Material Processing Technology, 209 :
3408-3415
Guo, G., Sun, Y., Wang, Z., and Guo, H., 2005, Preparation of Hydroxyapatite
Nanoparticles by Reserve Microemultion, Journal of Ceramic, Int., 31 : 869-872
Han, Y., Li, S., Wang, X., Jia, L., and He, J., 2007, Preparation of Hydroxyapatite Rod-Like Crystals by Protein Precursor Method. Journal of Mater. Res. Bull. 42 : 11691177
Jarudilokkul, S., Tanthapanichakoon, W., and Boonamnuayvittaya, V., 2007, Synthesis of Hydroxyapatite Nanoparticles Using An Emultion Liquid Membrane System, Journal of Colloids Surf, A296 : 149-153
JCPDSCard File No. 9-432 (Hydroxyapatite), 1996, Joint Comittee on Powder Diffractions Standarts. Swathmore, PA.
Kasem, M.A., Gonzalez, J.J., Russo, R.E., and Harith, M.A., 2013, LIBS Analysis of
Artificial Calcified Tissues Matrices. Science Journal. 108 : 53-58
Koutsopoulos, S., 2002, Synthesis and
Characterization Of Hydroxyapatite Crystals; A Review Study On Analytical Methods. J. Biomed. Mater, Res, 62 (4) : 600-612
Kumar, P., Jasra, R.V., and Bhat, T.S.G., 1995, Evolution of Porosity and Surface Acidity in Montmorilonit Clay on Acid Activation, J. Ind. Eng. Chem. Res., 34 (4) : 298-307
Kusrini, E. and Sontang, M., 2012,
Characterization of X-Ray Diffraction and Electron Spin Resonance: Effects of Sintering Time and Temperature on Bovine Hydroxyapatite. Journal of Rad. Physical and Chem, 81 : 118-125
Laghzizil, A., El Herch, N., Bouhaouss, A., Lorente, G., and Macquete, J., 2001,
Comparison of Electrical Properties between Fluoroapatite and Hydroxyapatite Materials, Journal of Solid State Chemistry, 156 : 57-60
Liu, J., Li, K., Wang, H., Zhu, M. and Yan, H., 2004, Rapid Formation of Hydroxyapatite Nanostructures by Microwave Irradiation, Journal of Chem. Phys. Lett, 396 : 429432
Lowell, S. and Shields, J.E., 1984, Powder Surface Area and Porosity, Powder Technology Series, 2nd, Chapmand and Hall, New York.
Ooi,C.Y., Hamdi, M. and Ramesh, S. 2007, Properties Of Hydroxyapatite Produced By Annealing Of Bovine Bone. Ceramics International. 33 : 1171-1177
Pang, Y.X. and Bao, X., 2003, Influence of
temperature, ripening time and calcination on the morphology and crystallinity of hydroxyapatite nanoparticle. J. Eur. Ceram. Soc, 23 : 1697-1704
Parhia, P., Ramanan, A., and Ray, A.R., 2004, A Convenient Route for the Synthesis of Hydroxyapatite Through A Novel Microwave-Mediated Metathesis Reaction, Mater. Lett, 58 : 3610-3612
Samuel, L., Turek, M.D., Lippincott, J.B., 1985, Orthopaedics : Principles and
Applications, 2nd ed, Pitman Medical Publishing Co. Ltd., London 113, 136
Sarig, S. and Kahana, F., 2002, Rapid Formation of Nanocrystalline Apatite, Journal of Crystal. Growth 37 : 55-59
Shaltout, Abdallah A., Allam, Moussa A., Moharrama, and Mohamed, A., 2011,
FTIR Spectroscopic, Thermal and XRD Characterization of Hydroxyapatite from New Natural Sources, Journal of Spectrochimica Acta, 83 : 57-58
Shih, W.J., Chen, Y.F., Wang, M.C. and Hon, M.H., 2004, Crystal Growth and
Morphology of the Nano-Sized Hydroxyapatite Powders Synthesized from CaHPO4.2H2O and CaCO3 by Hydrolysis Method. Journal of Crystal. Growth 270 : 21-218
Sobczak, A., Kowalski, Z. and Wzorek, Z., 2009, Preparation of Hydroxyapatite from Animal Bones, Acta of Bioengineering and Biomechanics, 11 : 4
Venkateswarlu, K., Chandra Bose, A. and Rameshbabu, N., 2010. X-ray peak
broadening studies of nanocrystalline hydroxyapatite by Williamson-Hall analysis. Physica B, 405 (20) : 4256-4261
Wahl D. A. and Czernuszka J T., 2006, Collagenhydroxyapatite composites for hard tissue repair. Journal of European Cells and Materials, 11 : 43-56
Xu, J.L., Khor, K.A., Dong, Z.L., Gu, Y.W., Kumar, R., and Cheang, P., 2004,
Preparation and Characterization of Nano-ized Hydroxyapatite Powders Produced in A Radio Frequency (rf) Thermal Plasma, Mater. Sci. Eng. A 374 : 101-108
235
Discussion and feedback