7-HIDROKSI-6-METOKSI KUMARIN (SKOPOLETIN) DARI KULIT BATANG Chisocheton celebicus (MELIACEAE)
on
ISSN 1907-9850
7-HIDROKSI-6-METOKSI KUMARIN (SKOPOLETIN) DARI KULIT BATANG Chisocheton celebicus (MELIACEAE)
Dewa G. Katja1,2, Andre A. Sonda1, Desi Harneti P. Huspa1, Tri Mayanti1, dan Unang Supratman1,*
-
1Laboratorium Kimia Organik Bahan Alam, Departemen Kimia, Fakultas Matematika dan
Ilmu Pengetahuan Alam, Universias Padjadjaran, Jl. Raya Bandung-Sumedang
KM 21, Jatinangor45363, Sumedang
-
2Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sam
Ratulangi, Jl. Kampus Unsrat, Manado 95115
*Email : u_supratman@unpad.ac.id
ABSTRAK
7-hidroksi-6-metoksi kumarin (skopoletin) telah diisolasi dari kulit batang Chisocheton celebicus (Meliaceae) dengan berbagai teknik kromatografi. Struktur kimia 7-hidroksi-6-metoksi kumarin diidentifikasi berdasarkan data-data spektroskopi meliputi UV, IR, NMR-1D, NMR-2D dan massa, serta perbandingan dengan data spektra yang diperoleh dari literatur. Penemuan senyawa skopoletin dari kulit batang Chisocheton celebicus dilaporkan untuk pertama kalinya pada penelitian ini.
Kata kunci : Chisocheton celebicus, skopoletin, kumarin, Meliaceae
ABSTRACT
7-hydroxy-6-methoxy coumarin (scopoletin) has been isolated from the bark of Chisocheton celebicus (Meliacee) using several chromatographic techniques. The chemical structure of 7-hydroxy-6-methoxy coumarin was identified on the basis of spectroscopic data including UV, IR, 1D-NMR, 2D-NMR and mass along with by comparison with those spectral data previously reported. The discovery of scopoletin from the bark C. celebicus reported for the first time in this study.
Keywords : Chisocheton celebicus, coumarin, scopoletin, Meliaceae
PENDAHULUAN
TumbuhanChisocheton celebicus adalah salah satu spesies dari genus Chisocheton yang terdistribusi secara luas di daerah tropis dan subtropis seperti Nepal, India, Bhutan, Myanmar, Indo-China, Thailand, Malaysia dan Papua Nugini (Vosen and Umali, 2002). Tumbuhan Chisocheton pada umumnya sering ditemukan di dataran rendah hutan hujan tropis dan beberapa spesies tumbuhan ini secara tradisional telah digunakan sebagai obat pencuci perut, berbau khas (tengik) dan susah untuk dikeringkan serta dimanfaatkan sebagai racun untuk penangkapan ikan (Lim, 2008).
Genus Chisocheton telah banyak dilaporkan dan menghasilkan senyawa aktif yang bersifatantikanker, sitotoksik, antitumor, antiinflamasi, antimalaria, antimikroba, antilipiddanapoptosis (Wong et al.,2011; Mohamadet al., 2008; Yang et al., 2009; Awanget al., 2012; Najmuldeenet al., 2012).
Studi fitokimia terdahulu dari genus Chisocheton dilaporkan mengandung senyawa limonoid (Mohammad et al., 2008; Wong et al., 2013;Awanget al., 2012), triterpenoid (Inada et al., 1993) dan steroid (Najmuldeenet al., 2012), namun kandungan kimia dari C. celebicus belum dilaporkan.
Pada komunikasi ini kami akan melaporkan isolasi dan penentuan struktur senyawa 7-hidroksi-6-metoksi kumarin (skopoletin).
MATERI DAN METODE
Bahan
Kulit batang tumbuhan C. celebicus diperoleh dari Kebun Raya Bogor Jawa Barat pada bulan September 2012. Tumbuhan ini dideterminasi di Herbarium Bogoriense Bogor Jawa Barat (No. B0-129212) dan contoh specimen ini tersimpan di Herbarium tersebut.
Peralatan
Titik leleh ditentukan dengan ‘Fisher-Johnmicro meliting point apparatus’ dan tidak terkoreksi. Spektra UV-Visible diperoleh dengan spektrofotometer Shimazu series 1800. Spektra IR diukur dengan spektrofotometer FTIR Shimadzu 8400 dan FTIR spectrum One Perkin Elmer. 1H-dan13C-NMR spektra diperoleh dari spektrometer NMR JEOL JNM ECA-500, Spektra massa diperoleh dengan Water, Qtof HR-MS XEVotm mass spectrometer. Pergeseran kimia diberikan pada skala (ppm) dengan TMS sebagai standar internal. Kolom kromatografi dilakukan menggunakan Silika gel Merck (70-270 dan 230400 Mesh), dan analisis KLT pada pada plat (Merck, 0.25 mm), noda pada KLT ditampakkan dengan pereaksi penampak noda 10% H2SO4 dalam etanol dan diikuti dengan pemanasan.
Cara Kerja
Kulit batang kering tumbuhan C. celebicus (1,5 kg) dilahaluskan, diekstraksi berturut-turut mengunakan teknik maserasi dengan n-heksana, etil asetat dan metanol pada suhu kamar. Ekstrak yang diperoleh selanjutnya dipekatkan pada tekanan rendah sehingga dihasilkan ekstrak pekat n-heksana (4,5 g), etil asetat (13.8 g) dan metanol (15 g). Sebagian dari fraksi etil asetat (12.5 g) dipisahkan dengan teknik kromatografi cair vakum (KCV) pada fasa diam silika gel G60dengan eluen campuran n-heksana-etil asetat-metanol yang meningkat kepolarannya sehingga diperoleh 8 fraksi (A1-A8), digabungkan berdasarkan analisis kromatografi lapis tipis (KLT). Fraksi A5 (3,2 g)
dipisahkan lebih lanjut dengan kromatografi kolom pada silika gel (230-400 mesh) menggunakan campuran pelarut n-heksana : etil asetat (9:1) dihasilkan 7 fraksi utama (A5.1-A5.7), digabungkan berdasarkan analisis KLT. Fraksi A5.4 (278,7 mg) dipisahkan lebih lanjut dengan kromatografi kolom pada ODS menggunakan campuran pelarut metanol : air (4:6) sehingga dihasilkan isolat murni berupa padatan amorf berwarna kuning pucat sebanyak 2,5 mg.
HASIL DAN PEMBAHASAN
Isolat diperoleh berupa padatan amorf berwarna kuning pucat. Rumus molekul isolat ditetapkan sebagai C10H8O4 berdasarkan spektrum HR-ESI-TOFMS (m/z 191.1681, [M-H]+, perhitungan untuk C10H8O4m/z192,0423), bersama dengan data NMR (Tabel 1), dengan demikian sesuai dengan tujuh derajat ketidakjenuhan. Spektrum UV isolat menunjukkan serapan maksimum pada panjang gelombang 256 nm ( 2.600) dan 324 nm ( 6.500), menunjukkan
adanya sistem keton terkonyugasi tak jenuh- , . Spektrum IR menunjukkan adanya serapan untuk gugus hidroksil (3357 cm-1), lakton tak jenuh- , (1712 cm-1), ikatan rangkap terkonyugasi (1564 cm-1) dan eter (1136 cm-1).
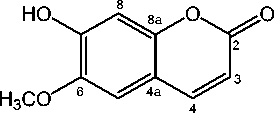
Gambar 1. Struktur kimia senyawa skopoletin
Spektrum 1H NMR isolat menunjukkan adanya dua sinyal proton olefinik tipe AB pada H 6,12 (1H, d, J=7,2 Hz) dan h 7,36 (1H, d, J=7,2 Hz), dua sinyal singlet proton aromatik pada H 6.61 (1H, s) dan H 6.38 (1H, s) dan satu proton metoksi pada H 3,73 (3H, s). Resonansi dari sepuluh sinyal karbon diamati pada spektrum 13C NMR, yang diperinci dengan percobaan Distortionless Enhancement by Polarization Transfer (DEPT) sebagai satu sinyal karbonil lakton pada C 160,9, empat sinyal metin sp2, dua sinyal karbon sp2 kuarterner, dua sinyal karbon sp2
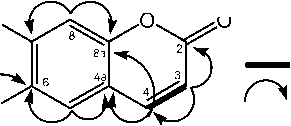
teroksigenasi dan satu sinyal metoksi pada H 56,2. Fungsionalitis ini dihitung sebagai lima dari total tujuh derajat ketidakjenuhan. Dua derajat ketidakjenuhan yang tersisa sesuai dengan kerangka struktur kumarin (Chunet el., 2015; Moreno et al., 2014). Untuk menentukan posisi gugus fungsi pada isolat, percobaan1H-1H correlated spectroscopy (1H-1H COSY) dan1H-multilicity bond connectivity (HMBC), dan hasilnya terlihat pada Gambar 2. Proton metoksi pada H 3,73 berkorelasi pada C-6 ( C 148,1), sedangkan proton aromatik pada H 6,61 berkorelasi pada C-4a ( c115,9) dan C-6 ( C 148,1), menunjukkan bahwa gugus metoksi terletak pada C-6. Proton aromatik pada H 6,36 berkorelasi dengan C-8a ( C 143,9) dan C-7 ( C 145,3), menunjukkan bahwa gugus hidroksi terletak pada C-7. Dua proton olefinik pada H 7,36 dan 6,12 saling terjodoh dan berkorelasi dengan sinyal karbonil lakton pada C 160,9, C-4a ( C 143,6) dan C-8a ( C 143,9), menunjukkan bahwa cincin lakton tak jenuh- , terletak pada C-2, C-3, C-4, C-4a dan C-8a, yang terbentuk melalui reaksi laktonisasi intramolekular dari o-hidroksi sinamat.
HO
H3CO
8a
4a
COSY
HMBC
Gambar 2. Korelasi 1H-1H COSY dan HMBC
untuk senyawa 1
Perbandingan data NMR senyawa isolat dengan 7-hidroksi-6-metoksi kumarin (Nam et al., 2015; Li et al., 2015); Jia et al., 2015), menunjukkan bahwa kedua senyawa tersebut memiliki kesesuaian yang sangat tinggi, dengan demikian senyawa isolat diidentifikasi sebagai 7-hidroksi-6-metoksi kumarin atau yang dikenal dengan nama skopoletin. Penemuan senyawa kumarin pada genus Chisocheton pertama kali dilaporkan pada penelitian ini, sehingga dapat memberikan petunjuk adanya kemampuan tumbuhan Chisocheton yang tumbuh di Indonesia menghasilkan senyawa fenolik dan dapat
memberikan pengetahuan fitokimia tumbuhan Chisocheton.
*
Table 1. Data NMRuntuk isolat*
|
Position |
13C NMR Cppm (mult.) |
1H NMR Hppm (integral, mult., JHz) |
|
2 |
160,9 (s) |
- |
|
3 |
113,5 (d) |
6,12 (1H, 7,2) |
|
4 |
143,6 (d) |
7,36 (1H, 7,2) |
|
4a |
115,9 (s) |
- |
|
5 |
112,4 (d) |
6,61 (1H, s) |
|
6 |
148,1 (s) |
- |
|
7 |
145,3 (s) |
- |
|
8 |
110,2 (d) |
6,38 (3H, s) |
|
8a |
143,9 (s) |
- |
|
6-OCH3 |
56.2 (s) |
3.73 (3H, s) |
|
*(500 MHz untuk 1H dan 125 MHz untuk 13C, | ||
|
dalam CD3OD) | ||
SIMPULAN DAN SARAN
Simpulan
7-hidroksi-6-metoksi kumarin (skopoletin) telah diisolasi dari kulit batang Chisochetoncelebicus (Meliaceae).Struktur kimia senyawa skopoletin tersebut telah diidentifikasi berdasarkan data-data spektroskopi dan perbandingan data spektra yang diperoleh sebelumnya. Penemuan senyawa kumarin pada genus Chisocheton pertama dilaporkan pada penelitian ini dan mempertegas kemampuan tumbuhan Chisocheton yang tumbuh di Indonesia untuk menghasilkan senyawa fenolik, sehingga membuka pengetahuan kemotaksonomi keberadaan senyawa fenolik pada genus Chisocheton.
Saran
Dengan ditemukannya senyawa fenolik pada genus Chisochetonmembuka peluang keberadaan senyawa fenolik lainnya pada tumbuhan Chisocheton yang tumbuh di Indonesia, untuk itu perlu dilakukan penelitian senyawa pada fraksi polar lainnya dari ekstrak kulit batang Chisochetoncelebicusvdan tumbuhan Chisocheton lainnya untuk mendapatkan struktur senyawa fenolik baru.
UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih Direktorat Jenderal Pendidikan Tinggi, kementerian Pendidikan dan Kebudayaan, Indonesia atas dana penelitian Hibah Pascasarja. Terima kasih kami ucapkan juga kepada Dr. Ahmad Darmawan dan Sofa Fajriah, M.Si di Pusat Penelitian Kimia, Lembaga Ilmu Pengetahuan Indonesia, Serpong, Tangerang atas pengukuran NMR serta Uji Pratomo di Laboratorium Bersama Universitas Padjadjaran atas pengukuran HR-ESI-TOFMS.
DAFTAR PUSTAKA
Awang, K., Chong, L., Marthi, M.T., Mokhtar, R.M., Chan, G., Litaudon, M., Gueritte, F., and Mohamad, K. 2012. Malayanines A and B, two novel limonoids from Chisocheton erythrocarpus Hiern, Tetrahedron Letters, 53 : 5355-5359
Chun, L., Wenxiu, X., Jia, W., Sujuan, W., Sun, J,Q., Zhangyu, C., Guangyu, Y., 2015. Coumarins from the roots and stem of Nicotiana tabacum and their anti-tabacco mosaic virus activity. Chemistry of Natural Compound, 51(1), 43-46.
Inada, A., Sukemawa, M., Murata, H., Nakanishi, T., Tokuda, H., Nishino, H., Iwashima, Darnaedi, D., and Murata, J. 1993. Phytochemical studies on Maleaceous Plant. Part VII. Structures and Inhibitory Effects on Epstein-Barr Virus Activation of Triterpenoida from leaves of Chisocheton macrophyllus King. Chem. Pharm. Bull. 41 ( 3): 617-619
Lim, C.S. 2008. Master Science Thesis, Department of Chemistry, University Malaya, Malaysia
Li, L., Zhao, P., Hu, J., Liu, J., Liu, Y., Wang, Z., Xia, Y., Dai, Y., Chen, L. 2015. Synthesis, in vitro and in vivo antitumor activity of scopoletin-cinnamic acid hybrids. European Journal of Medicinal Chemistry, 93, 300-307.
Jia, H,Y., Liao, Z,X., Liu, F,Y., Wu, L., Xu, C., Zuo, B. 2015. A new phenylpropanoid from the roots of Euphorbia nematocypha. Natural Products Research, 29(7), 650655.
Mohamad, K., Hirasawa, Y., Lim, C.S., Awang, K., Hamid, A., Hadi, A., Takeya, K., & Morita, H. 2008. Ceramicines A and walsogyne A, novel limonoids from two species of Meliaceae. Tetrahedron Letters, 49: 4276-4278.
Moreno, B,P., Fioruca, R., Lopes, L., Barrotto, C., Regina, M., Sarragiotto, H, M., Cristina, B,D. 2014. Terpenoids and a coumarin from aerial parts of Psychotria vellosiana Benth. (Rubiaceae). Biochemical Systematics and Ecology, 56, 80-82.
Najmuldeen, I.A., Ibrahim, A., Tasyriq, M., Lionel, L.A.I., Mohamad, K., Awang, K., and Hasima, N. 2012. 7α-hidroxy-β-sitosterol from Chisocheton tomentosus Induces Apoptosis via Dysregulation of Cellular Bax/Bcl-2 Ratio and Cell Cycle Arrest by Downregulating ERK1/2 Activation. Volume 2012. 12-18.
Nam, H., Kim, M,M. 2015. Scopolotin ha a potential activity fro anti-aging via autophagy in human lung fibroblast. Phytomedicine, 22(3), 362-368.
Vossen, V.D., H.A.M., and Umali, B.E. (Editors). 2002. Plant resources of south-east Asia no. 14 vegetable oils and fats, Prosea Foundation, Bogor, Indonesia. 150.
Wong, C.P., Shimada, M., Nagakura, Y., Nugroho, A.E., Hirasawa, Y., Kaneda, T., Awang, K., Hamid, A., Hadi, A., Mohamad, K., Shio, M., and Morita, H. 2011. Ceramicines E-I, New Limonoids from Chisocheton ceramicus. Chem. Frm Bull. 59:407-411.
Wong, C.P., Kaneda, T., Hamid, A., Hadi, A., Morita, H. 2013. Ceramicine B. a limonoid with anti-lipid droplets accumulation activity from Chisocheton ceramicus. J. Nat Med. Doi: 10.1007/s11418-013-0755-2.
Yang, M.H., Wang, J.S., Luo, J.G., Wang, X.B., and Kong, L.Y. 2009. Tetranortriterpenoids from Chisocheton Paniculatus. J. Nat. Prod. 72: 2014-2018
270
Discussion and feedback