PENGARUH JENIS PELARUT TERHADAP KANDUNGAN SENYAWA KURKUMIN DAN AKTIVITAS ANTIOKSIDAN EKSTRAK KUNYIT (Curcuma domestica Val.)
on
Jurnal ITEPA Vol. 6 No. 2, Tahun 2017
Hal 61 - 70
PENGARUH JENIS PELARUT TERHADAP KANDUNGAN SENYAWA KURKUMIN DAN AKTIVITAS ANTIOKSIDAN EKSTRAK KUNYIT (Curcuma domestica Val.)
The Effect of The Kinds of Solvent to Curcumin Content and Antioxidant Activity of The Extract Turmeric (Curcuma domestica Val.)
Sasy Eka Putri Wahyuningtyas1, I Dewa Gede Mayun Permana2, A.A.I. Sri Wiadnyani2 1Mahasiswa Jurusan Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Universitas Udayana 2Dosen Jurusan Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Universitas Udayana E-mail :sasyekaputriwahyuningtyas@gmail.com
ABSTRACT
This research was conducted to determine effect of type of solvent to curcumin content and antioxidant activity of turmeric extract. The experimental design used in this study a randomized block design with 4 different types of solvent (96% ethanol, 95% methanol, acetone 90% and isopropanol 96%). The whole treatment was repeated four times to get 16 results of experimental. Data were analyzed by analysis of variance (ANOVA) and if treatments have effect on the observed parameters, followed by Duncan test. Parameters observed were yield, curcumin content, total phenols, antioxidant capacity, and antioxidant activity.The results showed that the type of solvent significant effect on curcumin content, total phenols, antioxidant capacity and antioxidant activity, but did not significantly effect the yield. Solvent of ethanol showed the best results with the yield of 14.90%, curcumin content of 1.90%, total phenols of 51.56 mg GAE/100 g sampels, the antioxidant capacity of 5.49 mg GAEAC/100 g sampels, and antioxidant activity (IC 50) of 51.17 mg/l.
Key word: turmeric, curcumin, extraction, ethanol antioxidant.
PENDAHULUAN
Kunyit sudah dikenal sejak lama di kalangan masyarakat sebagai pelengkap bumbu masakan dan obat tradisional, hal ini diikuti dengan berkembangnya berbagai industri berbasis bahan baku alami.Rahayu (2010) melaporkan bahwa rimpang kunyit diketahui banyak memiliki kandungan kimia, diantaranya mengandung glukosa, fruktosa, protein, minyak atsiri dan kurkumin beserta turunannya yaitu monodesmetoksikurkumin dan bidesmetoksikurkumin sebanyak 50-60%. Kurkumin merupakan komponen penting yang memberikan warna kuning atau kuning jingga yang khas (Jaruga, 1998). Kurkumin termasuk golongan senyawa
polifenol yang berpotensi sebagai antioksidan dalam menangkal radikal bebas (Jayaprakasha et al., 2005; Jayaprakasha et al., 2006).
Senyawa kurkumin bersifat polar, sehingga dibutuhkan pelarut yang bersifat polar untuk menghasilkan senyawa kukumin dan aktivitas antioksidan yang tinggi. Selain itu sifat kimia kurkumin adalah memiliki sifat tidak stabil akibat perubahan pH lingkungan. Kurkumin dalam suasana asam akan berwarna kuning atau kuning jingga, sedangkan dalam suasana basa akan berwarna merah (Tonnesen and Karlsen, 1985).
Pengambilan kurkumin dari suatu tanaman dapat dilakukan dengan cara ekstraksi. Ekstraksi dapat dilakukan dengan 3 metode yaitu metode
soxletasi, metode perkolasi, dan metode maserasi. Dari ketiga metode diatas metode maserasi adalah metode yang paling banyak digunakan dalam berbagai jenis ekstraksi. Maserasi merupakan proses ekstraksi simplisia dengan menggunakan pelarut yang bertujuan untuk mendapatkan zat-zat yang terkandung di dalam bahan. Kelebihan dari metode maserasi adalah biayanya yang murah, mudah untuk dilakukan, peralatannya sederhana, dan tanpa pemanasan sehingga tidak merusak senyawa kurkumin (Hargono, 1986; Noerono, 1994).
Anggitha (2012) menyatakan bahwa efektivitas ekstraksi suatu senyawa oleh pelarut sangat tergantung kepada kelarutan senyawa tersebut dalam pelarut, sesuai dengan prinsip suatu senyawa akan terlarut pada pelarut dengan sifat kepolaran yang sama. Penggunaan jenis pelarut berkaitan dengan polaritas dari pelarut tersebut sehingga memberikan pengaruh terhadap senyawa fitokimia yang dihasilkan.
Hal yang perlu diperhatikan dalam proses ekstraksi adalah senyawa yang memiliki kepolaran yang sama akan lebih mudah terlarut.Pelarut yang bersifat polar diantaranya adalah etanol, metanol, aseton air, dan isopropanol (Sudarmadji et al., 1997). Penelitian ini bertujuan untuk mendapatkan jenis pelarut yang tepat sehingga diperoleh senyawa kurkumin dan aktivitas antioksidan yang tinggi dari ekstrak kunyit.
METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Analisis Pangan, Laboratorium Pengolahan Pangan,Jurusan Ilmu dan Teknologi Pangan,Fakultas Teknologi Pertanian Universitas Udayana, Kampus Sudirman.Pelaksanaan penelitian ini dilakukan pada bulan Juni-Agustus 2016.
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah kunyit dengan umur rimpang 9 bulan. Kunyit yang akan digunakan berasal dari Desa Plaga, Kabupaten Badung, Bali. Bahan kimia yang digunakan antara lain:metanol 98%, etanol 96%, aseton 90%, isopropanol 96%, asam galat, Na2CO3, aquades, metanol PA, Folin – Ciocalteau 50%, 1,1-diphenyl-2-picrylhydrazil (DPPH).
Alat-alat yang digunakan adalah blender (Philips), Oven (Memmert), kertas saring Whatman no 42, ayakan 60 mesh, desikator, timbangan analitik (Shimadzu), mikropipet (Socorex), cawan aluminium, spektrofotometer UV–Vis (Genesys 10s Uv-Vis), rotary vakum evaporator (Ika Labortechnik), tabung reaksi (pyrex), pipet volume 1 ml (pyrex), pipet volume 5 ml (pyrex), gelas beker 200 ml (pyrex), Erlenmeyer 200 ml (pyrex), labu ukur (pyrex) dan alumunium foil.
Pelaksanaan penelitian a. Persiapan sampel
Kunyit yang sudah dibersihkan kemudian diiris dengan ketebalan ± 3-5 mm dan diblanching pada suhu 70°C selama 15 menit. Kunyit yang
sudah diblanching kemudian dikeringkan dengan oven pada suhu 40-500C selama 40 jam.Pengeringan dianggap selesai apabila bahan dapat mudah dipatahkan ketika diremas dengan tangan. Kunyit yang telah dikeringkan kemudian dihaluskan dengan menggunakan blender, selanjutnya diayak menggunakan ayakan 60 mesh.Bubuk yang diperoleh selanjutnya diekstrak (Harini, et al., 2012).
Proses pembuatan ekstrak kunyit menggunakan metode maserasi. Masing-masing bubuk kunyit ditimbang sebanyak 50 g, dilarutkan dengan pelarut sesuai dengan perlakuan (metanol 98%, etanol 96%, aseton 90%, isopropanol 96%) sebanyak 250 ml, dan dimasukkan dalam erlemayer 500 ml.Campuran serbuk kunyit dengan pelarutkemudian dishaker sebanyak 2 kali selama 5 menit dan dimaserasi selama 2 x 24 jam. Larutan disaring menggunakan kertas whatman no 42. Filtrat yang didapat kemudian dievaporasi menggunakan rotary vakum evaporator dengan tujuan untuk menguapkan pelarut yang bercampur dengan bahan saat proses ektraksi (Harini, et al., 2012).
Analisis Data
Penelitian ini menggunakan Rancangan Acak Kelompok (RAK) dengan faktor lama waktu pengambilan sampel rimpang kunyit. Penelitian ini dilakukan dengan 4 perlakuan jenis pelarut yaitu: etanol 96%, metanol 98%, aseton 90% dan
isopropanol 96%. Masing-masing perlakuan diulang sebanyak 4 kali sehingga diperoleh 16 unit percobaan.Data yang diperoleh dianalisis dengan sidik ragam dan dilanjutkan dengan uji Duncan (Steel and Torrie, 1993).Variabel yang diamati pada penelitian meliputi rendemen (Jayanudin, et al., 2014), uji kandungan senyawa kurkumin (Harini, et al., 2012), uji kandungan total fenol(Pourmorad, et al., 2006), uji kapasitas antioksidan metode DPPH (Yun, 2001), uji aktivitas antioksidan (Sompong, et al., 2011).
HASIL DAN PEMBAHASAN
Rendemen
Hasil sidik ragam menunjukkan perlakuan jenis pelarut tidak berpengaruh nyata (P>0,05) terhadap rendemen ekstrak kunyit. Rata-rata rendemen ekstrak kunyit dapat dilihat pada Gambar 1. Berdasarkan Gambar 1 dapat dilihat bahwa rendemen ekstrak kunyit berkisar antara 11,78% hingga 14,90%.
Tingkat kepolaran antara etanol, metanol, aseton, dan isopropanol memiliki perbedaan yang tidak terlalu jauh yaitu dilihat dari konstanta dielektrik secara berurutan (24.30, 33.60, 20.70, dan 18.30). Hal ini menyebabkan kemampuan mengekstrak komponen yang terkandung didalam kunyit tidak berbeda nyata. Dari hasil penelitian didapatkan rendemen ekstrak kunyit dari pelarut etanol, metanol, aseton, dan isopropanol memiliki kemampuan yang relatif sama untuk menghasilkan rendemen.
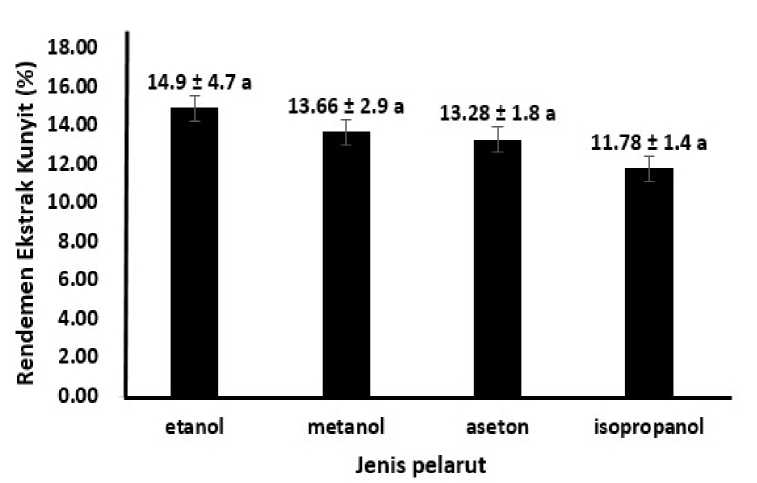
Keterangan: Notasi yang sama menunjukkan perlakuan tidak berpengaruh nyata (P>0,05)
Gambar 1. Rendemen ekstrak kunyit dengan berbagai jenis pelarut
Kurkumin
Hasil sidik ragam menunjukkan perlakuan jenis pelarut berpengaruh sangat nyata (P<0,01) terhadap kadar kurkumin ekstrak kunyit. Rata-rata kurkumin ekstrak kunyit dapat dilihat pada Gambar 2.Berdasarkan Gambar 2 dapat dilihat bahwa kadar kurkumin tertinggi terdapat pada pelarut etanol menghasilkan kadar kurkumin sebesar 1,89% tidak berbeda nyata dengan pelarut metanol sebesar 1,78% dan aseton sebesar 1,81%, dan berbeda sangat nyata dengan pelarut isopropanol sebesar 1,66%.
Tingginya sifat kelarutan kurkumin dalam etanol menyebabkan kurkumin dapat terekstrak dengan baik pada pelarut etanol.Hasil ini sesuai dengan penelitian yang sebelumnya sudah
dilakukan oleh Popuri (2013) yang menyatakan bahwa pelarut etanol sebagai pelarut terbaik dibandingkan berbagai pelarut hidrokarbon lainnya.Anggoro et al., (2015), melakukan penelitian terhadap ekstraksi multi tahap kurkumin dari temulawak (curcuma xanthorriza roxb.) menggunakan pelarut etanol dengan berbagai konsentrasi yang menunjukkan bahwa kurkumin dengan menggunakan pelarut etanol dengan konsentrasi 96% dengan waktu 180 menit menghasilkan kurkumin paling tinggi sebesar 1,782,61%. Ramdja (2009) melakukan penelitian terhadap ekstraksi kurkumin dari temulawak menggunakan pelarut etanol dengan lama waktu 4 jam, rasio bahan 50 g, dan konsentrasi pelarut
etanol 80% menghasilkan kurkumin paling tinggi
sebesar 2,69%.
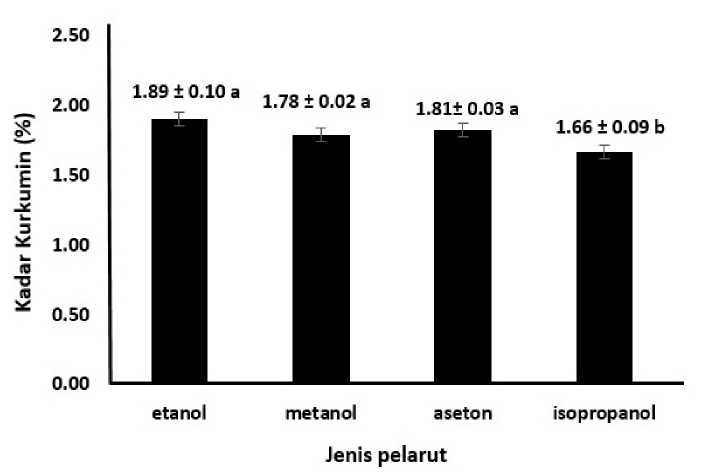
Keterangan: Notasi yang sama menunjukkan perlakuan tidak berbeda nyata (P>0,05)
Gambar 2. Kadar kurkumin ekstrak kunyit dengan beberapa jenis pelarut
Selain itu ada beberapa penelitian kadar kurkumin dengan pelarut selain etanol yang juga menghasilkan kadar kurkumin, salah satunya penelitian yang dilakukan Ria (1989) yang melakukan ekstraksi rimpang temulawak dengan metode maserasi terhadap oleoresin temulawak dengan pelarut metanol yang menghasilkan kadar kurkumin sebesar 1,86%-3,06%. Aan (2004) yang melakukan ekstraksi dengan metode maserasi terhadap ekstraksi kurkumin dari temulawak menggunakan pelarut aseton dengan lama ekstraksi 18 jam, suhu 35°C, dan nisbah pelarut 1:8 menghasilkan kadar kurkumin sebesar 1,52%.
Total Fenol
Hasil sidik ragam menunjukkan perlakuan jenis pelarut berpengaruh sangat nyata (P<0,01) terhadap total fenol. Rata-rata total fenol ekstrak kunyit dapat dilihat pada Gambar 3. Berdasarkan Gambar 3 dapat dilihat bahwa total fenol tertinggi terdapat pada pelarut etanol yaitu 51,56 mg GAE/100 g sampel dan total fenol terendah pada pelarut isopropanol sebesar 44,98 mg GAE/100 g sampel yang tidak berbeda nyata dengan pelarut metanol sebesar 45,63 mg GAE/100 g sampel dan pelarut aseton sebesar 45,16 mg GAE/100 g sampel.
Fenol merupakan senyawa yang banyak ditemukan pada tumbuhan.Fenolik memiliki cincin aromatik dengan satu atau lebih gugus hidroksil (OH-) dan gugus-gugus lain penyertanya.Senyawa fenolik kebanyakan memiliki gugus hidroksil lebih
dari satu sehingga disebut polifenol (Lestari et al.,
yang bersifat polar sehingga dapat larut dalam
2014).Lenny (2006) menyatakan bahwa flavonoid
pelarut polar seperti etanol, metanol, air, aseton,
merupakan senyawa polifenol (gugus hidroksil)
butanol, dimetil formamida, dimetil sulfoksida.
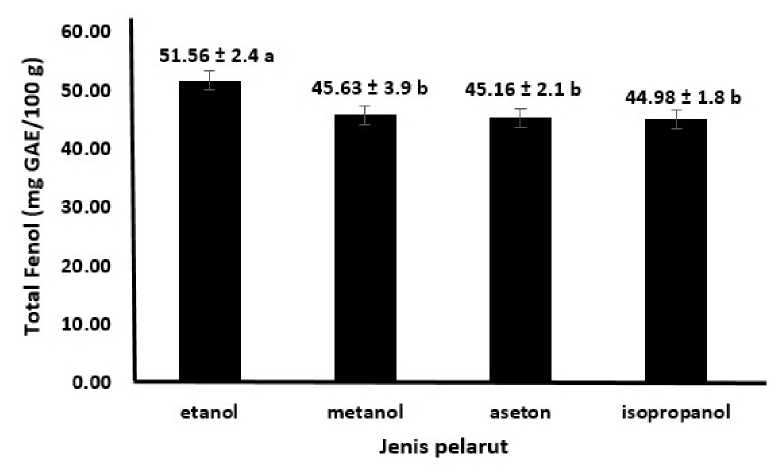
Keterangan: Notasi yang sama menunjukkan perlakuan tidak berbeda nyata (P>0,05)
Gambar 3. Total fenol ekstrak kunyit dengan beberapa jenis pelarut
Dari hasil data diatas menunjukkan bahwa total fenol pada ekstrak kunyit dengan pelarut etanol lebih tinggi hal ini menunjukkan bahwa pelarut etanol memiliki tingkat kepolaran yang sama dan lebih efektif dalam melarutkan senyawa polifenol pada ekstrak kunyit, sehingga ekstrak kunyit dengan pelarut etanol menghasilkan senyawa total fenol yang lebih tinggi.Kusriani et al., (2015) melakukan penelitian terhadap penetapan kadar fenolik ekstrak rimpang lengkuas merah dan lengkuas putih dengan beberapa jenis pelarut (n-heksan, etil asetat, dan etanol) menghasilkan kadar total fenol dengan pelarut etanol pada lengkuas merah sebesar 19,60 mg GAE/100 g.
Kapasitas antioksidan
Hasil sidik ragam menunjukkan perlakuan jenis pelarut berpengaruh nyata (P<0,05) terhadap kapasitas antioksidan. Rata-rata kapasitas antioksidan ekstrak kunyit dapat dilihat pada Gambar 4. Berdasarkan Gambar 4 dapat dilihat bahwa kapasitas antioksidan tertinggi terdapat pada pelarut etanol yaitu 5,49 mg GAEAC/100 g sampel, terendah pada pelarut isopropanol sebesar 4,30 mg GAEAC mg/100 g sampel, dan tidak berbeda nyata pada pelarut metanol sebesar 4,99 mg GAEAC/100 g sampel dan pelarut aseton sebesar 4,37 mg GAEAC/100 g sampel.
Hal ini menunjukan bahwa senyawa bioaktif yang terdapat pada ekstrak kunyit diperoleh
dengan pelarut etanol yang menghasilkan kurkumin dan kadar fenol yang paling tinggi yang bersifat sebagai antioksidan. Menurut Harborne (1987) terdapat senyawa-senyawa metabolit didalam bahan
yang mudah larut dalam pelarut etanol seperti beberapa senyawa polifenol berfungsi sebagai antioksidan.
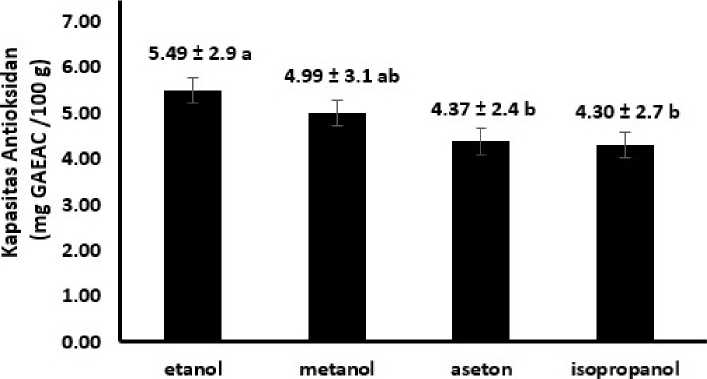
Jenis pelarut
Keterangan: Notasi yang sama menunjukkan perlakuan tidak berbeda nyata (P>0,05)
Gambar 4. Kapasitas antioksidan ekstrak kunyit dengan beberapa jenis pelarut
Aktivitas Antioksidan
Hasil sidik ragam menunjukkan perlakuan jenis pelarut berpengaruh sangat nyata (P<0,01) terhadap aktivitas antioksidan (IC 50) ekstrak kunyit. Rata-rata aktivitas antioksidan dapat dilihat pada Gambar 5. Berdasarkan Gambar 5 dapat dilihat bahwa aktivitas antioksidan (IC 50) tertinggi terdapat pada perlakuan pelarut etanol yaitu 51,17 mg/l, sedangkan aktivitas antioksidan (IC 50) terendah terdapat pada perlakuan pelarut isopropanol yaitu 59,43 mg/l. Berdasarkan hasil analisis aktivitas antioksidan (IC 50), diperoleh
bahwa perlakuan dengan pelarut etanol memiliki persentase aktivitas antioksidan (IC 50) terbaik.
Penentuan IC 50 masing-masing ekstrak bertujuan untuk memperoleh jumlah dosis ekstrak yang dapat menghambat radikal bebas sebesar 50%.Ekstrak kunyit dengan menggunakan pelarut etanol, metanol, aseton, dan isopropanol tergolong antioksidan aktif, tetapi ekstrak kunyit dengan pelarut etanol memiliki aktivitas antioksidan yang lebih aktif dibandingkan dengan ekstrak kunyit dengan pelarut metanol, aseton, dan isopropanol. Hal ini juga disebabkan oleh kadar kurkumin dan fenol dari ekstrak kunyit dengan pelarut etanol lebih
tinggi dibandingkan dengan pelarut hidrokarbon lainnya, sehingga mempengaruhi hasil dari aktivitas antioksidan.
Hasil penelitian ini sesuai dengan penelitian yang dilakukan oleh Suryani (2012) terhadap dengan pelarut etanol dengan konsentrasi 95% sebesar 51,92 mg/L.
Menurut Jun et al., (2001), suatu senyawa memiliki antioksidan kuat apabila IC50 < 50 mg/L, antioksidan aktif IC50 50-100 mg/L, antioksidan sedang IC50 101-250 mg/L, antioksidan lemah IC50 250-500 mg/L dan antioksidan tidak aktif IC50 > 500 mg/L. Berdasarkan hal tersebut, antioksidan
optimasi metode ekstraksi fenol dari rimpang jahe emprit (zingiber officinalle var. rubrum) menggunakan pelarut etanol dengan berbagai konsentrasi dan lama waktu maserasi, yang menunjukkan bahwa IC 50 pada ekstrak jahe emprit dari ekstrak kunyit dengan pelarut etanol termasuk antioksidan aktif. Semakin kecil nilai IC 50 maka semakin tinggi aktivitas antioksidan suatu bahan (Molyneux, 2004) dan senyawa bioaktif yang terdapat pada ekstrak kunyit dengan pelarut etanol lebih berperan aktif sebagai antioksidan dalam menghambat radikal bebas.
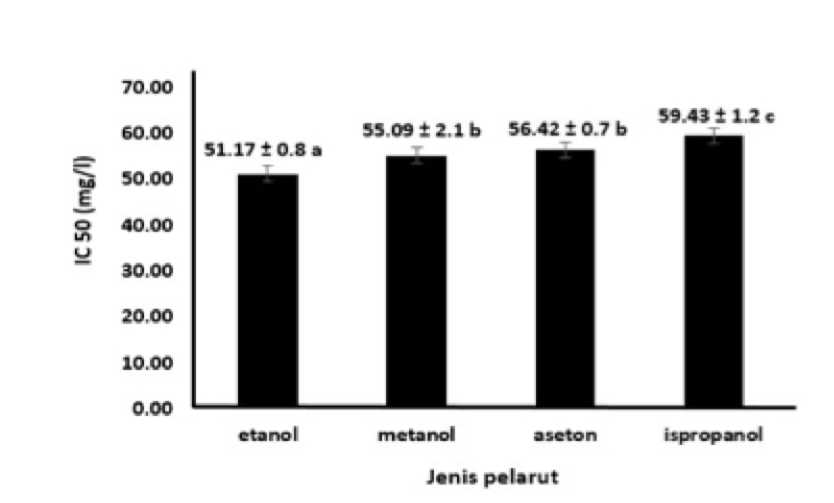
Keterangan: Notasi yang sama menunjukkan perlakuan tidak berbeda nyata (P>0,05)
Gambar 5. Aktivitas antioksidan dengan beberapa jenis pelarut
KESIMPULAN DAN SARAN Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka dapat disimpulkan beberapa hal sebagai berikut:
-
1. Perlakuan jenis pelarut berpengaruh nyata terhadap kapasitas antioksidan, dan berpengaruh sangat nyata terhadap kurkumin, total fenol, serta aktivitas antioksidan ekstrak kunyit, namun tidak berpengaruh nyata terhadap rendemen.
-
2. Jenis pelarut terbaik untuk ekstraksi kunyitadalah etanol yang menghasilkan rendemen sebesar 14,90%, kurkumin sebesar 1,74%, total fenol sebesar 51,56mg GAE/100 g sampel, kapasitas antioksidan sebesar 5,49mg GAEAC/100g sampel, dan aktivitas antioksidan (IC 50) sebesar 51,17 mg/L.
Saran
-
1. Perlu dilakukan penelitian lebih lanjut mengenai pengaruh metode dan konsentrasi pelarut yang tepat pada ekstrak kunyit.
-
2. Perlu dilakukan ekstraksi lebih lanjut terhadap perbandingan simplisia dengan pelarut yang digunakan.
DAFTAR PUSTAKA
Aan. 2004. Pengaruh waktu, suhu, dan nisbah bahan baku-pelarut pada ekstraksi kurkumin dari temulawak dengan pelarut aseton. Skripsi.Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor
Aini, S. 2013.Ekstraksi Kurkumin dari Rimpang Temulawak dengan Metode Maserasi.Skripsi. Departemen Teknologi Industri Pertanian IPB : Bogor.
Anggitha, I. 2012. Performa Flokulasi
Bioflokulan DYT pada Beragam
Keasaman dan Kekuatan Ion terhadap Turbiditas Larutan Kaolin. Universitas Pendidikan Indonesia, Jakarta.
Anggoro, D., R.S. Rezki.danM.Z. Siswarni. 2015. Ekstraksi Multi Tahap Kurkumin dari Temulawak (Curcuma xanthorriza Roxb.) Menggunakan Pelarut Etanol.Departemen Teknik Kimia, FakultasTeknik, Universitas Sumatera Utara, Medan.
Harborne, J. B. 1987. Metode Fitokimia. Edisi II. Penerjemah. Padmawinata K, Soediro I,. Bandung. Terjemahan dari: Phytochemical Methods.
Hargono, D. 1986.Obat Tradisional dalam Zaman Teknologi. Majalah Kesehatan MasyarakatNo. 56, Hal: 3-5.
Harini, B.W., R. Dwiastuti. danL. C. Wijayanti. 2012. Aplikasi Metode Spektrofotometri Visibel Untuk Mengukur Kadar Kurkuminoid Pada Rimpang Kunyit (Curcuma domestica). Prosiding Seminar Nasional Aplikasi Sains & Teknologi (SNAST) Periode III. Universitas Sanata Dharma Yogyakarta.
Jaruga. 1998. Kunyit (Curcuma longa Linn.). http://ccrcfarmasiugm.wordpress.com.
Diakses tanggal 25 April 2016.
Jayaprakasha, G. K., J. M. Rao. danK. K.Sakariah. 2005. Chemistryand biological activities of C. longa. Trends in Food Science and Technology. 16:533-548.
Jayaprakasha, G. K., J. M. Rao. danK. K. Sakariah. 2006. Antioxidantactivities of curcumin, demethoxycurcumin and
bisdemethoxycurcumin. Food Chemistry. 98:720-724.
Jayanudin, A.Z., F.Lestari.dan Nurbayanti. 2014. Pengaruh Suhu dan Rasio Pelarut ekstrasi Terhadap Rendemen dan Viskositas Natrium Alginat dari Rumput Laut Cokelat (Sasrgassum sp.).Jurnal Integasi Proses. 5(1):51-56
Jun, M.H., X, Fong.,C. S.Wan.andC. T. Yang. 2001. Camparison of Antioxidant Activities of Isoflavones from Kudzu Root ( Puerarua labata 0) Journal Food ScienceInstitute of Technologist. 6(8):2117-2122.
Kusriani, R. H.danS. Az Zahra.2015. Skrining Fitokimia dan Penetapan Kadar Senyawa Fenolik Total Ekstrak Rimpang Lengkuas Merah dan Rimpang Lengkuas Putih (alpinia galangal L.).Prosiding SNaPP Kesehatan, Pisnn 2477-2364, Eisnn 24772356.
Lenny, S. 2006. Senyawa Flavonoida, Fenil Propanoida dan Alkaloida. Makalah Seminar. Fakultas Matematika dan Ilmu Alam. Universitas Sumatera Utara.
Lestari, T., R. Ira.danM. Siti. 2014. Pengaruh Metode dan Variasi Pelarut Ekstraksi terhadap Kadar Polifenolat Bunga Kecombrang (Etlingera elatior(Jack)
R.M.Sm).Jurnal Kesehatan Bakti Tunas Husada Vol 12, No. 1.
Molyneux P. 2004.The Use of The Stable Free Radikal Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Journal Science of Technology 26(2):211-219.
Noerono S. 1994. Buku Teknologi Farmasi. UGM Press. Yogya.
Pourmorad, F., S. J. Hossenimehr.andN. Shahabimajd. 2006. Antioxidant activity, phenol and flavonoid contents of some selected Iranian medicial plants. African Journal of Biotechnology. 5(11):1142-1145.
Rahayu H.D.I. 2010. Pengaruh Pelarut Yang Digunakan Terhadap Optimasi Ekstraksi Kurkumin Pada Kunyit (Curcuma
domestica Vahl.). Skripsi.Universitas
Muhammadiyah Surakarta.
Ramdja, A. F., R. M.ArmyAulia. danM. Pradita. 2009. Ekstraksi Kurkumin Dari Temulawak Dengan Menggunakan Etanol. Jurnal Teknik Kimia, no. 3, vol. 16. Universitas Sriwijaya.
Ria, E. B. 1989. Pengaruh Jumlah Pelarut, Lama Ekstraksi, dan Ukuran Bahan Terhadap Rendemen dan Mutu Oleoresin Temulawak (Curcuma xanthorrhiza Roxb). Skripsi. IPB, Bogor.
Sompong, R.,S. Siebenhandl-Ehn., G. L. Martin. andE. Berghofer. 2011. Physicochemical and Antioxidative Properties of Red and Black Rose Varieties from Thailand, China, and srilanka. Journal Food Chem. 14(2):135-148.
Steel, R.G.D and J. H. Torrie.1993. Prinsip dan prosedur statistika Suatu Pendekatan Biometrik. Penerjemah B. Sumantri. PT. Gamedia Pustaka, Jakarta.
Sudarmadji, S., B. Haryono. dan Suharji. 1997. Prosedur Analisis untuk Bahan Makanan dan Pertanian. Penerbit Liberti, Yogyakarta.
Suryani, Ch L. 2012. Optimasi Metode Ekstraksi Fenol dari Rimpang Jahe Emprit (Zingiber officinalle var. rubrum). Jurnal Agisains vol.3 no.4, (ISSN : 2086-7719 63). Progam Studi Teknologi Hasil Pertanian Fakultas Agoindustri, Universitas Mercu Buana : Yogyakarta.
Tonnesen. H.H. and J. Karlsen. 1985. Studies on Curcumin and Curcumin oids:V. Alkaline Degadation of Curcumin, Lebenum Uniers Forch, 180: 132-134.
Yun, L. 2001. Free Radical Scavenging Properties of Conjugated Linoic Acids.Journal of Agricultural and Food Chemistry. 49: 34523456.
70
Discussion and feedback