Stabilitas Antosianin Serbuk Terung Belanda (Solanum Betaceum Cav.) Terkopigmentasi dan Terenkapsulasi Dengan Perubahan pH
on
Itepa: Jurnal Ilmu dan Teknologi Pangan, ISSN: 2527-8010
NLK Ayu Gayatri P. Andini dkk / Itepa 12 (2) 2023 347-360
Stabilitas Antosianin Serbuk Terung Belanda Solanum Betaceum Cav.) Terkopigmentasi dan Terenkapsulasi Dengan Perubahan pH
Anthocyanin Stability of Tamarillo (Solanum Betaceum Cav.) Powder Copigmented and Encapsulated with Changes in pH
Ni Luh Ketut Ayu Gayatri Pradnya Andini1, Gusti Ayu Kadek Diah Puspawati1, Komang Ayu Nocianitri1
Program Studi Teknologi Pangan, Fakultas Teknologi Pertanian, Universitas Udayana Kampus Bukit Jimabaran, Badung-Bali
* Penulis korepondensi: Gusti Ayu Kadek Diah Puspawati. Email: diahpuspawati@unud.ac.id
Abstract
Tamarillo (Solanum betaceum Cav.) contain bioactive components such as anthocyanin. Anthocyanin in tamarillo act as a source of red pigment. This research aimed to determine the effect of pH on the anthocyanin stability of copigmented and encapsulated tamarillo powder and to determine the right pH to produce the best anthocyanin stability of copigmanted and encapsulated tamarillo powder. This research used a Complete Randomized Design with pH treatment consisted of five levels; pH 3, pH 4, pH 5, pH 6, pH7. Each treatment was repeated three times so obtain 18 experimental units. The data obtained were analyzed using analysis of variance and if the treatment had an significant effect on the test parameters, then continued with the Duncan Multiple Range Test (DMRT). The results showed that pH had a significant effect on anthocyanin color degradation, anthocyanin content, absorbance retention, L* values, a*, b*, hue and chroma. The best best treatment to maintain anthocyanin stability of copigmented and encapsulated tamarillo powder is pH 3 with the anthocyanin color with result degradation of 8.48%, anthocyanin content of 0.63 mg/g, absorbance retention of 96.51%, L* value of 40.03, value of a* 51.07, value of b* 56.30, hue of 47.79° and chroma of 76.01. Tamarillo powder copigmented and encapsulated can be used as a functional food ingredient in food products with an acidic pH.
Keywords: anthocyanin stability, tamarillo powder, pH, ingredient fungsional food
PENDAHULUAN
Terung belanda (Solanum betaceum Cav.) disebut juga tamarillo atau tomato tree merupakan buah yang memiliki kombinasi rasa asam dan manis. Terung belanda mengandung provitamin A dan vitamin C serta mineral penting seperti potasium, fosfor dan magnesium serta komponen bioaktif seperti antosianin dan karotenoid yang dapat menjaga sekaligus memelihara kesehatan tubuh (Sari et al., 2018). Komponen bioaktif seperti antosianin pada
terung belanda berperan sebagai sumber pigmen merah.
Nugaheni (2012) melaporkan penggunaan pigmen antosianin memiliki kelemahan seperti pemakainnya yang kurang praktis dan warna yang kurang stabil terhadap perubahan pH, oksidasi, cahaya dan suhu selama pengolahan pangan. Kelemahan tersebut menjadi faktor penyebab pigmen antosianin kurang dapat bersaing dengan pewarna sintetik, meskipun pigmen antosianin memiliki keunggulan
sebagai pangan fungsional dan berpengaruh positif bagi kesehatan. Puspawati et al., (2019) melaporkan bubuk pewarna antosianin dari terung belanda pada penerimaan keseluruhan, lebih disukai dari pewarna merah yang beredar dipasaran tetapi, stabilitasnya masih belum bisa menyamai pewarna sintetik.
Salah satu cara untuk meningkatkan stabilitas dan kepraktisan pigmen antosianin dari terung belanda adalah kombinasi teknik kopigmentasi dan enkapsulasi pada pembuatan serbuk pewarna alami terung belanda. Kopigmentasi adalah teknik meningkatkan stabilitas warna dengan mereaksikan antosianin dengan senyawa lain sebagai kopigmen (Talcott et al., 2003). Sementara, enkapsulasi adalah teknik penjerat bahan inti dalam bahan penyalut tertentu untuk melindungi komponen bahan inti atau bahan aktif sehingga mampu mempertahankan stabilitas warna (Palupi et al., 2014).
Pembuatan serbuk pewarna alami dengan kombinasi metode kopigmentasi dan enkapsulasi telah dilakukan oleh Puspawati et al., (2021) dengan perlakuan terbaik yaitu serbuk yang diekstrak dengan metode sonikasi dan dikopigmentasikan dengan asam galat serta dienkapsulasi dengan maltodektrin 5%. Asam galat menjadi kopigmen terbaik karena mampu membentuk senyawa kompleks dengan antosianin. Pembentukan senyawa kompleks ini menyebabkan terjadinya keseimbangan
elektron sehingga terjadi kestabilan. Selain itu, asam galat juga berperan dalam menurunkan pH sehingga pelarut dalam suasana asam sehingga antosianin yang dikopigmentasikan menjadi lebih stabil. Maltodekstrin sebagai enkapsulan memiliki kemampuan membentuk lapisan disekitar pigmen warna sehingga dapat melindungi warna dari kerusakan. Ekstrak yang dikopigmentasi dengan asam galat dan dienkapsulasi dengan maltodekstrin 5% menghasilkan total antosianin dan intensitas warna terbaik dibandingkan dengan asam ferulat, ekstrak kayu secang dan ekstrak kulit buah naga merah (Puspawati et al., 2021). Raharjo et al., (2019) melaporkan peningkatan stabilitas antosianian pada beras hitam pada proses pembuatannya juga menggunakan teknik kopigmentasi yaitu dengan asam fenolik dan dienkapsulasi dengan maltodekstrin. Pada penelitian tersebut juga diamati stabilitas antosianinnya dengan perubahan pH.
Derajat keasaman (pH) sangat mempengaruhi stabilitas antosianin dimana, pada suasana asam antosianin berbentuk garam flavilium yang lebih stabil dan semakin tinggi nilai pH maka warna akan memudar dan berubah menjadi biru. Fathinatullabibah et al., (2014) melaporkan stabilitas antosianin ekstrak daun jati paling baik pada pH 3, dimana semakin tinggi pH maka stabilitas semakin menurun. Fedri et al, (2019) melaporkan ekstrak cair kulit buah terong belanda merah stabil pada pengaruh
pH yaitu pH 1 dan 3 dengan menghasilkan warna merah yang stabil dan degradasi warna paling rendah. Loypimai et al., (2015) melaporkan degradasi warna visual dan kandungan antosianin bubuk pewarna bekatul hitam (BCP) sangat dipengaruhi oleh pH dan stabilitas terbaik pada pH 2,0. Penelitian ini bertujuan untuk menentukan pengaruh pH terhadap stabilitas antosianin serbuk terung belanda terkopigmentasi dan terekapsulasi dan menentukan pH yang tepat untuk stabilitas antosianin serbuk terung belanda terkopigmentasi dan terenkapsulasi terbaik.
METODE
Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah terung belanda varietas merah (Solanum Betaceum Cav.) dengan karakteristik matang optimal (kulit berwarna merah merata) dari petani di Bedugul, Kabupaten Tabanan, Provinsi Bali, aquades, asam sitrat (Gajah), asam galat diperoleh dari Sigma Aldrich St. Lous, MO, USA, tween 80, Carboxyl Methyl Cellulose (CMC), maltodekstrin, larutan buffer sitrat (pH 3, pH 4, pH 5, pH 6), buffer phosphate (pH 7) Merck). Bahan kimia untuk analisis meliputi; larutan buffer kalium klorida (pH 1), larutan buffer natrium asetat (pH 4,5) Merck), HCL, metanol dan etanol dibeli di Toko Chemical Pratama, Yogyakarta.
Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah pisau, timbangan
digital, timbangan analitik (Shimadzu ATY224), blender Philips), magnetic stirrer DLAB MS-S), mixer Philips), kertas baking, aluminium foil, gelas ukur, kain saring, kertas saring whatman No. 42, kertas label, loyang, oven (ESCO Isotherm), baskom, pH meter (TOA HM 605), Color reader CR-10 Konica Minolta Sensing), corong kaca, pipet mikro Socorex), tip mikropipet, gelas beaker Pyrex), labu ukur 5ml Pyrex), pipet tetes, buret, vortex Maxi Mix II Type 367000), tissue Nice), tabung reaksi Pyrex), rak tabung reaksi Pyrex), spektrofotometer UV-Vis Genesys 10S UV – Vis), centrifuge Oregon) dan digital ultrasonic cleaner Digital Pro+).
Rancangan Percobaan
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL) dengan perlakuan pH terhadap stabilitas serbuk terung belanda terkopigmentasi dan terenkapsulasi yang terdiri dari lima taraf, meliputi: P1 = pH 3; P2 = pH 4; P3 = pH 5; P4 = pH 6; P5 = pH 7. Masing-masing perlakuan dilakukan pengulangan sebanyak tiga kali, sehingga diperoleh total 15 unit percobaan.
Pelaksanaan Penelitian
Pelaksanaan penelitian dilakukan dengan beberapa langkah, meliputi pembuatan ekstrak terung belanda, kopigmentasi ekstrak terung belanda, enkapsulasi dan stabilisasi pigmen antosinain dengan pengaruh pH.
Pembuatan Ekstrak Terung Belanda
Ekstraksi buah terung belanda mengacu pada Puspawati et al., (2018). Pembuatan ekstrak buah terung belanda diawali dengan sortasi kemudian dicuci dengan air mengalir. Selanjutnya dibelah dua, dihilangkan kulitnya dan dihaluskan dengan blender (tanpa penambahan air) sehingga didapatkan bubur terung belanda. Bubur terung belanda ditambahkan pelarut aquades yang mengandung asam sitrat tiga persen dengan perbandingan bahan dan pelarut 1:4. Selanjutnya diekstraksi sonikasi pada suhu 27-30°C selama 20 menit pada panjang gelombang 37kHz. Kemudian disaring dengan kain saring dan disetrifuse dalam 1500 rpm selama 15 menit dan diambil ekstrak jernih.
Kopigmentasi Ekstrak Terung Belanda
Metode kopigmentasi mengacu pada Jamei dan Babaloo, (2017) dan Puspawati et al., (2021). Bahan kopigmen yaitu asam galat dipersiapkan dengan konsentrasi 960 mg/L, selanjutnya dicampur dengan ekstrak terung belanda dengan perbandingan 1:2 kemudian dihomogenisasi dengan magnetic stirrer selama 15 menit.
Enkapsulasi
Metode enkapsulasi mengacu pada Puspawati et al., (2021) yang dimodifikasi. Ekstrak terung belanda yang telah terkopigmentasitasi sebanyak 75 ml dimasukkan ke dalam gelas ukur kemudian ditambahkan tween 80 sebanyak satu persen kemudian
dihomogenisasi dengan mixer, selanjutnya ditambahkan maltodekstrin sebanyak lima persen kemudian dihomogenisasi dan ditambahkan CMC sebanyak 0,3 persen kemudian ditambahkan ekstrak terung belanda sampai volume total 100ml dihomogenisasi dengan mixer selama ±15 menit sampai terbentuk busa yang kompak. Langkah selanjutnya dimasukkan dalam loyang yang sudah dialasi dengan baking paper dengan ketebalan 5 mm kemudian dikeringkan dalam oven pada suhu 50°C selama 4 jam. Setelah kering dihaluskan dengan blender (kecepatan: 3) dan diayak dengan ayakan 40 mesh untuk mendapatkan serbuk terung belanda.
Stabilisasi Pigmen Antosianin dengan Pengaruh pH
Stabilisasi pigmen antosianin dengan pengaruh pH mengacu pada Loypimai et al., (2015) yang dimodifikasi. Sebanyak 3 g serbuk pewarna alami terung belanda dilarutkan dalam 15 ml buffer pH sesuai perlakuan (3, 4, 5, 6, 7) di homogenisasi dengan vortex mixer selama 10 detik kemudian disentrifugasi (3000 rpm selama 30 menit) dan disaring.
Parameter Uji
Parameter uji pada penelitian yaitu degradasi warna antosianin (Sari, 2011 dalam Fendri et al., 2020), total antosianin (Giusti dan Wrolstad, 2001), retensi
absorbansi (Raharjo et al., 2019), pengukuran nilai L* a* b* (Francis, 2002), hue dan chroma (Hutching, 1999).
Analisis Data
Data dianalisis secara statistik menggunakan uji sidik ragam dan apabila perlakuan berpengaruh terhadap parameter yang diamati, maka dilanjutkan dengan uji beda nyata Duncan Multiple Range Test (DMRT) dengan tingkat signifikan 5%
(p<0,05) (Gomez et al., 1995) menggunakan program Statistical Package for the Social Sciens 25 (SPSS 25)
HASIL DAN PEMBAHASAN
Rata-rata degradasi warna antosianin, total antosianin dan retensi absorbansi dapat dilihat pada Tabel 1, sedangkan nilai L*, a*, b*, hue dan chroma dilihat pada Tabel 2.
Tabel 1. Rata-Rata Degradasi Warna Antosinin, Total Antosianin, Retensi Absorbansi Serbuk Terung Belanda Terkopigmentasi dan Terenkapsulasi terhadap Perlakuan pH
|
Perlakuan |
Degradasi Warna Antosianin (%) |
Total Antosianin (mg/g) |
Retensi Absorbansi (%) |
|
P1 (pH 3) |
8,48±0,18e |
0,63±0,01a |
96,51±0,13a |
|
P2 (pH 4) |
18,36±0,15d |
0,51±0,01b |
94,02±0,04b |
|
P3 (pH 5) |
22,10±0,18c |
0,46±0,01c |
93,56±0,13c |
|
P4 (pH 6) |
30,16±0,21b |
0,43±0,01d |
91,58±0,40d |
|
P5 (pH 7) |
43,45±0,10a |
0,40±0,01e |
89,27±0,24e |
Keterangan: Nilai rata-rata pada yang diikuti oleh huruf yang berbeda pada kolom yang sama menunjukkan perlakuan berpengaruh nyata pada taraf signifikansi 5%.
Tabel 2. Rata-rata Nilai L*, a*, b*, Hue dan Chroma Serbuk Terung Belanda Terkopigmentasi dan Terenkapsulasi terhadap Perlakuan pH
|
Perlakuan Nilai L* |
Nilai a* Nilai b* Nilai hue (°) Nilai C* |
|
P1 (pH 3) 40,03±0,15e P2 (pH 4) 42,10±0,10d P3 (pH 5) 43,97±0,15c P4 (pH 6) 45,87±0,15b P5 (pH 7) 48,07±0,15a |
51,07±0,15a 56,30±0,10e 47,79±0,08e 76,01±0,14a 48,10±0,10b 57,43±0,15d 50,05±0,02d 74,89±0,08b 44,00±0,10c 59,33±0,25c 53,44±0,15c 73,87±0,19c 39,03±0,15d 60,17±0,15b 57,03±0,13b 71,72±0,14d 36,97±0,15e 61,10±0,10a 58,83±0,10a 71,41±0,13e |
Keterangan: Nilai rata-rata pada yang diikuti oleh huruf yang berbeda pada kolom yang sama menunjukkan perlakuan berpengaruh nyata pada taraf signifikansi 5%.
Degradasi Warna Antosianin
Degradasi warna antosianin adalah laju kerusakan warna antosianin yang ditunjukkan dalam persen dari hasil pengurangan absorbansi sampel tanpa perlakuan dengan absorbansi sampel dengan perlakuan kemudian dibandingkan dengan absorbansi sampel tanpa perlakuan (Sari,
2011). Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap degradasi warna antosianin serbuk terung belanda terkopigmentasi dan terenkapsulasi. Tabel 1 menunjukkan, degradasi warna antosianin terendah diperoleh pada perlakuan pH 3 yaitu sebesar 8,48% sedangkan degradasi warna tertinggi
diperoleh pada perakuan pH 7 yaitu sebesar 43,45%. Semakin tinggi nilai pH semakin tinggi juga degradasi warna antosianin dan warna antosianin semakin pudar. Hal ini karena terjadinya perbedaan struktur antosianin dimana pada peningkatan pH akan membuat antosianin dalam bentuk yang tidak stabil atau semakin tinggi kerusakan pigmennya.
Pada pH 3 antosianin berwarna merah (kation flavilium) dan semakin tinggi nilai pH degradasi warna antosianin semakin besar yang ditandai dengan warna merah yang semakin pudar dan cenderung berwarna kekuningan. Hal ini karena antosianin mengalami perubahan struktur dari kation flavilium yang menghasilkan warna merah menjadi bentuk pseudobasa hemiketal karbinol yang berwarna kuning (Marco et al., 2011, Burton-Freeman et al., 2016). Fedri et al, (2019) yang menyatakan degradasi warna antosianin ekstrak cair kulit buah terong belanda merah pada pH 3 (51,73%) dan meningkat seiring dengan peningkatan nilai pH. Pernyataan tersebut juga sesuai dengan penelitian (Farida, 2015) melaporkan bahwa pada kisaran pH 1-3 antosianin berada pada bentuk flavilium berwarna merah yang paling stabil, ketika nilai pH naik maka akan menyebabkan hilangnya proton dengan lebih cepat sehingga terjadi deprotonisasi dan hidrasi kation flavilium sehingga terjadi perubahan struktur antosianin dan mengalami
transformasi stabilitas pigmen (Bridgers et al., 2010).
Total Antosianin
Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap total antosianin serbuk terung belanda terkopigmentasi dan terenkapsulasi. Tabel 1 menunjukkan rata-rata tertinggi diperoleh pada perlakuan pH 3 yaitu sebesar 0,63mg/g, sedangkan total antosianin terendah diperoleh pada perakuan pH 7 yaitu sebesar 0,40mg/g. Semakin tinggi nilai pH, semakin rendah total antosianin. Hal ini karena peningkatan nilai pH menyebabkan kerusakan pada antosianin dimana kation flavylium akan kehilangan proton basa kuinodal yang merupakan bentuk tidak stabil sehingga dengan cepat dapat menjadi bentuk antosianin yang tidak berwarna.
Pada pH asam antosianin berbentuk kation flavilium yang menghasilkan warna merah yang lebih stabil sedangkan pada pH yang semakin meningkat antosianin akan menjadi bentuk pseudobasa hemiketal karbinol yang berwarna kuning kemudian menjadi bentuk kuinodal dan kalkon yang tidak berwarna (Marco et al., 2011) (BurtonFreeman et al., 2016) (Parisa et al., 2007). Pada pH yang semakin meningkat antosianin akan mengalami hidrolisis menjadi kalkon dan terhidrolisis sempurna, inilah yang menyebabkan antosianin akan menghasilkan warna merah yang semakin pudar seiring dengan peningkatan pH (Hanum et al., 2000). Hal ini sejalan dengan penelitian
Fathinatullabibah et al (2014) yang melaporkan bahwa antosianin daun jati pada berbagai perlakuan pH mengalami penurunan seiring dengan meningkatnya pH yaitu 284,72mg/l pada pH 2, 273,03mg/l pada pH 3 dan terus menurun hingga 230,45mg/l pada pH 7. Permatasari et al (2010) melaporkan total antosianin bubuk pewarna alami bayam merah pada pH 3 adalah 0,581 mg/g. Laleh et al (2006) juga melaporkan meningkatnya pH menyebabkan kerusakan pada antosianin dari buah berberies. Cevallos-Casals (2004) melaporkan bahwa antosianin dari ekstrak ubu jalar merah, jagung ungu dan wortel ungu komersial lebih stabil pada pH 3 dan stabilitasnya menurun seiring dengan penigkatan pH.
Retensi Absorbansi
Retensi absorbansi adalah jumlah zat atau bahan yang dapat tertahan setelah mengalami suatu proses tertentu yang dinyatakan dalam persen yang dihitung berdasarkan perbandingan absorbansi dari sampel (Meutia et al., 2019) dalam penelitian ini perbandingan hari ke-0 dengan hari ke-30. Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap retensi absorbansi serbuk terung belanda terkopigmentasi dan terenkapsulasi. Tabel 1 menunjukkan rata-rata retensi absorbansi dengan penyimpanan selama 30 hari tertinggi diperoleh pada perlakuan pH 3 yaitu sebesar 96,51%, sedangkan retensi absorbansi terendah diperoleh pada
perakuan pH 7 yaitu sebesar 89,27%. Semakin tinggi nilai pH semakin rendah retensi absorbansi. Hal ini karena adanya perubahan struktur antosianin seiring dengan peningkatan nilai pH dari kation falvilium hingga kalkon yang sudah akan menurunkan nilai absorbansi pada hari ke-0 dan akan semakin menurun absorbansinya selama penyimpanan sehingga terjadinya penurunana retensi absorbansi.
Antosianin dalam bentuk kation flavilium (berwarna merah) yang sangat reaktif ini mudah terhidrolisis pada nilai pH yang semakin tinggi sehingga membentuk basa karbinol, hemiasetal, pseudobosa dan kalkon yang tidak berwarna, sehingga retensi absorbansi dapat mengalami penurunan selama penyimpanan (Castaneda-Ovando et al., 2009) (Brouillard et al., 1982). Penurunan stabilitas antosianin ditunjukkan dengan semakin kecilnya persen retensi absorbansi (Raharjo et al., 2019). Hal ini sejalan dengan penelitian Wahyuni et al (2017) yang melaporkan bahwa retensi absorbansi ekstrak kulit terung belanda yang disimpan selama 40 hari pada kondisi pH 3,5 adalah 63,56% dan menurun seiring dengan peningkatan nilai pH. Raharjo et al (2019) melaporkan bahwa serbuk beras hitam yang telah terkopigmentasitasi pada pH 1 dan 3 kemudian dienkapsulasi dan diuji retensi absorbansinya selama 4 minggu tanpa terpapar cahaya dan pada suhu 5°C memiliki rentang rentensi absorbansi 90,1- 93,8%.
Nilai L* (Kecerahan)
Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap nilai L* serbuk terung belanda terkopigmentasi dan terenkapsulasi. Tabel 5 menunjukkan, nilai L* terendah diperoleh pada perlakuan pH 3 yaitu sebesar 40,03, sedangkan nilai L* tertinggi diperoleh pada perakuan pH 7 yaitu sebesar 48,07. Semakin tinggi nilai pH semakin tinggi juga nilai L*. Hal ini menandakan warna yang dihasilkan semakin terang (pudar) seiring dengan peningkatan nilai pH sedangkan akan semakin gelap (pekat) pada nilaia pH yang lebih rendah.
Peningkatan nilai L* berkaitan dengan total antosianin pada bahan, dimana nilai L* yang tinggi menunjukkan total antosianin yang rendah begitu pula sebaliknya (Montes et al.,2005). Pada penelitian Montes et al (2005) ekstrak buah Jaboticaba menggunakan etanol dengan HCL dan pH 2-4 memiliki nilai L* yang rendah dengan total antosianin tertinggi. Hal ini juga sejalan dengan penelitian Vieira et al., (2018) kubis ungu yang diekstrak dengan pelarut asam memiliki nilai L* terendah yang menunjukkan warna ekstrak lebih gelap (lebih pekat) dengan total antosianin tertinggi. Menurut Sari et al., (2005) semakin meningkatnya nilai pH maka antosianin akan terdegradasi menjadi senyawa kuinonoidal dan kalkon yang menyebabkan tidak berwarna sehingga nilai L* (kecerahannya) juga akan semakin
tinggi. Hal ini sejalan dengan penelitian Fathinatullabibah et al (2014) yang menyatakan bahwa nilai L* ekstrak pigmen antosianin daun jati pada perlakuan pH 2, pH 3, pH 5 dan pH 7 mengalami peningkatan seiring dengan peningkatan nilai pH dengan nilai L* terendah pada pH 2 yaitu 2,58.
Nilai a* (Kemerahan)
Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap nilai a* serbuk terung belanda terkopigmentasi dan terenkapsulasi. Tabel 5 menunjukkan, nilai a* tertinggi diperoleh pada perlakuan pH 3 yaitu sebesar 51,07, sedangkan nilai a* terendah diperoleh pada perakuan pH 7 yaitu sebesar 36,97. Nilai a* pada penelitian ini bernilai positif yang berkisar antara 36,97-51,07 yang artinya memiliki derajat warna merah. Semakin tinggi nilai pH semakin rendah juga nilai a*, yang menandakan warna merah yang dihasilkan semakin sedikit.
Penururnan nilai a* karena terjadinya perubahan bentuk antosianin pada pH asam (1-3) yang masih stabil yaitu dalam bentuk kation flavilium (warna merah) akan terdegrasasi seiring dengan peningkatan nilai pH menjadi bentuk pseudobasa hemiketal karbinol yang berwarna kuning (Marco et al., 2011) (Burton-Freeman et al., 2016). Hal ini sejalan dengan penelitian
Fathinatullabibah et al (2014) yang menyatakan bahwa Nilai a* ekstrak pigmen antosianin daun jati pada perlakuan pH 2, pH 3, pH 5 dan pH 7 mengalami penurunan seiring dengan peningkatan nilai pH dengan nilai a* tertinggi pada pH 3 yaitu 7,29 dimana semakin meningkatnya nilai pH maka nilai a* semakin rendah dan nilai b* semakin tinggi. Nilai a* juga dapat berhubungan dengan total antosianin pada bahan, dimana bahan dengan total antosianin lebih tinggi juga memiliki nilai a* yang lebih tinggi. Hal ini dibuktikan dengan penelitian Vieira (2018) dimana ekstrak buah dengan nilai a* yang lebih tinggi juga memiliki total antosianin yang lebih tinggi.
Nilai b* (Kekuningan)
Hasil sidik ragam menunjukkan bahwa pH berpengaruh nyata (P<0,05) terhadap nilai b* serbuk terung belanda terkopigmentasi dan terenkapsul. Tabel 5 menunjukkan, nilai b* tertinggi diperoleh pada perlakuan pH 7 yaitu sebesar 61,10, sedangkan nilai b* terendah diperoleh pada perakuan pH 3 yaitu sebesar 56,30. Nilai b* pada penelitian ini berkisar antara 56,3061,10 yang artinya memiliki derajat warna kuning. Semakin tinggi nilai pH semakin tinggi juga nilai b*. Hal ini menandakan kecenderungan lebih besarnya dihasilkan warna kuning seiring dengan peningkatan nilai pH akibat adanya degradasi warna
antosianin yang mengubah bentuk struturnya.
Hal ini karena terjadinya degradasi warna antosianin dari antosianin dimana bentuk kation flavilium yang menghasilkan warna merah akan berubah menjadi bentuk pseudobasa hemiketal karbinol yang berwarna kuning seiring dengan peningkatan nilai pH (Marco et al., 2011) (Burton-Freeman et al., 2016). Hal ini sejalan dengan penelitian Fathinatullabibah et al (2014) yang menyatakan bahwa Nilai b* ekstrak pigmen antosianin daun jati pada perlakuan pH 2, pH 3, pH 5 dan pH 7 mengalami peningkatan seiring dengan peningkatan nilai pH dengan nilai b* tertinggi pada pH 7 yaitu -6,66 dimana semakin meningkatnya nilai pH maka nilai b* semakin tinggi dan nilai a* semakin rendah.
Hue
Hue adalah kisaran derajat yang menunjukkan karakteristik atau jenis warna sampel pada diagram warna (Agusandi et al., 2013). Hue digunakan untuk mengetahui karakteristik warna yang dihasilkan yang ditunjukkan dari kisaran derajat atau sudut pada diagram warna (Winarno, 2004). Tabel 2 menunjukkan, hue serbuk terung belanda terkopigmentasi dan terenkapsulasi yang mendapat perlakuan pH berkisar antara 47,79°-58,83°. Nilai hue berkaitan dengan nilai a dan b, pada penelitian ini semua perlakuan menghasilkan nilai a* dan nilai b* positif
sehingga warna pada setiap perlakuan terletak pada kuadran I. Peningkatan nilai b* dan penurunana nilai a* akibat peningkatan nilai pH menghasilkan kisaran hue yang semakin tinggi.
Kisaran hue pada perlakuan pH 3-5 adalah 47,79°-53,44° yang tergolong dalam warna merah (R) sementara perlakuan pH 6 dan pH 7 dengan kisaran hue 57,03°-58,83° tergolong dalam warna kuning-merah (YR) (Hutching, 1999). Hue berhubungan dengan besarnya nilai a* dan b* dan kisaran warnanya dapat diketahui dengan tabel deskripsi warna (Purnomo et al., 2014). Hal ini sejalan dengan penelitian Permatasari et al (2020) pada bubuk pewarna alami buah buni nilai a* 11,64, b* 7,13 dan derajat hue 29,43° (merah) dan penelitian Purnomo et al (2014) derajat hue mikroenkapsuln pewarna alami daun jati 32,855° (merah) (b*14,610 dan a* 22,640), 41,287° (merah) (b*17,405 dan a* 19,803) dan 43,965° (merah) (17,655 dan a*18,275).
Kisaran hue yang tergolong dalam warna merah (R) dan kuning-merah (YR) pada penelitian ini karena pada nilai pH yang rendah (asam) antosianin stabil dalam bentuk kation flavilium yang menghasilkan warna merah dan pada nilai pH yang lebih tinggi maka antosianin akan terdegrasasi menjadi bentuk pseudobasa hemiketal karbinol yang berwarna kuning (Marco et al., 2011) (Burton-Freeman et al., 2016). Hal ini sejalan dengan penelitian Hurtado et al (2009) yang menyatakan antosianin murni
dari buah terung belanda pada pH asam akan menunjukkan warna merah pada kisaran derajat hue 10°-30° dan secara bertahap akan berubah menjadi warna kekuningan-kuning seiring dengan meningkatnya nilai pH. Sejalan juga dengan penelitian yang dilakukan Fathinatullabibah et al (2014) yang mendapatkan hasil bahwa Nilai hue ekstrak pigmen antosianin daun jati mengalami peningkatan seiring dengan peningkatan nilai pH.
Selain itu, kisaran hue berkolerasi negatif dengan kandungan antosianin pada bahan. Hue pada bahan semakin kecil ketika total antosianin pada bahan tersebut semakin tinggi (Vieira et al., 2018). Hal ini sejalan dengan penelitian Widyasanti et al (2018) yang melaporkan bahwa ekstrak kulit buah naga merah dengan hue terendah yaitu 27,22° memiliki rata-rata total antosianin tertinggi yaitu 29,64 mg/l.
Nilai C* (Chroma)
Nilai chroma (C*) menunjukkan intensitas warna yang dihasilkan (Winarno, 1997) dalam hal ini berkaitan dengan kejernihan atau pudarnanya warna tersebut dimana semakin rendah nilai C* maka warna tersebut akan semakin pudar atau pucat sebaliknya nilai C* yang tinggi menandakan bahwa warana yang dihasilkan sangat kuat sehingga terlihat sangat pekat dan mencolok (Agusandi et al., 2013). Hasil sidik ragam menunjukkan bahwa pH
berpengaruh nyata (P<0,05) terhadap nilai C* (chroma) serbuk terung belanda terkopigmentasi dan terenkapsulasi terhadap perlakuan pH. Tabel 2 menunjukkan, nilai C* berkisar antara 76,01-71,41. Semakin
tinggi nilai pH semakin rendah nilai C*. Hal ini karena pada nilai pH yang semakin tinggi warna yang dihasilkan pada sampel semakin pudar akibat terjadinya perubahan struktur antosianin.
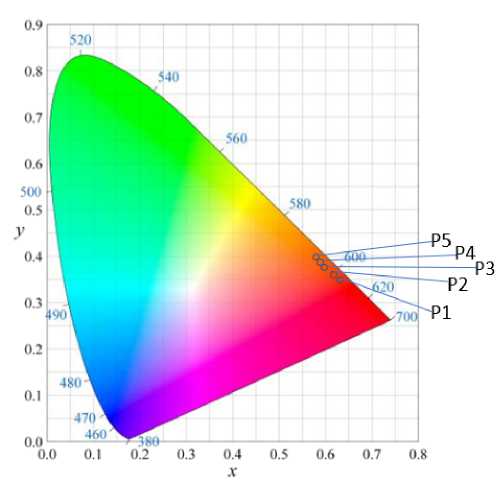
Gambar 1.Warna Serbuk Terung Belanda Terkopigmentasi dan Terenkapsulasi terhadap Perlakuan pH pada Diagram Kromatisasi CIE xy
Warna serbuk terung belanda terkopigmentasitasi dan terenkapsulasi yang mendapatkan perlakuan pH dapat dilihat pada Gambar 1. Meningkatnya nilai C menunjukkan bahwa pewarna tersebut semakin menuju warna asli yang diukur (pekat) (Ann et al., 2012). Semakin rendah nilai C* maka warna tersebut akan semakin pudar atau pucat sebaliknya nilai C* yang tinggi menandakan bahwa warna yang dihasilkan sangat kuat sehingga terlihat sangat pekat dan mencolok (Agusandi et al., 2013).
Pudarnya warna merah seiring dengan peningkatan nilai pH dapat terjadi akibat adanya perubahan struktur antosianin sehingga mempengaruhi kelarutan setiap molekul dimana pada kondisi yang semakin basa kelarutan akan berkurang sehingga menurunnya stabilitas terhadap perubahan pH. Ahmadiani et al (2014) menyatakan nilai Chroma pada pH yang lebih rendah (asam) cenderung lebih tinggi. Hal ini sejalan dengan hasil penelitian Lukitasari et al (2017) dimana nilai C* enkapsulan pigmen kubis merah pada pH 3-11 cenderung mengalami penurunan.
Nilai C juga menunjukkan kemungkinana korelasi positif dengan kandungan antosianin, dimana semakin tinggi nilai C* maka total antosianin pada bahan semakin tinggi (Vieira et al., 2018). Hal ini sejalan dengan penelitian Heredia et al (1998) peningkatan nilai pH 1,5 - pH5 bahan pengekstrak untuk kulit buah anggur menyebabkan menurunkan nilai C* yang juga sejalan dengan menurunnya total antosianin. Sejalan juga dengan penelitian Bao et al (2005) peningkatan nilai pH bahan pengekstrak buah barberry cina menyebabkan terjadinya penurunana nilai C* dan antosianin.
KESIMPULAN
Derajat keasaman (pH) mempengaruhi stabilitas antosianin serbuk terung belanda terkopigmentasi dan terenkapsulasi dengan hasil berpengaruh nyata terhadap degradasi warna antosianin, total antosianin, retensi absorbansi, nilai L*, a*, b*, hue dan chroma. Stabilitas antosianin serbuk terung belanda terkopigmentasi dan terenkapsulasi paling baik diperoleh pada pH 3 dengan degradasi warna antosianin 8,48%, total antosianin 0,63 mg/g, retensi absorbansi 96,51, nilai L* 40,03, nilai a* 51,07, b* 56,30, hue 47,79° (merah) dan chroma 76,01. Serbuk terung belanda terkopigmentasi dan terenkapsulasi dapat diaplikasikan pada produk pangan dengan pH asam.
DAFTAR PUSTAKA
Agusandi, A., Agus. S, dan D. L. Shanti. 2013. Pengaruh Penambahan Tinta Cumi-Cumi Terhadap Kualitas Nutrisi dan
Penerimaan Sensori Mi Basah. Journal Of Fishtech, 2(1), 22–37.
Ahmadiani. N., R.J. Robbins, T.M. Collins and M.M. Giusti. 2014. Anthocyanins Contents, profile and color characteristic of Red Cabbage Extracts from Different Cultivars and Maturity Stage. Food Chem 62: 7524-7531.
Ann E. Haggerman. 2002. The Tannin Book. USA: Miami University.
Bao, J., Y. Cai, M. Sun, G. Wang, and H. Corke. 2005. Anthocyanins, Flavonols, and Free Radical Scavenging Activity Of Chinese Bayberry (Myrica Rubra) Extracts and Their Color Properties and Stability. Journal of Agricultural and Food Chemistry. 53(6). 2327-2332.
Brouillard, R. 1982. Chemical Structure of Anthocyanins. In P. Markakis (Ed). Anthocyanins as Food Colors. Academic Press. New York. 1-40.
Bridgers, N. E., S. M. Chin and V Den Truong,. 2010. Extraction of Anthocyanins from Industrial Purple-Fleshed Sweetpotatoes and Enzymatic Hydrolysis of Residues for Fermentable Sugars. Industrial Crops and Products 32 (2010) 613-620.
Burton-Freeman, B. M., Sandhu, A. K, and Edirisinghe, I. 2016. Red Raspberries and Their Bioactive Polyphenols: Cardiometabolic and Neuronal Health Links. Advances in Nutrition, 7(1), 4465.
Castaneda-Ovando, A., Pacheco-Hernandez, M. L., Páez-Hernández, M. E.,
Rodríguez, J. A and Galan-Vidal, C. A. 2009. Chemical Studies of Anthocyanins: A review. Food Chemistry, 113, 859– 871.
Cevallos-Casals, B. A., and L. Cisneros-Zevallos. 2004. Stability of Anthocyanin Based Aqueous Extracts of Adean Purple Corn and Red-fleshed Sweet Potato Compared to Synthetic and Natural Colorants. Food chemistry, 86(1), 69-77.
Farida, R., dan F. C. Nisa. 2015. Ekstraksi Antosianin Limbah Kulit Manggis Metode Microwave Assisted Extraction (Lama Ekstraksi dan Rasio Bahan : Pelarut). Jurnal Pangan dan Agroindustri
3 (2): 362 – 373.
Fathinatullabibah, Kawiji dan L.U. Khasanah. 2014. Stabilitas Antosianin Ekstrak Daun Jati (Tectona gdanis) terhadap Perlakuan pH dan Suhu. Jurnal Aplikasi Teknologi Pangan. 3 (2) 3(2):60–63.
Fendri, S.T.J. Verawati dan P.S. Nuras. 2020. Stabilitas Antosianin dari Kulit Terung Belanda Merah (Solanum
betaceum Cav.) terhadap pH dan Suhu. Jurnal Katalisator. 5(1):64–73.
Francis FJ. 1996. Color Analysis. Chapter 12 In Food Analysis 2nd. Gaithersburg. (DE) : Aspen Publishers, Inc.
Giusti, M. M., and Wrolstad, R. E. 2001. Characterization and Measurement of Anthocyanins by UV– Visible Spectroscopy. Current Protocols in Food Anal Chem. F1.2.1-F2.2.13
Gomez, K. A dan Anturo. (1995). Prosedur Statistik untuk Penelitian Pertanian. Jakarata. UI Press.
Hanum T. 2000. Ekstraksi dan Stabilitas Zat Pewarna dari Bekatul Beras Ketan Hitam (Oryza sativa Glutinosa). Buletin Teknologi dan Industri Pangan Vol XI. No. 1, 2000.
Heredia, F. J., E. M. Francia-Aricha, J. C. Rivas-Gonzalo, I. M. Vicario, and C. Santos-Buelga. 1998. Chromatic
Characterization of Anthocyanins From Red Grapes - I. pH effect. Food Chemistry, 63(4), 491-498.
http://dx.doi.org/10.1016/S0308-8146(98)00051-X.
Hutching, J. B. 1999. Food Color and Appearance Second Edition. Maryland (US): Aspen Publishers, Inc.
Jamei, R., and F. Babaloo. 2017. Satbility of Bluberry (Cornus- mas- Yulyush) Antocyanin Pigment Under pH anda Copigment Treatment. Intern J Food Properties. 20 (9). 2128-2133.
Laleh, G. H., H. Frydoonfar, R. Heidary, R. Jameei and S. Zare. 2006. The Effect of Light, Temperatur, pH and Species on Stability of Anthocyanin Pigment in Four Berberies Species. Pakistan Journal of Nutrition 5(1):90-92.
Loypimai, Patiwit, A. Moongngarm, and P. Chottanom. 2016. Thermal and PH Degadation Kinetics of Anthocyanins in Natural Food Colorant Prepared from Black Rice Bran. Journal of Food Science and Technology . 53(1):461–70.
Lukitasari, D. M., R. Indrawati, R. D. Chandra, dan L. Limantara. 2017.
Mikroenkapsulasi Pigmen dari Kubis Merah: Studi Intensitas Warna dan Aktivitas Antioksidan. Jurnal Teknologi dan Industri Pangan, 28(1), 1-9.
Marco, P.H., Poppi, R.J, Scarminio, I.S, Tauler R. 2011. Investigation of The pH Effect and UV Radiation on Kinetic Degradation of Anthocyanin Mixtures Extracted from Hibiscus acetosella.. Food Chem 125: 1020–1027.
Meutia, Y. R., Susanti, I., & Siregar, N. C. (2019). Uji Stabilitas Warna Hasil Kopigmentasi Asam Tanat dan Asam Sinapat pada Pigmen Brazilin Asal Kayu Secang (Caesalpinia sappan L.). Warta Industri Hasil Pertanian, 36(1), 30-39.
Montes, C., Vicario, I. M., Raymundo, M., Fett, R. and Heredia, F. J. (2005). Application of Tristimulus Colorimetry To Optimize The Extraction of Anthocyanins from Jaboticaba (Myricia Jaboticaba Berg.). Food Research
International, 38(8–9), 983-988.
http://dx.doi.org/10.1016/j.foodres.2005. 01.016
Nugaheni, M. 2012. Pewarna Alami Makanan dan Potensi Fungsionalnya. Skripsi. Fakultas Teknik Universitas Negeri Yogyakarta.
Palupi, N. Widya, P. Khrisna, J. Setiadi, dan S. Yuwanti. 2014. Enkapsulasi Cabai Merah Dengan Teknik Coacervation Menggunakan Alginat Yang disubstitusi Dengan Tapioka Terfotooksidasi. Jurnal Aplikasi Teknologi Pangan. 3(3):87–93.
Parisa, Setareh, H. Reza, G. Elham and J. Rashid, (2007). Effect Of Heating, UV Irradiation And Ph On Stability Of The Anthocyanin Copigment Complex. J. Biol. Sci., 10: 267-272.
Permatasari, N. A dan Y.K. Deofsila. 2021. Perubahan Kualitas Bubuk Pewarna Alami Buah Buni (Antidesma Bunius (L) Spreng) Selama Penyimpanan dFengan Menggunakan Metode Akselerasi. Jurnal Teknologi Industri Pertanian, 31(2), 176189.
Purnomo, W., L. U. Khasanah dan R. B. K. Anindito. 2014. Pengaruh Ratio Kombinasi Maltodekstrin, Karagenan dan Whey terhadap Karakteristik Mikroenkapsulan Pewarna Alami Daun Jati (Tectona grandis L. f.). Jurnal
Aplikasi Teknologi Pangan 2 (3) : 121129.
Puspawati, G. A. K. D., Y. Marsono, R. Armunanto, and Supriyadi. 2018. Inhibitory Potency of Indonesian Tamarillo (Solanum Betaceum Cav) Crude Extract against α-Glucosidase Enzyme Activity. Current Research in Nutrition and Food Science. 6(2):392– 403.
Puspawati, G. A. K. D, P.T. Ina, dan G.A. Ekawati. 2019. Proses Pembuatan Ekstrak Pewarna Merah Alami Bubuk dari Tamarillo (Solanum betacum Cav.). Kementrian Hukum dan Hak Asasi Manusia. Indonesia.
Puspawati, G. A. K. D, I. N. K. Putra, P.T. Ina, dan G.A. Ekawati. 2021. Inovasi Stabilitas Antosianin dari Ekstrak Tamarillo (Solanum betacum Cav.): Teknik Kopigmentasi dan Enkapsulasi. Laporan Penelitian. Unpublish. Universitas Udayana. Bukit Jimbaran.
Raharjo, S., F.A. Purwdanari, P.Hastuti, dan K.Olsen. 2019. “Stabilization of Black Rice (Oryza Sativa, L. Indica)
Anthocyanins Using Plant Extracts for Copigmentation dan Maltodextrin for Encapsulation.” Journal of Food Science 84(7):1712–20.
Sari,P., F. Agustina, M. Komar, Unus, M. Fauzil dan T. Lindriati. 2005. Ekstraksi dan Stabilitas Antosianin dari Kulit Buah Duwet (Syzigium cumini). Jurnal
Teknologi dan Industri Pangan 16(2).
Talcott, S.T., C.H. Brenes, D.M. Pires, dan D.D. Pozo-Insfran. 2003. “Phytochemical Stability dan Color Retention of Copigmented dan Processed Muscadine Gape Juice.” Journal of Agicultural dan Food Chemistry 51(4):957–63.
Vieira, L. M., Marinho, L. M. G, Rocha, J. D. C. G, Barros, F. A. R dan Stringheta, P. C. 2010. Chromatic analysis for predicting anthocyanin content in fruits and vegetables. Food Science and Technology, 39, 415-422.
Wahyuni, H., T. Hanum dan M. Murhadi. 2017. Pengaruh Kopigmentasi terhadap Stabilitas Warna Antosianin Ekstrak Kulit Terung Belanda (Cyphomandra betacea Sendtn). Jurnal Teknologi dan Industri Hasil Pertanian, 22(1), 40-51.
Widyasanti, A., N. Nurlaily dan E. Wulandari. 2018. Karakteristik Fisikokimia Antosianin Ekstrak Kulit Buah Naga Merah Menggunakan Metode UAE (Physicochemical Characteristics of Red Dragon Fruit Skin Anthocyanin Extracts using UAE Method): Physicochemical Characteristics of Dragon Fruit Peels (Hylocereus polyrhizus) Anthocyanin Extracts using UAE (Ultrasound Assisted Extraction) Method. Jurnal Ilmiah Rekayasa Pertanian dan Biosistem, 6(1), 27-38.
Winarno, F.G. 2004. Kimia Pangan dan Gizi. Gramedia Pustaka Utama. Jakarta.
360
Discussion and feedback