POTENSI SIANIDIN POLY(LACTIC-CO-GLYCOLIC ACID)-POLYETHYLEN GLYCOL YANG DIMODIFIKASI FUSED FOLLICLE UNTUK MENINGKATKAN SENSITIVITAS DAN SEKRESI INSULIN DALAM MENANGANI PENYAKIT DIABETES MELITUS TIPE 2
on
ARTIKEL TINJAUAN PUSTAKA

Essence of Scientific Medical Journal (2022), Volume 20, Number 1:19-26
P-ISSN.1979-0147, E-ISSN. 2655-6472
TINJAUAN PUSTAKA
POTENSI SIANIDIN POLY(LACTIC-CO-GLYCOLIC ACID)-POLYETHYLEN GLYCOL YANG DIMODIFIKASI FUSED FOLLICLE UNTUK MENINGKATKAN SENSITIVITAS DAN SEKRESI INSULIN DALAM MENANGANI PENYAKIT DIABETES MELITUS TIPE 2
Adrian Wiryanata Gorintha1, Stevina Debora1, Natasya Eiffeline Chandra1
ABSTRAK
Pendahuluan: Diabetes melitus tipe 2 merupakan salah satu dari empat prioritas penyakit tidak menular menurut WHO. Data WHO pada tahun 2015 menunjukkan bahwa sebanyak 415 juta jiwa di dunia menderita diabetes melitus tipe 2. Sementara itu di Indonesia pada tahun 2013, prevalensi orang dengan diabetes mengalami peningkatan menjadi 6.9%. Saat ini penatalaksanaan diabetes melitus tipe 2 yang umum adalah pemberian obat metformin. Namun pemberian jangka panjang akan menyebabkan asidosis laktat. Oleh karena itu dibutuhkan alternatif baru yang dapat meminimalisir efek samping yang dapat timbul, salah satunya dengan menggunakan sianidin yang merupakan flavonoid alami serta dapat memberikan efek peningkat sensitivitas dan sekresi insulin.
Pembahasan: Sianidin berpotensi sebagai peningkat sensitivitas reseptor insulin dan meningkatkan sekresi insulin. Dalam upaya meningkatkan sensitivitas insulin, sianidin mampu menghambat penurunan regulasi ekspresi GLUT4 dan menurunkan tingkat ekspresi RBP 4. Sebagai peningkat sekresi insulin, Sianidin meningkatkan ekspresi gen GLUT2, Kir6.2 dan Cav1.2 yang berperan dalam sekresi insulin. Walaupun sianidin memiliki bioavailabilitas rendah dan tidak stabil. Oleh karena itu, enkapsulasi sianidin akan meningkatkan ketersediaan siandin dalam darah dan mudah terkonsentrasi ke sel pankreas.
Simpulan: Kombinasi sianidin PLGA-PEG yang dimodifikasi FC dapat menjadi alternatif baru dalam pengobatan penyakit diabetes melitus tipe 2.
Kata kunci: Diabetes Melitus tipe 2, PLGA-PEG yang dimodifikasi Fc, Sianidin
ABSTRACT
Introduction: Type 2 diabetes mellitus is one of the four priority non-communicable diseases according to WHO. WHO data in 2015 showed that as many as 415 million people in the world suffer from type 2 diabetes mellitus. Even in Indonesia in 2013, the prevalence of people with diabetes has increased to 6.9%. Currently, the most common treatment for type 2 diabetes mellitus is the administration of metformin. However, long-term administration will cause lactic acidosis and kidney damage. Because of this, new alternatives are needed that minimize the side effects, for example by using herbal ingredients. Cyanidin is a natural flavonoid that has the effect of increasing insulin sensitivity and secretion.
Discussion: Cyanidin has the potential to increase insulin receptor sensitivity and increase insulin secretion. To increase insulin sensitivity, cyanidin can inhibit the downregulation of GLUT4 expression and decrease the level of RBP 4 expression. As an increase in insulin secretion Cyanidin increases the expression of GLUT2, Kir6.2, and Cav1.2 genes that play a role in insulin secretion. Unfortunately, Cyanidin has low bioavailability and is unstable. Therefore, Cyanidin encapsulation will increase the availability of cyanidin in the blood and is easily concentrated into pancreatic cells.
Conclusion: The Fc-modified Cyanidin PLGA-PEG combination has the potential to be a new alternative in the treatment of type 2 diabetes mellitus.
Keywords: Cyanidin, Fc-modified Cyanidin PLGA-PEG, Type 2 Diabetes Mellitus
1 Program Studi Sarjana Kedokteran dan Profesi Dokter, Fakultas Kedokteran, Universitas Udayana, Bali
PENDAHULUAN
Diabetes melitus tipe 2 merupakan salah satu dari empat prioritas penyakit tidak menular menurut World Health Organization (WHO).[1] Hal ini didasarkan pada data yang menyatakan bahwa sebanyak 415 juta jiwa di dunia menderita diabetes melitus pada tahun 2015 dimana setiap 11 orang dewasa terdapat 1 orang yang terkena diabetes melitus. Angka tersebut mengalami peningkatan yang cukup signifikan jika dibandingkan dengan angka penderita diabetes melitus pada tahun 1980-an yaitu sekitar 108 juta jiwa.[1,2] Apabila penyakit diabetes melitus ini tidak mendapatkan penanganan dan perhatian yang serius maka jumlah penderita akan terus mengalami peningkatan dimana diperkirakan pada tahun 2040 dapat mencapai angka 642 juta jiwa.[1]
Hingga saat ini, diabetes melitus belum dapat disembuhkan, namun deteksi sejak dini memungkinkan pengendalian kadar gula darah penderita diabetes melitus dan juga meningkatkan kualitas hidup mereka. Selain dengan menjaga pola makan dan memulai gaya hidup sehat, kini ada pula obat-obatan yang dapat dikonsumsi oleh penderita
diabetes melitus untuk mengatur keseimbangan kadar gula darah.4 Obat-obatan tersebut adalah metformin, sulfonilurea, pioglitazone, gliptin (penghambat DPP-4), penghambat SGLT-2, argonis GLP-1, acarbose, dan nateglinde.[3,4]
Metformin adalah obat antidiabetes yang paling umum digunakan. Obat ini dapat dikonsumsi secara tunggal maupun dikombinasikan dengan obat antidiabetes lainnya atau diberikan bersama insulin.[3,4,5] Metformin bekerja dengan cara menghambat proses glukoneogenesis dan glikogenolisis, memperlambat penyerapan glukosa pada usus, serta meningkatkan sensitivitas insulin dalam tubuh. Namun, penggunaan metformin dalam jangka panjang dapat menyebabkan asidosis laktat walaupun hanya kecil kemungkinan terjadinya.. Efek samping lainnya dari metformin yaitu mual, muntah, gangguan pencernaan, penurunan nafsu makan, nyeri otot dan kram, sakit perut, dan diare dimana setiap individu mengalami efek samping yang berbeda satu sama lain.[5]
Semakin meningkatnya prevalensi kasus diabetes melitus ditambah dengan adanya efek samping yang ditimbulkan dari obat-obatan yang sekarang beredar di masyarakat memicu penelitian lebih lanjut mengenai pengobatan alternatif diabetes melitus di antaranya melalui penggunaan buah gung-gung (Rubus flaxinifolius Poir). Rubus flaxinifolius Poir banyak terdapat di Bali namun kurang dimanfaatkan padahal buah ini bermanfaat untuk penanganan diabetes melitus. Hal ini karena buah Rubus flaxinifolius Poir mengandung antosianin yang merupakan salah satu jenis senyawa flavonoid dimana antosianin ini mempunyai zat aktif yang berguna untuk pencegahan dan pengobatan diabetes melitus yaitu sianidin.[6]
Beberapa studi praklinis menunjukkan sianidin dapat berperan dalam pengobatan diabetes dengan meningkatkan sekresi insulin pada sel beta pankreas dan sensitivitas insulin.[7,8] Walaupun demikian,
sianidin memiliki beberapa masalah dalam proses penyerapan atau memiliki bioavailabilitas yang rendah di dalam tubuh[9] untuk itu penggunaan teknologi nanopartikel terutama poly(lactic-co-
glycolic acid) (PLGA) dapat menjadi pilihan alternatif dalam mengatasi permasalahan bioavailabilitas yang rendah dari sianidin.[10] PLGA adalah salah satu polimer biodegradable yang sering digunakan sebagai nanocarrier yang efektif untuk penghantaran obat ke dalam sel dan telah disetujui oleh Food and Drug Administration (FDA).[11] Dengan memodifikasi PLGA dengan Poli (ethylene glycol) (PEG) dan memodifikasinya sehingga terkonjugasi dengan Fused Follicle (Fc), penghantaran sianidin ke dalam tubuh bisa dilakukan melalui oral degan efisiensi yang tinggi.[12]
PEMBAHASAN
Sianidin
Sianidin (C15H11O6+) adalah senyawa organik alami yang merupakan bagian dari antosianin (jenis flavonoid). Sianidin merupakan pigmen yang larut dalam air dan banyak ditemukan pada buah beri merah termasuk anggur, bilberry, blackberry, blueberry, ceri, cranberry, elderberry, hawthorn, loganberry, açai berry, dan raspberry. Warna dari sianidin bergantung pada pH larutan. Pada pH < 3 sianidin berwarna merah, pH > 11 berwarna biru, dan berwarna ungu dalam keadaaan netral (pH = 7). Sianidin memiliki ativitas biologis dan farmakologis yang luas, meliputi anti kanker, vasoprotective, anti-inflamasi, anti-obesitas, dan efek anti-diabetes.[13]
Polyethylene Glycol-Poly(Lactic-Co-Glycolic Acid) (PEG-PLGA) Nano Particles Dimodifikasi dengan Fc (NPs-Fc)
Poly (lactic-co-glycolic acid) (PLGA) adalah salah satu polimer biodegradable yang paling berhasil digunakan karena metabolit monomernnya ialah asam laktat dan asam glikolat. Dua buah monomer ini bersifat endogen dan mudah dimetabolisme oleh tubuh melalui siklus Krebs. Penggunaan PLGA sebagai pengirim obat atau aplikasi biomaterial berefek pada minimalnya toksisitas sistemik. Selain itu, PLGA juga memiliki formulasi dan metode produksi yang dapat disesuaikan dengan berbagai jenis obat. PLGA telah disetujui oleh Food and Drug Association (FDA) dan European Medicine Agency (EMA) dalam berbagai sistem pengiriman obat pada manusia.[10,11]
Untuk meningkatkan bioavailabilitas obat-obatan hidrofilik yang tidak stabil seperti sianidin, penggunaan nanopartikel berbasis polimer yaitu PLGA karena sifatnya yang unik seperti stabilitas yang tinggi, meningkatkan bioavailabilitas, dan efisiensi pemuatan obat yang larut dalam air yang tinggi.[11] Namun, sianidin tidak stabil karena memiliki gugus hidroksil fenolik yang mudah teroksidasi menjadi quinones sehingga menyebabkan berkurangnya aktivitas biologis.[9] Untuk mengatasi kekurangan ini dan meningkatkan bioavailabilitas sianidin akan dimasukkan ke dalam formulasi nanopartikel biodegradable.
Modifikasi permukaan PLGA dengan bahan yang tidak beracun dan darah yang kompatibel sangat penting untuk menghindari pengenalan oleh makrofag.[14] Modifikasi ini dilakukan untuk memperpanjang waktu sirkulasi darah dan pelepasan secara berkelanjutan dari obat yang terkapsul dalam PLGA. Poli (ethylene glycol) (PEG) secara luas digunakan sebagai segmen nontoksik hidrofilik yang dikombinasikan dengan poliester biodegradable hidrofobik seperti PLGA. Penggabungan kelompok PEG hidrofilik pada permukaan nanopartikel menunjukkan resistensi terhadap opsonisasi dan fagositosis dan waktu tinggal yang lama dalam darah dibandingkan dengan nanopartikel yang disiapkan tanpa PEG.[15]
Penyerapan seluler yang spesifik dan transpor transepitelial dapat ditingkatkan dengan mengonjugasikan permukaan nanocarrier dengan ligan spesifik reseptor epitel atau antibodi. Ligan yang penulis gunakan untuk pengiriman oral obat adalah fused follicle (Fc). Fc berhasil menstimulasi hormon mencapai sirkulasi melalui adminitrasi oral. Reseptor Fc diekspresikan di daerah apikal sel epitel di usus halus dan di seluruh usus besar baik pada janin maupun pada orang dewasa. Nanopartikel yang terkonjugasi Fc dapat menyeberangi epitel usus dan mencapai sirkulasi sistemik pada tikus dengan efisiensi penyerapan yang lebih tinggi dibandingkan dengan nanopartikel yang tidak ditargetkan (13,7% vs 1,2%) oleh pemberian oral dan bahwa peningkatan nanopartikel secara khusus karena FcRn.[12,16]
Mekanisme konstruksi
-
1. Persiapan sampel
Buah Rubus fraxinifolius dibersihkan, ditimbang, dan dipotong kecil-kecil. Kemudian, buah disimpan dalam lemari pembeku bersuhu -80°C semalam sebelum dimasukkan ke dalam mesin pengeringan beku selama tiga hari. Sampel beku kering selanjutnya digiling menjadi bubuk halus dengan menggunakan mesin penggiling kering. Sampel diayak untuk mendapatkan ukuran partikel yang seragam dan disimpan dalam wadah kedap udara dan disimpan dalam freezer bersuhu -20°C untuk analisis lebih lanjut.[6]
-
2. Pengekstrasian sampel
Sekitar 0,1 g sampel beku-kering ditambahkan ke 30 mL 80% (v / v) metanol. Campuran dikocok selama dua jam dengan menggunakan pengocok orbital yang ditetapkan pada 200 rpm pada suhu kamar (25 °C). Supernatan dituangkan ke dalam vial untuk analisis lebih lanjut.[17]
-
3. Kandungan total antosianin
Secara singkat, 0,5 mL ekstrak dicampur secara menyeluruh dengan 3,5 mL buffer kalium klorida (0,025 M; pH 1,0). Campuran dicampur dengan vortex dan dibiarkan selama 15 menit. Nilai
absorbansi diukur pada 515 dan 700 nm terhadap air suling kosong. Ekstrak dicampur dengan 3,5 mL buffer natrium asetat (0,025 M; pH 4,5) dan dibiarkan selama 15 menit. Nilai absorbansi diukur pada panjang gelombang yang sama. Kandungan total antosianin dihitung dengan menggunakan rumus berikut:
Kandungan Total Antosianin (mg/g dari sampel kering) :
A × Mw × DF × 10
(ε × C)
dimana A adalah nilai absorbansi = (A515 – A700) pH 1,0 - (A515 – A700) pH 4,5; Mw (molecular weight) = 287,24 g/mol; Dilution Factor (DF) faktor pengenceran dari sampel, ε adalah absorbtivitas molar sianidin~13,000-30,000 L/mol cm; C merupakan kosentrasi dari buffer dalam mg/ml. Hasilnya dinyatakan sebagai Cyanidin-3-glucoside (mg) / sampel kering (g)[18]
Umumnya ada beberapa metode untuk mikroenkapsulasi obat yang saat ini telah dikembangkan seperti phase separation spray-drying dan emulsion solvent evaporation (O/W, W/O/O, W/O/W). Walaupun metode water-in-oil-in-water (W/O/W) double emulsion solvent evaporation lebih sering digunakan (process and formulation) namun menurut penelitian Wang, dkk metode water-in-oil-inoil (W/O/O) lebih baik digunakan untuk mengurangi fenomena initial burst (HP) yang mengakibatkan toksisitas yang parah.[19]
Sianidin pertama kali dilarutkan ke dalam larutan sukrosa (2%) untuk mendapatkan larutan sianidin. Kemudian larutan itu diemulsi lebih lanjut dengan menambahkan larutan PEG PLGA di dichloromethane (DCM). Larutan yang dihasilkan disonikasi selama 60 detik dan direndam di dalam es
untuk menghasilkan emulsi primer (W/O). Setelah itu, minyak silicon ditambahkan di emulsi primer sambil diaduk terus selama tiga menit di rendaman es untuk mendapatkan nanopartikel yang tidak berbentuk. Emulsi yang dihasikan segera dipindahkan ke wadah khusus yang berisi campuran antara heptane dan ethanol (10:1) yang sebelumnya telah disimpan pada suhu 4 ̊C dan terus diaduk selama 15 menit. Setelah segala persiapan itu, tunggu selama 5 menit dalam posisi berdiri, cairan supernatant dibuang dan endapannya dicuci dengan heptane segar untuk menghilangkan DCM yang tersisa. Proses pencucian diulangi sebanyak tiga kali. Setelah itu nanopartikel kasar yang dihasilkan tertahan di atas saringan 600-mesh (0,025 mm) dan divakum kering pada suhu 4 ̊ C selama 12 jam lalu pada suhu 37 ̊C selama 24 jam. Pada tahap akhir nanopartikel kering dilewatkan pada saringan 100-mesh (0,150mm).[10]
Mekanisme administrasi
Ada beberapa cara untuk mengadministrasikan obat dalam PLGA-PEG seperti sublingunal, intervena, intramuskular, rektal, dan juga oral. Sampai saat ini, cara yang paling sering digunakan untuk administrasi obat antidiabetes PLGA-PEG dengan injeksi subkutan maupun intravena.[11] Namun baru-baru ini penelitian oleh Yanan Shi dkk menemukan bahwa nanopartikel PLGA-PEG dapat diadministrasikan secara oral dengan modifikasi penambahan Fc. Administrasi oral dipilih karena dapat dilakukan oleh semua orang tanpa keahlian khusus dan untuk kenyamanan pasien sendiri. Dengan memodifikasikannya dengan Fc efesiensi sianidin dengan nanopartikel PLGA-PEG dapat mencapai 80% dan memperpanjang efek hipoglikemik dibandingkan dengan injeksi larutan sianidin. [12]
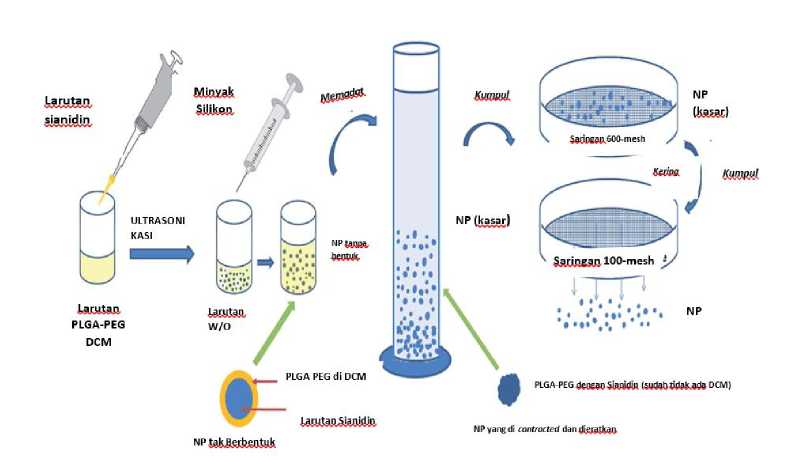
Gambar 1. Skema Ilustrasi Metode W/O/O yang Digunakan untuk Persiapan Nanopartikel. [10]
Farmakokinetik
Penelitian in vivo menggunakan tikus (rat) sebagai hewan coba membuktikan bahwa sianidin dapat memberikan efek yang bermanfaat jika
diberikan dengan dosis 10 mg/kg. Selanjutnya dengan konversi berdasarkan translasi dosis Reagen Shaw, diperoleh dosis potensial sianidin pada manusia sebesar 1,62 mg/kg. [20]
Tabel 1. AUC: Tingkat Serapan Obat Pada Tubuh, Cmax: Konsentrasi Tertinggi Obat Pada Plasma, Tmax : Waktu Yang Diperlukan Untuk Mencapai Konsentrasi Tertinggi, Dan T1/2: Waktu Paruh Obat Pada Sianidin Bebas.[21]
Parameter Hari 1 Hari 14
|
AUClast (ng • h/ml) |
4.26±1.40 |
4.85±1.65 |
|
Cmax (ng/ml) |
2.10±0.60 |
2.17±0.68 |
|
Tmax (h) |
0.73±0.29 |
0.75±0.34 |
|
T1/2(h) |
1.58±0.33 |
1.47±0.29 |
Sianidin adalah molekul hidrofilik yang memiliki bioavailabilitas bioavailability rendah dan tidak stabil. Oleh karena itu diperlukan nanopartikel yang memiliki stabilitas tinggi dan solubilitas yang tinggi juga dengan sianidin untuk menahan terlepasnya sianidin sebelum sampai ke sel target. Nanopartikel (NP) PLGA dan stabilisator PEG telah banyak dipelajari karena memiliki potensi yang besar untuk dapat bertahan di sirkulasi dengan waktu yang lebih lama. Karakter PEG yang hidrofilik dapat meningkatkan biokompatibilitas. Selain itu, kulit PEG juga mampu melindungi nanopartikel dari serangan enzimatik pada saluran pencernaan dan juga rantai PEG ini
mampu menembus lapisan mukosa saluran pencernaan.[21,22] Nanopartikel PLGA-PEG sangat cocok digunakan untuk mengekpasulasi sianidin karena sifatnya akan mudah terkonsentrasi di pankreas, meningkatkan jumlah serapan obat dalam tubuh, meningkatkan konsentrasi obat di plasma. Terlebih lagi telah dikembangkan modifikasi dengan Fc, sianidin akan mampu diberikan dengan rute yang non-invasif dan sebagai rute alternatif bagi terapi diabetes yang sering diadministrasikan dengan injeksi.[12,23]. Fluorescence digunakan untuk melabeli nanopartikel dan menginvestigasi efek dari Fc.[12]
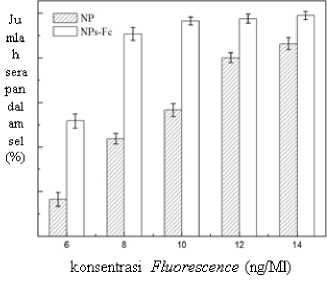
Gambar 2. Perbandingan Penyerapan dalam Sel Antara Nanopartikel Biasa dengan Nanopartikel yang Telah Dimodifikasi Fc , Ditandai dengan Konsentrasi Fluorescence [12]
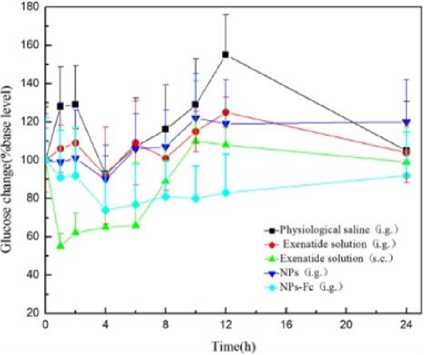
Gambar 3. Kadar Glukosa dalam Darah Pada Administrasi Oral NP, NP yang Dimodifikasi Fc, Larutan Sianidin dan larutan saline fisiologis.[12]
Efek hipoglikemik dari sianidin PEG-PLGA terlihat pada Gambar 3 dimana nilai rata-rata glukosa darah sebelum pengobatan pada tiap-tiap eksperimen di angka 100%. Nanopartikel (NP) dan Nanopartikel yang dimodifikasi Fc, keduanya menunjukkan tingginya efek hipoglikemik, dibanding dengan sianidin yang diadministrasikan secara oral. Hal ini juga mendemonstrasikan lemahnya absorpsi oral sianidin bebas di usus halus. Larutan salin fisiologi oral tidak menunjukkan efek hipoglikemik malah sebaliknya. Efek hipoglikemik untuk adminitrasi oral PEG-PLGA yang dimodifikasi Fc menunjukkan waktu kerja yang lebih lama dibanding dengan larutan sianidin yang diinjeksi. Selain itu, efek hipoglikemik NP yang telah dimodifikasi lebih signifikan dibanding dengan NP biasa pada semua titik waktu.[12]
Mekanisme pelepasan obat yang dienkapsulasi dengan PLGA-PEG dalam tubuh terjadi akibat adanya proses degredasi PLGA-PEG yang menyebabkan obat di dalamnya terlepas. Proses degredasi ini diakibatkan oleh faktor kimia melalui proses oksidasi dan hidrolisis, serta faktor fisika di dalam tubuh.[11,12]
Sianidin PLGA-PEG yang terkonjugasi Fc yang diadminitrasi secara oral, akan diabsorbsi dan melewati epitel usus dan masuk ke dalam lamina propria.[24] Pada beberapa organ NP-Fc juga dapat masuk ke dalam sirkulasi sitemik. Hal ini menujukan bahwa NP-Fc dapat menembus epithelial barrier dan masuk ke dalam sirkulasi.[25] Sianidin dalam darah dapat dengan mudah terkonsentrasi ke sel pankreas karena dienkaspulasi oleh PLGA yang membantu kerja sianidin untuk meningkatkan produksi insulin.[26,8] Sianidin juga dapat menyebar dan terserap di jaringan normal seperti jaringan lemak.[27] Sianidin dimetabolisme di hati bersama dengan
empedu dan disekresikan melalui feses. Sebagian sianidin akan menuju ke ginjal dan diekskresikan melalui urin.[20]
Farmakodinamik
Farmakodinamik Sianidin PLGA-PEG yang dimodifikasi Fc dalam meningkatkan sensitivitas insulin
Menurut penelitian Sasaki, dkk diperoleh hasil bahwa Cyanidin-3-glucoside (C3G) memberikan pengaruh yang signifikan sebagai anti-diabetik melalui peningkatan ekspresi glucose transporter 4 (GLUT4) dan penurunan ekspresi retinol binding 4 (RBP4).[8]
Monocyte chemoattranctant protein – 1 (MCP-1) dan tumor necrosis factor-α (TNF-α) merupakan molekul inflamasi yang diekspresikan dan mengalami peningkatan regulasi pada tingkat obesitas termasuk pada diabetes melitus tipe 2. Studi terbaru menunjukkan bahwa peningkatan ekspresi MCP-1 dan TNF-α berkontribusi pada peningkatan resistensi insulin.9 Beberapa laporan menunjukkan antosianin khususnya C3G memiliki potensi dalam menurunkan regulasi MCP-1 dan TNF-α untuk memperbaiki keadaan diabetes.[8] Penurunan ekspresi MCP-1 oleh C3G dapat berkontibusi pada penghambatan penurunan regulasi ekspresi GLUT4 sehingga dengan penurunan ekspresi MCP-1 dapat meningkatkan regulasi dari ekspresi GLUT4. C3G juga mengaktivasi adenosine monophospate protein kinase (AMPK), dimana aktivasi AMPK merangsang glukosa melalui peningkatan ekspresi GLUT4 di adiposit.[27] Hal tersebut memberikan hasil yang signifikan terhadap penurunan tingkat ekspresi RBP-4 yang menyebabkan peningkatan sinyal insulin dan penyerapan glukosa di otot rangka, serta penurunan aktivitas glukoneogenesis di hati
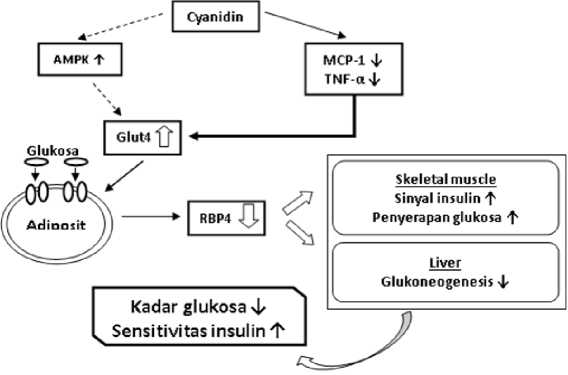
Gambar 4. Farmakodinamik Sianidin dalam Meningkatkan Sensitivitas Insulin9
Farmakodinamik Sianidin sebagai Stimulan Sekresi Insulin pada sel pankreas
Hasil penelitian Suantawee, dkk menunjukkan bahwa sianidin dapat meningkatkan sekresi insulin dengan jalan meningkatkan konsentrasi kalsium di dalam sel pankreas. Sekresi insulin dapat ditingkatkan melalui peningkatan ekspresi gen GLUT2, Kir6.2, dan Cav1.2. Gen GLUT2 berperan dalam sintesis glucose transporter 2 protein, tipe protein integral pada sel pankreas yang digunakan untuk mentransport glukosa ke dalam sel. Kir6.2
adalah gen yang berperan dalam sintesis ATP-sensitive K+ Channel (KATP), dimana protein ini berperan dalam memunculkan peristiwa depolarisasi sel. Cav1.2 adalah gen yang berperan dalam sintesis voltage-dependent Ca2+ Channel (VDCC), dimana protein ini akan menjadi tempat masuknya ion Ca2+ saat depolarisasi sel terjadi. Alur kerja ketiganya dapat dihubungkan demikian. Sianidin yang masuk ke sel pankreas dapat memicu ekspresi gen GLUT2 yang menyebabkan akan semakin banyaknya glukosa yang masuk ke dalam sel. Glukosa akan
digunakan oleh mitokondria untuk menghasilkan ATP. ATP yang dihasilkan akan menyebabkan KATP teraktivasi sehingga terjadilah proses depolarisasi membran dari sel pankreas tersebut. Depolarisasi membran akan berdampak pada protein VDCC yang
teraktivasi sehingga memungkinkan ion Ca2+ masuk ke dalam sel. Keberadaan ion Ca2+ dalam kadar yang tinggi dapat menyebabkan ekspresi insulin meningkat. [7]
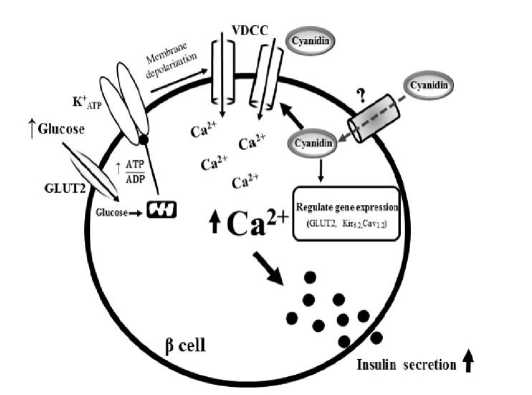
Gambar 5. Mekanisme Kerja Sianidin Sebagai Stimulan Sekresi Insulin. [7]
Efek klinis
Efek klinis sianidin PLGA-PEG yang dimodifikasi Fc dalam meningkatkan sensitivitas insulin
Sianidin diketahui dapat menghambat penurunan regulasi ekspresi GLUT4 sehingga menyebabkan terjadinya peningkatan GLUT4. Tingkat ekspresi gen GLUT4 pada WAT mesentrika meningkat dengan signifikan (2,4 kali lipat) . Selain itu, tingkat ekspresi protein GLUT4 pada keseluruhan sel lisat (whole lysate) dan membran plasma juga mengalami peningkatan. Tingkat ekspresi gen C3G meningkat 2,6 kali lipat (whole lysate) dan 3,1 kali
lipat (plasma membrane) dibanding kelompok kontrol.[8]
Efek sianidin dapat menurunkan tingkat ekspresi RBP telah dibuktikan dalam penelitian Sasaki, dkk. Pada penelitian ini menunjukkan bahwa sianidin mampu menurunkan ekspresi gen RBP di WAT mesentric dengan cukup signifikan, yaitu 57%. Namun, pada liver tidak terjadi perubahan yang signifikan. Serum RBP4 mengalami penurunan ekspresi gen pada kelompok C3G dibandingkan kelompok kontrol (47%). [8]
Tabel 2. Berat Badan, Serum Glukosa, dan Serum Insulin pada Kelompok Kontrol dan Kelompok C3G.[8]
|
Periode Kontrol C3G | |
|
Berat badan |
0 minggu 19.2 ± 1.0 18.8 ± 1.2 5 minggu 37.4 ± 0.8 37.0 ± 1.2 |
|
Serum glukosa |
0 minggu 244.6 ± 20.6 231.9 ± 18.4 |
|
(mg/dL) |
3 minggu 393.9 ± 15.3 300.1 ± 14.0 5 minggu 454.2 ± 26.1 356.5 ± 28.0 |
|
Serum insulin |
5 minggu 17.4 ± 1.2 14.4 ± 1.2 |
Pada pemberian C3G tidak memberikan pengaruh yang signifikan terhadap berat badan selama periode eksperimen sehingga aman untuk digunakan. Konsentrasi glukosa darah mengalami penurunan yang signifikan pada kelompok C3G pada minggu ke 3 dan 5. Hasil toleransi insulin menunjukkan bahwa C3G dapat memperbaiki resistensi insulin.[8]
Efek klinis dari Sianidin PLGA-PEG yang dimodifikasi Fc dalam meningkatkan sekresi insulin
Sianidin menunjukkan efek peningkatan ekspresi gen GLUT2 dan gen Kir6.2 secara bermakna pada pemberian selama empat, enam, dan 12 jam (P < 0.05) .Selain itu pemberian sianidin juga meningkatkan ekspesi gen Cav1.2 secara berarti dalam pemberian sianidin selama 6 jam. [7]
Efek dari sianidin untuk meningkatkan sekresi insulin telah ditunjukkan oleh Suantawee, dkk, bahwa semakin tinggi dosis sianidin yang diberikan maka semakin besar sekresi insulin. Pemberian dosis sebanyak 300 µM akan menghasilkan sekresi tiga kali lipat dari metabolisme basal.[7]
SIMPULAN
Sianidin PLGA-PEG dengan dimodifikasi Fc memiliki potensi sebagai pengobatan pada penyakit diabetes melitus tipe 2. Efek klinis yang dimiliki Sianidin PLGA-PEG dengan dimodifikasi Fc adalah meningkatkan sensitivitas dan sekresi insulin.
Mekanisme konstruksi dari sianidin PLGA-PEG dengan dimodifikasi Fc adalah dengan metode waterin-oil-in-water (W/O/W) double emulsion solvent evaporation lebih sering digunakan (Proses dan Formulasi), namun menurut penelitian Wang, dkk metode water-in-oil-in-oil (W/O/O) lebih baik digunakan untuk mengurangi fenomena initial burst (HP) yang mengakibatkan toksisitas yang parah.
Farmokodinamik sianidin PLGA-PEG dengan dimodifikasi Fc adalah dengan memberikan pengaruh yang signifikan sebagai anti-diabetik melalui peningkatan ekspresi glucose transporter 4 (GLUT4) dan penurunan ekspresi retinol binding 4 (RBP4). Sianidin meningkatkan sekresi insulin dengan jalan meningkatkan konsentrasi kalsium di dalam sel pankreas. Sekresi insulin dapat ditingkatkan melalui peningkatan ekspresi gen GLUT2, Kir6.2, dan Cav1.2.
SARAN
Perlunya dilakukan penelitian lebih lanjut untuk mengetahui jumlah dosis yang tepat, lama terapi, penelitian mengenai sianidin dengan PLGA-PEG yang dimodifikasi Fc lebih lanjut, dan juga efek klinis yang lebih lanjut dari sianidin sebagai obat dalam penanganan diabetes melitus. Selain itu perlu dilakukan evaluasi klinis terhadap efektivitas kombinasi dan metode konstruksti sianidin PLGA-PEG yang dimodifikasi Fc agar dapat diadministrasikan secara sempurna melalui oral
DAFTAR PUSTAKA
-
1. Diabetes programme [Internet]. World Health Organization. 2018 [diakses 8 November 2018].
Dapat diakses di :
http://www.who.int/diabetes/en/
-
2. K D, years N, possible Y. Number of people living with diabetes doubles in twenty years [Internet]. Diabetes UK. 2018 [diakses 8 November 2018].
Dapat diakses di
:https://www.diabetes.org.uk/about_us/news/dia betes-prevalence-statistics
-
3. Diabetes Drugs [Internet]. Diabetes.co.uk. 2018 [diakses 8 November 2018]. Dapat diakses di : https://www.diabetes.co.uk/Diabetes-drugs.html
-
4. List of Common Diabetes Medications [Internet]. Healthline. 2018 [diakses 8 November 2018].
Dapat diakses di :
https://www.healthline.com/health/diabetes/medi cations-list
-
5. Metformin: medicine to treat type 2 diabetes -NHS.UK [Internet]. NHS.UK. 2018 [diakses 8 November 2018]. Dapat diakses di : https://beta.nhs.uk/medicines/metformin/
-
6. Abu Bakar M, Ismail N, Isha A, Mei Ling A. Phytochemical Composition and Biological
Activities of Selected Wild Berries (Rubus
moluccanusL.,R. fraxinifoliusPoir., andR.
alpestrisBlume). Evidence-Based
Complementary and Alternative Medicine. 2016;2016:1-10.
-
7. Suantawee, Tanyawan; T.Elazab, Sara; Hsu, Walter H. Cyanidin Stimulates Insulin Secretion and Pancreatic β-Cell Gene Expression through
Activation of L-type Voltage-Dependent Ca2+ Channel.Nutrients.2017, 9,814-828
-
8. Sasaki R, Nishimura N, Hoshino H, Isa Y, Kadowaki M, Ichi T et al. Cyanidin 3-glucoside ameliorates hyperglycemia and insulin sensitivity due to downregulation of retinol binding protein 4 expression in diabetic mice. Biochemical Pharmacology. 2008;74(11):1619-1627.
-
9. De Ferrars R, Czank C, Zhang Q, Botting N, Kroon P, Cassidy A et al. The pharmacokinetics of anthocyanins and their metabolites in humans. British Journal of Pharmacology.
2014;171(13):3268-3282.
-
10. Wang Y, Sun T, Zhang Y, Chaurasiya B, Huang L, Liu X et al. Exenatide loaded PLGA microspheres for long-acting antidiabetic therapy: preparation, characterization, pharmacokinetics and pharmacodynamics. RSC Advances. 2016;6(44):37452-37462.
-
11. Makadia H, Siegel S. Poly Lactic-co-Glycolic Acid (PLGA) as Biodegradable Controlled Drug Delivery Carrier. Polymers. 2011;3(3):1377-1397.
-
12. Shi Y, Sun X, Zhang L, Sun K, Li K, Li Y et al. Fc-modified exenatide-loaded nanoparticles for oral delivery to improve hypoglycemic effects in mice. Scientific Reports. 2018;8(1).
-
13. Cyanidin [Internet]. Phytochemicals.info. 2019 [cited 2 January 2019]. Available from: http://www.phytochemicals.info/phytochemicals/ cyanidin.php
-
14. Amin F, Shah S, Badshah H, Khan M, Kim M. Anthocyanins encapsulated by PLGA@PEG nanoparticles potentially improved its free radical scavenging capabilities via p38/JNK pathway against Aβ1–42-induced oxidative stress. Journal of Nanobiotechnology. 2017;15(1).
-
15. Li M, Panagi Z, Avgoustakis K, Reineke J. Physiologically based pharmacokinetic modeling of PLGA nanoparticles with varied mPEG content. Int J Nanomedicine. 2012;7:1345–56.
-
16. Pridgen E, Alexis F, Kuo T, Levy-Nissenbaum E, Karnik R, Blumberg R et al. Transepithelial Transport of Fc-Targeted Nanoparticles by the Neonatal Fc Receptor for Oral Delivery. Science Translational Medicine. 2013;5(213):213ra167-213ra167.
-
17. Velioglu Y, Mazza G, Gao L, Oomah B.
Antioxidant Activity and Total Phenolics in
Selected Fruits, Vegetables, and Grain Products. Journal of Agricultural and Food Chemistry.
1998;46(10):4113-4117.
-
18. Zhishen J, Mengcheng T, Jianming W. The determination of flavonoid contents in mulberry and their scavenging effects on superoxide radicals. Food Chemistry. 1999;64(4):555-559.
-
19. Hoffman A. Corrigendum to “The early days of PEG, PEGylation (1970s–1990s)” [Acta Biomater. 40 (2016) 1–5]. Acta Biomaterialia.
2017;49:606.
-
20. Li W, Chen S, Zhou G, Li H, Zhong L, Liu S. Potential role of cyanidin 3-glucoside (C3G) in diabetic cardiomyopathy in diabetic rats: An in vivo approach. Saudi Journal of Biological Sciences. 2018;25(3):500-506.
-
21. Jeon S, Han S, Lee J, Hong T, Yim D. The Safety and Pharmacokinetics of Cyanidin-3-Glucoside after 2-Week Administration of Black Bean Seed Coat Extract in Healthy Subjects. The Korean
Journal of Physiology & Pharmacology. 2012;16(4):249.
-
22. Lawrence SA, Blankenship R, Brown R, Estwick S, Ellis B, Thangaraju A, et al. Influence of FcRn binding properties on the gastrointestinal absorption and exposure profile of Fc molecules. Bioorganic Med Chem [Internet]. 2021;32 (November 2020):115942. Available from: https://doi.org/10.1016/j.bmc.2020.115942
-
23. Rekha M, Sharma C. Oral delivery of therapeutic protein/peptide for diabetes – Future perspectives. International Journal of
Pharmaceutics. 2013;440(1):48-62.
-
24. Banerjee A, Lee J, Mitragotri S. Intestinal mucoadhesive devices for oral delivery of insulin. Bioengineering & Translational Medicine. 2016;1(3):338-346.
-
25. Shrestha N, Araújo F, Shahbazi M, Mäkilä E, Gomes M, Airavaara M et al. Oral hypoglycaemic effect of GLP-1 and DPP4 inhibitor based nanocomposites in a diabetic animal model. Journal of Controlled Release. 2016;232:113-119.
-
26. Kobes J, Daryaei I, Howison C, Bontrager J, Sirianni R, Meuillet E et al. Improved Treatment of Pancreatic Cancer With Drug Delivery Nanoparticles Loaded With a Novel AKT/PDK1 Inhibitor. Pancreas. 2016;45(8):1158-1166.
-
27. Yamaguchi S, Katahira H, Osawa S, Nakamichi Y, Tanaka T, Shimoyama T, et al. Activators of AMP-activated protein kinase enhance GLUT4 translocation and its glucose transport activity in 3T3-L1 adipocytes. Am J Physiol Endcrinol Metab 2015;289:E643-9
-
28. Kamal, R., Novendrianto, D., Chadijah, F., Prasetya, G., Pratama, G., Ariadnya, M., Larasati, N., Darain, N., Nanda, O., Mavita, S., Usamah, U. and Prajitno, J. (2017). DIABETES RISK FACTOR SCREENING IN ADULTS USING PERKENI QUESTIONNAIRE AND ORAL GLUCOSE TOLERANCE TEST IN SOCAH COUNTY, BANGKALAN. Folia Medica Indonesiana, 53(3), p.199.
26
Discussion and feedback