UJI AKTIVITAS EKSTRAK METANOL DAUN KEBIUL (Caesalpinia bonduc L.) SEBAGAI BAHAN AKTIF SEDIAAN TABIR SURYA
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 9 Nomor 2, Oktober 2021

UJI AKTIVITAS EKSTRAK METANOL DAUN KEBIUL (Caesalpinia bonduc L.) SEBAGAI BAHAN AKTIF SEDIAAN TABIR SURYA
Novita Sari*dan Dwi Fitri Yani
Program Studi Kimia, Fakultas Sains dan Teknologi, Universitas Islam Negeri Raden Fatah Palembang, Indonesia 30126
*E-mail: Novitasari.ns24@gmail.com
ABSTRAK: Penelitian ini bertujuan untuk menentukan aktivitas tabir surya dari nilai SPF (Sun Protection Factor) Aktivitas tabir surya ditentukan dengan Penentuan SPF dilakukan dengan metode Spektrofotometri Uv-Vis. Kandungan senyawa kimia ditentkan dengan uji fitokimia. Hasil penelitian menunjukkan bahwa nilai SPF yang diperoleh dari konsentrasi 200, 400, 600, 800, dan 1000 ppm berturut-turut yaitu sebesar 2,4 (proteksi minimal); 4,7 (proteksi sedang); 7,8 (proteksi ekstra); 9,2 (proteksi maksimal) dan 11,3 (proteksi maksimal). Berdasarkan uji fitokimia, ekstrak metanol daun kebiul positif mengandung flavonoid, tanin, steroid, dan saponin.
Kata Kunci : Daun Kebiul (Caesalpinia bonduc L.), tabir surya, SPF.
ABSTRACT: This study aims to determine the activity of sunscreen from the value of SPF (Sun Protection Factor). Sunscreen activity was determined by determining the SPF using the Uv-Vis Spectrophotometry method. The content of chemical compounds is determined by phytochemical tests. The results showed that the SPF values obtained from concentrations of 200, 400, 600, 800, and 1000 ppm were 2.4 (minimum protection); 4.7 (moderate protection); 7.8 (extra protection); 9.2 (maximum protection) and 11.3 (maximum protection). Based on the phytochemical test, the methanol extract of kebiul leaves was positive for flavonoids, tannins, steroids, and saponins.
Keywords: Kebiul (Caesalpinia bonduc L.) leaves, sunscreen, SPF.
Indonesia adalah negara beriklim tropis yang memiliki paparan sinar matahari yang tinggi [1]. Sinar matahari diperlukan oleh makhluk hidup untuk melakukan metabolisme dan menghasilkan energi. Namun paparan sinar matahari yang berlebih dan terus menerus dapat memberikan dampak buruk bagi kesehatan, terutama untuk sebagian besar penduduk yang bekerja diluar ruangan.
Radiasi sinar matahari terdiri atas sinar inframerah (>760 nm), sinar tampak (400-760 nm ), dan sinar UV (ultraviolet) yang terdiri atas UV A (320-400 nm) UV B (290-320 nm) dan UV C (200-290 nm [2]. Sinar UV A dan UV B akan sampai kepermukaan bumi dan memberikan
dampak negatif terhadap kulit [3]. Seperti kemerahan (eritema), noda hitam (pigmentasi), penuaan dini, kulit kering, keriput, dan kanker kulit [4].
Kanker kulit merupakan salah satu kanker yang paling umum didiagnosis di seluruh dunia. Badan Kesehatan Dunia (WHO) memperkirakan ada sekitar 2 juta kasus kanker kulit baru setiap tahunnya. Berdasarkan data RISKESDAS 2018 di Indonesia kanker kulit menempati urutan ke-4 dari 10 jenis kanker terbanyak setelah kanker leher rahim [5].
Secara alamiah manusia telah memiliki sistem perlindungan terhadap sinar UV (ultraviolet) yaitu penebalan stratum korneum dan pigmentasi kulit. Namun sistem pertahanan alamiah tersebut
tidak cukup untuk menahan paparan sinar UV yang berlebihan [6]. Sehingga diperlukan suatu perlindungan tambahan yaitu dengan pemakaian tabir surya [7].
Tabir surya merupakan zat yang megandung bahan pelindung kulit terhadap sinar matahari sehingga sinar UV tidak dapat memasuki kulit (mencegah gangguan kulit karena radiasi sinar). Tabir surya mengandung senyawa kimia yang dapat mengabsorpsi dan memantulkan sinar UV dengan cara menyebarkan sinar matahari atau menyerap energi radiasi matahari yang mengenai kulit, sehingga energi radiasi tersebut tidak langsung mengenai kulit [8].
Efektivitas tabir surya didasarkan pada penentuan nilai SPF (Sun Protected Factor) yang menggambarkan kemampuan produk tabir surya dalam melindungi kulit dari eritema [9]. Untuk melindungi kulit dari eritema dikembangkan tabir surya, namun pengembangan tabir surya biasanya menggunakan bahan aktif kimia sintetik [10]. Bahan aktif sintetik pada tabir surya seperti avobenzone, oxybenzone, dan octocrylene dilaporkan telah menimbulkan beberapa dampak negatif, seperti reaksi alergi maupun reaksi toksisitas ringan, bahkan sampai menimbulkan kanker kulit [11]. Oleh karena itu dibutuhkan bahan aktif sediaan tabir surya alami yang diyakini aman dan minim efek samping. Salah satu bahan alam yang berpotensi dijadikan sebagai tabir surya alami adalah daun kebiul (Caesalpinia bonduc L.).
Tumbuhan kebiul (Caesalpinia bonduc L.) banyak ditemukan di daerah Bengkulu tepatnya di kabupaten Bengkulu Selatan. Tumbuhan Kebiul (Caesalpinia bonduc L.) masih memiliki habitat alami di hutan dan juga ada yang tumbuh liar di perkebunan masyarakat yang tidak terawat [12]. Analisis fitokimia Caesalpinia bonduc L mengandung senyawa metabolit sekunder yaitu tanin, flavonoid, saponin, steroid, dan terpenoid [13].
Senyawa metabolit sekunder tersebut diduga merupakan senyawa yang memiliki potensi aktivitas tabir surya karena adanya gugus kromofor (ikatan
rangkap tunggal terkonjugasi) yang mampu menyerap sinar UV baik UV A maupun UV B sehingga mengurangi intensitasnya pada kulit [14].
Bahan yang digunakan pada penelitian ini adalah daun kebiul (Caesalpinia bonduc L.), metanol, kloroform, reagen Meyer, bubuk Mg, larutan HCl pekat, larutan FeCl3 1%, larutan H2SO4 pekat, etanol 96%, pereaksi Lieberman Burchard, dan akuades.
Alat yang digunakan pada penelitian ini adalah, beaker glass (iwaki), tabung reaksi (iwaki), rak tabung, labu ukur (pyrex), gelas ukur (pyrex), kuvet, pipet tetes, neraca analitik (pioneer), batang pengaduk (pyrex), spatula,corong kaca (pyrex), spektrofotometer UV-Vis (biochrom libra S12) dan rotary evaporator (yamato Re 301).
Daun kebiul (Caesalpinia bonduc L.) diambil dari Kabupaten Bengkulu Selatan. Daun kebiul yang telah diambil dicuci dengan air mengalir kemudian diangin-anginkan. Daun kebiul yang telah kering lalu dihaluskan dengan menggunakan blender, setelah itu diayak lalu diperoleh serbuk simplisia daun.
Ekstraksi Sampel
Metode ekstraksi yang digunakan dalam penelitian ini adalah maserasi. Diambil simplisia sebanyak 353 g lalu ditimbang kemudian dimasukan ke dalam wadah, selanjutnya serbuk simplisan di rendam dalam metanol teknis 96% dalam wadah sampai semua sampel tertutup pelarut. Kemudian disimpan ditempat yang terlindung dari cahaya selama 1x24 jam. Perlakuan dilakukan sebanyak 3x pengulangan. Ekstrak yang diperoleh diuapkan menggunakan rotary evaporator pada suhu 40º C hingga diperoleh ekstrak
metanol kental. Kemudian ekstrak pekat di hitung rendemen dan dilanjutkan ke pengukuran dengan UV-Vis.
Identifikasi senyawa metabolit sekunder daun Caesalpinia bonduc L.
Uji Flavonoid
Sejumlah ekstrak dimasukkan ke dalam tabung reaksi. Serbuk magnesium 2 mg ditambahkan dan diberikan 3 tetes HCl pekat. Sampel dikocok dan diamati perubahan yang terjadi, terbentuknya warna merah, kuning atau jingga pada larutan menunjukkan adanya flavonoid [15].
Uji Alkaloid
Sebanyak 3 tetes ekstrak dimasukkan ke dalam tabung reaksi, kemudian ditambahkan 3 tetes asam klorida pekat dengan pereaksi Meyer dan diamati selama beberapa menit, hasil uji dinyatakan positif jika terbentuk warna kuning atau jingga [16].
Uji Tanin
Ekstrak dilarutkan dengan 20 mL air lalu ditambahkan beberapa tetes FeCl3 1%, warna hijau tua menunjukkan uji positif tanin [16].
Uji Terpenoid
Ekstrak dimasukkan sebanyak 3 tetes pada papan tetes, ditambahkan 2 mL etanol, 2 mL kloroform, dan 3 mL asam sulfat. Uji positif terpenoid ditandai dengan terbentuknya warna merah [16].
Uji Steroid
Ekstrak dimasukkan sebanyak 3 tetes pada papan tetes ditambahkan dengan reagen Lieberman Burchard sebanyak 2 tetes dan 1 tetes asam sulfat. Uji positif adanya steroid pada larutan dengan perubahan warna menjadi coklat [16].
Uji Saponin
Ekstrak dimasukkan ke dalam tabung reaksi dan ditambahkan 20 mL akuades yang mendidih, kemudian disaring. Filtrat
dikocok selama 15 menit. Terbentuknya lapisan busa setinggi 2 cm mengidentifikasi adanya saponin [15].
Pembuatan Larutan Uji
Ekstrak metanol daun kebiul (Caesalpinia bonduc L.) diambil sebanyak 0,0025 mg, diencerkan dengan metanol sampai tanda batas dalam labu ukur 25 mL sehingga didapatkan larutan ekstrak metanol dengan konsentrasi 1000 ppm. Larutan ekstrak metanol konsentrasi 1000 ppm diencerkan lagi dengan masing-masing konsetrasi 200; 400; 600; dan 800 ppm. Kemudian dilakukan penentuan nilai SPF, menggunakan spektrofotometer UV-Vis.
Penentuan Nilai Sun Protection Factor ( SPF)
Penentuan nilai SPF dengan spektrofotometer UV-Vis. Spektrofotometer UV-Vis di kalibrasi dengan metanol 96% dengan cara metanol 96% sebanyak 3 mL dimasukkan kedalam kuvet, kemudian kuvet tersebut dimasukkan dalam spektrofotometer Uv-Vis untuk proses kalibrasi.
Ekstrak yang telah dibuat dengan masing-masing konsentrasi untuk larutan uji dimasukkan ke dalam kuvet sebanyak 3 mL. Kurva serapan uji dibuat dengan panjang gelombang antara 290 – 320 nm. Metanol 96% digunakan sebagai blanko. Pengukuran nilai SPF dilakukan dengan mengukur serapan sediaan pada spektrofotometer setiap 5 nm pada rentang panjang gelombang dari 290 – 320 nm, nilai SPF dihitung dengan persamaan matematika yang sangat sederhana dengan menggunakan persamaan berikut :
SPFspectro = CF ×∑290 ЕЕ(λ) × I(λ) × Abs (λ)
dimana CF adalah faktor koreksi dengan nilai sebesar 10, EE adalah erythermal effect, I adalah intensitas sinar matahari, dan Abs adalah absorbansi ekstrak.
Daun kebiul dipreparasi dengan cara dicuci bersih kemudian dikeringkan. Pengeringan dilakukan dengan cara diangin-anginkan tanpa terkena sinar matahari langsung, fungsinya adalah agar kandungan senyawa aktif yang ada pada sampel tetap terjaga dengan baik dan tidak rusak karena panas dan suhu yang tinggi.
Metode ekstraksi yang digunakan adalah metode maserasi dengan 3 kali pengulangan (remaserasi). Proses remaserasi dilakukan untuk mengoptimalisasi proses ektraksi pelarut dalam mengikat senyawa yang terkadung dalam sampel. Metode maserasi dipilih karena metode ini tidak memerlukan peralatan yang rumit, relatif murah dan dapat menghindari penguapan komponen senyawa kimia karena tidak menggunakan panas, sehingga dapat menghindari rusaknya senyawa-senyawa yang bersifat termolabil [17].
Pelarut metanol dipilih karena metanol memiliki titik didih yang lebih rendah sehingga lebih mudah diuapkan [18]. Sampel dipekatkan dan diuapkan menggunakan rotary evaporator, penguapan dilakukan agar pelarut yang digunakan tidak tersisa sehingga pelarut tidak mempengaruhi efektifitas dari sampel yang diuji. Ekstrak metanol didapatkan rendemen total seperti Tabel 1.
|
Tabel 1. |
Rendemen Kebiul |
Ekstrak Metanol Daun | |
|
Berat Simplisia (g) |
Berat Ekstrak Kental (g) |
Rendemen (%) |
Warna Ekstrak |
|
353 |
55 |
15,58 |
Hijau pekat |
Kandungan senyawa di dalam sampel dapat ditentukan dengan uji fitokimia. Skrining fitokimia dilakukan untuk memberikan gambaran tentang golongan senyawa yang terkandung dalam sampel
-
[19] . Hasil uji fitokimia dapat dilihat pada Tabel 2.
Hasil skrining fitokimia ekstrak daun Kebiul (Caesalpinia bonduc L.) yang diperoleh dalam penelitian ini
menunjukkan bahwa senyawa flavonoid, tanin, steroid, saponin dapat tertarik dalam pelarut metanol. Hal ini disebabkan karena metanol memiliki gugus (-OH) dan gugus (-CH3) yang bisa mempengaruhi kepolaran dari pelarut metanol sehingga dapat menarik senyawa yang bersifat polar maupun nonpolar.
Tabel 2. Kandungan Fitokimia Ekstrak
Daun kebiul (Caesalpinia bonduc L.).
|
Golongan Senyawa |
Hasil Uji |
Uji Positif |
|
Flavonoid |
(+++) Berwarna jingga |
Berwarna Kuning/ jingga |
|
Terpenoid |
(-) Tidak ada perubahan warna |
Berwarna merah |
|
Tanin |
(+++) Berwarna hijau kehitaman |
Hijau Tua /Kehitaman |
|
Steroid |
(+++) Berwarna cokelat |
Berwarna Cokelat |
|
Alkaloid |
(-) Berwarna cokelat |
Berwarna Kuning/ jingga |
|
Saponin |
(+++) Terdapat buih atau busa berwarna putih |
Terbentuk Busa |
Keterangan : (+) uji positif; (-) uji negatif
Aktivitas tabir surya dapat diketahui berdasarkan nilai Sun Protection Factor (SPF). SPF menyatakan lamanya kulit mampu dilindungi oleh tabir surya di bawah sinar matahari yaitu dalam waktu 10 menit per satu nilai SPF [20]. Nilai SPF ekstrak methanol daun kebiul disajikan pada Tabel 3.
Berdasarkan pengukuran rata-rata nilai SPF yang disajikan pada angka tabel diatas menunjukkan bahwa ekstrak metanol memiliki aktivitas tabir surya yang paling baik pada konsentrasi 1000 ppm dan tergolong proteksi maksimal (nilai SPF 815) sebesar 11,3 diikuti oleh konsentrasi 800 ppm pada proteksi yang sama. Pada konentrasi 600 ppm tergolong proteksi ekstra dengan nilai SPF sebesar 7,8 pada konsentrasi 400 tergolong pada proteksi sedang dengan nilai SPF 4,7 dan pada konsentrasi 200 ppm tergolong proteksi minimal dengan nilai SPF yang paling rendah diantara konsentrasi yang lain yaitu sebesar 2,4.
Tabel 3. Nilai SPF Ekstrak Metanol Daun
Kebiul
|
Konsentrasi ekstrak (ppm) |
Nilai SPF |
Tipe Proteksi |
|
200 |
2,4 |
Proteksi minimal |
|
400 |
4,7 |
Proteksi sedang |
|
600 |
7,8 |
Proteksi |
|
ekstra | ||
|
800 |
9,2 |
Proteksi maksimal |
|
1000 |
11,3 |
Proteksi maksimal |
Menurut More et al. [21] salah satu faktor yang mempengaruhi penentuan nilai SPF yaitu konsentrasi dari tabir surya, dimana faktor ini dapat menambah atau mengurangi penyerapan UV pada setiap tabir surya. Hal ini menunjukkan bahwa seiring bertambahnya konsentrasi, maka daya proteksi terhadap sinar UV juga semakin tinggi. Dengan demikian, hal ini sesuai dengan hasil yang diperoleh, dimana dapat dilihat pada Gambar 1. Berdasarkan grafik dari pengujian dapat dilihat bahwa semakin tinggi konsentrasi maka semakin tinggi nilai SPF nya, seiring peningkatan konsentrasi maka fungsi perlindungan terhadap sinar UV juga semakin besar dan semakin efektif aktivitas tabir surya nya [22]. Tabir Surya yang memiliki nilai Sun Protection Factor (SPF) lebih dari 2 mampu melindungi kulit kita dari paparan
sinar UV [23]. Sehingga penelitian ini menyatakan bahwa ekstrak daun kebiul memiliki potensi tabir surya karena terbukti mempunyai aktivitas dan nilai SPF yang cukup tinggi.
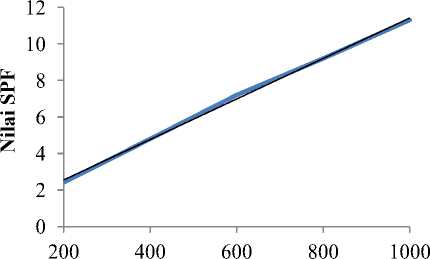
Konsentrasi ekstrak (ppm)
Gambar 1. Grafik hubungan SPF dengan konsentrasi ekstrak
Ekstrak daun kebiul memiliki aktivitas sebagai tabir surya karena mengandung senyawa kimia (Chemical sunscreen) yang bekerja dengan cara mengabsorbsi radiasi sinar UV. Kemampuan menghambat gelombang tertentu dari cahaya matahari menyebabkan sunscreen dapat berperan sebagai filter penyaring dan mengurangi radiasi cahaya matahari pada panjang gelombang tertentu [9].
Secara umum semua ekstrak aktif sebagai tabir surya, hal ini disebabkan oleh adanya senyawa metabolit sekunder. Senyawa metabolit sekunder yang dapat berperan sebagai tabir surya antara lain adalah flavonoid dan tanin [24]. Tanin merupakan polifenol yang memiliki aktivitas antioksidan kuat yang dapat melindungi kerusakan terhadap radikal bebas yang disebabkan oleh paparan sinar UV, sehingga mengurangi resiko kanker kulit dan penuaan dini. Tanin mampu mengurangi produksi H2O2 menghambat induksi ornitin dekarboksilase dan menstimulasi sintesis DNA pada epidermis kulit. Menurut Hagerman [25] tanin efektif sebagai pendonor elektron/atom hidrogen karena senyawa ini memiliki gugus hidroksil dan ikatan rangkap terkonjugasi
yang memungkinkan terjadinya
delokalisasi elektron.
Flavonid tergolong senyawa fenol (C6H5OH) dimana yang mendasari semua golongan dari senyawa tersebut berupa cincin aromatik benzena [26]. Senyawa flavonoid ini memiliki ikatan yang saling berkonjugasi dalam inti benzena dimana saat terkena sinar UV akan terjadi resonansi dengan cara transfer elektron. Adanya kesamaan sistem konjugasi pada senyawa kimia yang biasanya terkandung didalam tabir surya menyebabkan senyawa-senyawa ini berpotensi sebagai bahan aktif tabir surya.
Berdasarkan hasil penelitian yang dilakukan nilai SPF ekstrak metanol daun kebiul (Caesalpinia bonduc L.) yang di dapatkan pada konsentrasi 200, 400, 600, 800 dan 1000 ppm yaitu sebesar 2,4; 4,7; 7,8; 9,2; dan 11,3. Ekstrak metanol daun kebiul (Caesalpinia bonduc L.) memiliki potensi sebagai tabir surya dengan proteksi maksimal dan dapat dijadikan sebagai zat aktif dalam pembuatan sediaan tabir surya.
-
[1] Yulianti, E., Adelsa, A., Putri, A. 2015. Penentuan nilai SPF (sun protection factor) ekstrak etanol 70% temu mangga (Curcuma mangga) dan krim ekstrak etanol 70% temu mangga (Curcuma mangga) secara in vitro menggunakan metode
spektrofotometri. Majalah Kesehatan FKUB, 2(1): 41-50.
-
[2] Matts, P.J. 2006. Solar ultraviolet radiation: definitions and terminology. Dermatologic clinics: 24 (1): 1-8.
-
[3] Wang, S.Q. Stanfield, J.W. and Osterwalder, U. 2008. In Vitro Assessment of UV A Protection by Populer Sunscreen Available in The United States, J. Am. Dermatology. 59(6): 934-42.
-
[4] Tranggono, R.I. dan Latifah F. 2007, Buku Pegangan Ilmu Pengetahuan Kosmetik, Jakarta: PT. Gramedia
Pustaka: 12: 26-30, 48, 81-86.
-
[5] Laporan Nasional RISKESDAS 2018. Badan Penelitian dan Pengembangan Kesehatan Kementerian Kesehatan RI.
-
[6] Wilkinson, J. B. dan Moore, R. J., 1984, Harry’s Cosmeticology, 7th Ed., Chemical Publishing Company, 223224, 236.
-
[7] Sahasrabuddhe, H.S. 2011. Lycopene: an antioxidant. Pharma Times, 43 (12): 13-14.
-
[8] Rai, R., Shanmuga, S.C., and Srinivas, C. 2012. Update on Photoprotection. Indian Journal of Dermatology, 57(5): 335–342.
-
[9] Stanfield, J.W. 2010, Sun Protectans: Enhancing Product Functionality with Sunscreen, in Schueller, R. and
Romanowski, P. Multifunctional
Cosmetic, Marcell Dekker Inc, New York, USA.
-
[10] Garoli, D., Pelizzo, M.G., Nicolossi, P., Peserico, Tonin, E. and Alaibac, M. 2009. Effectiveness of different substrate materials for in vitro sunscreen test. J. of Dermatological Science, 56(2): 89-98.
-
[11] Brezova, V., Gabcova, S., Dvoranova, D., Stasko, A. 2005. Reactive Oxygen Spesies Produced Upon
Photoexcitation of Sunscreens
Containing Titanium. Dioxide (an EPR Study), Journal of Photochemistry and Photobiology B: Biology, 79: 121-134.
-
[12] Muryati, T. S. 2019. Pengembangan E-Modul KOBA Berbasis Penelitian Sintesis Nanopartikel Lemak Padat Minyak Sawit Merah Ekstrak Caesalpinia bonduc L Terhadap
Penurunan Jumlah P . Berghei, Tesis, Fakultas Keguruan dan Ilmu Pendidikan Universitas Bengkulu.
-
[13] Ogunlana, O.O. Ogunlana, O.E., Ntube, C.A., Olagunju,
J.A., and Akindahunsi,
A.A. 2012. Phytochemical Screening and in vivo antioxidant activity of Ethanolic extract of Caesalpinia bondus (L.) Roxb. Global R J Pharm Sci., 1(1): 1-4.
-
[14] Walters, C. Keeney, A., Wigal, C.T., Johnston, C.R., and Cornelius, R.D. 1977. The Spectrophotometric
Analysis and modelling of sunscreens. J. Chem. Educ. 74(1): 99-109.
-
[15] Purwati, S., Lumora, S.V.T., dan Samsurianto, 2017. Skrining Fitokimia Daun Saliara (Lantara camara L) sebagai Pestisida Nabati Penekan Hama dan Insidensi Penyakit Pada Tanaman Holtikultura di Kalimantan Timur” Prosiding Seminar Nasional Kimia: 153-158.
-
[16] Asmara, A. P. 2017. Uji Fitokimia Senyawa Metabolit Sekunder Dalam Ekstrak Metanol Bunga Turi Merah (Sesbania grandiflora L. Pers), Al-Kimia, 5 (1): 48-59.
-
[17] Tetti, M. 2014. Ekstraksi, pemisahan Senyawa, dan Identifikasi Senyawa Aktif. Jurnal Kesehatan. 7(2): 361
367.
-
[18] Astarina. N.W.G., Astuti, K.W. Warditiani, N. K. 2013. Skrining Fitokimia Ekstrak Metanol Rimpang Bangle (Zingiber purpureum roxb.). Jurnal Farmasi Udayana, 2(4): 1-6.
-
[19] Kristanti, A. N., Aminah, N. S. Tanjung, M. dan Kurniadi. B. 2008. Buku Ajar Fitokimia. Airlangga University Press.Surabaya: Hal. 23, 47.
-
[20] Shovyana, H.H., & Zulkarnain, A.K. 2013. Stabilitas Fisik dan Aktivitas Krim W/O Ekstrak Etanolik Buah Mahkota Dewa (Phaleria
macrocarpha) Sebagai Tabir Surya. Trad. Med. J., 18(2): 109-117.
-
[21] More, B.H., Sakharwade, S., Thembrune S., and Sakarkar D. 2013.
Evaluation of Sunscreen Activity of Cream Containing Leaves Extract of Butea monosperma for Topical Application. International Journal of Research in Cosmetic Science, 3(1): 16.
-
[22] Draelos, Z.D. and Thaman, L.A. 2006, Cosmetic Formulation of Skin Care Products, Volume 2. Taylor and Francis Group, New York. 157-159.
-
[23] Daun, N.S., La Ode, Z.A.H., dan Ervianingsih. 2016. Formulasi Lotion Tabir Surya Ekstrak Etanol Beras Merah. Kendari, Jurnal Ilmiah Ibnu Sina, 1(2), 143-150.
-
[24] Svobodová, A., Psotová, J., and Walterová. D. 2004. Natural phenolic inthe prevention of UV-induced skin damage, a review. J. Biomed. Papers, 147 (2):137-145.
-
[25] Hagerman, A.E., Riedl, K.M., Jones, G.A., Sovik, K.N., Ritchard, N.T., Hartzfeld, P.W., and Riechel, T.L. 1998. High molecular weight plant polyphenolics (tannins) as biological antioxidants. J. of Agricultural and Food Chemistry, 46(5): 1887-1892.
-
[26] Prasiddha, I. J., Laellocattleya, RA., Estiasih, T., Maligan, J.M. 2016. Potensi Senyawa Bioaktif Rambut Jagung Untuk Tabir Surya Alami: KajianPustaka. Jurnal pangan dan argoindustri, 4(1): 40-45.
74
Discussion and feedback