PEMANFATAAN CANGKANG TELUR AYAM SEBAGAI MATERIAL DASAR DALAM SINTESIS HIDROKSIAPATIT DENGAN METODE PRESIPITASI BASAH
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 9 Nomor 1, Mei 2021
PEMANFATAAN CANGKANG TELUR AYAM SEBAGAI MATERIAL DASAR DALAM SINTESIS HIDROKSIAPATIT DENGAN METODE
PRESIPITASI BASAH
Jumilah Gago1*, Yulius Dala Ngapa2
-
1 Program Studi Pendidikan Biologi, Fakultas Keguruan dan Ilmu Pendidikan - Universitas Flores, Jl. Sam Ratulangi Ende-Flores, Indonesia, 86319
-
2 Program Studi Pendidikan Fisika, Fakultas Keguruan dan Ilmu Pendidikan - Universitas Flores, Jl. Sam Ratulangi Ende-Flores, Indonesia, 86319
ABSTRAK: Sintesis hidroksiapatit (HAp) dari cangkang telur ayam melalui proses presipitasi basah telah berhasil dilakukan. Tujuan dari penelitian ini adalah untuk mendapatkan kondisi proses yang optimal dan juga untuk mengetahui pengaruh rasio mol Ca/P dan suhu sintesis terhadap karakteristik HAp. Bubuk cangkang telur ayam dikalsinasi untuk mendapatkan CaO yang kemudian direaksikan dengan diammonium hidrogen fosfat dengan menggunakan air sebagai pelarut. Proses presipitasi dilakukan dengan sistem tertutup untuk menghindari terjadinya pelarut hilang saat pemanasan di atas titik didih pelarut. Sampel kemudian diambil untuk dikarakterisasi dengan menggunakan FTIR (Fourier Transform Infrared), XRD (X-Ray Diffraction), dan SEM (Scanning Electron Microscopy). Kelompok fungsional diamati di FTIR HAp yang disintesis adalah fosfat (PO43-), hidroksil (OH-), karbonat (CO32-), dan hidrogen fosfat (HPO42-). Kelompok fungsional ini menunjukkan bahwa HAp telah terbentuk. Data XRD menunjukkan puncak utama untuk HAp yang memperkuat kebenaran karakterisasi FTIR. SEM digunakan untuk mengamati morfologi HAp hasil sintesis yang terdiri dari aglomerat. Kondisi terbaik dalam sintesis ini terjadi pada perbandingan mol Ca/P sebesar 1,60 pada suhu 160oC
Kata kunci: Cangkang telur ayam, hidroksiapatit, presipitasi basah
ABSTRACT: Synthesis of hydroxyapatite (HAp) from eggshell by precipitation method has been successfully done. The aim of this research was to get the optimum process condition and also to investigate the influence of the Ca/P mole ratio andthe synthesis temperature toward HAp characteristic. The powder of eggshell was calcined to get CaO which then was reacted with diammonium hydrogen phosphate by using water as solvent. Precipitation process was done by closed system in order to avoid the solvent be lost while heating up above the solvent’s boiling point. The samples then were characterized by using FTIR (Fourier Transform Infrared), XRD (X-Ray Diffraction), and SEM (Scanning Electron Microscopy). The functional groups were observed in the FTIR of the synthesized HAp are phosphate (PO43-), hydroxyl (OH-), carbonate (CO32-), and hydrogen phosphate (HPO42-). These functional groups indicate that HAp has been formed. XRD data showed the main peaks for HAp that strenghtened the truth of FTIR characterization. SEM was used to observe the morphology of the synthesized HAp that consisted of agglomerates. The best conditions in this synthesis occured at Ca/P mole ratio of 1,60 and the synthesis temperature of 160oC.
Keywords: eggshell, hydroxyapatite, precipitation
Penggunaan material sebagai implan di dalam maupun di luar tubuh manusia merupakan hal yang telah lama dikenal dalam dunia kesehatan. Pemanfaatan material asing tersebut dalam kurun waktu 10-20 tahun terakhir ini menunjukkan perkembangan yang cukup pesat. Material polimer yang digunakan hanya dapat menggantikan suatu organ, tetapi akan menghambat pertumbuhan jaringan tulang [1]. Oleh karena itu dibutuhkan suatu material pengganti tulang yang harus memiliki sifat biokompatibel, bioaktif, biodegradasi, dan tidak mengandung racun bagi jaringan tubuh [2].
Hidroksiapatit (HAp) merupakan salah satu biomaterial yang memenuhi syarat sebagai material pengganti tulang yang baik. Biomaterial merupakan suatu bahan sintesis yang dapat diimplan ke dalam sistem hidup sebagai fungsi dari jaringan hidup atau organ [3]. Hidroksiapatit telah dipelajari selama bertahun-tahun dan telah digunakan secara luas untuk implan karena terbukti biokompatibel dengan tulang dan gigi manusia [4]. HAp merupakan anggota dari mineral apatit dengan rumus kimia Ca10(PO4)6(OH)2. Struktur kimia tersebut sama dengan struktur kimia yang dimiliki komponen mineral pada tulang. Kesamaan stuktur inilah yang menyebabkan tingginya kebutuhan akan biomaterial ini, sintesis HAp menjadi suatu hal yang cukup bermanfaat untuk dilakukan [5].
Potensi limbah cangkang telur di Ende – Nusa tenggara Timur cukup tinggi karena telur merupakan salah satu sumber protein untuk masyarakat. Cangkang telur ayam tidak dapat diuraikan oleh mikroba tanah, sehingga akan berdampak pada menigkatnya pencemaran lingkungan. Cangkang telur ayam mengandung CaCO3 yang tinggi yanitu sebesar 94% sehingga berpotensi sebagai starting material untuk sintesis biomaterial [6]. Di Indonesia, dikenal dua jenis telur ayam yaitu telur ayam kampung dan telur ayam ras. Perbedaan pakan antara ayam ras dan ayam kampung diduga berpengaruh terhadap
kandungan cangkang telurnya. Oleh karena itu, perlu diamati hidroksiapatit yang berasal dari telur ayam kampung dan ayam ras.
Hidroksiapatit dapat disintesis dengan berbagai metode yaitu: metode kering, metode basah (presipitasi), dan metode hidrotermal [7]. Metode basah (presipitasi) merupakan metode sintesis HAp yang umum digunakan karena sederhana dan dapat menghasilkan HAp yang sebagian besar amorf. Keuntungan lain, hasil samping sintesisnya adalah air sehingga kemungkinan kontaminasi selama
pengolahan sangat rendah [8]. Pada penelitian ini digunakan cangkang telur ayam kampung dan ayam ras dan K2HPO4 sebagai sumber fosfat dalam sintesis HAp. Berdasarkan latar belakang di atas maka tujuan dari penelitian ini adalah mensintesis HAp dari cangkang telur ayam dan menentukan kadar kalsium fosfat yang terkandung dalam senyawa HAp hasil sintesis kedua cangkang telur ayam tersebut.
Bahan yang digunakan adalah cangkang telur ayam, aquades, dan H3PO4. Alat yang digunakan adalah cawan porselain, alat gelas yang biasa digunakan di laboratorium kimia, pemanas listrik, magnetik stirrer, termometer, buret, statip, dan neraca analitik. Untuk menentukan kadar kalsium dalam cangkang kerang dengan menggunakan AAS SHIMADZU AA-7000. Untuk karakterisasi
hidroksiapatit dilakukan dengan
Spektrofotometer FTIR Simadzu IR Prestige-21, SEM, EDXA, dan XRD Shimadzu 7000.
Preparasi sampel dimulai dengan pembersihan cangkang telur dari kotoran yang menempel dengan air kemudian dikeringkan di udara terbuka sampai cangkang benar-benar kering. Setelah
cangkang kering, dilakukan proses kalsinasi yang bertujuan untuk memperoleh kalsium dari cangkang lokan tersebut. Kalsinasi dilakukan sesuai dengan Dahlan et al. 2009. Kalsinasi dilakukan pada suhu 900°C selama 6 jam. Setelah proses kasinasi, sampel dihaluskan dengan mortal dan diayak selanjutnya dilakukan uji kadar kalsium dengan AAS. Uji kadar kalsium dilalukan untuk mengetahui besarnya kalsium yang terkandung didalam cangkang.
Uji kadar kalsium diidentifikasi dengan dengan menggunakan AAS. Sebanyak 0,1 gram sampel serbuk cangkang kerang lokan hasil kalsinasi 900°C dilarutkan dengan 5 mL HCl 37% lalu dimasukkan kedalam labu takar 100 mL dan ditera dengan air bebas ion. Sebanyak 1 mL larutan sampel dimasukkan kedalam labu takar 100 mL dan ditera dengan air bebas ion. Blanko dibuat dari 5 mL HCl 37% yang ditera dengan air bebas ion. Panjang gelombang yang digunakan adalah 422,5 nm dengan flame yang digunakan adalah etilen.
Sintesis Hidroksiapatit
Suspensi Ca(OH)21M dibuat dengan cara ditimbang sebanyak 18,5195 g serbuk Ca(OH)2 dan ditambahkan dengan 500 mL air bebas ion. Larutan H3PO40,6M dibuat dengan mengencerkan larutan H3PO4 85%.
Sintesis hidroksiapatit dilalukan berdasarkan modifikasi metode Santos et al. (2004). Sebanyak 500 mL larutan H3PO40,6 M di dalam buret diteteskan dengan kecepatan 6 ml/menit ke dalam gelas piala berisi 500 ml suspensi Ca(OH)2 1 M pada suhu 40 ± 2 °C sambil diaduk konstan, pH dimonitor namun tidak dikoreksi. Campuran yang terbentuk didiamkan selama 1 malam dan disonikasi menggunakan alat ultrasonik dengan variasi waktu 6 jam. Kemudian disentrifugasi dua kali dengan kecepatan 4500 rpm selama 15 menit. Endapan yang diperoleh lalu dikeringkan dalam oven suhu 105°C selama 3 jam, dimasukkan ke dalam tanur
suhu 900°C selama 2 jam. Sampel digerus hingga berbentuk serbuk halus dan dimasukkan ke dalam desikator.
Karakterisasi hidroapatit dengan XRD
Sebanyak 2 gram sampel dimasukkan dalam holder yang berukuran (2 x 2) cm2 pada difraktometer.Pengukuran dilakuka dengan sudut awal diambil pada 50 dan sudut akhir pada 1000 dengan kecepatan baca 20 per menit.
Karakterisasi dengan FTIR
0,2 mg sampel dibuat pellet dengan menambahkan 202 mg KBr kemudian dianalisis dengan IR dengan bilangan gelombang 4000-400 cm-1.
Karakterisasi dengan SEM dan EDXA
Sampel diletakkan pada lempeng aluminium yang memiliki 2 sisi.Kemudian dilapisi dengan logam platina selama 50 detik. Analisis dilakukan pada tegangan 20 kV dengan perbesaran 1.000X, 5.000X,
10.000X, dan 20.000X.
Proses kalsinasi Cangkang telur dilakukan pada suhu 1000 oC berfungsi untuk menguraikan CaCO3 menjadi CaO dan gas CO2. Panas dari tanur membuat ikatan kimia menjadi renggang dan atom yang berikatan bergerak bebas. Pada suhu 850 sampai 1000 oC ikatan kimia pada CaCO3 terputus membentuk CaO [9]. Persamaan reaksi pada proses kalsinasi: CaO(s) + CO2(g) →CaCO3(s)
Penurunan massa cangkang telur selama kalsinasi disebabkan pelepasan gas CO2 dan penguraian senyawa organik [10]. Komponen organik dari Cangkang telur yang hilang selama proses kalsinasi dapat berasal dari protein. Protein pada cangkang telur adalah mukopolisakarida yang terdiri dari kondrotin sulfat A dan B, glukosamin, galaktosamin, galaktosa, manosa, dan asam sialat [11]. Komponen lain pada Cangkang telur adalah MgCO3 sebesar 1% MgCO3
yang dikalsinasi pada suhu 800 sampai 900 oC akan membentuk MgO disertai pelepasan CO2. Setelah suhu MgO turun, MgO dapat bereaksi dengan air di udara membentuk Mg(OH)2. Sampel CaO dari cangkang telur ayam didominasi fasa CaO karena adanya puncak pada 37,383o [12]. Adanya puncak CaO didukung beberapa puncak lain yang bersesuaian dengan database Joint Committee on Powder Diffraction Standards (JCPDS). Puncak tersebut = 32,220o ditunjukkan pada sudut 2θ ; 37,383o ; 53,904o ; 64,187o ; 67,396o ; 79,671o ; 88,547o ; dan 91,482o [13]. Fasa lain pada CaO dari cangkang telur ayam adalah Ca(OH)2 yang bersesuian dengan data standar JCPDS . Fasa Ca(OH)2 pada sudut 18,029o , 28,669o , dan 34,138o sesuai dengan JCPDS no. 84-1263 [14]. Puncak-puncak ini memiliki intensitas yang lebih kecil dibandingkan dengan fasa CaO. Difraktogram CaO hasil kalsinasi dibandingkan dengan CaO standar untuk memperkuat bahwa yang dihasilkan merupakan fasa CaO [15]. Hasil analisis fasa kristal dengan menggunakan XRD diperoleh bahwa hidroksiapatit hasil sintesis pada suhu sintering 900oC mempunyai fasa utama hidroksiapatit dengan derajat kristalinitas 95,15 [16].

Gambar 1. Difraktogram CaO Dari
Cangkang Telur dan CaO Standar
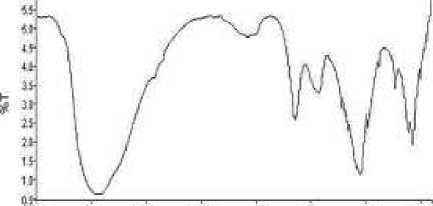
Pada hasil FTIR Hap pada Gambar 2 terdapat gugus fungsional utama milik HA yaitu gugus OHdan PO43- . Ikatan gugus fosfat (PO43- ) paling kuat pada HA dengan vibrasi stretching terdapat pada 1000-1050
370 cm-1 dan medium pada bilangan gelombang 960 cm-1 serta vibrasi bending diamati pada 560-610 cm-1 . Pada HA gugus PO4 3- dengan intensitas paling tinggi terdeteksi pada bilangan gelombang 495,29; 1046,86; 566,76 cm-1 . Gugus OH terdeteksi pada bilangan gelombang 3436,50 cm-1 [17]
Tabel 1. Komposisi Fasa CaO
«MO MOJ 3000 JHO »» 100 IOOO SN4W
oπ4
|
Sampel |
Fasa |
Komposisi massa (% b/b) |
|
CaO |
CaO |
94,812 |
|
Cangkang |
Ca(OH)2 |
5,188 |
|
CaO |
62,900 | |
|
CaO Standar |
Ca(OH)2 |
37,100 |
Gambar 2. Spektrum FTIR HAp

Gambar 3 Morfologi SEM HAp
Puncak ini menunjukkan ikatan gugus fosfat (PO43- ) dengan vibrasi ulur dan tekuk dari P-O. Hasil analisis morfologi permukaan dengan SEM menunjukkan bahwa HAp yang disinterring
pada suhu 900oC tidak mengalami aglomerasi [18]. Pada HAp tersebut menunjukkan proses sintering telah mencapai tahap akhir yang ditunjukkan dengan batas butir yang mulai membesar dan pori yang tertutup/terisolasi oleh butir HAp. HAp memiliki ukuran pori yang seragam yaitu 200 nm.
Analisis menggunakan instrumen SEM untuk mengetahui morfologi permukaan hidroksiapatit. Morfologi permukaan HAp menunjukkan butiran halus yang tidak teratur. Pada sampel CaO standar, menunjukkan sampel yang tidak memiliki bentuk karena terjadi aglomerasi (menggumpal) [19]. HAp yang dihasilkan memiliki permukaan yang tidak merata, namun tidak terdapat permukaan yang memiliki tepi yang runcing dan tajam yang menyerupai bentuk jarum. Hal tersebut menunjukkan bahwa morfologi HAp yang disintesis pada penelitian ini tidak membahayakan bagi tulang manusia. Implan yang memiliki tepi yang tajam dapat melukai jaringan lunak pada tulang disekelilingnya sehingga dapat terjadi peradangan [20].
Hidroksiapatit dapat disintesis dari cangkang telur dengan metode presipitasi basah. Kadar kalsium dalam bahan baku CaO hasil kalsinasi cangkang telur yang diukur menggunakan AAS adalah sebesar 76,6% . Dari hasil analisa XRD, puncak HAp dengan intensitas tertingi diperoleh pada variasi rasio Ca/P yaitu 1,67 dan ukuran partikel HAp menurun seiring kenaikan rasio Ca/P, yaitu berturut-turut dari rasio Ca/P 0,67; 1,67; dan 2,67 adalah 69, 56, dan 53 nm. Dari hasil analisa SEM dan EDX menunjukkan ukuran partikel HAp terbesar pada rasio Ca/P 0,67. Rasio Ca/P HAp hasil sintesis menurun seiring kenaikan rasio Ca/P awal sintesis, berturut-turut dari rasio Ca/P 0,67 ke 2,67 yaitu 1,05 menjadi 1,17. Dari hasil analisa FTIR, pada tiap sampel terdapat gugus PO43- dan OH-yang mengindikasikankan adanya kandungan hidroksiapatit pada sampel.
Penulis mengucapkan terima kasih kepada Yayasan Perguruan Tinggi Flores yang telah mendanai penelitian ini melalui Hibah PDP tahun 2020 serta LPPM Universitas Flores yang memberikan dukungan dan kesempatan sehingga penelitian ini dapat terlaksana.
-
[1] Khandelwal H, Prakash S. 2016.
Synthesis and characterization of hidroxyapatite powder by eggshell. Journal of Minerals and Materials Characterization and Engineering. 4:119-126.
-
[2] Mozartha M, Praziandithe M,
Sulistiawati. 2015. Pengaruh
penambahan hidroksiapatit dari cangkang telur terhadap kekuatan tekanan glass ionomer cement. Jurnal B-Dent. 2(1):75-81.
-
[3] Toibah AR, Misran F, Shaaban A, Mustafa Z. 2019. Effect of pH condition during hydrothermal synthesis on the properties of hydroxyapatite from eggshell waste. Journal of Mechanical Engineering and Sciences. 13(2):4958-4969.
-
[4] Agarwal A, Gupta PK. 2015.
Adsorption study of Cr(II) from aqueous solution using animal bone charcoal as low cost adsorbent. International Journal Engineering Technology, Management and Applied Sciences. 3(1):151-163.
-
[5] Amalia V, Hadisantoso EP, Hidayat
-
D, Diba RF, Dermawan MF, Tsaniyah SW. 2018. Isoalasi dan karaterisasi hidroksiapatit dari limbah tulang hewan. Alchemy Journal of Chemistry. 5(4):114-119.
-
[6] Pinangsih AC, Wardhani S, Darjito.
2014. Sintesis biokeramik
hidroksiapatit Ca10(PO4)6(OH)2 dari limbah tulang sapi menggunakan metode sol-gel. Kimia Student Journal. 1(2):203-209.
-
[7] Wadu I, Soetjipto H, Cahyanti MN. Sintesa dan penentuan kadar kalsium-fosfat hidroksiapatit (HAp) dari kerabang telur ayam. Jurnal Kimia dan Pendidikan Kimia. 3(3):1-5.
-
[8] Noviyanti AR, Haryono, Pandu R, Eddy DR. 2017. Cangkang telur ayam sebagai sumber kalsium dalam pembuatan hidroksiapatit untuk aplikasi graft tulang. Chimica et
Natura Acta. 5(3):107-111.
-
[9] Pankew P, Hoonnivathana E,
Limsuwan P, Naemchanthara K.
2010. Temperature effect phosphate synthesized from chicken eggshells and amonnium phosphate. ApplSci. 10(24):3337-3342.
-
[10] Dahlan K, Prasetyanti F, Sari YW. 2009. Sintesis Hidroksiapatit dari Cangkang Telur Menggunakan Dry Metode. J. Biofisika. 5(2):71-78.
-
[11] Singh V, Meeraj N. 2012. Synthesis of Nano Crystalline Hydroxyapatite from Egg Shells by Combustion Method. J. Science and Engineering Investigations 1(3): 92-95.
-
[12] Thamaraiselvi TV, Prabakaran K, Rajeswari S. 2006. Synthesis of Hydroxyapatite that Mimic Bone Mineralogy. Trends Biomater.Artif. Organs. 19(2):81-83.
-
[13] Manafi AM, Joughehdoust S. 2009. Synthesis of Hydroxyapatite
Nanostructure by Hydrothermal Condition for Biomedical
Application. Iranian J
Pharmaceutechal Science 5(2):89-94.
-
[14] Hatha, AAM, Christi, KS, Singh R. & Kumar S. 2005. Bacteriology of the fresh water bivalve clam Batissa violacea (Kai) sold in the Suva Market. The South Pacific Journal of Natural Science. 23 48-50.
-
[15] Sasikumar S, Vijayaraghavan R. 2006. Low Temperature Syntesis of Nanocrystaline Hydroksiapatite from Egg Shells by Combustion Method. Trens Biomater.Artif.Organs
19(2):70-73
-
[16] Dahlan K, Prasetyanti F, Sari YW. 2009. Sintesis Hidroksiapatit dari Cangkang Telur Menggunakan Dry Metode. J. Biofisika 5(2):71-78.
-
[17] Anggresani L., Perawati S., Rahayu I.J. Limbah tulang ikan tenggiri (Scomberomorus guttatus) sebagai sumber kalsium pada pembuatan hidroksiapatit, Jurnal Katalisator.
2019, 4(2), 133-140.
-
[18] Dedourkova T., Zelenka J., Zelenkova M., Benes L., Svoboda L. Synthesis of sphere-like nanoparticles of hydroxyapatite, Procedia
Engineering. 2012, 42, 1816–1821.
-
[19] Poinern G., Brundavanam R.,
Fawcett D. Nanometre scale
hydroxyapatite ceramics for bone tissue engineering, American Journal of Biomedical Engineering. 2013,
3(6):148-168.
-
[20] Szczes A., Holysz L., Chibowski E. Synthesis of hidroxyapatite for biomedical applications, Advances in Colloid and Interface Science. 2017, 249, 321-330.
34

Discussion and feedback