VALIDASI METODE ANALISIS BAHAN KIMIA OBAT PARASETAMOL DAN FENILBUTASON PADA PRODUK OBAT TRADISIONAL DENGAN HPTLC-SPEKTROFOTODENSITOMETRI
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 7 Nomor 1, Mei 2019
I Ca⅛ra I ; eKimia ∣
VALIDASI METODE ANALISIS BAHAN KIMIA OBAT PARASETAMOL DAN FENILBUTASON PADA PRODUK OBAT TRADISIONAL DENGAN
HPTLC-SPEKTROFOTODENSITOMETRI
I Putu Ngurah Apri Susilawan1*, I Made Siaka2, I Made Oka Adi Parwata2
1*
-
1 Magister Kimia Terapan,Pascasarjana Universitas Udayana, Jl.PB.Sudirman, Denpasar, Indonesia 2Jurusan Kimia FMIPA,Universitas Udayana, Bukit Jimbaran, Denpasar,Telp (0361)703137, Indonesia * apri_susilawan@yahoo.co.id
ABSTRAK : Tujuan dari penelitian ini adalah untuk melakukan validasi metode analisis secara simultan bahan kimia obat parasetamol dan fenilbutason yang terdapat pada produk obat tradisional dengan menggunakan high performance thin layer chromatography (HPTLC)-spektrofotodensitometri. Validasi ini dilakukan dengan menentukan spesifitas, linieritas, presisi dan akurasi pengukuran. Spesifitas ditentukan dengan membandingkan profil analit dalam larutan baku, sampel dan spike. Selanjutnya, noda yang telah terpisah secara kromatografi lapis tipis discan menggunakan spektrofotodensitometer. Linieritas, batas deteksi (limit of detection, LoD), batas kuantitasi (limit of quantitation, LoQ) ditentukan dengan konsentrasi 25 – 700 ng/spot untuk parasetamol sementara 75 – 2100 ng/spot untuk fenilbutason. Presisi dan akurasi dilakukan dengan menambahkan baku campuran ke dalam larutan uji menggunakan satu konsentrasi dengan 6 kali pengulangan. Hasil validasi metode analisis parasetamol dan fenilbutason pada produk obat tradisional dengan HPTLC-Spektrofotodensitometri menunjukkan metode ini valid dengan spesifisitas, linieritas, batas deteksi, batas kuantitasi, presisi dan akurasi yang memenuhi persyaratan.
Kata Kunci: Parasetamol, Fenilbutason, HPTLC-Spektrofotodensitometri, Validasi
ABSTRACT : The aim of this study was to validate the simultaneous analysis method of paracetamol and phenylbutazone contained in traditional drugs using high performance thin layer chromatography(HPTLC)-Spectrophotodensitometry. The validation was carried out by determination of the specificity, linierity, limit of detection (LoD) and limit of quantitation (LoQ), precision and accuracy. The specificity was determined by comparing the profile of analytes in standart solution, sample solutions, and spike. Further, the seperated spots on thin layer chromatograms were scanned using spectrophotodensitometry. The liniarity, LoD and LoQ were determined using 25 – 700 ng/spot of paracetamol concentrations while 75 – 2100 ng/spot of phenylbutazone concentrations. The precision and accuracy were determined by adding a centain concentration of the chemicals into sample solutions with 6 time of repetitions. The results showed that the simultaneous analysis method of paracetamol and phenylbutazone contained in traditional drug products with HPTLC- Spectrodensitometry is valid since the specificity, linearity, LoD and LoQ, and precision and accuracy of the analysis meet the requirements.
Key words: Paracetamol, Phenylbutazone, HPTLC-Spectrophotodensitometry, Validation
Parasetamol dan fenilbutason merupakan obat analgetika dan anti inflamasi non-steroid (AINS) yang banyak sekali digunakan masyarakat, baik dengan resep maupun tanpa resep dokter, untuk mengurangi rasa nyeri dan inflamasi pada penyakit rematik [1]. Bahan kimia obat (BKO) yang teridentifikasi tersebut bercampur dalam produk obat tradisional (OT) sehingga terlihat efek kerja obat tersebut sangat berkhasiat. BKO tersebut sering ditambahkan pada jamu pegal linu atau rematik.
Sesuai dengan Permenkes No. 07 Tahun 2012 tentang Registrasi Obat Tradisional, OT dilarang mengandung BKO yang merupakan hasil isolasi atau sintesis berkhasiat obat, narkotika atau psikotropika dan/atau bahan lain yang berdasarkan pertimbangan kesehatan
dan/atau berdasarkan penelitian
membahayakan kesehatan [2].
Metode analisis yang digunakan oleh BPOM RI dalam menyimpulkan produk OT mengandung BKO yaitu KLT, Spektrofotodensitometri/Spektrofotometri UV-Vis, KCKT/KG dan LCMS/MS. Analisis OT mengandung BKO Parasetamol dan Fenilbutason pada produk OT menggunakan Uji Screening (pendahuluan) dengan KLT-
Spektrofotodensitometri [3], apabila terindikasi positif kemudian dianalisis kembali dengan metode tunggal Parasetamol dan Fenilbutason dengan beberapa eluen. Apabila sampel positif mengandung BKO dilanjutkan dengan spektrofotometri atau
Spektrofotodensitometri. Banyaknya
tahapan metode analisis yang dilalui untuk menyimpulkan bahwa produk OT mengandung BKO membuat waktu pengujian semakin lama dan produk OT yang diduga mengandung BKO kemungkinan akan habis di pasaran. Disamping itu, terjadi pemborosan dalam penggunaan reagensia dan baku pembanding.
Untuk mengurangi masalah tersebut, maka dilakukan modifikasi terhadap metode analisis identifikasi BKO dalam produk OT dengan mengutamakan akurasi dan waktu pengujian yang cepat. Hal ini dapat dilakukan dengan melakukan uji identifikasi secara sekaligus terhadap BKO Parasetamol dan Fenilbutason pada produk OT dalam satu tahapan uji dengan metode HPTLC-Spektrofotodensitometri. Metode ini dapat mengurangi tahapan analisis, karena tidak diperlukan uji identifikasi terhadap masing-masing BKO.
Beberapa penelitian telah dilakukan untuk analisis parasetamol dalam campuran BKO lainnya baik dalam produk farmasi maupun obat tradisional [4,5]. Validasi metode analisis parasetamol, asam mefenamat, dan ibuprofen dalam jamu pegel linu telah dilakukan dengan hasil spesifisitas, linieritas, Presisi, dan akurasi yang memenuhi persyaratan [4].
Tujuan penelitian ini adalah untuk menganalisis secara simultan BKO parasetamol dan fenilbutason pada produk OT dengan HPTLC-Spektrofotodensitometri dan memperoleh validitas metode analisis BKO parasetamol dan fenilbutason pada produk OT dengan HPTLC-Spektrofotodensitometri.
Bahan yang digunakan dalam penelitian ini adalah Baku Pembanding yang digunakan adalah parasetamol Baku Pembanding Farmakope Indonesia (BPFI) dan fenilbutason BPFI yang diperoleh dari BPOM RI. 2. Reagensia terdiri dari HPTLC Silica gel 60 F254, 20x10 cm, etil asetat, metanol, amonia 25%, dietil eter pro analisa, etanol absolut dengan grade pro analisa, NaOH 1 N, HCl 1 N (Merck), kertas lakmus, aquabidest (Water purifier), penyaring millex 0.2 µm (Millipore), dan pipet tip.
Peralatan yang digunakan adalah timbangan mikro dan analitik (sartorius), TLC System (ATS, ADC, TLC Scanner IV, dan TLC Visualizer, Camag)
-
2.2 Metode
Pembuatan larutan baku induk dan campuran Parasetamol dan Fenilbutason
Larutan Baku Induk Parasetamol dan fenilbutason 1000 ng/ul dibuat dengan menimbang secara seksama 5 mg parasetamol BPFI dan fenilbutason BPFI kedalam masing-masing labu ukur 5 ml dan diencerkan dengan 2 ml etanol, disonikasi hingga larut dan ditepatkan volumenya sampai tanda
Penyiapan Larutan Baku Campur
Sejumlah 60 µL masing-masing larutan baku induk parasetamol dan fenilbutason dipipet ke dalam vial 1.5 ml yang sama, diencerkan dengan etanol 880 µL (Larutan B)
Penyiapan Larutan Uji
Dilakukan homogenisasi terhadap sampel. Sejumlah 5 mL (cairan) atau 500 mg (padatan) sampel dimasukkan ke dalam labu Erlenmeyer 250 mL, ditambah 50 mL air bebas mineral, dibasakan dengan larutan natrium hidroksida 1 N sampai pH 10-11, lalu dikocok selama 30 menit. Larutan disaring atau disentrifugasi selama 15 menit dengan kecepatan 3000 rpm. Filtrat yang diperoleh dimasukkan ke dalam corong pisah 250 mL, kemudian diasamkan dengan penambahan larutan asam klorida 1 N sampai pH 1-2. Selanjutnya diekstraksi tiga kali, tiap kali dengan 50 mL eter. Ekstrak eter dikumpulkan kemudian diuapkan di atas penangas air pada suhu 60-70°C atau diuapkan dengan penguap putar vakum pada suhu 55 °C sampai kering. Sisa yang diperoleh dilarutkan dengan etanol hingga 8,0 mL dan disaring. (Larutan C)
Penyiapan Larutan Spike
Dengan cara yang sama seperti prosedur penyiapan larutan uji, 5 mL
(cairan) atau 500 mg (padatan) sampel dimasukkan ke dalam labu erlenmeyer 250 ml, kemudian dari masing-masing larutan baku induk dipipet 100 µL dan dimasukkan ke dalam labu erlenmeyer yang berisi sampel. (Larutan D)
Validasi Metode Analisis Uji Spesifisitas
Ditotolkan larutan B, C, dan D pada pelat HPTLC dan dieluasi dengan kondisi seperti pada penetapan secara KLT. Spesifisitas ditentukan dengan membandingkan profil analit dalam larutan baku, sampel, dan spike [4]. Selanjutnya, noda/bercak yang telah terpisah secara KLT discan secara spektrofotodensitometer seperti pada penetapan secara spektrofotodensitometri.
Linieritas, LOD, dan LOQ
Dibuat larutan standar parasetamol dan fenilbutason masing-masing dengan konsentrasi parasetamol antara 25 sampai 700 ng/spot dan fenilbutason 75 sampai 2100 ng/spot sebanyak dua kali replikasi dengan cara dipipet masing-masing larutan baku induk dan pelarut matrik sampel. Masing-masing larutan baku kerja ditotolkan pada pelat HPTLC dan dieluasi seperti pada penetapan secara KLT. Noda yang terbentuk kemudian discanning seperti pada penetapan secara spektrofotodensitometri.
Penentuan rentang dan linieritas dilakukan dengan membuat persamaan regresi linear larutan baku kerja y = bx + a (y = AUC dan x = konsentrasi masing-masing larutan) dan polynomial berdasarkan persamaan kuadrat y = ax2 + bx + c (y = tinggi bercak dan x = konsentrasi) kemudian ditentukan koefisien determinasi (r2) nya. Rentang dikatakan linier jika nilai r tidak kurang dari 0.951 [1]. Persamaan regresi yang diperoleh tersebut dimanfaatkan untuk menghitung LoD dan LoQ. Batas deteksi dihitung sebagai LoQ = 3.3 σ/S dan Batas kuantisasi dihitung sebagai LoQ = 10 σ/S, dimana σ adalah standar deviasi dari respon dan S
adalah slope dari kurva kalibrasi yang diperoleh dari linieritas.
Presisi dan Akurasi
Uji presisi dan akurasi dilakukan dengan menambahkan baku campuran ke dalam larutan uji menggunakan satu konsentrasi dan enam kali replikasi untuk masing-masing konsentrasi. Masing-masing konsentrasi ditotolkan pada pelat HPTLC seperti pada penetapan secara KLT. Selanjutnya, noda/bercak yang telah terpisah secara KLT discan secara spektrofotodensitometri seperti pada penetapan secara spektrofotodensitometri. Dengan cara yang sama, dilakukan pengulangan pada dua hari yang berbeda minimal dua kali replikasi dengan metode, alat, dan analis yang sama kemudian dihitung % RSD dan % recovery pada satu hari (intraday) dan hari yang berbeda (interday). Presisi dan akurasi diterima apabila nilai RSD < 4% [6] dan rentang % recovery diantara 95-105 % [7].
Instrumentasi dan Kondisi Penetapan
Penetapan secara KLT [3]
Larutan uji, larutan baku, dan larutan spike sampel ditotolkan secara terpisah dan dilakukan KLT dengan kondisi sebagai berikut:
Fase diam : HPTLC silika gel 60 F254 ukuran 20 x 10 cm
Fase gerak
Penjenuhan Pengeringan Jarak rambat Penotolan Bentuk pita Deteksi bercak Pencucian pelat
Etil Asetat-Metanol-Amonia (80 : 10 : 10) Automatis 20 menit Automatis 5 menit 7,5 cm
5 µL 6 mm
UV 254 nm
Metanol : Air (3:1) dipanaskan pada 1200 C selama 15 menit
Penetapan secara Spektrofotodensitometri [6]
Lempeng HPTLC hasil eluasi dipindai dengan kondisi sebagai berikut:
Slit dimensi : 4,00 x 0,30 mm,
Micro
Kecepatan deteksi : 20 mm/s
Resolusi data : 100 µm/step
Lampu : D2
Panjang gelombang : 200 – 400 nm
Profil spektrum dan panjang gelombang serapan maksimum direkam.
Analisis sampel positif BKO pada produk OT
Analisis parasetamol dan fenilbutason dilakukan pada berbagai jamu dengan cara menambahkan BKO parasetamol dan fenilbutason kedalam jamu tersebut. Dilakukan tiga kali replikasi terhadap masing-masing jamu. Prosedur analisis seperti pada penyiapan larutan uji dan spike.
-
3. HASIL DAN PEMBAHASAN
Spesifisitas
Sampel 01 dan 02 merupakan jamu masuk angin/demam yang berbentuk cair sedangkan sampel 04 merupakan jamu pegal linu yang berbentuk serbuk. Penambahan baku (spike) ke dalam masing-masing sampel tidak
mempengaruhi Rf parasetamol dan fenilbutason serta tidak ada interferensi matriks sampel terhadap analit. Parasetamol dan fenilbutason terpisah dengan Rf masing-masing 0,6 dan 0,3 begitu juga baku campur antara parasetamol dan fenilbutason memiliki Rf yang hampir sama seperti terlihat pada Gambar 1.
Kromatogram parasetamol dan fenilbutason dalam larutan spike sampel terpisah sempurna demikian juga terhadap matriks sampel. Profil spektrum baku parasetamol dan fenilbutason memiliki bentuk yang mirip namun berbeda panjang gelombang maksimumnya. Profil spektrum matriks sampel yang dibandingkan dengan larutan baku tidak memiliki bentuk yang sama seperti terlihat pada Gambar 2 dan 3.
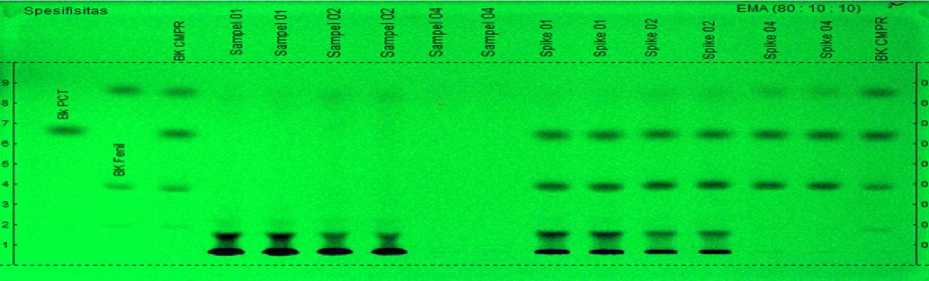
Gambar 1.Kromatogram KLT larutan baku parasetamol, fenilbutason, larutan uji, dan spike dalam penentuan spesifisitas
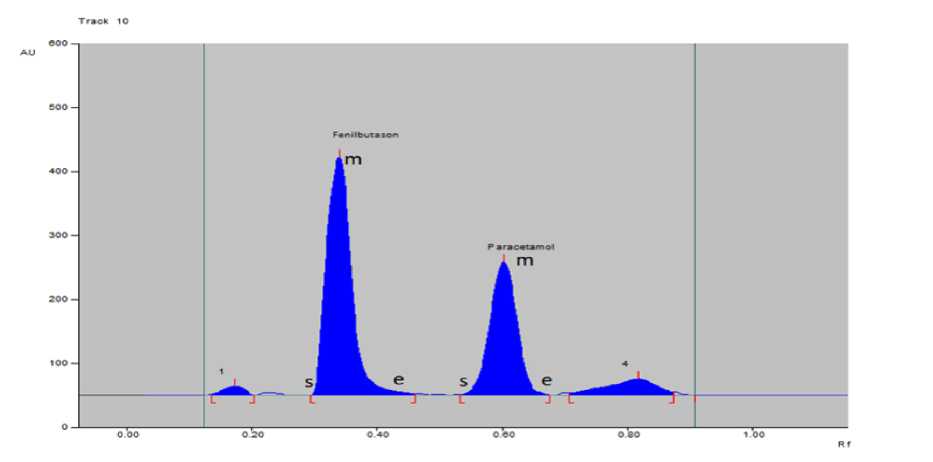
Gambar 2. Densitogram parasetamol dan fenilbutason dalam larutan spike sampel
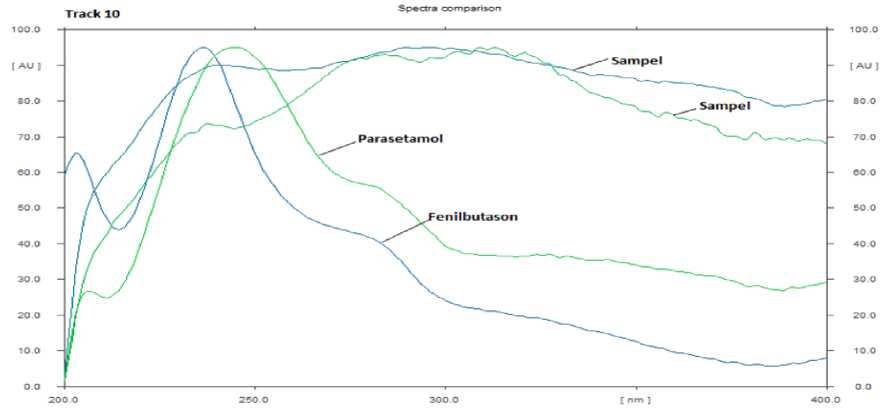
Gambar 3. Perbandingan spektum parasetamol dan fenilbutason dalam larutan baku dan sampel
Profil spektrum parasetamol dalam penelitian ini identik dengan profil parasetamol dalam penelitian yang dilakukan oleh Hayun dan Karina [4] dan Pyka et al. [5] walaupun berbeda eluen.
Linieritas, LoD, dan LoQ
Penentuan linieritas parasetamol dan fenilbutason dilakukan secara duplo dengan menggunakan minimal lima konsentrasi yang berbeda dalam pelarut matriks sampel dengan hasil KLT seperti pada Gambar 4. Pengukuran linieritas dengan spektrofotodensitometer dilakukan simultan dengan dua panjang gelombang sekaligus yaitu λ maks parasetamol 244 nm dan fenilbutason 237 nm. Kromatogram tiga dimensi dari parasetamol dan fenilbutason dalam beberapa konsentrasi yang berbeda dapat dilihat pada Gambar 5. Penentuan rentang dan linieritas dilakukan dengan membuat persamaan regresi linear dari larutan spike sampel y = ax + b (y = tinggi bercak dan x = konsentrasi masing-masing larutan) dan polynomial berdasarkan persamaan kuadrat y = ax2 + bx + c (y = tinggi bercak dan x = konsentrasi) kemudian ditentukan koefisien determinasi (r2) dan koefisien korelasi (r) seperti pada Gambar 6.
Koefisien regresi dan determinasi linear parasetamol sebesar r2 = 0,9962 dan r = 0,9981 sedangkan polynomial sebesar r2 = 0,9999 dan r = 0,9999.
Koefisien regresi dan determinasi linear fenilbutason sebesar r2 = 0,9563 dan 2 r = 0,9779 sedangkan polynomial sebesar r2 = 0,9917 dan r = 0,9958. Penentuan linieritas dalam KLT menggunakan regresi polynomial karena sampel yang ditotolkan pada pelat KLT bersifat tidak homogen dan terdistribusi tidak merata pada permukaan dan bagian dalam adsorben. Penentuan linieritas larutan dalam kuvet dengan spektrofotometer bersifat homogen (Reich & Schibli, 2006). Hasil penelitian ini menunjukkan linieritas parasetamol yang diperoleh pada rentang 25-700 ng dan fenilbutason pada rentang 75-1200 ng dikatakan linear karena r2 > 0,951 [1].
Hasil perhitungan LoD dan LoQ secara kuantitatif dilakukan dengan spektrofotodensitometri dengan kurva regresi polynomial seperti pada Tabel 1. Batas deteksi parasetamol dan fenilbutason adalah 15,77 ng dan 14,60 ng sedangkan batas kuantisasi parasetamol dan fenilbutason adalah 52,56 ng dan 48,60 ng. Hasil LoD dan LoQ parasetamol pada penelitian ini jauh lebih rendah dibandingkan dengan penelitian yang dilakukan oleh Hayun dan Karina [4] yang menggunakan perhitungan dengan regresi linear dengan LoD dan LoQ parasetamol 65,72 ng dan 219 ng.
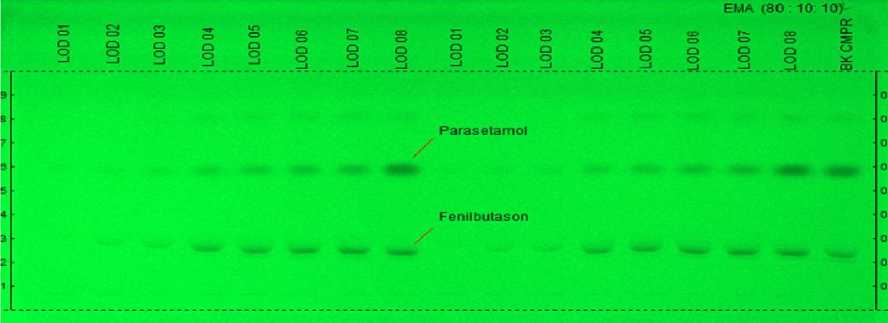
Gambar 4. Kromatogram KLT parasetamol dan fenilbutason dalam penentuan linieritas dengan eluen EMA (80:10:10)
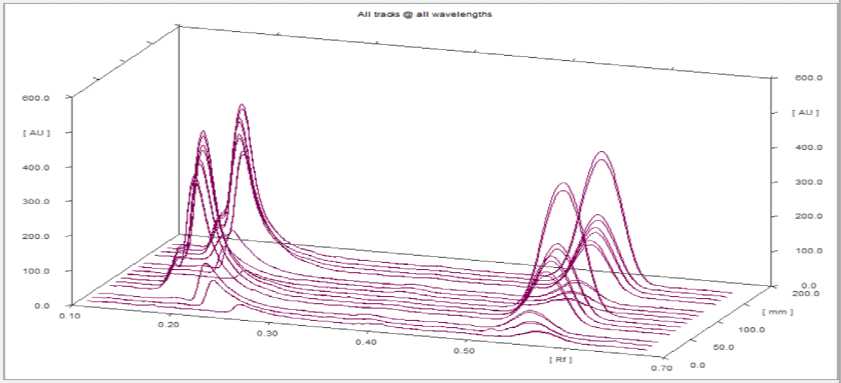
Gambar 5. Densitogram tiga dimensi puncak parasetamol dan fenilbutason dalam larutan spike sampel pada penentuan linieritas
Tabel 1. Linieritas, LoD, dan LoQ Parasetamol dan Fenilbutason
|
No |
Parameter |
Senyawa | |
|
Parasetamol |
Fenilbutason | ||
|
1 |
Kurva Kalibrasi | ||
|
a. Liuiear |
Y = 8,1527+ 2,5949X |
Y= 12,44035+ 2,01 IX | |
|
b. Polynomial |
Y = 10,3106 ÷ 2,4354X+0,01 IX2 Y = -8,8752 + 3,3946X-0,077X2 | ||
|
2 |
Ia | ||
|
a. Liniear |
0,9962 |
0.9563 | |
|
b. Polynomial |
0.9999 |
0.9917 | |
|
3 |
Batas Linier (ng/spot) |
25-700 |
75-1200 |
|
4 |
LoD | ||
|
a. ng/spot |
15,77 |
14.60 | |
|
b. mg g |
0,60 |
0,55 | |
|
c. % (b∕b) |
0,06 |
0,06 | |
|
5 |
LoQ | ||
|
a. ng/spot |
52,56 |
48,67 | |
|
b∙ mg/g |
1,99 |
1,84 | |
|
c. % (b∕b) |
0,20 |
0,18 | |
Presisi dan Akurasi
Penentuan presisi dan akurasi pada penelitian ini dilakukan dengan menggunakan satu konsentrasi dengan enam kali replikasi. Konsentrasi
parasetamol dan fenilbutason yang ditetapkan berturut-turut 200 ng/spot dan150 ng/spot. Presisi diukur sebagai % RSD dan akurasi diukur sebagai % perolehan kembali (% recovery). Hasil
penentuan presisi dan akurasi dalam waktu kurang dari satu hari (Intraday Precision) untuk parasetamol RSD=1,21% dan recovery =102,82%, untuk fenilbutason RSD= 2,99% dan recovery =100,62%.
Hasil presisi dan akurasi parasetamol dan fenilbutason pada hari yang berbeda (Intermediate Precision) yaitu pada hari ke 2 untuk parasetamol RSD=0,65% dan recovery =103.17%, untuk fenilbutason RSD=3,80% dan recovery =102,94% sedangkan pada hari ke-3 adalah untuk parasetamol RSD=2,19% dan recovery =101,00%, untuk fenilbutason RSD= 2,36% dan recovery =103,75% seperti terlihat pada Tabel 2.
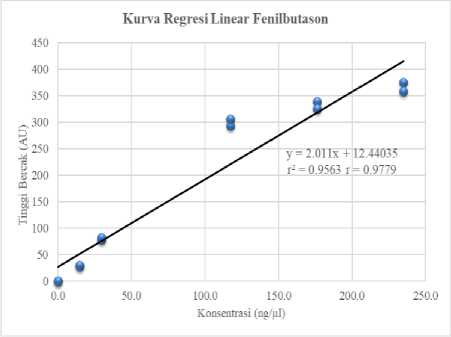
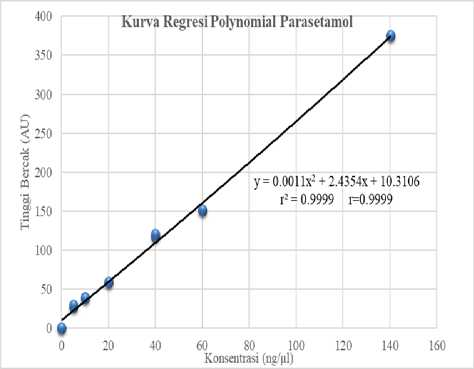
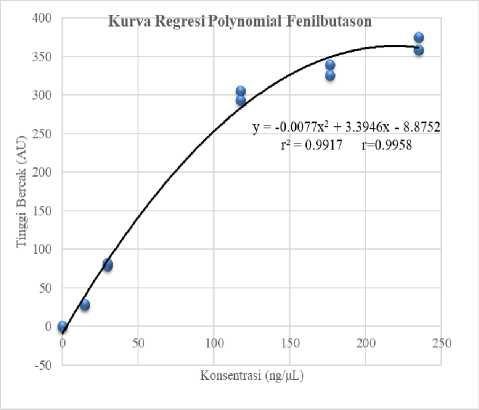
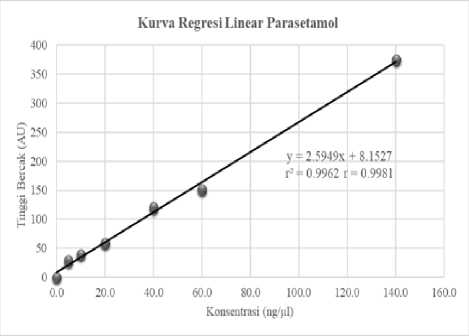
Gambar 6. Kurva kalibrasi linear parasetamol dan fenilbutason dalam pelarut matriks sampel
Gambar 7. Kurva kalibrasi polynomial parasetamol dan fenilbutason dalam pelarut matriks sampel
Analisis BKO Parasetamol dan Fenilbutason dalam Berbagai Jamu
Analisis BKO parasetamol dan fenilbutason dalam jamu pegal linu, masuk angin, dan demam secara HPTLC-Spektrofotodensitometri dilakukan terhadap sampel jamu sediaan padat (pegal linu dan demam) dan jamu sediaan cair (masuk angin). Jamu yang digunakan adalah jamu yang tidak mengandung BKO parasetamol dan fenilbutason serta jamu positif BKO. Larutan baku parasetamol, fenilbutason, baku campur, sampel, dan spike sampel ditotolkan pada HPTLC dan dieluasi sesuai
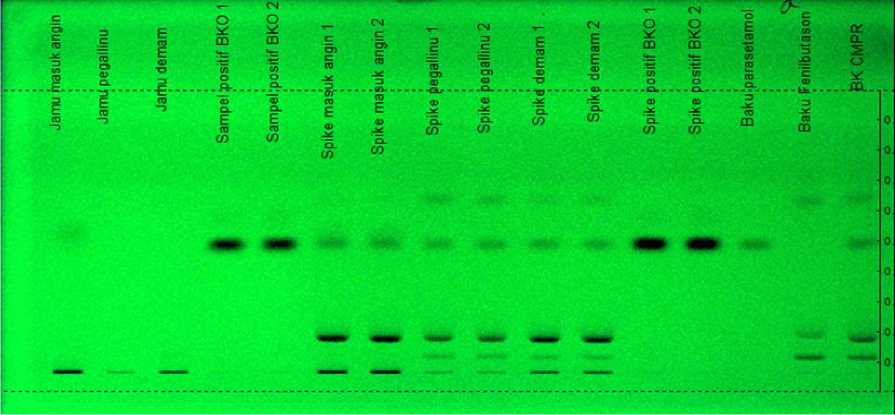
Gambar 8. Kromatogram KLT analisis parasetamol dan fenilbutason dalam Berbagai Jamu dengan eter
Tabel 2. Hasil Penentuan Presisi dan Akurasi Parasetamol dan Fenilbutason dengan Spektrofotodensitometri
|
Hari |
Parasetamol (200 πg⅛wθ |
Fenilbutason (150 πg⅛pt>t) | ||||||
|
Tinggi bercak |
% RSD |
% Jieeoveiy' |
n (sampel) |
Tinggi bercak |
% RSD |
% Recovery |
Il (sampel) | |
|
128,81 |
59,05 | |||||||
|
131,39 |
62,41 | |||||||
|
1 |
128,96 |
1,21 |
102.82 |
6 |
60,09 |
2.99 |
100.62 |
6 |
|
127,86 |
58,69 | |||||||
|
130,57 |
62,13 | |||||||
|
128,63 |
59,92 | |||||||
|
129,77 |
58,88 | |||||||
|
130,36 |
62,14 | |||||||
|
2 |
130,57 |
0,65 |
103,17 |
6 |
63,34 |
3,80 |
102.94 |
6 |
|
128,70 |
59,25 | |||||||
|
129,10 |
62,37 | |||||||
|
129,96 |
63,48 | |||||||
|
87,04 |
43,38 | |||||||
|
89,54 |
44,94 | |||||||
|
3 |
88,85 84,65 |
2,19 |
101,00 |
6 |
45,60 43,26 |
2.36 |
103,75 |
6 |
|
87,69 |
44,91 | |||||||
|
86,91 |
45,54 | |||||||
metode analisis. Hasil kromatogram KLT dapat dilihat pada Gambar 8.
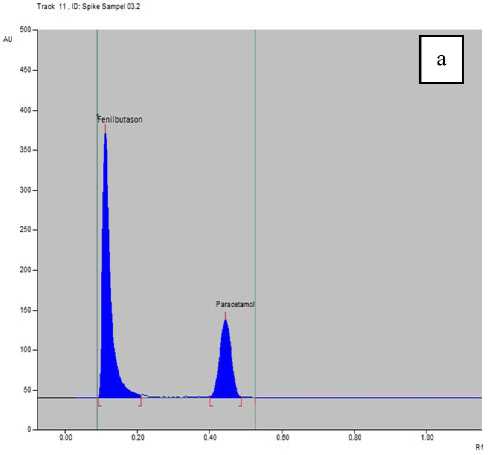
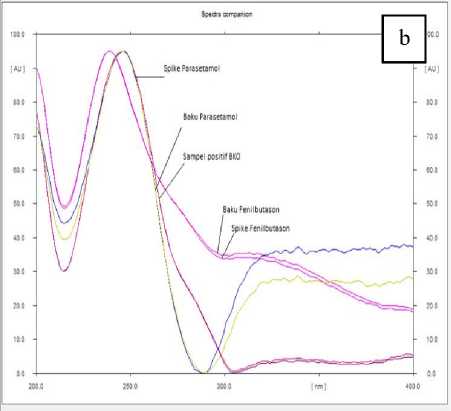
Penetapan secara KLT disimpulkan bahwa sampel jamu pegal linu dan demam tidak mengandung BKO sedangkan jamu masuk angin harus dilakukan uji konfirmasi dengan spektrofotodensitometri karena terdapat noda samar-samar walaupun tidak sejajar baku pembanding parasetamol dan fenilbutason. Spike sampel jamu pegal linu, demam, dan masuk angin positif mengandung BKO parasetamol dan fenilbutason. Sampel public warning mengandung parasetamol, sedangkan spike sampel jamu pegal linu, demam, masuk angin, dan spike sampel public warning positif mengandung BKO parasetamol dan fenilbutason. Pengujian selanjutnya dilakukan dengan uji konfirmasi secara spektrofotodensitometri dimana noda hasil KLT pada Gambar 8 discan dengan spektrofotodensitometer. Alat spektrofotodensitometer diset multi wavelength untuk panjang gelombang maksimum parasetamol 244 nm dan fenilbutason 237 nm. Setiap track baik noda pada sampel, spike, maupun larutan baku discan pada panjang gelombang tersebut secara simultan dan menghasilkan densitogram dan profil spektrum spike sampel seperti Gambar 9.
-
1. Analisis BKO parasetamol dan fenilbutason pada produk OT yang ditambah BKO dengan HPTLC-Spektrofotodensitometri memberikan hasil positif atau mengandung BKO.
-
2. Validasi metode analisis BKO parasetamol dan fenilbutason pada produk OT dengan metode HPTLC-Spektrofotodensitometri memberikan hasil yang valid.
Gambar 9. Densitogram (a) dan spektrum (b) parasetamol dan fenilbutason dalam spike sampel dan sampel positif BKO dengan eter
Pada kesempatan ini, penulis mengucapkan terimakasih kepada BPOM RI, BBPOM Denpasar, dan Mataram, dan semua pihak yang telah membantu penelitian ini.
-
[1] Lawson, Larry. 1996. Evaluation of Calibration Curve Linearity. Guidance memo No. 96-007: 1-9
-
[2] MenKes RI. 2012. Peraturan Menteri Kesehatan Nomor 007 Tahun 2012 Tentang Registrasi Obat Tradisional. Jakarta : Depkes. psl. 07 ayat 1.
-
[3] PPOMN. 2012. Skrining Parasetamol, Fenilbutason, Asam Mefenamat, Piroksikam, Deksametason, Prednison, Ibuprofen, Natrium Diklofenak, dan
Indometasin Dalam Obat Tradisional Sediaan Padat Secara KLT dan
Spektrofotodensitometri. Jakarta : BPOM RI. Metode No. 01. p. 1-3
[4]Hayun, dan Karina, M.A. 2016. "Pengembangan dan Validasi Metode KLT-Densitometri untuk Analisis secara simultan Parasetamol, Asam Mefenamat dan Ibuprofen dalam Jamu “Pegel Linu”." Jurnal Sains Farmasi & Klinis 2 (2): 150-161.
[5] Pyka, A., Budzisz, M., & Dołowy, M.
2013. Validation thin layer
chromatography for the determination of acetaminophen in tablets and comparison with a pharmacopeial method. BioMed research international.
Volume 2013, Article ID545703,10 pages
http://dx.doi.org/10.1155/2013/545703
[6]Harmita. 2004. Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Jakarta : Majalah Ilmu Kefarmasian, I: 117-135
[7] Yuwono, M, dan Indrayanto, G.. (2005). Validation of chromatographic methods of analysis. Profiles of Drug Substances, Excipients and Related Methodology, 32: 243-259
11
Discussion and feedback