AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL DAUN UNGU (Graptophyllum pictum L. Griff)
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 5, Nomor 2, Oktober 2017
AKTIVITAS ANTIOKSIDAN DARI EKSTRAK ETANOL DAUN UNGU (Graptophyllum pictum L. Griff)
Ni Luh Rustini1 , Ni Komang Ariati2
Jurusan Kimia, FMIPA, Universitas Udayana, Kampus Bukit Jimbaran, Bali-Indonesia rustini.niluh@yahoo.co.id
ABSTRAK: Penelitian ini dilakukan untuk mengetahui kandungan total fenol, total flavonoid, dan aktivitas antioksidan berbagai fraksi dan ekstrak etanol daun ungu (Graptophyllum pictum L. Griff) secara in vitro. Penentuan total fenol menggunakan metode Manian dengan pereaksi Folin Ciocalteu dan total flavonoid dengan metode Aluminium Klorida. Penentuan aktivitas antioksidan menggunakan metode penangkapan radikal bebas 2,2-difenil-1-pikrilhidrazil (DPPH). Hasil ekstraksi 700 g serbuk kering daun ungu dengan 6000 mL etanol 96% menghasilkan 31 g ekstrak kental yang berwarna ungu kehijauan. Hasil partisi 15 g ekstrak kental etanol dengan pelarut kloroform, etik asetat dan n-butanol menghasilkan 12,5 g ekstrak pekat kloroform, 1,4 g ekstrak pekat etil asetat dan 1,0 g ekstrak pekat n-butanol yang semuanya berwarna ungu. Kandungan total fenol ekstrak etanol, kloroform, etil asetat dan n-butanol berturut-turut sebesar 3870,75 ; 2851,63 ; 7540,12 dan 18455,30 mg/100 g GAE. Kandungan total flavonoid ekstrak etanol, kloroform, etil asetat dan n-butanol berturut-turut sebesar 402,88 ; 98,14 ; 374,45 dan 345,95 mg/100 g QE. Hasil uji aktivitas antioksidan menunjukkan bahwa ekstrak etanol, etil asetat dan n-butanol daun ungu mempunyai kemampuan menangkap radikal bebas DPPH dengan nilai IC50 berturut-turut sebesar 83,25 ppm ; 271,04 ppm dan 385,82 ppm. Ekstrak kloroform daun ungu tidak memiliki kemampuan menangkap radikal bebas DPPH karena memiliki nilai IC50 lebih dari 500 ppm, yaitu sebesar 1365,73 ppm.
Kata kunci : Daun ungu, fenol, flavonoid, antioksidan
ABSTRACT: This research has been done to determine the content of total phenol, total flavonoids and antioxidant activity in vitro of various fractions and ethanol extract of ungu leaves (Graptophyllum pictum L. Griff). Determination of total phenols using Manian method with Folin Ciocalteau reagent and total flavonoids using Aluminium chloride methode. Determination of antioxidant activity using DPPH method. The extraction of 700 g of dry powder ungu leaves with 6000 mL ethanol of 96 % produces 31 g of concentrated extract greenish purple. The partition of 15 g concentrated ethanol extract with chloroform, ethyl acetate and n-butanol to yield of 12.5 g concentrated chloroform extract, 1.4 g concentrated extract of ethyl acetate and 1.0 g of n-butanol concentrated extracts of which were purple. The content of total phenol of ethanol, chloroform, ethyl acetate and n-butanol extract in a row amounted to 3870.75; 2851.63; 7540.12 and 18455.30 mg/100 g GAE. The content of total flavonoid of ethanol, chloroform, ethyl acetate and n-butanol extract in a row amounted to 402.88; 98.14; 374.45 and 345.95 mg / 100 g QE. The result of antioxidant activity of ethanol, ethyl acetate and n-butanol extract of ungu leaf have the potent scavenger of free radicals DPPH with IC50 values were 83.25 ppm; 271.04 ppm and 385.82 ppm. Ungu leaf chloroform extract does not have potent scavenger of free radicals DPPH because it has IC50 values was 1365,73 ppm , more than 500 ppm,
Keywords : Ungu leaves, phenol, flavonoid, antioxidant
Radikal bebas merupakan salah satu faktor penyebab penyakit degeneratif. Radikal bebas dapat menyebabkan kerusakan sel dan juga merusak biomolekul seperti DNA, protein dan lipoprotein di dalam tubuh yang akhirnya dapat memicu terjadinya penyakit degeneratif seperti kanker, jantung, atritis, katarak, diabetes dan hati (Halliwell, 2007). Radikal bebas terdiri dari Reactive Oxigen Species (ROS) atau radikal oksigen seperti O2. , OH. , ROO. dan H2O2 (David, 2000).
Secara alami tubuh memiliki mekanisme pertahanan terhadap radikal bebas. Senyawa atau molekul pertahanan alami tubuh terhadap radikal bebas disebut dengan antioksidan. Antioksidan dalam tubuh (antioksidan endogen) kebanyakan dakam bentuk enzim seperti enzim superoksida dismutase (SOD), glutation peroksidase (GPx) dan katalase (CAT) (Chiang et al. 2006). Tubuh tidak memiliki sistem pertahanan antioksidatif yang berlebihan, sehingga jika terjadi paparan radikal bebas berlebih, tubuh membutuhkan antioksidan eksogen. Kekhawatiran terhadap efek samping antioksidan sintetik, maka antioksidan alami menjadi alternatif pilihan.
Ada banyak bahan pangan yang menjadi sumber antioksidan alami. Kebanyakan sumber antioksidan alami adalah tumbuh-tumbuhan dan umumnya merupakan senyawa fenolik yang tersebar diseluruh bagian tumbuhan (Rice evans, 1996). Senyawa fenolik atau polifenol antara lain dapat berupa golongan flavonoid, tanin dan saponin (Zhang, 2011).
Salah satu bahan tanaman yang mengandung senyawa fenolik adalah daun ungu (Graptophyllum pictum L. Griff). Daun tersebut mengandung senyawa flavonoid, tanin, alkaloid, sitosterol, glikosida dan saponin. Oleh karena itu perlu dilakukan pengujian aktivitas antioksidan berbagai fraksi dan ekstrak etanol daun ungu secara in vitro dengan
metode DPPH serta penentuan kandungan total fenol dan flavonoidnya, sehingga nantinya dapat dikembangkan sebagai obat untuk mencegah berbagai penyakit degeneratif.
Bahan yang digunakan dalam penelitian ini adalah daun ungu yang diperoleh dari daerah Dalung, Kuta Utara, Badung. Bahan kimia yang digunakan adalah etanol (teknis dan p.a), kloroform (teknis dan p.a), etil asetat (teknis dan p.a), n-butanol (teknis dan p.a), pereaksi Folin-Ciocateu, aluminium klorida, dan buffer sodium fosfat.
Peralatan yang digunakan dalam penelitian ini adalah seperangkat alat gelas, blender, ayakan, ekstraktor, rotary vacum evaporator, sentrifuge, neraca analitik, termometer, pH meter, pipet mikro, pipet tetes, labu ukur, syringe, dan spektrofotometer UV-vis.
Sebanyak 1 kg serbuk kering daun ungu dimaserasi dengan etanol selama 24 jam. Ekstraknya disaring, sedangkan ampasnya dimaserasi kembali dengan etanol sampai senyawa yang terkandung didalamnya terekstrak habis. Filtrat yang diperoleh diuapkan dengan rotary vacum evaporator sehingga diperoleh ekstrak pekat etanol. Ekstrak pekat etanol selanjutnya dilarutkan dengan campuran etanol-air (7:3) kemudian dipartisi berturut-turut dengan kloroform, etilasetat, dan n-butanol. Ekstrak yang diperoleh diuapkan dan ditimbang.
Uji Fitokimia
Identifikasi senyawa fenol dilakukan dengan cara mereaksikan 1 mL ekstrak etanol daun ungu dengan 3 tetes larutan FeCl3 . Adanya perubahan warna
menjadi ungu kehitaman menunjukkan adanya senyawa fenol
Identifikasi senyawa flavonoid dilakukan dengan mereaksikan 1 mL ekstrak etanol daun ungu dengan serbuk Mg dan 1 mL HCl pekat. Adanya perubahan warna menjadi merah menunjukkan adanya senyawa flavonoid.
Penentuan Kandungan Total Fenol
Penentuan kadar total fenol menggunakan metode Folin-Ciocalteu. Sebanyak 100 mg sampel ditambahkan 5 ml etanol, kemudian diencerkan 10 kali. Campuran ditambahkan 0,1 ml reagen Folin-Ciocalteu dan diinkubasi pada suhu kamar selama 15 menit. Sebanyak 2,5 ml Na2CO3 ditambahkan kemudian divorteks, diinkubasi selama 30 menit, dan diukur absorbansinya pada 765 nm. Asam galat dengan konsentrasi 10, 40, 60 dan 80 ppm digunakan sebagai larutan standar (Diaz et al., 2012).
Penentuan Kandungan Total Flavonoid
Kandungan total flavonoid ditentukan dengan metode aluminium klorida. Sebanyak 100 mg sampel dilarutkan dengan 5 mL etanol, kemudian diencerkan 10 kali. Campuran ditambahkan 300 µL NaNO2, dikocok selama 10 detik dan dibiarkan pada suhu kamar selama 10 detik. Sebanyak 300 µL AlCl3 , 2 mL NaOH 1 M dan 1,9 mL akuades ditambahkan pada campuran reaksi, kemudian dikocok selama 10 detik dan diukur serapannya pada panjang gelombang 510 nm. Kuersetin dengan konsentrasi 10, 20, 40, 60 dan 80 ppm digunakan sebagai larutan standar (Diaz et al., 2012).
Penentuan Aktivitas Antioksidan
Aktivitas antioksidan diuji secara in vitro dengan metode DPPH. Sebanyak 2,5 ml ektrak daun ungu (konsentrasi 40, 60, 80 dan 100 ppm) dimasukkan ke dalam masing-masing tabung gelap, dan dicampur dengan 2,5 ml DPPH. Campuran dikocok dan diinkubasi selama 30 menit, kemudian diukur absorbansinya pada panjang
gelombang 515 nm. Persentase daya hambat dihitung dengan menggunakan persamaan : (Chandra and Dave, 2009)
√4g - Aχ
% Daya Hambat = 100%
Dimana A0 merupakan absorbansi control dan Ax merupakann absorbansi sampel
Ekstraksi dan Fraksinasi
Ekstraksi ± 700 g serbuk daun ungu dengan 6000 mL etanol 96 % menghasilkan 31,7724 g ekstrak pekat etanol yang berwarna ungu kehijauan. Sebanyak 15 g ekstrak pekat etanol kemudian dipartisi dengan pelarut kloroform, etil asetat, dan n-butanol, diperoleh 12,5 g ekstrak pekat kloroform, 1,4 g ekstrak pekat etil asetat, 1,0 g ekstrak pekat n-butanol yang semuanya berwarna ungu. Masing-masing ekstrak dilakukan uji fitokimia, penentuan kandungan total fenol dan kandungan total flavonoid serta aktivitas antioksidannya. Hasil uji fitokimia menunjukkan adanya kandungan senyawa fenol dan flavonoid pada semua ekstrak daun ungu.
Hasil Kandungan Total Fenol Berbagai Ekstrak Daun Ungu
Analisis kandungan total fenol dilakukan dengan metode Folin-Ciocalteu.
Kandungan total fenol ekstrak etanol, kloroform, etil asetat dan n-butanol berturut-turut sebesar 3870,75 ; 2851,63 ; 7540,12 ; 18455,30 mg/100 g GAE
(ditampilkan pada Gambar 1). Kandungan total fenol terendah terdapat pada ekstrak kental klorofom dan terbesar terdapat pada ekstrak n-butanol. Hasil pengukurannya dapat dilihat pada Table 1
Hasil Kandungan Total Flavonoid Ekstrak Etanol, Kloroform, Etil Asetat dan N-Butanol Daun Ungu
Analisis kandungan total flavonoid dilakukan dengan metode aluminium
|
Tabel 1. Kadar Total Fenol Ekstrak Etanol, Kloroform, Etil Asetat dan n-Butanol Daun Ungu | ||||
|
Sampel |
Konsentrasi awal (mg/mL) |
Konsentrasi akhir (mg/mL) |
Faktor pengenceran |
Kadar (mg/100 g GAE) |
|
Ekstrak etanol |
20,6 |
0,0797 |
10 |
3870,75 |
|
Ekstrak kloroform |
6,84 |
19,5052 |
10 |
2851,63 |
|
Ekstrak etil asetat |
6,18 |
4,6598 |
100 |
7540,12 |
|
Ekstrak n-butanol |
6,10 |
11,2577 |
100 |
18455,30 |
20000
18000
16000
14000
12000
10000
8000
6000
4000
2000
0
etanol kloroform etil asetat n-butanol
Gambar 1. Perbandingan kadar total fenol ekstrak etanol, kloroform, etil asetat dan n-butanol daun ungu
klorida. Kadar total flavonoid ekstrak etanol, kloroform, etil asetat dan n-butanol berturut-turut sebesar 402,88 ; 98,14 ; 374,45 ; 354,95 mg/100 g QE (ditampilkan pada Gambar 2). Kadar flavonoid terendah terdapat pada ekstrak kloroform dan tertinggi terdapat pada ekstrak etanol. Hasil perhitungan kadar total flavonoid berbagai ekstrak dapat dilihat pada Tabel 2.
Hasil Uji Aktivitas Antioksidan Ekstrak Etanol, Kloroform, Etil Asetat dan n-Butanol
Aktivitas antioksidan berbagai ekstrak daun ungu diuji dengan metode DPPH. Hasil uji aktivitas antioksidan menunjukkan bahwa ekstrak etanol, etil asetat dan n-butanol daun ungu mempunyai kemampuan menangkap radikal bebas DPPH dengan nilai IC50 berturut-turut sebesar 83,25 ppm ; 271,04 ppm ; 385,82
ppm. Ekstrak kloroform daun ungu tidak mempunyai kemampuan meredam radikal bebas DPPH karena memiliki nilai IC50lebih dari 500 ppm yaitu sebesar 1365,73 ppm. Hasil uji aktivitas antioksidan keempat ekstrak dengan metode DPPH ditampilkan pada Gambar 3.
IC50 yaitu suatu nilai yang menggambarkan besarnya konsentrasi ekstrak yang dapat menangkap radikal bebas sebesar 50 %. Nilai IC50 yang semakin kecil menunjukkan keefektifan ekstrak sebagai penangkap radikal bebas yang lebih baik. Ekstrak etanol memiliki kemampuan meredam radikal bebas DPPH paling kuat dan kemampuan meredam radikal bebas paling lemah terdapat pada ekstrak kloroform. Kandungan total fenol tertinggi terdapat pada ekstrak n-butanol dan terendah terdapat pada ekstrak kloro-
Tabel 2. Kadar Total Flavonoid Ekstrak Etanol, Kloroform, Etil Asetat dan n-Butanol Daun Ungu
|
Sampel |
Konsentrasi awal (mg/mL) |
Konsentrasi akhir (mg/mL) |
Faktor pengenceran |
Kadar Total Flavonoid (mg/100 g GAE) |
|
Ekstrak etanol |
20,32 |
0,0082 |
10 |
402,88 |
|
Ekstrak kloroform |
6,34 |
3,11 |
2 |
98,14 |
|
Ekstrak etil asetat |
6,26 |
4,69 |
5 |
374,45 |
|
Ekstrak n-butanol |
6,20 |
4,40 |
5 |
354,95 |
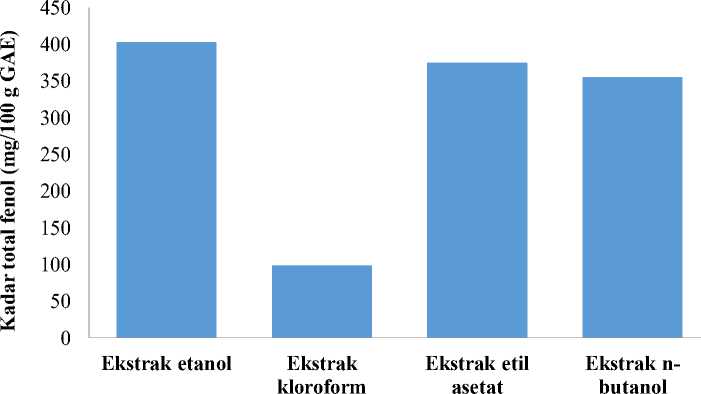
Gambar 2. Perbandingan kadar total flavonoid ekstrak etanol, ekstrak kloroform, ekstrak etil asetat dan ekstrak n-butanol daun ungu
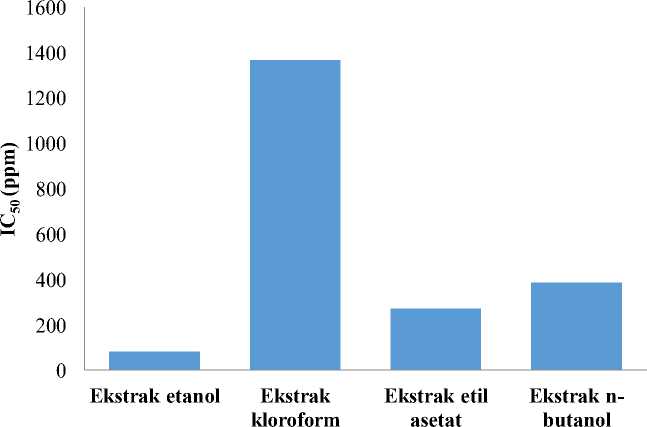
Gambar 3. Perbandingan nilai IC50 ekstrak etanol, ekstrak kloroform, ekstrak etil asetat dan ekstrak n-butanol daun ungu terhadap DPPH.
form. Kandungan total flavonoid tertinggi terdapat pada ekstrak etanol dan terendah terdapat pada ekstrak kloroform. Terdapat korelasi antara kandungan flavonoid dalam suatu ekstrak daun ungu dengan kemampuannya meredam radikal bebas. Semakin tinggi kandungan flavonoidnya, semakin kuat kemampuan ekstrak tersebut meredam radikal bebas. Kemampuan ekstrak dalam menangkap radikal bebas ternyata tidak dipengaruhi oleh kandungan total fenolnya. Senyawa fenolat bisa berupa flavonoid, tanin, dan saponin. Adanya kandungan total fenol yang tinggi dalam suatu ekstrak, belum tentu memiliki kandungan total flavonoid yang tinggi, sehingga kemampuannya meredam radikal bebas juga belum tentu kuat. Kemampuan meredam radikal bebas tidak hanya dipengaruhi oleh jumlah gugus hidroksi pada suatu senyawa fenol, tetapi juga dipengaruhi oleh posisi dari gugus hidroksi tersebut, dan adanya gugus 4-oxo dalam kerangka dasarnya. Senyawa fenolat dan flavonoid mampu mendonorkan atom hidrogen kepada radikal DPPH, sehingga terbentuk senyawa DPPH-H (molekul pikrilhidrazin) yang stabil.
Kandungan total fenol ekstrak etanol, ekstrak kloroform, ekstrak etil asetat dan ekstrak n-butanol daun ungu berturut-turut adalah 3870,75 ; 2851,63 ; 7540,12 ;
18455,30 mg/100g GAE, dan kandungan total flavonoidnya berturut-turut sebesar 402,88 ; 98,14 ; 374,45 ; 345,95 mg/100g
QE. Ekstrak etanol, etil asetat dan n-butanol daun ungu mempunyai kemampuan meredam radikal bebas DPPH dengan nilai IC50 berturut-turut sebesar 83,25 ppm ; 271,04 ppm dan 385,82 ppm. Ekstrak kloroform daun ungu tidak memiliki kemampuan menangkap radikal bebas DPPH karena memiliki nilai IC50 lebih besar dari 500 ppm, yaitu sebesar 1365,73 ppm.
Pada kesempatan ini, penulis menyampaikan terimakasih banyak kepada FMIPA Unud yang telah memberikan dana melalui Dana Hibah Unggulan Program Studi (HUPS) PNBP Unud. Penulis juga menyampaikan terima kasih yang sebesar-besarnya kepada semua pihak yang turut serta membantu dalam proses penyelesaian penelitian ini.
-
[1] Cai, Y., Luo, Q., Sun, M., Corke, H.
-
2004. Atioxidant Activity and Phenolic Compound of 112 Traditional Cinese Medicine Plants Associated with Anticancer. Life Sci. 74: 2157-2184
-
[2] Chandra, S., and Dave R. 2009. In Vitro Models for Antioxidant Activyty and Some Medicinal Plants Possessing Antioxidant Properties. Afr. J. Microbio. Res. 3. 13: 981-996
-
[3] David, G.B., Erik, E.A., Rohini, S., and Alfins. 2000. Antioxidant
Enzyme Expression and ROS
Damage in Prostatic Intraephitelial Neoplasia and cancer. J.Cancer. 89: 124-134
-
[4] Halliwell, B., Gutterige, J.M.C. 2007. Free Radical in Biology and Medicine, 3rd edition. London:
Oxford University Press
-
[5] Harbone, J.B. 1987. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Jilid II. ITB. Bandung.
-
[6] Heyne, K. 1987. Tumbuhan Berguna Indonesia. Jilid 1. Cetakan I. Badan Litbang Kehutanan. Ruygrok & Co. Jakarta..
-
[7] Montgomery, R. 1993. Biokimia Suatu pendekatan Berorientasi Kasus. Yogyakarta. Gadjah Mada University Press.
-
[8] Osawa, T., and Namiki, M. 1981. A Novel Type of antioxidant Isolated
from Leaf Waxof Eucalyptus Leaves. Agric. Biol.Chem, 45: 735-739
-
[9] Rice-Evans, C. A.; Miller, N. J.; Paganga, G. 1996. Structure Antioxidant Activity Relationships of Flavonoids and Phenolic Acids. Free. Rad. Biol. Med. 20: 933-935
-
[10] Osawa, T., and Namiki, M. 1981. A Novel Type of antioxidant Isolated from Leaf Waxof Eucalyptus Leaves. Agric. Biol.Chem. 45: 735-739
-
[11] Purnawati, L. Suryanto, E. dan Yudistital, A. 2012. Aktivitas Antioksidan dari Ekstrak Tongkol Jagung (Zea mays L.). J. Pharmacon. 1. 2: 20-24
-
[12] Rice-Evans, C. A.; Miller, N. J.; Paganga, G. 1996. Structure Antioxidant Activity Relationships of Flavonoids and Phenolic Acids. Free. Rad. Biol. Med. 20: 933-956
-
[13] Silverstein, R. 2005. Spectrometric Identification of Organic
Compounds. New York : Wiley. ISBN 0471134570
-
[14] Tang, S.Y., Whitemen, M., Peng, Z.F., Jenner, A., Yong, E.L, Halliwell. 2004. Characeization of Antioxidant and Antiglycation Properties and Asolation of Active Ingredient from Traditional Chinese Medicine. Free Radioc Biol Med. 36: 1575-1587
-
[15] Upston, J.M., Niu, X., Brown, A.J., Mashima, R., Wang, H.,
Senthilmohan, R., Kettle, A.J., Dean, R.T., and Stocker, R. 2002. Disease Stage-dependent Accumulation of Lipid and Protein Oxidation Products in Human Atherosclerosis. Am J Pathol. 160: 701–710
-
[17] Williams, G.M., Latropoulus, M.J., Whysner, J. 1999. Safety Assessment of Butylated Hydroxyanisole and Butylated Hydroxyltoluene as Antioxidant Food Additives. Food Chem.Toxicol. 37: 1027-1038
-
[18] Zhang, L., Ravipati, A.S., Koyyalamudi, S.R., Jeong, S.C., Reddy, N., Smith, P.T., Bartlett, J., Shanmugan, K., Unch, D.G., Wu, M.J. 2011. Antioxidant and Antiinflammatory Activities of Selected Medicinal Plants Containing Phenolic and Flavonoid Compounds. J Agr Food Food Chem. 59: 12361-12367
151
Discussion and feedback