PERBANDINGAN ANALISIS KROMATOGRAFI CAIR KINERJA TINGGI ELUASI GRADIEN DENGAN ISOKRATIK PADA PENENTUAN VITAMIN B1, B2 DAN B6 DALAM SEDIAAN SIRUP MULTIVITAMIN SECARA SIMULTAN
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 3, Nomor 12, Mei 2015
I Ca∣ira ■ iIQimia
PERBANDINGAN ANALISIS KROMATOGRAFI CAIR KINERJA TINGGI ELUASI GRADIEN DENGAN ISOKRATIK PADA PENENTUAN VITAMIN B1, B2 DAN B6 DALAM SEDIAAN SIRUP MULTIVITAMIN SECARA SIMULTAN
Ni Luh Kasih Ariani1, Ni Made Suaniti1,2*, James Sibarani1,2
1 Program Magister Kimia Terapan, Program Pacsasarjana, Universitas Udayana, Denpasar-Bali, Indonesia 2 Jurusan Kimia, Fakultas MIPA, Universitas Udayana, Jimbaran-Badung, Bali, Indonesia *suanitisr@yahoo.com
ABSTRAK: Vitamin B terutama B1 (Tiamin), B2 (Riboflavin), dan B6 (Piridoksin) sering terkandung dalam sirup multivitamin sehingga diperlukan analisis untuk mendeteksi secara simultan dalam campuran. Tujuan penelitian ini adalah membandingkan analisis vitamin B1, B2, dan B6 dalam sirup multivitamin secara simultan dengan kromatografi cair kinerja tinggi eluasi gradien dan isokratik, menggunakan kolom C18, panjang 15 cm, dan dengan pelarut campuran metanol: air : asam asetat glasial (10:90:1). Fase gerak adalah campuran natrium heksan sulfonat 5 mM dalam asam asetat glasial 0,5% dengan metanol yang dicampur secara gradien. Kondisi optimum metode gradien diperoleh pada laju alir 2,0 mL/menit, panjang gelombang 280 nm dengan waktu retensi 3,441 menit untuk piridoksin; 4,985 menit untuk riboflavin dan 7,393 menit untuk tiamin dengan resolusi 2,272 antara riboflavin dan piridoksin. Hasil uji presisi riboflavin dan piridoksin menggunakan metode isokratik (campuran natrium heksan sulfonat 5 mM dengan metanol dengan perbandingan 70 : 30) masing-masing dengan RSD adalah 1,377 dan 1,376 sedangkan metode gradien adalah 0,693 dan 0,825. Uji linearitas ketiga vitamin menggunakan dua metode isokratik dan gradien memenuhi persyaratan dengan R2 = 0,999.
Kata kunci : Vitamin B, sirup multivitamin, kromatografi cair kinerja tinggi
ABSTRACT: The aim of this research is to compare the simultaneous analytical results of B1 (Tiamin), B2 (Riboflavin), and B6 (Piridoxin) in multivitamin syrup between gradient and isocratic methods using high performance liquid chromatography (HPLC). The separation was performed on 15 cm length of C18 column and a mixture of methanol, water and glacial acetate acid with ratio of 10:90:1 was used as solvent. The eluent was a mixture of methanol and 5 mM sodium hexane sulfonate in 0.5% glacial acetate acid and gradually mixed using 2 different pumps. The optimal analytical conditions for gradient method were found to be 2,0 mL/min of flow rate and 280 nm of wavelength. On this gradient method, the vitamins were completely separated with retention times of 3.441 minutes, 4.985 minutes, and 7.393 minutes for piridoxin, riboflavin and tiamin respectively. Meanwhile, isocratic method (mixture of 5 mM sodium hexane sulfonate with metanol of 70 : 30) on the same conditions can only separate riboflavin and piridoxin. The RSD values for riboflavin and piridoxin were 1.377% and 1.376% respectively on isocratic methods and 0.693% and 0.825% respectively on gradient method. The linearity of both methods have fulfilled the requirement of R2 values that are higher than 0.999 for all vitamins.
Keywords: B Vitamins, Multivitamin Syrup, High Performance Liquid Chromatography
-
1. PENDAHULUAN seperti kapsul, tablet, sirup, dan injeksi.
Vitamin dalam suplemen, Suplemen ini diperlukan pada kasus
diperoleh dalam beberapa bentuk sediaan defisiensi sehingga vitamin dibutuhkan
oleh tubuh, untuk keseimbangan nutrisi yang pemakaiannya disesuaikan dengan yang dianjurkan oleh dokter dan ahli gizi.
Beberapa kasus defisiensi vitamin pada kondisi patologi atau metabolisme vitamin yang abnormal, kebutuhan nutrisi meningkat dari jumlah seharusnya seperti pada anemia, masa kehamilan, menstruasi, perdarahan, pada masa pertumbuhan dan usia lanjut [1].
Sirup multivitamin merupakan salah satu sediaan farmasi yang mengandung berbagai macam matriks dengan karakteristik yang berbeda-beda, sehingga dapat menganggu proses analisisnya. Pemilihan sediaan sirup umumnya diberikan pada pasien yang sulit untuk menelan sediaan padat seperti pada pasien anak-anak dan lanjut usia serta pasien lain yang kesulitan untuk menelan karena penyakitnya. Obat yang diberikan dalam bentuk larutan mudah tersedia untuk absorbsi, lebih cepat dan lebih efisien diabsorbsi dibandingkan dengan sejumlah obat yang sama yang diberikan dalam bentuk tablet atau kapsul [2].
Beberapa penelitian telah dilakukan yaitu menggunakan spektrofotometri UV untuk menganalisis kafein dan vitamin B6 secara simultan dalam minuman berenergi [3]. Yantih [4] menganalisis kadar Vitamin B1, B2, B3 dan B6 dalam sediaan sirup dengan metode eluasi isokratik KCKT. Penelitian berikutnya adalah penentuan Vitamin B1, B6, B12 dan Alfa Lipoic Acid dalam sediaan Kapsul dengan Kromatografi Cair Kinerja Tinggi (KCKT), diperoleh hasil bahwa validasi beberapa parameter seperti presisi, akurasi, dan linearitas telah memenuhi persyaratan analisis [4,5].
Analisis campuran senyawa dengan rentang polaritas yang lebar atau dengan kata lain pemisahan dengan waktu retensi yang panjang telah digunakan teknik eluasi gradien. Oleh karena itu maka metode ini dapat mengurangi waktu retensi sehingga analisisnya menjadi lebih efektif [6]. Selain itu dalam pengembangannya, diperoleh pula keuntungan metode eluasi
gradien antara lain: memungkinkan perkiraan rentang waktu retensi, pemiliham komposisi fase gerak yang sesuai, pemisahan yang lebih baik dan lebih cepat untuk sampel total, dan dapat memisahkan komponen dengan konsentrasi rendah yang sering terabaikan pada metode eluasi isokratik [7].
Pasangan ion jenis asam alkilsulfonat (-SO3(CH2)NCH3) dengan N antara 4–7 dapat membentuk pasangan ion dengan basa kuat dan lemah. Reagen pasangan ion adalah larutan sodium heksan sulfonat karena selain dapat membentuk pasangan ion dengan kation kuartener tiamin dan piridoksin dalam larutan asam juga diharapkan dapat memberikan waktu retensi yang tidak terlalu panjang [4].
Di antara semua teknik tersebut, bahwa metode kromatografi khususnya KCKT eluasi gradien merupakan salah satu metode yang cepat, sensitif dan akurat untuk penentuan vitamin secara simultan. Selain itu analisis dengan KCKT juga memiliki keuntungan yaitu ekonomis untuk pelarut, mudah dikombinasi dengan metode lain, dan memerlukan jumlah sampel yang sedikit.
Bahan: Standard Vitamin B1, B2 dan B6 BPFI, metanol (GT Baker), natrium hexan sulfonat (Merck), asam asetat glasial (Merck), aquabidest (Bratacho).
Alat: Kromatografi Cair Kinerja Tinggi Shimadzu 20-AD, dengan Kolom C18 (3.9 x 150 mm) merk Phenomenex dengan ukuran partikel 10 µm.
Pelarut adalah campuran Air: Metanol Asam asetat glasial (90: 10: 1) Fase Gerak: campuran larutan natrium heksan sulfonat 5 mM dalam asam asetat glasial 0,5% dengan metanol p.a. Larutan Baku Induk tiamin HCl, riboflavin HCl, dan piridoksin HCl dibuat berturut-turut dengan konsentrasi: 0,5; 0,075; 0,1 mg/mL.
Larutan Baku Campuran: dipipet masing-masing 4,0 mL larutan baku induk Tiamin HCl, 20,0 mL Riboflavin HCl, dan 4,0 mL Piridoksin HCl, dicampur dalam labu 50 ml. Ketiga campuran ini dikocok hingga homogen, setelah itu disaring menggunakan syringe filter 0,45 µm. Larutan sampel simulasi Tiamin, Piridoksin dan Riboflavin berturut-turut adalah 80%, 100% dan 120% dihomogenkan dengan ultrasonikator selama 20 menit pada suhu 60-75 oc.
Sebanyak 20 µL larutan baku kerja disuntikkan 6 kali, dihitung Relative Standard Deviation (RSD) atau simpangan baku relatif area dan RSD waktu retensi masing-masing komponen vitamin. Analisis dapat dilanjutkan jika nilai RSD lebih kecil dari 2 %.
Selektifitas
Larutan baku campuran disuntikkan ke dalam alat KCKT kemudian kromatogram larutan dibandingkan dengan kromatogram larutan pada percobaan uji kesesuaian sistem kromatografi.
Kelinieran
Dibuat satu seri larutan: 70%, 80%, 90%, 100%, 110% dan 120% dari kadar analit. Masing-masing larutan diinjeksikan ke dalam kolom KCKT sebanyak 20 µl dan diulang tiga kali.
Batas Deteksi (LOD) dan batas Kuantisasi (LOQ), Kecermatan, dan Keseksamaan
LOD dan LOQ dihitung menggunakan rumus Miller. Kecermatan dihitung persen perolehan kembali atau Spiked-placebo recovery method. Keseksamaan dihitung berdasarkan RSD dengan syarat lebih kecil dari 2%.
Panjang gelombang maksimal pada KCKT dengan detector Photo Diode Array (PDA) sebagai identifikasi awal memberikan serapan maksimum pada panjang gelombang 280 nm.
Hasil overlay dari ketiga jenis vitamin tersebut dapat dilihat pada Gambar 1.
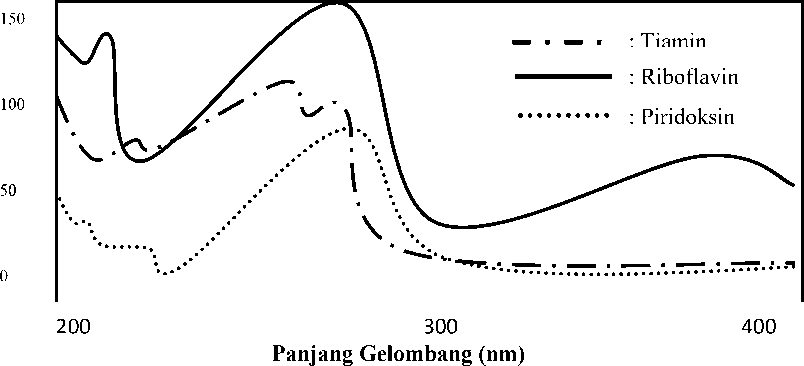
Gambar 1. Hasil Overlay Tiamin, Riboflavin dan Piridoksin dengan KCKT Menggunakan Detektor Photo Dio de Array (PDA)
Panjang kolom yang digunakan pada optimasi metode ada 2 yaitu 150 mm
dan 250 mm. Kolom 250 m, diperoleh hasil dengan waktu retensi piridoksin 4,328 menit, riboflavin 9,799 menit, dan tiamin 12,540 menit. Sedangkan kolom 150 mm dengan waktu retensi berturut– turut 3,441; 4,985 dan 7,393 menit.
Untuk variasi laju alir yaitu 1,0;1,5; dan 2,0 ml/menit dengan hasil pemisahan paling cepat pada laju alir 2,0 ml/menit dengan resolusi 2,272 pada eluasi gradien dan 2,222 pada eluasi isokratik. Resolusi yang diperoleh lebih besar dari 1,5 maka dapat dikatakan analit terpisah dengan baik seperti dalam Gambar 2.
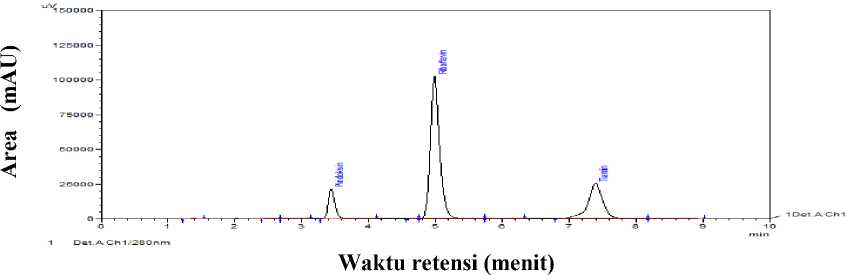
Gambar 2. Kromatogram Tiamin, Riboflavin dan Piridoksin pada Kondisi Optimum KCKT Metode Gradien
Uji parameter Kesesuaian Sistem (UKS) sebagai % Relatif Standard Deviasi (RSD) yang diperoleh pada analisis baik peak area maupun terhadap waktu retensi pada tiamin HCl, riboflavin HCl, dan piridoksin HCl menggunakan KCKT sebesar 0,2740,713% seperti pada Tabel 1. Hal ini
Uji Linearitas (Gambar 3) Persamaan kurva baku riboflavin adalah y = 42,453 x + 81072,80 dan nilai r2 = 0,9996; tiamin adalah y = 12,83 x – 9804,82 dengan nilai r2 = 0,9995; sedangkan untuk piridoksin y = 23,89 x + 420,29 dengan r2 = 0,9994. Dilihat dari
sesuai bahwa sistem dan prosedur dengan instrumen KCKT mampu memberikan hasil yang dapat diterima dengan %RSD ≤ 1% [10]. Hal ini dilakukan setiap kali melakukan analisis untuk tujuan memastikan kesesuaian sistem dan prosedur analisis
nilai r (koefisien korelasi) ≥ 0,999 maka kurva baku ketiga vitamin tersebut linier.
Tabel 1. Persentase (%) RSD luas puncak dan waktu retensi analit sebagai hasil Kesesuaian Sistem KCKT
|
Analit |
Konsentrasi (mg/mL) |
Peak Area |
Waktu retensi | ||
|
Rataan |
RSD (%) |
Rataan |
RSD (%) | ||
|
Tiamin HCl |
0,0394 |
378898 ± 1403 |
0,370 |
6,280 ± 0,025 |
0,402 |
|
Riboflavin |
0,0276 |
984209 ± 4089 |
0,415 |
4,422 ± 0,032 |
0,713 |
|
Piridoksin HCl |
0,0081 |
134026 ± 612 |
0,457 |
2,542 ± 0,007 |
0,274 |
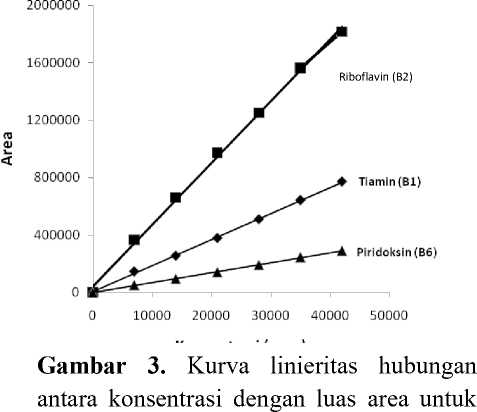
ketiga vitamin menggunakan metode
KCKT Gradien.
Presisi
Presisi adalah ukuran yang menunjukkan derajat kesesuaian antara hasil individual, diukur melalui penyebaran hasil individual
Terlihat dari tabel bahwa presisi ketiga jenis vitamin memenuhi persyaratan yaitu RSD bernilai lebih kecil dari 2 %. Dari data tabel dapat disimpulkan bahwa metode tersebut mempunyai ketelitian yang baik [7]. Sedangkan berdasarkan United State Pharmacopeia (USP) XXXI tahun 2008 untuk penentuan kadar masing-
LOD dan LOQ diperoleh dari persamaan garis yang dibuat dengan cara menghubungkan respon analit dengan konsentrasi yang dibuat secara bertingkat. Hasil perhitungan LOD dan LOQ menggunakan metode Miller disajikan pada Tabel 2. Dalam tabel terlihat bahwa nilai LOD adalah 2,8754 µg/mL, 260,5487 µg/mL, dan 6,7621 µg/mL berturut-turut untuk tiamin HCl, riboflavin HCl, dan piridoksin HCL. Sedangkan nilai LOQ masing-masing adalah 9,5848 µg/mL, 868,4956 µg/mL, dan 22,5404 µg/mL.
dari rata-rata jika prosedurditerapkan secara berulang pada sampel-sampel yang diambil dari campuran homogen. Pada penelitian ini, pengulangan dilakukan sebanyak 6 kali untuk masing-masing vitamin. Hasil uji presisi untuk ketiga jenis vitamin ditunjukkan oleh Tabel 3 di bawah ini.
masing vitamin memberikan hasil yang telah memenuhi syarat [8].
Akurasi
Akurasi merupakan ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya yang dinyatakan dengan persen perolehan kembali (recovery) analit
Tabel 2. Persamaan Garis Regresi, Batas Deteksi dan Batas Kuantitas Analit Dengan Metode
|
Analit |
Y = bx + a LOD (µg/mL) LOQ (µg/mL) |
|
Tiamin HCl Riboflavin Piridoksin HCl |
9730,63 x – 124268,98 2,8754 9,5848 16781,29 x + 127414,42 260,5487 868,4956 27627,11x + 83823,22 6,7621 22,5404 |
Tabel 3. Presisi Tiamin, Riboflavin dan Piridoksin Syarat kadar dari USP XXXI tahun 2008 [8]
|
Analit |
Kadar (%) Syarat* Rataan ±SD RSD (%) |
|
Tiamin HCl |
90,0 – 150,0 117,75 ± 1,874 1,592 |
|
Riboflavin |
90,0 – 150,0 104,83 ± 0,727 0,693 |
|
Piridoksin HCl |
90,0 – 150,0 97,68 ± 0,806 0,825 |
yang ditambahkan. Ada 3 level kadar yang ditetapkan pada penelitian ini yaitu 80%, 100% dan 120%. Replikasi untuk masing-masing level dilakukan sebanyak 3 kali. Pengujian dilakukan secara spiked-placebo recovery method yaitu dengan menambahkan analit pada matriks yang
Perbandingan Metode Isokratik dan Metode Gradien
Parameter uji yang dibandingkan adalah jumlah analit yang dapat dideteksi, waktu retensi, presisi, linearitas dan resolusi. Identifikasi awal menggunakan sampel, puncak tiamin pada sampel tidak terdeteksi dengan baik secara isokratik sehingga untuk selanjutnya analisis hanya dilakukan terhadap riboflavin dan piridoksin. Dengan menggunakan kolom, alat
diketahui komposisinya. Tabel 4 berikut menunjukkan hasil perolehan kembali analit dari uji akurasi metode terlihat perolehan kembali dari ketiga jenis vitamin tersebut telah memenuhi persyaratan karena nilai rerata kadar masih berada dalam rentang yang dipersyaratkan.
KCKT, laju alir yang sama diperoleh waktu retensi yang lebih pendek untuk metode KCKT gradien. Resolusi untuk metode gradien sebesar 2,272 sedangkan metode isokratik sebesar 2,222. Kedua metode memberikan hasil pemisahan yang baik dengan resolusi di atas 1,5 sesuai yang dipersyaratkan. Perbandingan hasil uji presisi riboflavin dan piridoksin dengan metode isokratik dan gradien dapat dilihat pada Tabel 5.
Tabel 4. Hasil Perolehan Kembali Analit dengan Metode KCKT Gradien
|
Analit |
Kons. (mg/ml) |
Perolehan Kembali (%) | |
|
Syarat * |
Rerata Kadar | ||
|
0,78 |
90,0 – 107,0 |
101,90 | |
|
Tiamin HCl |
0,61 |
90,0 – 107,0 |
100,80 |
|
1,13 |
90,0 – 107,0 |
99,97 | |
|
0,51 |
80,0 – 110,0 |
100,64 | |
|
Riboflavin |
0,62 |
80,0 – 110,0 |
101,30 |
|
0,76 |
80,0 – 110,0 |
101,11 | |
|
Piridoksin HCl |
1,35 |
90,0 – 107,0 |
100,17 |
|
1,59 |
90,0 – 107,0 |
99,23 | |
|
1,86 |
90,0 – 107,0 |
100,28 | |
*sumber [9]
Tabel 5. Perbandingan Hasil Presisi Riboflavin dan Piridoksin dengan Metode Isokratik dan Gradien
|
Vitamin |
Kadar (%) Syarat (Rataan ±SD) RSD (%) Isokratik Gradien Isokratik Gradien |
|
Riboflavin Piridoksin |
90,0 – 150,0 91,00 ± 1,253 104,83 ± 0,727 1,377 0,693 90,0 – 150,0 96,55 ± 1,329 97,68 ± 0,806 1,376 0,825 |
HCl
Presisi riboflavin dan piridoksin memperoleh nilai RSD yang lebih kecil dari 2 % sesuai persyaratan. Presisi riboflavin untuk metode gradien sebesar 1,98 kali lebih besar dibandingkan metode isokratik. Sedangkan untuk piridoksin HCl diperoleh presisi 1,66 kali lebih besar dibandingkan metode isokratik. Hasil tersebut menunjukkan bahwa metode gradien memiliki keseksamaan yang lebih optimal dibandingkan dengan metode isokratik. Pada Gambar 5 ditampilkan kurva linearitas riboflavin, piridoksin, dan
Persamaan kurva baku untuk riboflavin adalah y = 25951,23 x + 43050,46 dengan nilai r2 = 0,9999. Sedangkan persamaan kurva baku untuk piridoksin adalah y = 31627,91 x + 87988,76 dan nilai r2 = 0,9999. Berdasarkan nilai r hasil analisis maka kurva kalibrasi pada kedua metode dapat dikatakan linier [10].
Ke empat parameter yaitu waktu retensi, resolusi, uji linearitas dan uji presisi hanya waktu retensi dan uji presisi diperoleh hasil yang lebih baik menggunakan metode gradien. Resolusi antara antara
tiamin menggunakan metode isokratik.
dua senyawa memenuhi persyaratan analitik > 1,5
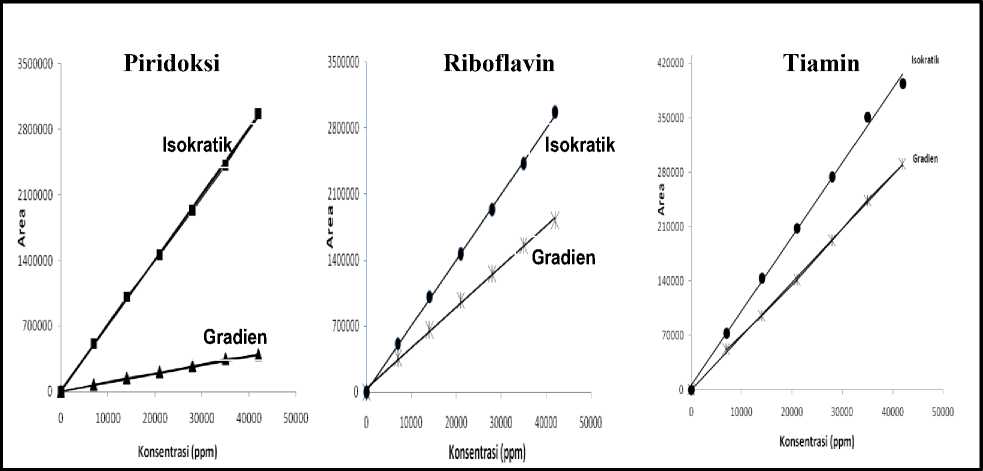
Gambar 5. Kurva linearitas hubungan antara konsentrasi (ppm) dengan peak area berturut-turut dari Piridoksin, Riboflavin, dan Tiamin menggunakan metode KCKT Isokratik dan Gradien
Resolusi pada metode isokratik hanya mampu memisahkan dengan baik dua komponen saja yaitu riboflavin dan piridoksin pada sampel yang digunakan.Uji linearitas memberikan hasil uji dengan nilai r yang memenuhi persyaratan untuk kedua metode. Dengan demikian dapat dikatakan bahwa metode gradien hasil optimasi lebih baik daripada metode isokratiknya dari segi waktu retensi, daya pisah dan presisi. Secara umum kedua metode dapat digunakan
untuk menganalisis vitamin riboflavin dan piridoksin dalam sediaan sirup multivitamin yang beredar di pasaran.
Metode KCKT gradien hasil optimasi pada penelitian ini dapat digunakan untuk analisis tiamin, riboflavin dan piridoksin pada sampel sediaan sirup multivitamin yang beredar di pasaran sedangkan metode isokratik hanya memisahkan riboflavin
dan piridoksin. Metode KCKT gradien hasil pengembangan dari metode isokratik tersebut memberikan hasil analisis yang lebih optimal dilihat dari parameter waktu retensi, daya pisah dan uji presisi.
Penulis mengucapkan terima kasih kepada Prof. Dr. Ir. I Gede Mahardika, M.Si; Dr. Drs. Manuntun Manurung, M.S; dan Dr. I Nengah Wirajana, S.Si., M.Si atas bimbingan, saran dan ide yang telah diberikan.
-
[1] Evert A., 2013, Medline Plus,
Vitamins, University of Washington Medical Center Diabetes Care
Center, Washington.
-
[2] Lachman L., Lieberman H.A., Kanig J.L., 1994, Teori dan Praktek
Farmasi Industri, UI Press, 942-943.
-
[3] Savitri M., 2007, Metode Cepat
Penentuan Simultan Kadar Kafein,
Vitamin B2 dan B6 dalam Minuman Berenergi dengan Teknik Zero
Crossing, IPB, Bogor.
-
[4] Yantih N., Widowati D., Wartini,
Aryani T., 2011, Validation of HPLC Method for Determination of Thiamine Hydrochloride, Riboflavin, Nicotiamide, and Pyridoxine
Hydrochloride in Syrup Preparation, Canadian Journal on Scientific and Industrial Research Vol. 2, No. 7.
-
[5] Poongothai S., Ilavarasan R., Karrunakaran C.M., 2010,
Simultaneous and accurate
Determination of Vitamins B1, B6, B12 and Alpha Lipoic Acid in Multivitamin Capsule by Reverse – Phase High Perfomance Liquid Chromatographic Method,
International journal of Pharmacy and Pharmaceutical Sciences Vol. 2, Suppl 4.
-
[6] Scoot, Paymond P.W., 1995,
Techniques and Practice of Chromatography, Marcel Dekker, Inc, USA 27-65, 284-287.
-
[7] Snyder L.R., Kirkland J.J., Dolan J.W., 2010, Introduction to Modern Liquid Chromatography, 24-30.
-
[8] US Pharmacopeial Covention, 2008, The United States Pharmacopeia, 31st rev., The National Formulary, 31st ed., The United States Pharmacopeial Convention, Inc., Rockville, 1034.
-
[9] Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya, Majalah Ilmu Kefarmasian, Vol. I No. 3, Departemen Farmasi F-MIPA, UI
-
[10] Ahuja S., Dong M.W., 2005,
Handbook of Pharmaceutical Analysis by HPLC, Elsevier Academic Press, New York, 21-35.
8
Discussion and feedback