HISTOPATHOLOGY OF RAT LIVER EXPOSED TO LEAD HEAVY METAL
on
Volume 15 No. 1: 1-9
Pebruari 2023
DOI: 10.24843/bulvet.2023.v01.i01.p01
Buletin Veteriner Udayana
pISSN: 2085-2495; eISSN: 2477-2712
Online pada: http://ojs.unud.ac.id/index.php/buletinvet
Terakreditasi Nasional Sinta 4, berdasarkan Keputusan Direktur Jenderal Pendidikan Tinggi, Riset, dan Teknologi No. 158/E/KPT/2021
Histopatologi Hati Tikus yang Terpapar Logam Berat Timbal
(HISTOPATHOLOGY OF RAT LIVER EXPOSED TO LEAD HEAVY METAL)
Elisabeth Karina1*, I Ketut Berata2, Ni Luh Eka Setiasih3
-
1Mahasiswa Sarjana Pendidikan Dokter Hewan, Fakultas Kedokteran Hewan, Universitas Udayana, JL. PB Sudirman, Denpasar, Bali, Indonesia, 80234;
-
2Laboratorium Patologi Veteriner, Fakultas Kedokteran Hewan, Universitas Udayana, JL. PB Sudirman, Denpasar, Bali, Indonesia, 80234;
-
3Laboratorium Histologi Veteriner, Fakultas Kedokteran Hewan, Universitas Udayana, JL. PB Sudirman, Denpasar, Bali, Indonesia, 80234;
*Email: feliciawen25@gmail.com
Abstrak
Timbal merupakan salah satu bahan pencemar udara yang sangat berbahaya. Toksisitas logam berat Pb dapat menimbulkan dampak yang berat, salah satunya pada organ hati. Penelitian ini bertujuan untuk mengetahui histopatologi hati pada tikus yang terpapar logam berat timbal dengan dosis yang berbeda. Penelitian ini menggunakan tikus putih jantan dengan strain Wistar, umur 2 bulan dan berat badan 250-300 g. Tikus yang digunakan 20 ekor dibagi atas empat kelompok perlakuan yaitu kontrol (P0), Pb asetat 0,5 ppm (P1), Pb asetat 1,0 ppm (P2), dan Pb asetat 2,0 ppm (P3) selama 30 hari. Pada hari ke 31 dilakukan nekropsi lalu organ hati diambil dan dimasukkan ke dalam netral buffer formalin 10%. Setelah organ hati difiksasi, dilakukan pembuatan preparat histopatologi menggunakan pewarnaan Hematoksilin dan Eosin. Pemeriksaan histopatologi dilakukan meliputi tiga variabel lesi yaitu kongesti, degenerasi melemak, dan nekrosis. Tingkat keparahan lesi tersebut dibuat skoring yaitu 0, 1, 2 dan 3 masing-masing apabila normal, lesi ringan, sedang dan berat. Data kemudian dianalisis dengan menggunakan uji non parametik Kruskal-Wallis dan Mann-Whitney. Hasil penelitian menunjukkan bahwa pemberian logam timbal dengan kandungan 0,5 ppm, 1,0 ppm, dan 2,0 ppm menyebabkan lesi histopatologi hati tikus berupa kongesti dan nekrosis yang signifikan dibandingkan kontrol, kecuali lesi degenerasi melemak.
Kata kunci: histopatologi, hati, timbal; tikus
Abstract
Lead is one of the most dangerous air pollutants. Lead toxicity can have a severe impact, one of which is on the liver. The purpose of this research was to determine the liver histopathology of rats exposed to lead at different doses. This study used white rats of the Wistar strain, 2 months old and weighing 250-300 g. The rats used were 20 given four treatments, control (P0), 0.5 ppm Pb acetate (P1), 1.0 ppm Pb acetate (P2), and 2.0 ppm Pb acetate (P3) for 30 days. On day 31, a necropsy was performed and the liver was removed and put into 10% neutral buffered formalin. After the liver was fixated, histopathological preparations were made using Hematoxylin and Eosin. Histopathological examination staining with three variables measured, which were congestion, fatty degeneration, and necrosis. The severity of the lesions was scored as 0, 1, 2, and 3 which could cause normal, mild, moderate, and severe lesions. The data was then analyzed using the Kruskal-Wallis and Mann-Whitney non-parametric tests. The result of this research showed that the administration of lead containing 0.5 ppm, 1.0 ppm, and 2.0 ppm had an effect on the histopathology of the liver of rats lesions as significant congestion and necrosis compared to controls, except for fatty degenerating lesions.
Keywords: lead; rats; liver; histopathology
PENDAHULUAN
Timbal (Pb) merupakan salah satu bahan pencemar udara yang sangat berbahaya (Sjamsudin, 1987). Makhluk hidup dapat terpapar oleh logam berat Pb di alam melalui oral, inhalasi udara, dan melalui permukaan kulit. Pada manusia timbal diserap dari proses inhalasi sebanyak 20-50% dan dari proses menelan sebanyak 5-15% (Minarti et al., 2016). Di dalam tubuh, timbal bersifat sebagai radikal bebas (Aulanni’am et al., 2019). Seperti yang dilaporkan oleh Pratama (2020), radikal bebas merupakan molekul yang memiliki sifat tidak stabil dan reaktif, dikarenakan memiliki satu atau lebih elektron yang tidak berpasangan, dimana radikal bebas ini dapat menyerang makromolekul penting, seperti DNA, protein, karbohidrat, dan lipid sehingga dapat menyebabkan kerusakan sel dan gangguan homeostasis. Timbal
merupakan bahan toksik yang mudah terakumulasi dalam tubuh manusia khususnya pada organ tertentu (Lidya, 2012). Toksisitas logam berat Pb dapat memberikan dampak yang berat, terutama pada organ hati (Setiawan, 2012). Adapun mekanisme kerusakan hati oleh timbal dapat terjadi akibat meningkatnya radikal bebas dan penurunan kemampuan sistem antioksidan tubuh sehingga memicu stres oksidatif (Rachmani et al., 2020).
Berdasarkan Standar Nasional
Indonesia (2019) batas maksimum cemaran timbal dalam pangan berupa daging dan produk daging adalah 1,0 ppm. Maka dari itu dalam penelitian ini menggunakan dosis timbal dibawah ambang batas (0,5 ppm), pada ambang batas (1,0 ppm), dan diatas ambang batas (2,0 ppm). Penelitian bertujuan untuk mengetahui dampak dari paparan logam berat timbal pada dosis di sekitar ambang batas (1,0 ppm) terhadap histopatologi hati pada tikus (Rattus norvegicus).
METODE PENELITIAN
Persetujuan Komisi Etik Penelitian
Seluruh prosedur pemakaian hewan coba telah mendapat persetujuan dari Komite Etik Hewan Fakultas Kedokteran Hewan Universitas Udayana, dengan Surat Persetujuan Etik Hewan nomor: B/37/UN14.2.9/PT.01.04/2022.
Objek Penelitian
Objek penelitian yang digunakan dalam penelitian ini adalah tikus putih jantan dengan strain Wistar, umur 2 bulan, dan berat badan 250-300 g. Sampel penelitian adalah hati tikus yang diambil setelah diberi perlakuan sesuai kelompok perlakuan.
Rancangan Penelitian
Perlakuan diberikan selama 30 hari dan pada hari ke 31 dilakukan euthanasia serta nekropsi untuk diambil organ hatinya. Bahan penelitian adalah bahan pakan tikus 511, air minum, larutan Pb asetat, set bahan pembuatan preparat dan pewarnaan Hematoxylin dan Eosin (HE). Peralatan yang digunakan dalam penelitian ini yaitu kandang tikus berupa kotak plastik ukuran 20x30 cm, tempat pakan, tempat minum, set alat nekropsi, sonde, set alat pembuatan preparat dan pewarnaan Hematoxylin-Eosin untuk pemeriksaan histopatologi.
Penelitian menggunakan rancangan acak lengkap (RAL) dengan 4 perlakuan, yaitu kontrol (P0), Pb asetat 0,5 ppm (P1), Pb asetat 1 ppm (P2) dan Pb asetat 2 ppm (P3). Jumlah total hewan coba yang digunakan 20 ekor dengan jumlah ulangan masing-masing perlakuan lima kali, sesuai penghitungan jumlah sampel: (t)(n-1)>15. Prosedur pembuatan larutan Pb asetat, timbang serbuk timbal (II) asetat trihidrat sebanyak 0,002 mg untuk membuat larutan 2 ppm Pb asetat, setelah sudah sesuai nominal masukan serbuk kedalam tabung gelas kaca berukuran 1 liter. Masukkan aquades sebanyak satu liter kedalam
tabung gelas kaca dan diaduk sampai larutan homogen. Ambil gelas ukur, lalu tuangkan larutan 2 ppm yang sudah jadi sebanyak 400 ml kedalam tabung gelas kaca kedua untuk pembuatan larutan 1 ppm Pb asetat. Tambahkan aquades sebanyak 400 ml, aduk sampai homogen. Ambil gelas ukur kembali, lalu tuangkan larutan 1 ppm yang sudah jadi sebanyak 300 ml kedalam kedalam tabung gelas kaca ketiga untuk pembuatan larutan 0,5 ppm Pb asetat. Tambahkan aquades sebanyak 400 ml, aduk sampai homogen.
Prosedur perlakuan terhadap objek penelitian alat dipersiapkan dan juga bahan yang akan digunakan pada meja perlakuan. Tikus dipersiapkan sesuai dengan pemberian perlakuan. Tandai tikus dengan spidol hitam pada ekor untuk mencegah pemberian perlakuan berulang. Ambil larutan Pb asetat dengan spuit 1 ml sesuai dosis yang dialokasikan pada tikus dan pasang sonde pada spuit. Lalu dengan hati-hati sonde dimasukkan melalui mulut sampai ke lambung dan tekan spuit untuk memasukkan larutan Pb asetat. Setelah larutan Pb asetat masuk dalam lambung, tarik kembali sonde dan tikus dikembalikan ke kandang. Demikian pula langkah selanjutnya pada tikus penelitian. Perlakuan pada tikus diberikan setiap hari selama 30 hari dan hari ke 31 dilakukan euthanasia dan nekropsi. Secara aseptis organ hati diambil dan dimasukkan ke dalam netral buffer formalin 10% (NBF) untuk dilanjutkan dalam pembuatan preparat histopatologi.
Pembuatan Preparat Histologi
Pembuatan preparat histopatologi dilakukan dengan metode Kiernan (2016) Organ hati difiksasi dengan larutan neutral buffer formalin 10% minimal 24 jam. Kemudian jaringan dipotong dan dimasukkan ke dalam wadah spesimen. Selanjutnya proses dehidrasi pada konsentrasi alkohol bertingkat yaitu alkohol 70%, 80%, 90%, alkohol absolut I dan absolut II. Tahapan selanjutnya adalah penjernihan dengan xylol dan pencetakan menggunakan parafin, lalu
disimpan dalam lemari es. Kemudian dipotong tipis 4-5 μm menggunakan mikrotom. Hasil potongan diapungkan dalam waterbath agar jaringan tidak berlipat. Kemudian sediaan diletakkan pada gelas objek untuk pewarnaan Hematoksilin dan Eosin.
Pada pewarnaan HE, sediaan direndam dalam xylol 1 dan 2 untuk dilakukan deparafinasi kemudian dehidrasi dengan perendaman pada alkohol absolut, alkohol 95%, dan alkohol 80% masing-masing selama 2 menit, lalu dicuci dengan air mengalir. Pewarnaan dengan Hematoksilin dilakukan selama 8 menit, dibilas dengan air mengalir, lalu dicuci dengan Lithium karbonat selama 15-30 detik, dibilas dengan air mengalir. Pewarnaan Eosin selama 2-3 menit. Sediaan yang diwarnai eosin dicuci dengan air mengalir lalu dikeringkan. Kemudian sediaan dimasukkan ke dalam alkohol 95% dan alkohol absolut masing-masing sebanyak 10 kali celupan dan ke dalam alkohol absolut 2 selama 2 menit. Selanjutnya ke dalam xylol 1 selama 1 menit dan xylol 2 selama 2 menit. Sediaan kemudian diteteskan dengan permount sebagai perekat dan ditutup dengan gelas penutup yang dilanjutkan pemeriksaan di bawah mikroskop.
Variabel Penelitian
Perubahan histopatologi hati yang diperiksa akibat paparan logam berat Pb meliputi lesi kongesti, lesi degenerasi melemak, dan lesi nekrosis. Masing-masing lesi diperiksa pada lima lapang pandang mikroskopik. Tingkat keparahan lesi tersebut dibuat skoring yaitu skor 0 berarti normal atau tidak ada lesi, skor 1 berarti ringan atau lesi bersifat fokal, skor 2 berarti sedang atau lesi bersifat multifokal, dan skor 3 berarti berat atau lesi bersifat difusa.
Analisis Data
Data hasil pemeriksaan histopatologi ditabulasi dan dianalisis dengan uji non parametrik Kruskal-Wallis. Jika ada perbedaan yang nyata (P<0,05) akan
dilanjutkan dengan uji Mann-Whitney. Semua proses analisis data dilakukan dengan program SPSS.
HASIL DAN PEMBAHASAN
Hasil
Hasil pengamatan histopatologi hati tikus yang diberikan timbal asetat dengan dosis 0,5 ppm, 1,0 ppm, dan 2,0 ppm sangat bervariasi perubahan kongesti ringan ditemukan pada satu jaringan hati masing-masing pada perlakuan kontrol (P0), P1, P2, sedangkan P3 ditemukan perubahan kongesti sedang pada empat jaringan hati. Perubahan degenerasi melemak ringan ditemukan pada satu jaringan hati dengan perlakuan P1, satu jaringan hati dengan perlakuan P2, satu jaringan hati dengan perlakuan P3. Sedangkan pada perlakuan kontrol (P0) tidak ditemukan perubahan degenerasi melemak (Tabel 1).
Perubahan nekrosis ringan ditemukan pada empat jaringan hati dengan perlakuan P2. Perubahan nekrosis sedang
ditemukan pada satu jaringan hati dengan perlakuan P3 dan perubahan nekrosis berat ditemukan pada empat jaringan hati dengan perlakuan P3. Sedangkan pada perlakuan kontrol (P0) dan P1 tidak ditemukan perubahan nekrosis.
Berdasarkan hasil pemeriksaan
histopatologi hati tikus setelah diberikan perlakuan, hasil pemeriksaan histopatologi hati tikus (data skoring) setelah diberi perlakuan tersaji di Tabel 1.
Dari hasil analisis Kruskal-Wallis menunjukkan perolehan nilai rerata perlakuan untuk lesi kongesti adalah 0,044, yang berarti terdapat perbedaan nyata (P<0,05) antara kelompok kontrol dengan kelompok perlakuan. Nilai rerata perlakuan untuk lesi degenerasi melemak adalah 0,773, yang menunjukkan tidak ada perbedaan nyata (P>0,05) antara perlakuan kontrol dengan kelompok perlakuan. Nilai rerata perlakuan untuk lesi nekrosis adalah 0,001, yang berarti terdapat perbedaan nyata (P<0,05) antara kelompok kontrol
dengan kelompok perlakuan (tersaji di Tabel 2). Karena pada uji Kruskal-Wallis didaparkan adanya perbedaan yang signifikan, maka akan dilanjutkan dengan uji Mann-Whitney (tersaji pada Tabel 3).
Hasil dari uji Mann-Whitney untuk lesi kongesti antara kelompok kontrol (P0) dengan kelompok perlakuan P1 (0,5 ppm) dan kelompok kontrol dengan kelompok perlakuan P2 (1,0 ppm) tidak terdapat perbedaan nyata (P>0,05). Namun antara kelompok kontrol dengan kelompok perlakuan P3 (2,0 ppm) tedapat perbedaan yang nyata (P<0,05). Kemudian antara kelompok perlakuan P1 dengan perlakuan P2 tidak terdapat perbedaan nyata (P>0,05). Untuk perlakuan P1 dengan P3 dan perlakuan P2 dengan P3 terdapat perbedaan nyata (P<0,05). Hasil dari uji Mann-Whitney untuk lesi degenerasi melemak antara kelompok kontrol dengan kelompok perlakuan P1, kelompok kontrol dengan kelompok perlakuan P2, kelompok kontrol dengan kelompok perlakuan P3, kelompok perlakuan P1 dengan kelompok perlakuan P2, kelompok perlakuan P1 dengan kelompok perlakuan P3, dan kelompok perlakuan P2 dengan kelompok perlakuan P3 tidak terdapat perbedaan nyata (P>0,05).
Hasil dari uji Mann-Whitney untuk lesi nekrosis antara kelompok kontrol dengan kelompok perlakuan P1 tidak terdapat perbedaan nyata (P>0,05). Sementara untuk kelompok kontrol dengan kelompok perlakuan P2, kelompok kontrol dengan kelompok perlakuan P3, kelompok perlakuan P1 dengan kelompok perlakuan P2, kelompok perlakuan P1 dengan kelompok perlakuan P3, dan kelompok perlakuan P2 dengan kelompok perlakuan P3 terdapat perbedaan nyata (P<0,05).
Hasil dari pengamatan di bawah mikroskop pada keempat perlakuan dengan perbesaran 40x dan pewarnaan Hematoxylin dan Eosin pada Gambar 1.
Hasil penelitian ini menunjukkan bahwa pemberian Pb asetat pada dosis 0,5 ppm (P1), 1,0 ppm (P2), dan 2,0 ppm (P3)
menyebabkan perubahan histopatologi hati tikus berupa lesi kongesti, degenerasi melemak dan nekrosis, dibandingkan tanpa pemberian Pb asetat (kontrol). Pada kontrol (P0) terlihat adanya perubahan histopatologi berupa lesi kongesti yang bersifat ringan atau fokal. Adanya perubahan histopatologi pada kontrol (P0) berupa lesi kongesti yang ringan dapat diakibatkan oleh status kesehatan tikus percobaan sebelum diberi perlakuan. Penggunaan hewan coba konvensional yang tidak bersifat specific pathogen free (SPF) sering mengakibatkan hewan kontrol (P0) mengalami perubahan histopatologi yang tidak diharapkan, dimungkinkan karena pengaruh makanan yang tidak higienis ataupun faktor lingkungan yang menyebabkan gangguan kesehatan pada tikus.
Lesi kongesti bervariasi diantara kelompok perlakuan. Pada perlakuan P1 (0,5 ppm) dan perlakuan P2 (1,0 ppm) terdapat kongesti ringan pada sel-sel hati, lain halnya dengan perlakuan P3 (2,0 ppm) terdapat kongesti sedang. Kongesti ini bisa disebabkan karena beberapa hal, diantaranya adalah reaksi peradangan akibat trauma, toksin atau mikroorganisme (Salbahaga et al., 2012). Pada penelitian ini, lesi kongesti yang terjadi disebabkan oleh adanya toksin berupa Pb asetat yang dipaparkan selama satu bulan. Lesi kongesti dapat dikategorikan ringan karena hanya terdapat satu lesi kongesti di dalam lima pandang dan lesi dapat dikategorikan sedang karena terdapat lebih dari satu lesi kongesti di dalam lima pandang mikroskopik.
Pembahasan
Kongesti merupakan lesi penimbunan eritrosit dalam pembuluh darah akibat gangguan patofisologis baik dari dalam pembuluh darah atau di luar pembuluh darah (Berata et al., 2011). Kongesti ditandai dengan warna merah pada sel, hal ini terjadi karena adanya peningkatan darah di dalam pembuluh darah. Menurut Royan et al. (2014), kongesti terjadi akibat reaksi keradangan dan kerusakan bagian
organ. Kongesti akan menunjukkan perubahan warna merah, sesuai dengan derajat oksigenasi darah. Kongesti juga merupakan gejala patologis pertama dari kerusakan jaringan dan terdapat peningkatan jumlah darah di dalam pembuluh darah sehingga akan tampak kapiler darah melebar dan sinusoidsinusoid di hati terisi banyak eritrosit. Seperti pada gambar 1, lesi kongesti perlakuan P1, perlakuan P2, dan P3 terlihat adanya banyak eritrosit pada sel-sel hati.
Lesi degenerasi melemak pada hati ditemukan pada perlakuan P1 (0,5 ppm), P2 (1,0 ppm), dan P3 (2,0 ppm) dengan tingkat ringan/fokal. Degenerasi merupakan perubahan abnormal dari morfologi jaringan atau sel (Berata et al., 2011). Pada organ hati, terdapat sel hati dengan inti sel yang berfungsi mengakumulasi lemak dan glikogen pada sitoplasma (Panigoro et al., 2007). Degenerasi melemak ditandai dengan adanya akumulasi lemak di dalam sitoplasma hepatosit. Degenerasi melemak (fatty degeneration) biasanya terjadi dalam sel-sel parenkimatosa, salah satunya pada sel hepar. Faktor penyebab terjadinya degenerasi melemak adalah bahan toksik, kekurangan oksigen, atau kelebihan konsumsi lemak dan protein (Dannuri, 2009).
Degenerasi melemak ini terjadi karena adanya akumulasi lemak di dalam sel hati yang terlihat dengan adanya vakuola-vakuola kecil di dalam sitoplasma, vakuola-vakuola ini dapat membesar dan mendesak inti sel ke bagian tepi sel hati. Radikal bebas yang berlebihan akan menimbulkan stres oksidatif yang memicu proses peroksidasi terhadap lipid dikarenakan terdapat peningkatan kadar malondialdehid (MDA). Penumpukan radikal bebas merupakan salah satu mekanisme yang berperan dalam kerusakan hati dan melibatkan pembentukan degenerasi melemak hingga nekrosis (Eric et al., 2016).
Nekrosis merupakan proses kematian sel yang abnormal akibat adanya reaksi terhadap zat tertentu seperti bahan kimia toksik. Nekrosis dapat diawali dengan perubahan morfologi piknosis atau inti sel menjadi lebih padat, karioheksis atau inti pecah, dan kariolisis atau inti menghilang (Adikara et al., 2013). Lesi nekrosis pada perlakuan P2 (1,0 ppm) terdapat satu jaringan hati mengalami nekrosis sedang, dan tikus dengan perlakuan P3 (2,0 ppm) terdapat empat jaringan hati mengalami nekrosis berat/difusa. Pada daerah nekrosis ditemukan adanya infiltrasi sel radang berupa limfosit serta proliferasi sel kuffer pada hati. Adanya sel-sel ini dikarenakan terdapat inflamasi yang bersifat kronis. Keracunan yang bersifat kronis ini terjadi karena adanya absorbsi timbal (Pb) dalam jumlah kecil yang terpapar dalam waktu cukup lama sehingga terakumulasi dalam organ hati (Hidayat et al., 2013).
Menurut Muselin et al. (2010), terdapat lesi nekrosis pada hati dapat disebabkan oleh stres oksidatif akibat terpapar timbal. Stres oksidatif terjadi akibat ketidakseimbangan antara jumlah radikal bebas yang masuk dan jumlah antioksidan di dalam tubuh untuk detoksifikasi (Jaishankar et al., 2014). Dalam kondisi stres oksidatif, konsentrasi oxidized glutathione (GSSG) melebihi konsentrasi reduced glutathione (GSH). Dapat juga disebabkan karena radikal bebas mendapatkan elektron dari molekul lipid yang ada di dalam membran sel pada organ hati yang akhirnya menyebabkan peroksidasi lipid. Jika konsentrasi radikal bebas yang masuk kedalam tubuh terlalu tinggi dapat menyebabkan kerusakan komposisi dari sel darah merah, membran protein dan lipid, menghambat sintesis hemoglobin (Sharma et al., 2014), yang berpotensi mengakibatkan apoptosis atau kematian sel (nekrosis) (Abdou et al., 2014).
Perubahan histopatologi hati tikus yang diberikan paparan timbal pada penelitian ini sejalan dengan penelitian yang
dilakukan oleh Offor (2017) yang menyatakan bahwa, logam berat timbal berpengaruh terhadap struktur jaringan hati tikus yaitu dapat menimbulkan lesi berupa kongesti, degenerasi melemak, dan nekrosis. Penelitian ini juga sejalan dengan laporan Berata, et al (2017), bahwa hati merupakan organ utama tempat akumulasi logam berat Pb pada sapi dengan beberapa lesi dibandingkan organ lainnya.
SIMPULAN DAN SARAN
Simpulan
Ada perbedaan signifikan perubahan histopatologi berupa kongesti dan nekrosis akibat pemberian Pb asetat dibandingkan kontrol, kecuali pada lesi degenerasi melemak. Pemberian Pb asetat dosis 2,0 ppm menyebabkan lesi kongesti maupun nekrosis yang terparah dibandingkan dosis 0,5 ppm, 1,0 ppm maupun kontrol.
Saran
Perlu penelitian lebih lanjut tentang pemberian Pb asetat dengan dosis yang berbeda yang meliputi berbagai jaringan dengan parameter perubahan histopatologi yang lebih banyak.
UCAPAN TERIMAKASIH
Penulis mengucapkan terima kasih kepada Kepala Balai Besar Veteriner Denpasar, Kepala Laboratorium Patologi Fakultas Kedokteran Hewan Universitas Udayana, yang memfasilitasi penelitian ini.
DAFTAR PUSTAKA
Abdou HM, Hassan MA. 2014. Protective role of omega-3 polyunsaturated fatty acid against lead acetate-induced toxicity in liver and kidney of female rats. BioMed Res. Int. 2014: 1-11.
Adikara IA, Winaya IBO, Sudira IW.
2013. Studi histopatologi hati tikus putih (rattus norvegicus) yang diberi ekstrak etanol daun kedondong
(spondias dulcis g. forst) secara oral. Bul. Vet. Udayana. 5(2): 107-113.
Aulanni’am A, Julianto A, Dewi MA, Dirgahariyawan TC, Chanif M, Wuragil DH, Herawati H. 2019. Potensi ekstrak beluntas (pluchea indica less) sebagai upaya preventif gangguan akibat paparan timbal (pb) pada berbagai organ tikus (rattus norvegicus). Vet. Biol. Cin. J. 1(1): 1-8.
Badan Standarisasi Nasional (BSN). 2009. Standar Nasional Indonesia (SNI) 73872009 tentang batas maksimum cemaran logam berat dalam pangan. Pp: 1-25.
Berata IK, Winaya IBO, Adi AAAM, Adnyana IBW. 2011. Patologi veteriner umum. Denpasar: Swasta Nulus.
Berata IK, Susari NNW, Kardena IM, Winaya I BO, Manuaba IBP. 2017. Comparison of lead contamination in innards and muscle tissues of bali cattle reared in Suwung Landfill. Bali. Med. J. 6(1): 147-149.
Dannuri H. 2009. Analisis enzim Alanin Amino Transferase (ALAT), Aspartat Amino Transferase (ASAT), urea
darah, dan histopatologis hati dan ginjal tikus putih galur sprague-dawley
setelah pemberian angklak. J. Teknol. Indon Pangan. 20(1): 1-9.
Eric Y, Arooj B, Moaz C, Matthew K, Nikolaos P. 2016.
AcetaminophenInduced hepatotoxicity: a comprehensive update. J. Clin.
Transl. Hepatol. 4(2): 131-142.
Hidayat A, Christijanti W, Marianti A. 2013. Pengaruh vitamin E terhadap kadar SGPT dan SGOT tikus putih galur wistar yang dipapar timbal. Unnes. J. Life Sci. 2 (1): 16-21.
Jaishankar M, Tseten T, Anbalagan N, Mathew BB, Beeregowda KN. 2014. Toxicity, mechanism and health effects of some heavy metals. Interdisciplinary Toxicol. 7(2): 60-72.
Kiernan JA. 2016. Histological and histochemical merthods: theory and pratice. 5th edition. poland. Medical University of Gdansk.
Lidya F. 2012. Studi kandungan logam berat timbal (Pb), nikel (Ni), kromium (Cr) dan kadmium (Cd) pada kerang hijau (perna viridis) dan sifat fraksionasinya pada sedimen laut. Skripsi Fakultas Matematika Dan Ilmu Pengetahuan Alam Departemen Kimia Depok, (Cd).
Minarti FA, Setiani O, Joko T. 2016. Hubungan paparan timbal dengan kejadian gangguan fungsi hati pada pekerja pengecoran logam di CV. Sinar Baja Cemerlang Desa Bakalan, Ceper Kabupaten Klaten. J. Kes. Lingk. Indon. 14(1): 1-6.
Muselin F, Trif A, Brezofan D, Stancu C, Snejana P. 2010. The consequences of chronic exposure to lead on liver, spleen, lungs and kidney arhitectonics in rats. Lucrări Ştiinłifice Med. Vet. 43:(2): 123-127.
Offor SJ, Mbagwu HOC, Orisakwe OE. 2017. Lead induced hepato-renal damage in male albino rats and effects of activated charcoal. Front. Pharmacol. 8(3): 107.
Panigoro N, Indri A, Meliya B, Salifira, Prayudha DC, dan Kunika W. 2007. Teknik dasar histologi dan atlas dasar-dasar histopatologi ikan. Balai Budidaya Air Tawar dan Japan International Coperation Agency (JICA). Jambi.
Pratama AN, Busman H. 2020. Potensi antioksidan kedelai (glycine max l) terhadap penangkapan radikal bebas. Jurnal Ilmiah Kesehatan Sandi Husada, 11(1), 497-504.
Rachmani SD, Hestianah EP, Plumerastuti H, Darson R, Safitri E. 2020. Efektifitas propolis pada perbaikan histopatologi hepar mencit betina yang dipapar logam berat Pb asetat. Med. Ked. Hewan. 2020: 23-32.
Royan F, Rejeki S, dan Haditomo AHC. 2014. Pengaruh salinitas yang berbeda terhadap profil darah ikan nila. J. Aquaculture Manag. Technol. 3(2):
109-117.
Salbahaga DP, Supartika IKE, Berata IK. 2012. Distribusi lesi negri’s bodies dan peradangan pada otak anjing penderita rabies di Bali. Indon. Med. Vet. 1(3): 352-360.
Setiawan AM. 2012. Pengaruh pemberian timbal (Pb) dosis kronis secara oral terhadap peningkatan penanda
kerusakan organ pada mencit. El-Hayat. 3(1): 24-28.
Sharma B, Singh S, Siddiqi NJ. 2014. Biomedical implications of heavy metals induced imbalances in redox systems. BioMed Res. Int. 2014: 640754.
Sjamsudin U. 1987. Logam berat antagonis. Dalam Farmakologi dan Terapi. Edisi 3. Jakarta: Universitas Indonesia.
Tabel 1. Hasil Pemeriksaan Histopatologi Hati Tikus (Data Skoring) setelah Diberi Perlakuan
Perlakuan Kongesti Degenerasi Melemak Nekrosis
|
Skoring |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
|
P0 (Kontrol) |
4/5 |
1/5 |
- |
- |
5/5 |
- |
- |
- |
5/5 |
- |
- |
- |
|
P1 (Pb 0,5 ppm) |
4/5 |
1/5 |
- |
- |
4/5 |
1/5 |
- |
- |
5/5 |
- |
- |
- |
|
P2 (Pb 1 ppm) |
4/5 |
1/5 |
- |
- |
4/5 |
1/5 |
- |
- |
1/5 |
4/5 |
- |
- |
|
P3 (Pb 2 ppm) |
1/5 |
- |
4/5 |
- |
4/5 |
1/5 |
- |
- |
- |
- |
1/5 |
4/5 |
Keterangan: Skor 0= normal, Skor 1= ringan (fokal), 2= sedang (multifokal), 3= berat (difusa).
|
Tabel 2. Hasil Uji Kruskal-Wallis Data Skoring Berdasarkan Lesi yang Diperiksa | |||
|
Kongesti |
Degenerasi Melemak |
Nekrosis | |
|
Chi-Square |
8,075 |
1,118 |
17,257 |
|
Df |
3 |
3 |
3 |
|
Asymp. Sig |
0,044 |
0,773 |
0,001 |
|
Keterangan: Df= degree of freedom, Asymp. Sig.= asymptotic significance. | |||
|
Tabel 3. Hasil Uji Mann-Whitney Data Skoring Berdasarkan Lesi yang Diperiksa | |||
|
Uji Mann Whitney antar perlakuan |
Lesi Yang Diperiksa | ||
|
Kongesti |
Degenerasi Melemak |
Nekrosis | |
|
P0-P1 |
1,000 |
1,000 |
1,000 |
|
P0-P2 |
0,513 |
1,000 |
0,014* |
|
P0-P3 |
0,028* |
0,317 |
0,004* |
|
P1-P2 |
0,513 |
1,000 |
0,014* |
|
P1-P3 |
0,028* |
0,317 |
0,004* |
|
P2-P3 |
0,044* |
0,317 |
0,005* |
|
Tanda (*) menunjukkan adanya perbedaan signifikan dengan P<0,05 | |||
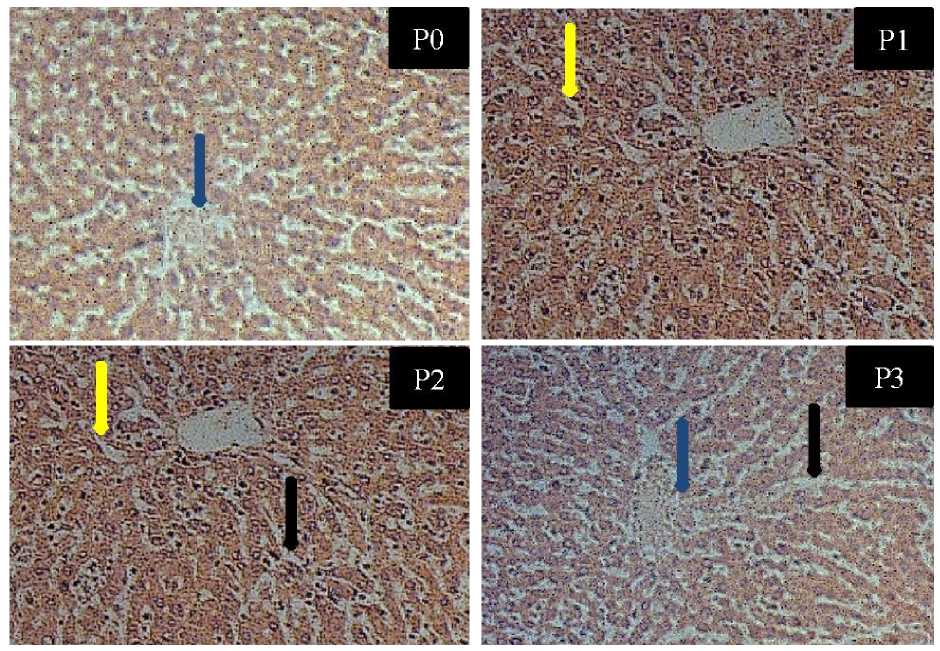
Gambar 1 Histopatologi Hati Tikus (Rattus norvegicus). P0 (Kontrol) Secara Umum Masih Normal. P1 (Pemberian Pb 0,5 Ppm) dan P2 (Pemberian Pb 1,0 Ppm) Terdapat Perubahan Ringan. P3 (Pemberian Pb 2,00 Ppm) Terdapat Kongesti dan Nekrosis Disekitar Vena Sentralis (HE, 40x). Keterangan: Panah Biru (Kongesti), Panah Kuning (Degenerasi melemak), Panah Hitam (Nekrosis).
9
Discussion and feedback