DEVELOPMENT OF A DNA VACCINE WITH NUCLEOPROTEIN GENE OF THE SARS-COV-2 VIRUS
on
Buletin Veteriner Udayana Volume 15 No. 5: 1002-1011
pISSN: 2085-2495; eISSN: 2477-2712 Oktober 2023
Online pada: http://ojs.unud.ac.id/index.php/buletinvet https://doi.org/10.24843/bulvet.2023.v15.i05.p37
Terakreditasi Nasional Sinta 4, berdasarkan Keputusan Direktur Jenderal
Pendidikan Tinggi, Riset, dan Teknologi No. 158/E/KPT/2021
Studi Pendahuluan Pengembangan Vaksin DNA Menggunakan Gen Nukleoprotein Virus SARS-COV-2
(DEVELOPMENT OF A DNA VACCINE WITH NUCLEOPROTEIN GENE OF THE SARS-COV-2 VIRUS)
Ni Putu Sutrisna Dewi1*, I Gusti Ngurah Kade Mahardika2, Ida Bagus Kade Suardana3
-
1Program Studi Magister, Fakultas Kedokteran Hewan, Universitas Udayana, Jl. PB. Sudirman, Denpasar, Bali, 80225, Indonesia;
-
2Laboratorium Biomedik dan Biologi Molekuler Fakultas Kedokteran Hewan, Universitas Udayana, Jl. Raya Sesetan Gang Markisa 6A, Denpasar, Bali, 80223, Indonesia;
-
3Laboratorium Virologi Fakultas Kedokteran Hewan, Universitas Udayana Jl. PB. Sudirman, Denpasar, Bali, 80225, Indonesia.
*Corresponding author email: sutrisnadewi99@gmail.com
Abstrak
Vaksin DNA telah menjadi bidang penelitian yang menarik dalam upaya melawan penyakit infeksius pada hewan. Vaksin DNA adalah formulasi vaksin yang menggunakan fragmen DNA sebagai antigen. DNA pada vaksin mengandung informasi genetik yang diambil dari agen penyakit, seperti virus atau bakteri, yang ingin ditargetkan. Penelitian ini bertujuan untuk mengembangkan vaksin DNA pada hewan dan manusia. Metode penelitian menggunakan klon plasmid DNA dengan gen nukleoprotein virus Covid-19 yang ditransformasikan pada bakteri E. coli stellar. Pengujian titer antibodi vaksin pada mencit dilakukan dengan uji Enzyme-linked immunosorbent assay. Hasil penelitian menunukkan klon plasmid DNA dengan gen nukleoprotein virus SARS-Cov-2 dapat dikembangkan dan dibuktikan. Pemberian klon plasmid DNA dengan gen nukleoprotein pada mencit dapat menginduksi terbentuknya antibodi spesifik terhadap nukleoprotein virus SARS-Cov-2. Pemberian plasmid rekombinan pcDNA-Nukleoprotein terbukti menginduksi terbentuknya antibodi terhadap nukleoprotein yang meningkat dari minggu ke-1 sampai minggu ke-4 dan ke-5 yang kemudian menurun pada minggu ke 6 pasca vaksinasi.
Kata kunci: Klon plasmid; nukleoprotein; respon imun; vaksin DNA
Abstract
DNA vaccines have become an interesting area of research in the fight against infectious diseases in animals and humans. DNA vaccines are vaccine formulations that use DNA fragments as antigens. The DNA in vaccines contains genetic information extracted from the disease agent, such as a virus or bacteria, that it is trying to target. This research aims to develop DNA vaccines in animals and humans. We developed plasmid DNA clones with the Covid-19 virus nucleoprotein gene that was transformed into E. coli stellar bacteria. The vaccine was injected in mice. The antibody was tested using an Enzyme-linked immunosorbent assay with purified recombinant NP protein. The results of the study showed that a clone of plasmid DNA with the nucleoprotein gene of the SARS-Cov-2 virus could be developed and proven. Administration of plasmid DNA clones with nucleoprotein genes in mice could induce the formation of specific antibodies against the nucleoprotein of the SARS-Cov-2 virus. The antibodies were increased from week 1 to weeks 4 and 5 then decreased in week 6 post-vaccination.
Keywords: DNA vaccine; immune response; nucleoprotein; plasmid clone
PENDAHULUAN
Coronavirus disease 2019 (Covid-19) merupakan penyakit menular yang disebabkan oleh severe acute respiratory syndrome virus corona 2 (Thanh et al., 2020). Kasus Covid-19 pertama kali di laporkan di kota Wuhan, China pada pertengahan Desember 2019 dan kemudian menyebar ke seluruh dunia (Liu et al., 2020). Pada 30 Januari 2020, WHO secara resmi menyatakan pandemi Covid-19 sebagai masalah kesehatan utama dan menjadi perhatian Internasional (Guo et al., 2020). Di Indonesia kasus positif Covid-19 pertama kali di deteksi pada tanggal 2 Maret 2020 (Burhan et al., 2020; Putra et al., 2021) Dampak pandemi Covid-19 sudah luar biasa di berbagai multisektor, selain ancaman kesehatan, pandemi ini mematikan ekonomi negara dan masyarakat. Sekarang diketahui bahwa SARS-CoV-2 tidak hanya dapat menginfeksi manusia tetapi juga hewan peliharaan, hewan domestik dan hewan liar lainnya. Kelelawar diduga sebagai inang reservoir awal SARS-CoV-2, dan trenggiling sebagai induk semang perantara (Kiros et al., 2020).
Virus SARS-COV 2 termasuk dalam kelompok β-CoVs keluarga Coronaviridae, yang merupakan virus RNA beruntai tunggal positif dan beramplop (Zhou et al., 2020). Genom SARS-CoV-2 berukuran lebih dari 29 kb, yang mengkode protein struktural yakni protein nukleokapsid (N) terfosforilasi, spike glikoprotein (S), hemagglutinin-esterase (HE), protein membran (M) dan envelope protein (E) protein, serta protein non-struktural ORF1a, ORF1b, ORF3a, ORF3b, ORF6, ORF7a, ORF7b, ORF8, ORF9a, ORF9b, dan ORF10 (Thanh Le et al., 2020; Zhou et al., 2020). ORF1a dan 1b juga ditranslasikan mengikuti -1 ribosomal frameshifting untuk menghasilkan protein ORF1ab (Skariyachan et al., 2019). Protein yang ditranslasi dari ORF1a, 1b, dan 1ab membentuk kompleks polimerase virus (Gu and Korteweg, 2007) sedangkan protein
dari ORF lain juga dikenal sebagai protein aksesori (Liu et al., 2014)
Berbagai strategi telah dilakukan sebagai upaya memutus mata rantai penyebaran Covid-19 salah satunya adalah melalui vaksinasi. Vaksinasi merupakan pemberian vaksin yang dapat merangsang terbentuknya antibodi di dalam tubuh. Vaksin dapat didefinisikan sebagai bahan yang mengandung antigen yang bila diberikan kepada orang atau hewan akan memicu pembentukan antibodi spesifik terhadap penyakit tertentu. Vaksin yang berkhasiat, efektif dan aman sangat diperlukan segera dan juga untuk jangka panjang. Pengembangan vaksin Covid-19 saat ini secara garis besar memiliki 4 tipe, yaitu vaksin whole virus (live
attenuated atau inactivated), protein subunit, nucleic (DNA atau
mRNA), dan viral vector (adenovirus) (Sharma et al., 2020)
Vaksin DNA adalah teknik baru dalam pembuantan vaksin (Liu dan Wahren, 2004). Komponen vaksin DNA meliputi unit propagasi plasmid sehingga plasmid dapat diperbanyak dalam sel bakteri, sesuai dengan jumlah dan volume yang diinginkan pada saat diproduksi. Komponen kedua adalah fragmen DNA yang mengandung gen vaksin yang telah dikloning ke dalam plasmid DNA, di mana gen itu diekspresikan di di dalam sel host (Liu dan Wahren, 2004
Lanskap vaksin pandemi Covid-19 menunjukkan bahwa sebagian besar vaksin yang sedang menjalani fase uji klinis menargetkan protein Spike (Thanh et al., 2020) yang dapat tidak optimal untuk diterapkan dalam populasi. Respon imun orang terhadap protein ini pada coronavirus SARS dan MERS tidak bisa dijadikan acuan bahwa respon imun terhadap coronavirus akan memberikan proteksi yang baik. Seroprevalensi terhadap virus itu rendah sekali. Dalam pathogenesis coronavirus MERS, pelepasan protein spike setelah infeksi menyebabkan antibodi terhadap protein itu dapat tidak efisien dalam menghasilkan proteksi. Disamping
itu, pelajaran dari SARS dan MERS (Gu and Korteweg, 2007; Skariyachan et al., 2019) telah diungkap bahwa beberapa protein virus berkontribusi dalam bentuk parah infeksi coronavirus. Protein tersebut adalah matriks, papain-like protease, dan ORF4. Vaksin juga harus menargetkan protein tersebut untuk mengurangi keparahan infeksi. Karena ORF4 tidak ada pada virus Covid19, peran ORF4 dalam MERS kemungkinan dimainkan oleh protein ORF3a dalam virus Covid-19.
Disamping protein diatas, Zhu (Zhu, 2004) mengembangkan DNA vaksin yang berisi gen nukleoprotein virus SARS. Peneliti lain mengembangkan vaksin berbasis sintetik peptida dari gen nucleoprotein (Harris et al., 2021).
Komponen nukleoprotein dipastikan
terdapat pada vaksin Covid-19 inaktif (Omma et al., 2022; Wang et al., 2023; Yuan et al., 2023).
Penelitian ini mengeksplorasi DNA vaksin dengan gen nukleoprotein virus Covid-19. Penelitian ini mencakup ekplorasi pengembangan DNA plasmid klon dan membuktikan respon imun pada mencit. Percobaan akan meliputi injeksi secara intramuscular.
METODE PENELITIAN
Transformasi bakteri E. coli Stellar dengan plasmid Nukleoprotein
Metode penelitian telah mendapat persetujuan dari Komisi Etik Hewan Fakultas Kedokteran Hewan, Universitas Udayana dengan nomor sertifikat: B/240/UN14.2.9/PT.01.04/2021. Plasmid pCDNA3.1+ yang telah disisip dengan DNA sintetik virus SARS-CoV-2 strain Wuhan-Hu-1 (Genbank accession number NC_045512) diperoleh secara komersial pada GenScript (www.genscript.com). Untuk transformasi, bakteri E. coli Stellar sebanyak 50 µL dicampurkan dengan 5 µL plasmid nukleoprotein, mendapatkan 50 µL bakteri pada microtube yang terpisah. Campuran dihomogenkan, dan didinginkan pada suhu 4°C selama 20 menit. Bakteri kemudian dipanaskan pada heatblock
dengan suhu 42 °C selama 2 menit. Semua campuran bakteri dimasukkan ke dalam media Terrific Broth (TB) 1 ml dan bakteri diinkubasi selama 1 jam. 200 µL bakteri diinokulasikan dan disebarkan ke cawan petri yang mengandung media Ampicilin Agar (AMP Agar). Cawan petri diinkubasi selama 1 hari pada suhu 37 °C. Koloni yang muncul diinokulasikan ke media TB selama 24 jam.
Konfirmasi Plasmid (pcDNA-
Nukleoprotein) dengan Pengujian PCR
Untuk konfirmasi klon, sebanyak 200 µL dari koloni bakteri transforman berumur 24 jam diambil dan disentrifugasi pada kecepatan tinggi (10000 rpm). Supernatan dibuang dan bakteri (pellet) diisolasi sesuai dengan protokol dari kit isolasi DNA (Thermoscientific). Hasil isolasi DNA di-amplifikasi dengan PCR. Campuran/mix PCR terdiri dari 5 µL mastermix gotaq green, 0,5 µL primer ADF, 0,5 µL ADR, 1 µL DNA plasmid, dan 3 µL akuabidest. Campuran dimasukkan ke dalam thermalcycler dengan pengaturan 95°C selama 7 menit, diikuti dengan 35 siklus pada suhu 94°C selama 45 detik, 52°C selama 1 menit, 72°C selama 2 menit, dan diselesaikan pada suhu 72°C selama 5 menit. Hasil amplicon di-elektroforesis pada gel agarose 1% yang ditambahkan 4 µL ethidium bromide, selama 30 menit pada voltase 100 V. Gel diamati dibawah sinar UV. Untuk PCR, primer yang digunakan primer ADF dengan sequen GTAACTATAACGGTCATGGATACAA TGAAGAGAGGGCTCT dan primer ADR dengan sequen
ATTACCTCTTTCTCCTTAACCCATTT GCTGTCCACCAGTC.
Isolasi plasmid pcDNA-Nukleoprotein
Bakteri yang hasil PCR-nya positif pada tahap sebelumnya ditumbuhkan pada media Terrific Broth (TB) 150 mL yang sudah ditambahkan dengan antibiotik ampicilin. Media diinkubasi selama 24 jam. Masing-masing bakteri dikulturkan pada media yang berbeda. Media disentrifugasi dengan sentrifuge dingin pada suhu 4°C dan
kecepatan 6000 rpm. Supernatan dibuang dan bakteri (pellet) diproses lebih lanjut untuk isolasi plasmid dengan menggunakan kit Plasmid isolation kit midiprep (Zymo research ©). Prosedur yang diikuti adalah prosedur high copy number DNA. Hasil plasmid murninya disimpan pada akuabidest 500 µL. Plasmid dikuantifikasikan dengan menggunakan Qubit fluorometer untuk menentukan dosis vaksinnya.
Preparasi vaksin gen Nukleoprotein dan vaksinasi pada mencit
Vaksin dipreparasikan dengan plasmid sebesar 10 µg dalam 200 µL. Formulasi dari vaksin terdiri dari 2 campuran, yakni: campuran 1 terdiri dari 500 µL media Gibco Opti-mem (Thermo-Fisher®) dicampurkan dengan lipofectamine sebanyak 150 µL; Campuran 2 terdiri dari 500 µL media Gibco Opti-mem dicampurkan dengan reagen p3000 sebanyak 200 µL dan 112,3 µg DNA plasmid Nukleoprotein untuk vaksin. Campuran 1 dan campuran 2 digabungkan ditambahkan 1,5 mL cholesterol dan 3 µL larutan polisorbat sebagai emulsifier. Dua belas mencit (Mus musculus). Dibagi menjadi dua kelompok, yaitu P0 (kelompok mencit sebagai kontrol), P1 (kelompok mencit yang menerima vaksin DNA gen Nukleoprotein secara injeksi). Serum dari lima ekor mencit kelompok P0 dan P1 disampling pada minggu ke 0 sebelum vaksinasi, 1,2,3 4,5 dan 6 pasca vaksinasi.
Uji titer antibodi mencit dengan menggunakan ELISA
Untuk ELISA, plate ELISA 96 well ditambahkan dengan larutan ELISA coating buffer dengan protein GST-NP murni yang diproduksi di Laboratorium Biomedik FKH Udayana masing-masing sebanyak 0,5 ug per well dengan tambahan BSA (bovine serum albumin, Sigma ©) 1µg/µL dan diinkubasi selama 24 jam. Sumuran yang ditambahkan buffer sesuai dengan jumlah serum yang diuji. Plate kemudian dicuci dengan larutan PBS-Tween sebanyak 3x. Plate ditambahkan
dengan susu skim 5% untuk proses blocking. Plate diinkubasi selama 1 jam. Susu skim dibuang dan plate dicuci dengan PBS-Tween sebanyak 3x. Sumuran ditambahkan dengan serum mencit yang sudah diencerkan. Plate diinkubasi selama 1 jam. Serum dibuang dan plate dicuci dengan larutan PBS-Tween sebanyak 3x. Sumuran ditambahkan dengan antibodi goat anti-mouse IgG AP 1:500 dengan PBS. Plate diinkubasi selama 1 jam. Antibodi dibuang dan plate dicuci dengan larutan PBS-Tween sebanyak 3x. Plate ditambahkan dengan larutan Alkaline Phospatase. Perubahan warna pada plate diamati. Plate diinkubasi selama 20 menit atau hingga kontrol negatif mulai menunjukan perubahan warna. Plate kemudian dibaca menggunakan ELISA reader pada panjang gelombang 492 nm. Data hasil absorbansi dicatat dalam bentuk Optical Density (OD) dianalisis lebih lanjut.
HASIL DAN PEMBAHASAN
Hasil
Tumbuhnya koloni bakteri pada media amp agar menandakan keberhasilan transformasi plasmid rekombinan (pcDNA-Nukleoprotein) pada sel inang e.coli stellar. Plasmid pcDNA memiliki gen ampR yang memiliki resistensi terhadap ampisilin, sehingga hanya koloni yang mengandung plasmid yang mampu tumbuh pada media amp agar. Hasil transformasi plasmid rekombinan (pcDNA-Nukleoprotein) pada E. coli stellar ditampilkan pada Gambar 1. hasil tersebut menunjukkan umlah koloni yang tumbuh sekitar 20-30 koloni.
Koloni yang tumbuh pada hasil transformasi, kemudian dianalisis dengan metode PCR untuk mengkorfirmasi keberhasilan transformasi. Koloni yang tumbuh diambil sebanyak empat koloni terpisah dan ditumbuhkan pada media cair dengan Ampicilin selama 24 jam. Selanjutnya diisolasi DNA untuk uji PCR menggunakan pasangan primer ADF dan ADR. Visualisai hasil amplikasi koloni yang mengandung plasmid rekombinan
(pcDNA-Nukleoprotein) pada gel agarose 1% ditampilkan pada Gambar 2. Hasil tersebut menunjukkan semua koloni yang diuji telah membawa plasmid dengan gen NP dengan panjang DNA sekitar 1200 bp.
Keterangan: Jalur 1: kontrol negatif; jalur 2,3,4, dan 5: koloni hasil transformasi NP; jalur 6: kontrol positif NP; jalur 7: DNA marker dari Invitrogen dengan panjang 100-2000 bp.
Koloni pada jalur 2,3,4, dan 5 tampak mempunyai produk sebesar sekitar 1200 bp. Koloni terpilih diperbanyak dalam kultur 150 ml media cair dengan ampisilin. Plasmid diisolasi dengan Plasmid Isolation Kit midiprep (Zymo) dan dikuantifikasi dengan QBIT. Hasil yang diperoleh adalah 2,9 ng/µL dalam 400 µL, sehingga total adalah 11.600 µG atau 11.6 mg.
Hasil deteksi antibodi terhadap nukleoprotein berdasarkan uji elisa dari sampel mencit dapat dilihat pada tabel titer antibodi di Tabel 1. Hasil merupakan nilai optical density (OD) mencit yang diberikan vaksin DNA menggunakan gen nukleoprotein dan mencit kontrol. Hasil dari 6 ekor mencit tiap kelompok dirata-ratakan sesuai dengan minggu pengambilan dari perlakuan dan kontrol. Hasil tersebut menunjukkan bahwa nilai OD elisa NP pada serum mencit yang yang diberi vaksin DNA adalah rata-rata 0.081 pada minggu ke-0 sebelum vaksinasi, 0.295 pada minggu ke-1, 0.284 pada minggu ke-2, 0.391 pada minggu ke-3, 0.493 pada minggu ke-4, 0.489 pada minggu ke-5, dan 0.361 pada minggu ke-6 pasca vaksinasi. Sedangkan rata-rata OD serum mencit kontrol adalah konstan antara 0.074-0.091 pada minggu ke-0 sebelum vaksinasi dan minggu ke-1, 2, 3, 4, 5, dan 6 pasca. Tampilan grafis hasil OD rata-rata mencit perlakuan pada minggu ke-0 sampai ke-6 ditampilkan pada Gambar 5.3. Hasil tersebut menunjukkan nilai OD tertinggi pada minggu ke-4 dan ke-5. Hasil titer antibodi dari perlakuan di minggu ke satu sampai minggu keenam memiliki nilai OD yang lebih tinggi dibanding kontrol pada minggu yang sama.
Pembahasan
Dalam naskah ini dipaparkan bahwa teknik produksi vaksin DNA menggunakan gen nukleoprotein dapat dengan mudah diproduksi melalui dna sintetik yang disisipkan pada vektor plasmid pcDNA3.1, yang dapat ditransformasi ke dalam e.coli dengan metode sederhana, serta dapat diproduksi dalam jumlah besar, dan respon imun terhadap gen sisipan itu dapat dibuktikan. Prosedur serupa dapat dilakukan dengan gen target yang lain untuk penyakit hewan dan manusia.
Pada penelitian ini plasmid rekombinan pcDNA-Nukleoprotein berhasil ditransformasikan pada bakteri e.coli stellar yang ditunjukkan pada koloni yang tumbuh di media amp agar dan hasil uji PCR. Transformasi menghasilkan jumlah koloni relatif sedikit yakni sekitar 20-30 koloni. Efisiensi transformasi menurut produsen seharusnya >5 × 108 cfu/µg.
Efisiensi transformasi bakteri bergantung pada beberapa faktor, termasuk spesies bakteri, kondisi pertumbuhan, dan metode transformasi yang digunakan. Terdapat beberapa faktor yang dapat mempengaruhi efisiensi transformasi bakteri yakni kompetensi sel yang merupakan kemampuan alami bakteri untuk mengambil DNA asing dari lingkungan. Beberapa bakteri seperti Escherichia coli (e.coli) secara alami tidak kompeten dan memerlukan perlakuan khusus untuk membuatnya mampu mengambil DNA asing. Kondisi pertumbuhan bakteri saat melakukan transformasi (suhu, pH, dan kepadatan sel) (Inoue et al., 1990).
Ukuran dan jenis DNA asing yang akan ditransformasikan juga dapat mempengaruhi efisiensi transformasi. Beberapa bakteri mungkin lebih mudah menerima DNA kecil daripada DNA yang lebih besar. Penggunaan bahan kimia atau perlakuan khusus tertentu dapat meningkatkan efisiensi transformasi (Liu et al., 2018). Meskipun jumlah koloni relatif sedikit, tetapi hasil menunjukkan semua koloni positif gen target. Dari 4 koloni yang
diperiksa, semuanya positif membawa gen NP.
DNA rekombinan pcDNA-Nukleoprotein covid-19 dapat diproduksi dalam jumlah yang besar. Dari 150 ml kultur bakteri, jumlah plasmid yang dihasilkan adalah 11.6 mg. Produksi DNA plasmid pada bakteri dapat bervariasi tergantung pada beberapa faktor, antara lain ukuran dan jumlah salinan plasmid, strain bakteri yang digunakan, kondisi pertumbuhan, dan metode ekstraksi plasmid, keberadaan gen toksik, dan penggunaan promotor.
Secara umum plasmid high copy number dapat menghasilkan jumlah DNA plasmid yang lebih tinggi dibandingkan dengan plasmid low copy number. Plasmid high copy number dapat menghasilkan mulai dari 10 hingga 500 per sel bakteri, sedangkan plasmid low copy number menghasilkan 1 hingga 10 per sel bakteri. Hasil penelitian Birnboim dan Doly (1979) melaporkan dari 1 liter biakan bakteri strain laboratorium standar seperti e.coli DH5α menghasilkan 10 sampai 20 mg.
Proses elisa dilakukan pada plate polystyrene yaitu suatu plate yang memiliki 96 sumuran/well yang diberi coating dengan protein GST-NP murni yang diproduksi di Laboratorium Biomedik FKH Udayana. Bukti dari vaksin DNA dengan plasmid rekombinan pcDNA-Nukleoprotein dapat menginduksi terbentuknya antibodi terhadap nucleoprotein dapat dilihat pada nilai OD elisa yang meningkat sejak minggu ke-1 sampai minggu ke-4 dan ke-5 yang kemudian menurun pada minggu ke 6. Sedangkan OD mencit kontrol selalu dibawah 0.1 selama pengamatan.
Kelompok peneliti (Jeewandara et al., 2022) melaporkan penerima vaksin Sinopharm/BBIBP-CorV pada minggu ke-2, minggu ke-4, dan minggu ke-12 dilakukan uji antibodi SARS-CoV-2 setelah dosis pertama. Respon antibodi menurun secara tidak signifikan antara minggu ke-6 dan minggu ke-16. Peningkatan antibodi yang signifikan
setelah vaksinasi merupakan indikator penting bahwa sistem kekebalan tubuh merespons dengan baik dan dapat memberikan perlindungan imun terhadap patogen. Selain respon antibodi, vaksinasi juga merangsang respons seluler yang melibatkan sel-sel T. Sel T membantu mengaktifkan sel B untuk memproduksi lebih banyak antibodi.
Respon imun pada penelitian ini belum maksimal. Nilai OD tertinggi pada satu hewan coba dengan OD lebih dari 1 pada minggu ke-4. Beberapa faktor yang dapat menyebabkan respon imun yang tidak optimal setelah vaksinasi antara lain keadaan imunologi mencit (usia, status imun dan kondisi kesehatan) dan interval dosis yang tidak tepat. Tampaknya riset lanjutan dalam pencampuran vaksin dna perlu diperbaiki.
Booster diberikan untuk meningkatkan atau mempertahankan tingkat kekebalan tubuh terhadap patogen. Waktu pemberian booster harus mempertimbangkan durasi perlindungan yang diberikan oleh dosis sebelumnya dan menargetkan titik di mana respon imun mulai menurun. Interval antara dosis pertama dan dosis booster penting dalam mempengaruhi keefektifan booster. Interval yang terlalu singkat mungkin tidak memberikan cukup waktu bagi sistem kekebalan tubuh untuk merespons dengan baik, sementara interval yang terlalu lama dapat mengakibatkan penurunan kekebalan sebelum booster diberikan.
Penelitian ini menujukkan kapasitas inovasi dalam produksi vaksin DNA sudah tersedia di Indonesia terutama di Universitas Udayana. Prototipe vaksin sudah berhasil dibuktikan. Pengembangan lebih lanjut dapat dilakukan dengan gen yang lain pada virus covid-19, termasuk pengujian pemberian vaksin DNA melalui tetes mulut. Teknologi terbukti mudah dan murah. Prototipe ini dapat dikembangkan menjadi kapasitas dalam negeri untuk memenuhi kebutuhan nasional. Vaksin covid yang digunakan di Indonesia antara lain vaksin Sinovac, vaksin AstraZeneca,
vaksin Pfizer-BioNTech, dan vaksin Moderna (Santi et al., 2022)
Teknologi yang dikembangkan berpeluang digunakan untuk vaksin hewan yang lebih mudah dan murah. Pemberian melalui oral juga dapat dipelaari lebih lanjut. Permasalahan yang belum diawab dalam peneitian ini adalah penemuan teknologi enkapsulasi vaksin DNA tanpa menggunakan bahan impor yang mahal seperti lipofektamin. Penggunaan
kolesterol terutama kolesterol nabati perlu dikaji lebih lanjut.
SIMPULAN DAN SARAN
Simpulan
Kesimpulannya adalah bahwa Klon plasmid DNA dengan gen nukleoprotein virus SARS-Cov-2 dapat dikembangkan dan dibuktikan. Pemberian klon plasmid DNA dengan gen nukleoprotein pada mencit dapat menginduksi terbentuknya antibodi spesifik terhadap nukleoprotein virus SARS-Cov-2.
Saran
Riset lanjutan untuk menghasilakan respon imun yang optimal seperti umur mencit dengan dosis yang lebih tinggi perlu dilakukan. Serta untuk mengetahui pengaruh pemberian vaksin ulangan (booster) perlu dilakukan dan inovasi enkapsulasi DNA yang berbasis lokal seperti kolesterol nabati perlu dieksplorasi.
UCAPAN TERIMAKASIH
Penelitian ini didanani dengan skema World Class Research Ristekdikti dengan peneliti utama Prof. IGNK Mahardika. Penulis berterimakasih kepada semua staf Laboratorium Biomedik dan Biologi Molekuler Hewan Universitas Udayana.
DAFTAR PUSTAKA
Burhan E, Prasenohadi P, Rogayah R, Isbaniyah F, Reisa T, Dharmawan I.
2020. Clinical progression of COVID-19 patient with extended incubation period, delayed RT-PCR time-to-
positivity, and potential role of chest CT-scan. Acta Med. Indon. 52: 80-83.
Gu J, Korteweg C. 2007. Pathology and pathogenesis of severe acute respiratory syndrome. Am. J. Pathol. 170: 11361147.
Guo YR, Cao QD, Hong ZS, Tan YY, Chen SD, Jin HJ, Tan KS, Wang DY, Yan Y. 2020. The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak - an update on the status. Mil. Med. Res. 7: 11.
Harris PE, Brasel T, Massey C, Herst CV, Burkholz S, Lloyd P, Blankenberg T, Bey TM, Carback R, Hodge T, Ciotlos S, Wang L, Comer JE, Rubsamen RM. 2021. A synthetic peptide CTL vaccine targeting nucleocapsid confers protection from SARS-CoV-2
challenge in rhesus macaques. Vaccines. 9(5): 520.
Inoue H, Nojima H, Okayama H. 1990. High efficiency transformation of Escherichia coli with plasmids. Gene. 96: 23-28.
Jeewandara C, Aberathna IS,
Pushpakumara PD, Kamaladasa A, Guruge D, Wijesinghe A, Gunasekera B, Ramu ST, Kuruppu H, Ranasinghe T, Dayarathna S, Dissanayake O, Gamalath N, Ekanayake D, Jayamali J, Jayathilaka D, Dissanayake M, Jayadas TT, Mudunkotuwa A, Somathilake G, Harvie M, Nimasha T, Danasekara S, Wijayamuni R, Schimanski L, Rijal P, Tan TK, Dong T, Townsend A, Ogg GS, Malavige GN. 2022. Persistence of immune responses to the
Sinopharm/BBIBP-CorV vaccine.
Immun. Inflam. Dis. 10: e621.
Kiros M, Andualem H, Kiros T, Hailemichael W, Getu S, Geteneh A, Alemu D, Abegaz WE. 2020. COVID-19 pandemic: current knowledge about the role of pets and other animals in disease transmission. Virol. J. 17: 143.
Liu DX, Fung TS, Chong KK, Shukla A, Hilgenfeld R. 2014. Accessory proteins
of SARS-CoV and other coronaviruses. Antiviral. Res. 109: 97-109.
Liu J, Chang W, Pan L, Liu X, Su L, Zhang W, Li Q, Zheng Y. 2018. An Improved method of preparing high efficiency transformation Escherichia coli with both plasmids and larger DNA fragments. Indian J. Microbiol. 58: 448-456.
Liu YC, Kuo RL, Shih SR. 2020. COVID-19: The first documented coronavirus pandemic in history. Biomed J. 43(4):328-333.
Omma A, Batirel A, Aydin M, Yilmaz Karadag F, Erden A, Kucuksahin O, Armagan B, Guven SC, Karakas O, Gokdemir S, Altunal LN, Buber AA, Gemcioglu E, Zengin O, Inan O, Sahiner ES, Korukluoglu G, Sezer Z, Ozdarendeli A, Kara A, Ates I. 2022. Safety and immunogenicity of inactive vaccines as booster doses for COVID-19 in Turkiye: A randomized trial. Hum. Vac. Immunother. 18: 2122503.
Putra A, Widyatmoko A, Ibrahim S, Amansyah F, Amansyah F, Berlian MA, Retnaningsih R, Pasongka Z, Sari FE, Rachmad B. 2021. Case series of the first three severe COVID-19 patients treated with the secretome of hypoxia-mesenchymal stem cells in Indonesia. F1000 Res. 10: 228.
Santi T, Sungono V, Kamarga L, Samakto B, Hidayat F, Hidayat FK, Satolom M, Permana A, Yusuf I, Suriapranata IM, Jo J. 2022. Heterologous prime-boost with the mRNA-1273 vaccine among CoronaVac-vaccinated healthcare
workers in Indonesia. Clin. Exp. Vac. Res. 11: 209-216.
Sharma O, Sultan AA, Ding H, Triggle CR. 2020. A Review of the Progress and Challenges of Developing a Vaccine for COVID-19. Front. Immunol. 11: 585354.
Skariyachan S, Challapilli SB, Packirisamy S, Kumargowda ST, Sridhar VS. 2019. Recent aspects on the pathogenesis mechanism, animal models and novel therapeutic interventions for middle east respiratory syndrome coronavirus infections. Front. Microbiol. 10: 569.
Thanh LT, Andreadakis Z, Kumar A, Gómez Román R, Tollefsen S, Saville M, Mayhew S. 2020. The COVID-19 vaccine development landscape. Nat. Rev. Drug Discovery. 19: 305-306.
Wang H, Gan M, Wu B, Zeng R, Wang Z, Xu J, Li J, Zhang Y, Cao J, Chen L, Di D, Peng S, Lei J, Zhao Y, Song X, Yuan T, Zhou T, Liu Q, Yi J, Wang X, Cai H, Lei Y, Wen Y, Li W, Chen Q, Wang Y, Long P, Yuan Y, Wang C, Pan A, Wang Q, Gong R, Fan X, Wu T, Liu L. 2023. Humoral and cellular immunity of two-dose inactivated COVID-19
vaccination in Chinese children: A prospective cohort study. J. Med. Virol. 95: e28380.
Yuan Y, Xu J, Ma B, Chen G, Wang Z, Wang S, Jing N, Zhang J, Wang B, Yan W, Zhang Q, Zhao Q, Li Y. 2023. Characteristics of humoral and cellular responses to coronavirus disease 2019 (COVID-19) inactivated vaccine in central China: A prospective,
multicenter, longitudinal study. Front. Immunol. 14: 1107866.
Zhou P, Yang XL, Wang XG, Hu B, Zhang L, Zhang W, Si HR, Zhu Y, Li B, Huang CL, Chen HD, Chen J, Luo Y, Guo H, Jiang RD, Liu MQ, Chen Y, Shen XR, Wang X, Zheng XS, Zhao K, Chen QJ, Deng F, Liu LL, Yan B, Zhan FX, Wang YY, Xiao GF, Shi ZL. 2020. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 579: 270-273.
Zhu M. 2004. SARS Immunity and vaccination. Cell Mol. Immunol. 1: 193198.
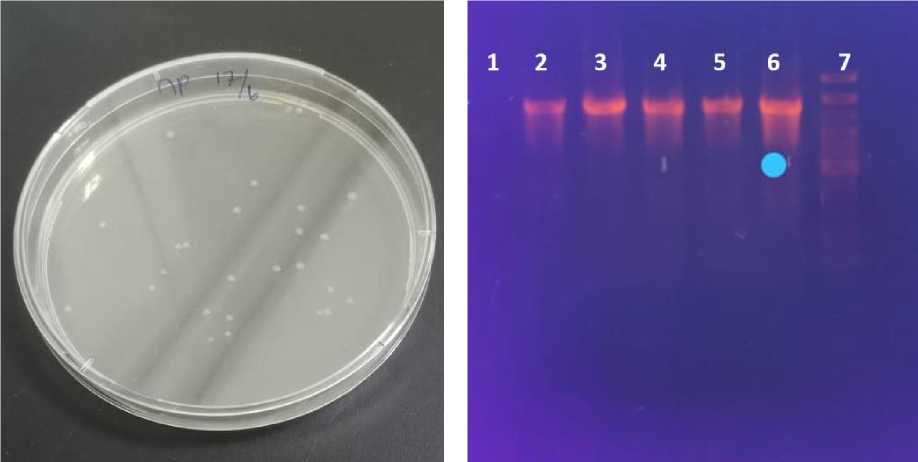
Gambar 1. Hasil transformasi plasmid rekombinan (pcDNA-Nukleoprotein) pada bakteri e.coli stellar
Gambar 2. Hasil analisis PCR koloni transformasi plasmid pada e.coli Stellar menggunakan pasangan primer ADF dan ADR.
Tabel 1. Nilai optical density (OD) serum mencit yang divaksinasi dengan vaksin DNA menggunakan gen Nukleoprotein virus SARS-Cov2 dan serum mencit kontrol yang diambil pada minggu ke-0 sebelum vaksinasi dan minggu ke-1,2,3,4,5 dan 6 pasca vaksinasi.
|
P |
W0 |
W1 |
W2 |
W3 |
W4 |
W5 |
W6 |
|
1 |
0.076 |
0.349 |
0.251 |
0.664 |
0.594 |
0.222 |
0.651 |
|
2 |
0.132 |
0.287 |
0.347 |
0.272 |
0.254 |
0.507 |
0.449 |
|
3 |
0.005 |
0.25 |
0.328 |
0.361 |
1.161 |
0.57 |
0.283 |
|
4 |
0.091 |
0.305 |
0.354 |
0.424 |
0.33 |
0.466 |
0.298 |
|
5 |
0.171 |
0.25 |
0.238 |
0.331 |
0.301 |
0.698 |
0.125 |
|
6 |
0.009 |
0.327 |
0.187 |
0.296 |
0.319 |
0.472 |
0.361 |
|
Rata-rata |
0.081 |
0.295 |
0.284 |
0.391 |
0.493 |
0.489 |
0.361 |
|
Kontrol |
WO |
W1 |
W2 |
W3 |
W4 |
W5 |
W6 |
|
1 |
0.081 |
0.076 |
0.067 |
0.054 |
0.069 |
0.134 |
0.074 |
|
2 |
0.112 |
0.098 |
0.103 |
0.096 |
0.105 |
0.082 |
0.096 |
|
3 |
0.065 |
0.074 |
0.021 |
0.032 |
0.032 |
0.057 |
0.063 |
|
4 |
0.073 |
0.086 |
0.034 |
0.096 |
0.078 |
0.089 |
0.106 |
|
5 |
0.121 |
0.103 |
0.201 |
0.112 |
0.089 |
0.078 |
0.094 |
|
6 |
0.093 |
0.004 |
0.078 |
0.006 |
0.108 |
0.059 |
0.078 |
|
Rata-rata |
0.091 |
0.074 |
0.084 |
0.066 |
0.080 |
0.083 |
0.085 |
|
Keterangan: P |
adalah |
mencit |
yang diinjeksi |
dengan |
vaksin |
DNA menggunakan gen | |
nucleoprotein; Kontrol adalah mencit yang tanpa diinjeksi dengan vaksin DNA
Nilai OD Mencit Perlakuan dan Mencit Kontrol
0.6
0.5
0.4
0.3
0.2
0.1
0
0
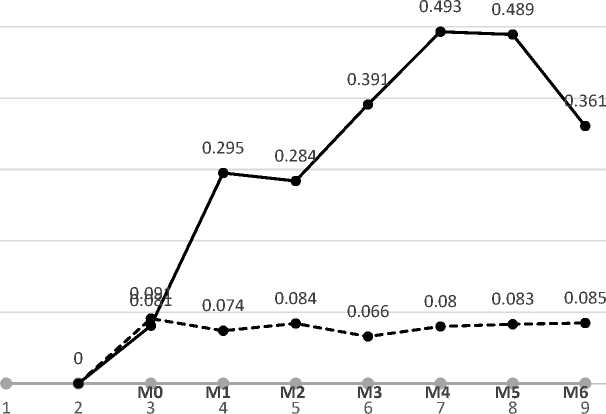
Gambar 3. Grafik nilai optical density (OD) mencit yang diberikan vaksin DNA dan mencit kontrol
1011
Discussion and feedback