Analisis Dinamika Model Penyakit Toksoplasmosis pada Populasi Kucing dan Manusia
on
Jurnal Matematika Vol. 11, No.2, Desember 2021, pp. 75-86
Article DOI: 10.24843/JMAT.2021.v11.i02.p138
ISSN: 1693-1394
Analisis Dinamika Model Penyakit Toksoplasmosis pada Populasi Kucing dan Manusia
Riza Rusdiani
Kampus IPB, Jl. Raya Dramaga, Babakan, Kec. Dramaga, Kota Bogor, Jawa Barat 16680 e-mail: rusdianiriza@gmail.com
Ali Kusnanto
Kampus IPB, Jl. Raya Dramaga, Babakan, Kec. Dramaga, Kota Bogor, Jawa Barat 16680 e-mail: ali_mat@apps.ipb.ac.id
Paian Sianturi
Kampus IPB, Jl. Raya Dramaga, Babakan, Kec. Dramaga, Kota Bogor, Jawa Barat 16680 e-mail: psianturi@apps.ipb.ac.id
Abstract: Toxoplasmosis is a disease that is identical to cats. This disease is caused by the parasite Toxoplasma gondii. In this study, a mathematical model of the spread of toxoplasmosis was reviewed with various population size. In this study, model construction, fixed point analysis and parameter sensitivity analysis were carried out. From the sensitivity analysis, it is shown that the cat transmission rate from a susceptible cat population to an infected cat population (horizontal transmission rate) and the probability of a susceptible cat born from an infected cat (vertical transmission rate) are found as sensitive parameters on production number (ℛ0). Decreasing the horizontal transmission rate and an increase value of the vertical transmission rate can reduce the value of ℛ0. A decrease in the value of ℛ0, results in a disease-free state will be achieved more quickly so that the disease is under control.
Keywords: cat, Toxoplasmosis, horizontal transmissions, vertical transmissions
Abstrak: Toksoplasmosis merupakan penyakit yang identik dengan kucing. Penyakit ini disebabkan oleh parasit Toxoplasma gondii. Pada penelitian ini, ditinjau model matematika penyebaran penyakit toksoplasmosis dengan menggunakan ukuran populasi yang bervariasi. Dalam penelitian ini dilakukan konstruksi model, analisis titik tetap dan analisis sensitivitas parameter. Dari analisis sensitivitas ditunjukkan bahwa laju transmisi kucing dari populasi kucing rentan ke populasi kucing terinfeksi (laju transmisi horizontal) dan peluang kucing rentan lahir dari kucing yang terinfeksi (laju transmisi vertikal) adalah parameter yang sensitif terhadap bilangan reproduksi dasar (ℛ0). Penurunan laju transmisi horizontal dan peningkatan laju transmisi vertikal akan menurunkan nilai ℛ0. Penurunan nilai ℛ0, berakibat keadaan bebas penyakit akan tercapai lebih cepat sehingga penyakit terkendali.
Kata Kunci: kucing, Toksoplasmosis, transmisi horizontal, transmisi vertikal
Toksoplasmosis merupakan penyakit yang dapat diderita manusia dan semua hewan berdarah panas seperti domba, kucing, dan kuda (Hill, Chirukandoth, & Dubey, 2005). Penyakit ini disebabkan oleh Toxoplasma gondii (T.gondii). T.gondii merupakan organisme bersel satu yang hidup sebagai parasit. Penyakit ini menyebar dari hewan ke manusia melalui makanan atau minuman yang telah terkontaminasi oleh ookista (Pereira, Franco, & Leal, 2010).
Prevalensi toksoplasmosis di Indonesia berkisar antara 2%-88% yang tersebar di seluruh kepulauan yang ada di Indonesia (Aditama, Nurjazuli, & Dina, 2016). Berdasarkan hal tersebut, dibentuklah suatu model matematika untuk memodelkan strategi pencegahan dan pengendalian terhadap penyakit ini dengan bantuan simulasi numerik.
Pada penelitian ini dikembangkan model penyakit toksoplasmosis pada populasi kucing dan manusia yang sebelumnya telah dikembangkan oleh Pei et al.(2018). Perbedaan penelitian ini dengan penelitian sebelumnya yaitu pada pemisahan model menjadi dua model. Model I menggunakan asumsi kelahiran pada populasi kucing dapat terjadi pada populasi rentan dan terinfeksi dan anaknya akan sesuai dengan induknya, sedangkan model II menggunakan asumsi kelahiran pada populasi kucing hanya dapat terjadi pada populasi rentan dan peluang bayi yang lahir dalam kondisi sehat dari ibu yang terinfeksi, serta peluang kucing lahir dalam keadaan rentan tidak diketahui. Penelitian ini bertujuan untuk mengamati pengaruh perubahan nilai parameter terhadap dinamika model.
Metode yang digunakan dalam penelitian ini adalah dengan melakukan rekonstruksi model yang telah dikembangkan oleh Pei et al.(2018) dan mengembangkannya dengan membuat dua jenis model. Langkah berikutnya adalah menentukan bilangan reproduksi dasar (K0), melakukan analisis sensitivitas terhadap parameter-parameter model, serta mengamati pengaruh parameter pada dinamika populasi kucing dan manusia dengan simulasi numerik.
Bilangan reproduksi dasar (K0) merupakan nilai harapan terjadinya infeksi per satuan waktu pada suatu populasi yang mengakibatkan seluruhnya bersifat rentan yang dihasilkan oleh satu jenis individu yang sudah terinfeksi. K0 dalam penelitian ini ditentukan dengan menggunakan metode yang dikenalkan oleh Driessche & Watmough (2008) yaitu mengkonstruksi suatu matriks yang berasal dari subpopulasi-subpopulasi yang menyebabkan infeksi saja. Matriks tersebut dikenal dengan “the next generation matrix”. Nilai K0 merupakan nilai eigen tak negatif terbesar dari matriks tersebut.
Kondisi yang mungkin dari bilangan reproduksi dasar menurut Driessche & Watmough (2008) adalah
-
1. Jika K0 < 1 maka jumlah individu yang terinfeksi akan menurun pada generasi, sehingga penyakit tidak akan menyebar.
-
2. Jika K0 > 1 maka jumlah individu yang terinfeksi akan meningkat pada generasi, sehingga penyakit akan menyebar.
Analisis sensitivitas merupakan analisis yang digunakan untuk memeriksa perubahan
K0 yang terjadi akibat adanya pengaruh perubahan nilai parameter pada model dan digunakan untuk menunjukkan parameter yang paling berpengaruh dalam menentukan hasil analisis model. Dalam analisis sensitivitas, indeks sensitivitas bilangan reproduksi
dasar K0 yang bergantung pada parameter p didefinisikan pada persamaan (1) berikut
Ko _ dK0 p
(1)
Kp dp ×K0
Indeks sensitivitas y^o digunakan untuk menunjukkan perubahan relatif pada bilangan
reproduksi K0 ketika parameter p diubah (Natkul, James, & Jim, 2008). Indeks sensitivitas bertujuan untuk melihat parameter-parameter terhadap perubahan nilai K0 • Indeks sensitivitas yang bernilai positif menunjukkan bahwa apabila parameter p ditingkatkan dan parameter yang lainnya dibuat tetap, maka akan meningkatkan nilai K0 dan setiap penurunan nilai parameter p menyebabkan nilai K0 menurun.
Populasi manusia terbagi menjadi tiga kelas yaitu Sh populasi manusia rentan (Susceptible), Ih populasi terinfeksi (Infected), dan R populasi yang pulih atau sembuh dari toksoplasmosis (Recovered). Sedangkan populasi kucing terbagi menjadi dua kelas yaitu Sc populasi kucing yang berisiko tertular penyakit (Susceptible) dan Ic populasi kucing yang terinfeksi parasit (Infected). Total populasi manusia dilambangkan dengan Nh dan total populasi kucing dilambangkan dengan Nc. Secara skematis, penyebaran penyakit toksoplasmosis dapat digambarkan dalam diagram kompartemen pada Gambar 1 berikut.

Gambar 1. Diagram kompartemen penyebaran penyakit toksoplasmosis
Berdasarkan diagram kompartemen pada Gambar 1 diperoleh sistem persamaan (2) sebagai berikut:
dSh(f) dt dIh(t) dt dR
-^ = γlh(t) - kR(t), Nh(f) = Sh(f) + Ih(f) + R(t),
dSc(f) dt dIc(t) dt
Ic(t)
= μcpcIc(t) - βcSc(t) N~φ,
Ic(t) =^tv
μcPcic(t),
Nc(t) = Sc(t) + Ic(t),
di mana konstanta μh, μc, ph, pc, k, γ, βh, βc > 0. Selanjutnya didefinisikan,
Si(t> m-!*®. ^ R(t
' Nh(t) y(t) Wft(t)' Z(t) Λ⅛(t)'
m SAD Ic(t)
u(t)=wi- v(t) = w-y
dan diketahui bahwa,
x(t) + y(t) + z(t) = 1 dan u(t) + v(t) = 1.
Selanjutnya, sistem persamaan (2) dapat disederhanakan menjadi :
{
x(t) = Vh- Vh(ι - Ph)y(t) - χ(t)(μh + βh(1 - u(t)), y(t) = βh×(t)(1 - u(t)) + y(t)(μh(1 - Ph) -(Y + Vh)) u(t) = μcPc(1 - u(f)) - βcu(t)(1 - u(t)),
(3)
dengan μh, μc,Ph,Pc,k,γ, βh, βc > 0. Deskripsi parameter pada (3) akan disajikan pada Tabel 1.
|
Tabel 1. Deskripsi parameter dari model | |
|
Parameter |
Deskripsi |
|
βh βc Y |
Laju transmisi individu dari populasi manusia rentan ke populasi manusia terinfeksi. Laju transmisi kucing dari populasi kucing rentan ke populasi kucing terinfeksi. Laju transmisi individu dari populasi manusia terinfeksi ke populasi manusia yang telah pulih atau sembuh. |
|
μh μc Ph |
Tingkat kelahiran manusia. Tingkat kelahiran kucing. Diasumsikan sama dengan tingkat kematian alaminya. Peluang bayi yang baru lahir dari seorang ibu yang terinfeksi toksoplasmosis dalam keadaan sehat. |
|
Pc k χ(t) y(t) z(t} u(t) V (t) |
Peluang kucing rentan lahir dari kucing yang terinfeksi toksoplasmosis. Tingkat kematian alami manusia. Proporsi populasi manusia yang rentan pada waktu t. Proporsi populasi manusia yang terinfeksi pada waktu t. Proporsi populasi manusia yang telah pulih atau sembuh pada waktu t. Proporsi populasi kucing yang rentan pada waktu t. Proporsi populasi kucing yang terinfeksi pada waktu t. |
Penentuan Titik Tetap
Berdasarkan (3) diperoleh dua jenis titik tetap, yaitu titik tetap bebas penyakit dan titik tetap endemik. Titik tetap bebas penyakit E1(x,y,u) = (1,0,1) dan titik tetap endemik adalah E2(x.y,u) = (x2.y2.u2). dengan ui=^. χi=-^-+μ^^ 2 _________β-μ-(1-u'2)_________
y2 βħ(1-U*2)(γ+μħ)+μħ(γ+Pħμhy
Bilangan Reproduksi Dasar
Bilangan reproduksi dasar (K0) merupakan nilai eigen maksimum tak negatif dari the next generation matrix, dan didapat
Ko = ■
μcUc
Teorema 1. Jika K0 < 1 maka titik tetap bebas penyakit E1 bersifat stabil asimtotik lokal.
Jika K0 > 1 maka tidak stabil.
Bukti. Untuk membuktikan Teorema 1, dilakukan linearisasi sistem persamaan (3) di titik
E1 yang akan menghasilkan matriks Jacobi sebagai berikut:
J-Ph -Ph(1 - Ph)
βh
-βh -PcPc + βc
)
Je1 = ∖ 0 -(y + PhPh)
00
Nilai eigen untuk titik tetap bebas penyakit E1 diperoleh dengan menyelesaikan persamaan karakteristik berikut :
∣Jei-ai∣ = 0.
atau
I-Ph-A -Ph(1-ph) βh I
0 -(γ + phPh) - A -βh = 0.
I 0 0 -PcPc+βc-A
Diperoleh tiga nilai eigen dengan dua nilai eigen bernilai negatif yaitu A1 = —Ph, A2 = —Y — PhPh dan nilai eigen lainnya yaitu A3 = -Pcpc + βc. Jika K0 < 1 maka A3 < 0.
Selanjutnya, jika K0 > 1 maka terdapat nilai eigen yang bernilai positif yaitu A3.
Teorema 2. Titik tetap endemik positif E2 bersifat stabil asimtotik lokal jika K0 > 1.
Bukti. Untuk membuktikan Teorema 2, dilakukan linearisasi sistem persamaan (3) di titik
E2 yang akan menghasilkan matriks Jacobi sebagai berikut:
|
/-ph-βh(1-u2) -Ph(1-Ph) βhx2 \ | |
|
jE2 = |
I βh(1 - u2) -(y + PhPh) -βhx2 . \ 0 0 -PcPc-βc + 2βc⅛/ |
Nilai eigen untuk titik tetap endemik E2 diperoleh dengan menyelesaikan persamaan
karakteristik berikut :
∣Je2 -a1∣=0.
atau
I(-P-h - βh(1 - u2)) - a -Ph(1-ph) βhx2 I
βh(1-u2) (-Y-phPh)-A -βhx2> = 0.
I 0 0 (-PcPc-βc + 2βcU*2)-A∖
Persamaan karakteristik di atas dapat ditulis sebagai berikut:
((-PcPc - βc + 2βcu2) - aAa2 + a1A + a2] = 0.
dengan,
aι=Ph+ βh(1 -u2)+γ + PhPh.
a2 = phβh(1 - Ph)(1 - u2) + (ph + βh(1 - u2))(y + PhPh).
Diperoleh tiga nilai eigen dengan satu nilai eigen bernilai negatif yaitu A1 = PcPc — βc. Jika K0 > 1 maka A1 < 0. Selanjutnya, dua nilai eigen lainnya ditentukan dengan menyelesaikan persamaan kuadrat berikut A2 + a1A + a2 = 0. Persamaan ini harus
memenuhi kriteria a1 > 0 dan a2 > 0. Karena semua nilai parameter positif dan R0 > 1, maka terbukti bahwa α1 > 0 dan a2 > 0 .
Perumusan Model II
Pada model II diasumsikan kelahiran pada populasi kucing hanya terjadi pada populasi yang rentan dan peluang bayi yang lahir dalam keadaan sehat dari seorang ibu yang terinfeksi (p^), serta peluang kucing rentan lahir(pc) tidak diketahui. Berdasarkan asumsi
tersebut maka didapat sistem persamaan sebagai berikut:
dSh(t) dt dIh(t) dt dR
-^ = Y1h(t) — kR(t),
Nh(t) = Sh(f) + 1h(t) + R(t),
ds(t- = μcNc(t) - μcSc(t) - βcSc(t) 1^
dt Nc(t)
dc(t) = βcSc(t) ⅛(t)- - μcIc(t), dt cc c Nc(t) cc
Nc(t) =Sc(t)+Ic(t).
Berdasarkan langkah-langkah seperti pada model I, sistem persamaan (4) dapat
disederhanakan menjadi:
x(t) =μh- μhy(t) - βhχ(t)(ι - u(t)) - μhx(t), y (t) = βhx(t)(1 - u(t)) - γy(f),
f
(5)
u(t) = μc(1-u(t))-βcu(t)(1-u(t)).
Penentuan Titik Tetap
Pada model II, dari sistem persamaan (5) diperoleh dua titik tetap, yaitu titik tetap bebas penyakit E3(x,y,u) = (1,0,1) dantitiktetapendemikE4(x, y, u) = (x*,y*,ub),dengan
-
* βcγμn
x* = --------T--------—-------:--------:------.
-
βcβhγ - βhγμc + βcβhμh + βcγμh - βhμcμh
-
* =___________Ph(Ec-Vc)Vh___________
-
b PcPhY-PhYVc+PcPhVh+PcYVh-PhVcVh
-
* _μc
ub βc'
Bilangan Reproduksi Dasar
Bilangan reproduksi dasar (R0) pada model II dari the next generation matrix (G') yaitu :
^0
Nilai parameter yang digunakan terlihat seperti dalam Tabel 2 dan nilai indeks sensitivitas diberikan dalam Tabel 3. Simulasi numerik yang dilakukan menggunakan proporsi nilai awal x(0) = 0.5, y(0) = 0.3, z(0) = 0.2, n(0) = 0.45.
Tabel 2. Nilai parameter dari model
|
Parameter |
Nilai Parameter |
Sumber |
|
Hh |
0.233 |
(Aranda et al, 2008) |
|
βh |
0.0206 |
(Aranda et al, 2008) |
|
Ph |
0.9898 |
(Aranda et al, 2008) |
|
y |
0.000232 |
(Aranda et al, 2008) |
|
k |
0.00601 |
(Aranda et al, 2008) |
|
Hc |
0.066 |
(González-Parra et al, 2009) |
Tabel 3. Nilai indeks sensitivitas dari model
|
Parameter |
Indeks Sensitivitas Model I |
Indeks Sensitivitas Model II |
|
βc |
1 |
1 |
|
HC |
-1 |
-1 |
|
Pc |
-1 |
- |
|
Ph |
0 |
- |
|
Hh |
0 |
0 |
|
βh |
0 |
0 |
|
y |
0 |
0 |
|
k |
0 |
0 |
Berdasarkan Tabel 3 dapat disimpulkan bahwa parameter yang berpengaruh terhadap ^0 untuk Model I dan Model II adalah βc (laju transmisi toksoplasmosis dari populasi kucing rentan ke populasi kucing terinfeksi). Simulasi numerik dilakukan untuk melihat pengaruh parameter βc ini terhadap dinamika populasi pada kedua model. Dengan menurunkan nilai parameter βc dan memperhatikan perubahan nilai ^0, akan mengakibatkan kondisi yang semula endemik menjadi bebas penyakit, seperti terlihat dalam Tabel 5.
Tabel 5. Perbedaan bilangan reproduksi dasar pada kedua model
|
Parameter βc |
^0 Model I |
^0 Model II |
|
0.08 |
3.0303 > 1 |
1.21212 > 1 |
|
0.05 |
1.89394 > 1 |
0.757576 < 1 |
|
0.02 |
0.757576 < 1 |
0.30303 < 1 |
|
0.0005 |
0.0189394 < 1 |
0.00757576 < 1 |
Dengan menurunkan nilai parameter βc, model II lebih cepat mencapai kondisi bebas penyakit dibandingkan model I. Selanjutnya untuk βc = 0.02 pada model I dan βc = 0.05 pada model II memiliki nilai ^0 yang sama yaitu 0.757576, untuk perbedaan dinamika yang terjadi pada kedua model tersebut dapat dilihat pada Gambar 2.


Populasi Manusia Model I

Populasi Kucing Model I
Populasi Manusia Model II

Populasi Kucing Model II
Gambar 2 Dinamika populasi manusia dan kucing Model I dan Model II pada saat βc = 0,05
Perbedaan pengaruh perubahan parameter βc terhadap populasi manusia terinfeksi dapat dilihat pada Gambar 3 berikut.

WaMiHt)
Model I

Model II
Gambar 3 Dinamika populasi manusia terinfeksi Model I dan Model II dengan perubahan nilai βc.
Selain itu, dilakukan simulasi penurunan nilai parameter βc = 0.08 sebesar 20%, 50%, 80%, dan 100% pada kedua model. Hal ini bertujuan untuk melihat pengaruh populasi manusia terinfeksi jika parameter βc diturunkan. Perbedaan pengaruh penurunan parameter βc terhadap populasi manusia terinfeksi dapat dilihat pada tabel berikut:
Tabel 6. Hasil simulasi perubahan nilai parameter βc = 0.08
|
Parameter βc |
y(0 Model I |
y(t) Model II |
|
0.08 |
0.0564104 |
0.938658 |
|
0.064 |
0.0498107 |
0 |
|
0.04 |
0.0294451 |
0 |
|
0.016 |
0 |
0 |
|
0 |
0 |
0 |
Berdasarkan Tabel 6, jika βc diturunkan 20%, 50%, 80%, dan 100% maka akan menyebabkan populasi manusia terinfeksi pada model II lebih cepat mencapai kondisi bebas penyakit dibandingkan dengan model I. Selanjutnya, dinamika populasi jika βc diturunkan 20%, 50%, 80%, dan 100% dapat dilihat pada gambar berikut.
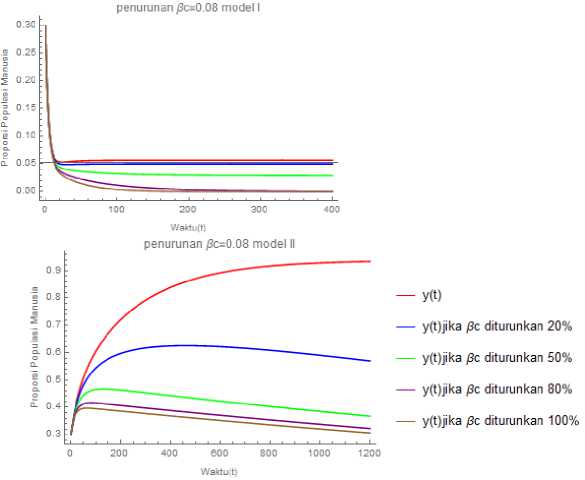
Model I
Model II
Gambar 1. Dinamika populasi saat βc diturunkan 20%, 50%, 80%, dan 100% pada
kedua model
Pada Gambar 4 dapat dilihat dinamika populasi manusia terinfeksi pada model I akan mengalami penurunan hingga mencapai kondisi stabil, sedangkan pada model II akan mengalami peningkatan hingga mencapai kondisi stabil. Proporsi populasi manusia terinfeksi ini sesuai dengan hasil pada Tabel 6.
4. Kesimpulan dan Saran
Kesimpulan
Dalam penelitian ini dianalisis dua model penyakit toksoplasmosis pada populasi kucing dan manusia. Model I menggunakan asumsi kelahiran pada populasi kucing dapat terjadi pada populasi rentan dan terinfeksi dan anaknya akan sesuai dengan induknya, sedangkan model II menggunakan asumsi kelahiran pada populasi kucing dapat terjadi pada populasi rentan dan peluang bayi yang lahir dalam keadaan sehat dari seorang ibu yang terinfeksi (ph) , serta peluang kucing lahir dalam keadaan rentan (p ') tidak diketahui. Kedua model yang dihasilkan dapat menggambarkan perilaku penyebaran penyakit.
Titik tetap bebas penyakit stabil asimtotik lokal terjadi saat bilangan reproduksi dasar kurang dari satu ^0 < 1, sedangkan titik tetap endemik stabil asimtotik lokal pada kondisi bilangan reproduksi dasar lebih satu ^0 > 1.
Hasil simulasi numerik kedua model juga menunjukkan bahwa penyakit akan punah atau tidak, bergantung pada parameter laju transmisi βc. Semakin kecil laju transmisi βc maka jumlah populasi manusia terinfeksi akan berkurang. Pada model II lebih cepat mencapai kondisi bebas penyakit dibandingkan Model I.
Saran
Penelitian selanjutnya diharapkan menambahkan parameter laju vaksinasi dan sterilisasi pada kucing sehingga penyebaran penyakit lebih sesuai dengan kondisi yang sebenarnya.
Ucapan Terima Kasih
Penulis mengucapkan terima kasih kepada Departemen Matematika IPB yang telah memberi dukungan financial terhadap makalah ini.
Daftar Pustaka
Aditama, N., Nurjazuli, & Dina, R.A. (2016). Determinan Lingkungan dan Perilaku Berhubungan dengan Terjadinya Penyakit Infeksi Toksoplasmosis di Wilayah Kota Semarang. Jurnal Kesehatan Masyarakat, 4(5), 67-76.
Aranda DF, Villanueva RJ, Arenas AJ, & González-Parra GC. 2008. Mathematical modeling of Toxoplasmosis disease in varying size populations. Comput Math with Appl. 56(3):690–696.
Driessche, V., & Watmough, J.( 2008). Further Notes on the Basic Reproduction Number.
Berlin Heidelberg: Springer-Verlag.
González-Parra, GC., Arenas AJ., Aranda, DF., Villanueva, RJ., & Jódar L. (2009). Dynamics of a model of Toxoplasmosis disease in human and cat populations. Comput Math with Appl, 57(10), 1692–1700.
Hill, DE., Chirukandoth, S., & Dubey, JP. (2005). Biology and epidemiology of Toxoplasma gondii in man and animals . Anim Heal Res Rev, 6(1), 41–61.
Natkul, C., James, MH., & Jim, MC. (2008). Determining important parameters in the spread of malaria through the sensitivity analysis of a mathematical model. Bull Math Biol, 70(5), 1272–1296.
Pei, Y., Ji, X., Li, C., & Gao, S. (2018). Dynamics of a model of Toxoplasmosis disease in cat and human with varying size populations. Math Comput Simul, 144, 52–59.
Pereira, KS., Franco, RMB., & Leal, DAG. (2010). Transmission of toxoplasmosis (Toxoplasma gondii) by foods. Ed ke-1. Volume ke-60. Elsevier Inc.
86
Discussion and feedback