Terapi Fibrinolitik Pada Pasien St-Segment Elevation Myocardial Infarction (Stemi) : Review Artikel
on

Novrianti, dkk
DOI : https://doi.org/10.24843/JFU.2021.v10.i01.p07
pISSN: 2301-7716; eISSN: 2622-4607
Jurnal Farmasi Udayana, Vol 10, No 1, Tahun 2021, 55 - 67
Terapi Fibrinolitik Pada Pasien St-Segment Elevation Myocardial Infarction (Stemi) : Review Artikel
Novrianti I.1*, Heriani1, Mustamin F.1
1Akademi Farmasi Kaltara, Jl. P. Lumpuran Kampung satu Skip, Tarakan, 77132
E-mail: irma.novrianti@gmail.com
Riwayat artikel: Dikirim: 30/06/2020; Diterima: 25/08/2020, Diterbitkan: 1/07/2021
ABSTRACT
Acute ST-elevation myocardial infarction (STEMI) occurs when there is a blockage caused by sudden atherosclerotic plaque that blocks blood flow to the heart. The goal of STEMI therapy is to restore myocardial blood flow, to save the heart. Coronary arterial reproduction recommended by the American Heart Association (AHA) and the Indonesian Cardiovascular Specialist Association (PERKI) is primary percutaneous coronary intervention (PCI) or fibrinolytic. However, not all hospitals have catheterization laboratory facilities, so they still use fibrinolytic as reperfusion therapy. To provide a review of currently available fibrinolytic therapies that can be used in STEMI patients. Four databases [Pubmed, Libgen, researchgate, and Scopus] were searched from 1987 to 2019. Include original articles including RCT, comparative, literature review, and observational study about fibrinolytics treatment in Acute STEMI. Fibrinolytic was divided into specific fibrin (alteplase, tenecteplase, and reteplase) and non-specific fibrin (streptokinase and urokinase). Fibrinolytic used in STEMI are streptokinase, alteplase, tenecteplase, and reteplase. Fibrinolytic can be given when the patient has no contraindications. Furthermore, the administration must follow protocols to minimize the risk of side effects such as bleeding. Fibrinolytic can be used as reperfusion therapy in STEMI patients when PCI cannot be done promptly.
Keywords: STEMI, Fibrinolytic, alteplase, Streptokinase, Tenecteplase
ABSTRAK
ST- Segment elevation myocardial infarction (STEMI) akut terjadi ketika terdapat sumbatan yang disebabkan plak aterisklerosis secara mendadak yang menghambat aliran darah ke jantung. Tujuan terapi STEMI adalah memulihkan kembali aliran darah miokardium, untuk menyelamatkan jantung. Reperfusi arteri koroner yang direkomendasikan oleh American Heart Association (AHA) dan Perhimpunan Dokter Spesialis Kardiovaskuler Indonesia (PERKI) adalah primary percutaneous coronary intervention (PCI) atau fibrinolitik. Namun tidak semua rumah sakit memiliki fasilitas laboratorium kateterisasi sehingga masih menggunakan fibrinolitik sebagai terapi reperfusi. Tujuan: untuk memberikan ulasan terapi fibrinolitik yang tersedia saat ini yang dapat digunakan pada pasien STEMI. Penelitian ini menggunakan empat databases [Pubmed, Libgen, researchgate, and Scopus] yang diterbitkan dari 1987 hingga 2019. Termasuk original artikel seperti RCT, Literatur Review, penelitian comparative, dan studi observasional yang terkait dengan terapi fibrinolitik pada pasien STEMI. Fibrinolitik terbagi menjadi spesifik fibrin (alteplase, tenecteplase dan reteplase) dan non-spesifik fibrin (streptokinase dan urokinase). Fibrinolitik yang digunakan pada STEMI adalah streptokinase, alteplase, tenecteplase dan reteplase. Fibrinolitik dapat diberikan ketika pasien tidak memiliki kontraindikasi. Dan pemberiannya harus mengikuti protokol untuk meminimalisir terjadinya resiko efek samping seperti perdarahan. Kesimpulannya fibrinolitik dapat digunakan sebagai terapi reperfusi pada pasien STEMI ketika PCI tidak dapat dilakukan secara tepat waktu.
Kata kunci : STEMI, Fibrinolytic, alteplase, Streptokinase, Tenecteplase
Acute Coronary Syndrome (ACS) adalah Penyempitan pembuluh darah yang disebabkan oleh plak aterosklerosis yang dapat menghambat aliran darah ke jantung. Penyumbatan ini mengakibatkan berkurangnya pasokan oksigen (O2) ke miokardium, dan memicu kerusakan sel jantung (Dipiro et al., 2009). ACS meliputi angina pektoris tidak stabil (UAP, Unstable angina pectoris), infark miokard tanpa peningkatan segmen ST (NSTEMI, non ST segment elevation myocardial infarction), infark miokard dengan elevasi segmen ST (STEMI, ST segment elevation myocardial infarction) (Tumade et al., 2016).
Acute ST-elevation myocardial infarction (STEMI) adalah penyebab utama kematian di seluruh dunia (Hermanides et al., 2018). STEMI atau infark miokard terjadi ketika terdapat sumbatan yang disebabkan plak aterisklerosis secara mendadak pada satu atau lebih arteri coroner dan menghambat aliran darah ke otot jantung (Rathore et al., 2018).
Gejala utama dari STEMI adalah sesak napas, mual dan muntah, dan pingsan. Nyeri terjadi di daerah yang sama dengan angina (bagian dada, tenggorokan, lengan, epigastrium, atau punggung) tetapi lebih parah dan berlangsung lebih lama sering digambarkan sebagai sesak, berat atau penyempitan di dada (Newby et al., 2010). Untuk penegakan diagnose dapat dilihat dari gambaran klinik pasien seperti chest pain, kemudian dilihat dari hasil EKG yang menunjukan adanya peningkatan segment ST di 12 lead, dan peningkatan cardiac marker seperti troponin I (Antman & Loscalzo, 2015)
STEMI disebabkan oleh adanya erosi atau ruptrunya plak aterosklerosis yang disertai adherence, aktivasi, dan agregasi platelet yang berkelanjutan, dan mengaktifkan clotting cascade sehingga menyebabkan pembentukan trombus. Trombus yang terbentuk di arteri coroner ini terdiri dari fibrin dan trombosit. Trombus akan mengalir mengikuti aliran darah kemudian akan menyebabkan sumbatan baik itu sumbatan sebagian ataupun sumbatan total atau penuh pada arteri koroner. STEMI merupakan akibat dari sumbatan penuh (complete occlusion) dan berkepanjangan dari suatu pembuluh darah koroner epikardial. Sumbatan ini dapat menyebabkan terjadinya nekrosis miokardium yang dapat merusak fungsi dari jantung (Hermanides et al., 2018; Antmann et al., 2010; Dipiro et al., 2009; Laksono, 2015; Daga et al., 2011).
Tujuan dari terapi STEMI adalah memulihkan kembali aliran darah miokardium, untuk menyelamatkan jantung dan menurunkan mortalitas serta menjaga fungsi ventrikel (Fox et al., 2013). Dan strategi dari managemen terapi dari STEMI adalah pemulihan cepat dari potensi oklusi total pada arteri koroner, memperpendek waktu iskemik, dan mengurangi ukuran infark (Ibanez et al., 2018; Kasper et al., 2016). Terapi reperfusi yang diekomendasikan oleh American Heart Association (AHA) dan Perhimpunan Dokter Spesialis Kardiovaskuler Indonesia (PERKI) adalah dengan cara primary percutaneous coronary intervention (PCI) atau fibrinolitik (Ibanez et al., 2018; PERKI, 2015).
Terapi reperfusi bertujuan memperbaiki aliran darah pada miokardium, untuk menyelamatkan miokard dan menurunkan mortalitas, serta menjaga fungsi ventrikel kiri.
Keberhasilan terapi reperfusi sangat bergantung pada banyaknya waktu yang terlewat sejak gejala timbul sampai pasien mendapat terapi. Tujuan utama adalah mencapai reperfusi dini dengan waktu “symptom-to-needle” dan “door-to-needle” yang pendek pada pasien infark miokard (Fox et al., 2013).
PCI lebih efektif dibandingkan fibrinolitik dalam membuka sumbatan di arteri korener. Strategi ini juga memiliki efek yang baik terhadap hasil klinis baik jangka pendek maupun jangka panjang serta dapat mengurangi risiko kematian, infark miokard atau stroke berulang. Penerapan PCI dibatasi oleh ketersediaannya, karena menggunakan teknik berbasis kateter (catheter based technique) (Laksono, 2015; Kasper et al., 2016). Namun, masih banyak rumah sakit yang tidak memiliki fasilitas kateterisasi jantung, sehingga fibrinolisis adalah pengobatan yang paling umum digunakan pada pasien STEMI (Fox et al., 2013; Sampson et al., 2015). Oleh karena itu diperlukan pengetahuan tambahan tentang penggunaan fibrinolitik pada pasien STEMI agar diperoleh keberhasilan reperfusi jaringan yang optimal. Dalam artikel ini kami mengulas terapi fibrinolitik yang tersedia saat ini yang dapat digunakan pada pasien STEMI.
-
2. PEMBAHASAN
Plak aterosklerotik merupakan penyebab penyakit arteri koroner dan Acute Coronary Syndrom di sebagian besar pasien. Adanya erosi, ruptur, atau fisur pada plak aterosklerotik yang tidak stabil, menyebabkan plak aterosklerotik lebih mudah mengalami rupture. Setelah terjadinya ruptur dari plak aterosklerotik, maka akan terjadi trombus
yang menyebabkan terjadinya oklusi sebagian atau oklusi total pada plak aterosklerotik yang telah ruptur. Paparan jaringan kolagen dan faktor jaringan di plak aterosklerotik yang mengalami ruptur akan menyebabkan adesi dan aktivasi platelet sehingga menyebabkan terjadinya pelepasan senyawa vasoaktif seperti adenosine diphosphate (ADP) dan tromboxan A2 senyawa tersebut akan menyebabkan terjadinya vasokonstriksi dan potensi platelet lebih lanjut (Antmann et al., 2010; Dipiro et al., 2009).
Aktivasi platelet juga akan menyebabkan perubahan konformasi pada permukaan reseptor glikoprotein IIb/IIIa pada platelet sehingga akan terjadi cross-link antar platelet melalui jembatan fibrinogen. Proses ini adalah jalur akhir dari proses agregasi platelet. Oklusi akibat agregasi platelet bersifat sebagian dan trombus yang terbentuk berwarna putih (white thrombus). Akan tetapi, seringkali terjadi agregasi platelet disertai dengan kaskade koagulasi jalur ekstrinsik secara simultan sehingga terjadi aktivasi trombin (faktor IIa) sehingga terjadi perubahan fibrinogen menjadi fibrin melalui aktivitas enzimatik. Fibrin akan menyebabkan stabilisasi agregat platelet dan menangkap sel darah merah dan menyebabkan terjadinya oklusi total dari pembuluh darah. Thrombus yang mengandung banyak sel darah merah akibat adanya fibrin disebut dengan thrombus merah (red thrombus) (Antmann et al., 2010).
Terapi fibrinolitik adalah terapi yang digunakan untuk mengatasi masalah yang timbul karena adanya bekuan darah atau thrombus seperti thrombosis vena, emboli paru, infark miokard (STEMI), stroke iskemik, dan tromboemboli arteri (Ali et al., 2014). Terapi fibrinolitik merupakan strategi
reperfusi penting dalam terapi STEMI ketika PCI primer tidak dapat dilakukan secara tepat waktu. Tujuan utama dari terapi fibrinolisis adalah pemulihan cepat dari patensi penuh arteri koroner (Newby et al., 2010). Terapi fibrinolitik direkomendasikan dalam 12 jam dari onset gejala jika PCI primer tidak dapat dilakukan dalam 120 menit dari diagnosis STEMI dan tidak terdapat kontraindikasi (Ibanez et al., 2018).
Pemberian fibrinolitik memberikan keuntungan yang baik dengan level evidence A jika onset gejala <30 menit. Manfaat fibrinolitik sebesar 5% pada pasien dengan elevasi ST yang dirawat dalam 6 jam dan 4% pada pasien dirawat antara 7 dan 12 jam setelah timbulnya gejala. Manfaatnya paling besar terlihat pada pasien yang dirawat dalam 2 jam pertama. Manfaat fibrinolitik lebih sedikit atau bahkan berbahaya ketika diberikan kepada pasien dengan onset gejala lebih dari 12 jam atau pada pasien yang mengalami depresi EKG atau segmen ST normal. (Newby et al., 2010). Hal ini disebabkan karena fibrinolitik memiliki efek samping perdarahan. Beberapa kondisi dapat dikontraindikasikan dengan penggunaan fibrinolitik, antara lain stroke hemoragik, stroke iskemik dalam 6 bulen terakhir, trauma operatif atau trauma kepala yang berat dalam 3 bulan terakhir, perdarahan saluran cerna dalam 1 bulan terakhir karena dapat meningkatkan resiko perdarahan setelah penggunaan fibrinolitik (PERKI, 2015). Ketika terapi fibrinolitik dikontraindikasikan, maka terapi PCI untuk keadaan darurat harus dipertimbangkan (Newby et al., 2010).
Faktor kunci dalam pengobatan STEMI adalah waktu iskemik (onset gejala), dengan kata lain, waktu dari timbulnya gejala hingga terapi reperfusi (Hendersoni et al.,
2019). Waktu ideal pemberian fibrinolitik adalah 30 menit setelah onset gejala dengan level evidence A (PERKI, 2015). Terapi fibrinolitik terbukti dapat mencegah 30 kematian dini per 1000 pasien yang dirawat dalam waktu 6 jam setelah onset gejala (Ibanez et al., 2018; PERKI, 2015). Menurut ACCF/AHA tahun 2013 penggunaan fibrinolitik diberikan dalam onset gejala kurang dari 12 jam (O’Gara et al., 2013), namun sebaiknya untuk hasil terbaik dapat diberikan dalam onset gejala iskemik 3 jam (Gulati & Gersh, 2009). Fibrinolitik menunjukan manfaat yang lebih sedikit ketika diberikan kepada pasien dengan onset gejala lebih dari 12 jam karena plak yang terbentuk bersifat mature sehingga sulit untuk dilisiskan (Newby et al., 2010). Setiap menit dalam penundaan reperfusi pasti akan menghasilkan nekrosis yang lebih luas dan outcome yang buruk (Werf, 2012).
Penggunaan terapi fibrinolitik yang tepat dapat mengurangi angka kematian di rumah sakit sebesar 25-50%. Manfaat terbesar terlihat ketika fibrinolitik diberikan kurang dari 2 jam setelah onset gejala dan pada pasien dengan risiko tertinggi, seperti lansia. Berdasarkan Myocardial Infarction Triage and Intervention (MITI) Randomized trial pemberian fibrinolitik pada pasien STEMI pada 70 menit pertama dapat menurunkan angka kematian sebesar dari 8,7% menjadi 1,2% dan mengurangi ukuran infark dari 11,2% menjadi 4,9% dibandingkan jika digunakan lebih lama hingga 180 menit (Fox et al., 2013). Menurut penelitian meta-analisis menyebutkan jika penggunaan fibrinolitik dapat mengurangi angka mortalitas (Jinatongthai et al., 2017).
Pemberian fibrinolitik harus melihat 3 hal yaitu onset gejala, ketersediaan obatnya
dan faktor klinis pasien (Pandie et al., 2016). Pada saat pemberian fibrinolitik, pertama-tama harus melihat riwayat kesehatan pasien, seperti operasi, trauma, alergi, penggunaan obat sebelumnya untuk mengetahui apakah pasien memiliki kontraindikasi terhadap fibrinolitik atau tidak. Jika tidak terdapat kontraindikasi, maka fibrinolitik dapat dilakukan. Pada saat pemberian fibrinolitik sangat disarankan untuk memantau tanda-tanda vital dan gejala-gejala perdarahan setiap 15 menit dalam 1 jam pertama dan setiap 30 menit 2 jam selanjutnya, kemudian diamati setiap jam hingga pemberian fibrinolitik selesai. Setelah pemberian fibrinolitik pemantauan terhadap tanda-tanda vital ataupun resiko efek samping masih terus dilakukan, selain itu melihat respon dari terapi seperti chest pain yang dialami pasien, merekam jantung (EKG) satu jam setelah fibrinolitik, dan timbulnya aritmia reperfusi, serta pasien harus tetap istirahat selama 6 jam (Ali et al., 2014).
Efektifitas fibrinolitik pada STEMI dilihat dari keberhasilan reperfusi yang terjadi. Keberhasilan reperfusi ditandai dengan hilangnya nyeri dada yang dialami pasien, terjadi resolusi EKG ≥ 50%, adanya aritmia reperfusi (Bendary et al., 2017; Churchhouse & Ormerod, 2017). Pembukaan infark yang cepat di arteri berhubungan dengan berkurangnya ukuran infark, perbaikan fungsi left ventrikel dan outcome klinis yang baik. Penurunan nyeri dada setelah trombolisis menunjukan korelasi dengan angiografi. Resolusi segmen ST setelah STEMI dipengaruhi oleh status arteri koroner (Varma et al., 2016).
Menurut Global Utilisation of Streptokinase and T-PA for Occluded coronary arteries-1 (GUSTO-1) diketahui
bahwa pemberian fibrinolitik menunjukan efektifitas dalam reperfusi sekitar 50-60% (The GUSTO, 1993). Sedangkan penelitian Ghaffari, Kazemi and Golzari (Ghaffari et al., 2013) menunjukan keberhasilan reperfusi dari fibrinolitik sebesar 59%. Serta penelitian Bendary et al (Bendary et al., 2017) keberhasilan penggunaan fibrinolitik adalah sebesar 62%.
Menurut EARLY-MYO Trial (Early Routine Catheterization After Alteplase Fibrinolysis Versus Primary PCI in Acute ST-Segment–Elevation Myocardial Infarction) oleh Pu et al, 2017 (Pu et al., 2017) yang merupakan uji Randomized Clinical Trial (RCT) yang pertama yang membandingkan Pharmaco-Invasive (PhI) strategy with halfdose alteplase fibrinolysis dengan Primary PCI (PPCI) pada pasien STEMI, menunjukan bahwa pada pasien STEMI yang memiliki resiko kecil dengan onset gejala ≤6 jam dengan rencana PCI ≥ 60 menit, memperlihatkan hasil bahwa Strategi PhI dengan half-dose alteplase dan PCI yang tepat waktu menawarkan reperfusi epikardial dan miokardial yang lebih lengkap di bandingkan terapi PPCI saja.
Mekanisme aksi dari fibrinolitik adalah streptokinase berikatan dengan plasminogen dimana mengubah plasminogen menjadi plasmin. Sedangkan alteplase, urokinase, reteplase dan tenecteplase bekerja dengan memecah plasminogen untuk menghasilkan plasmin dan kemudian memecah clot yang kaya akan fibrin menjadi fibrin degradation product. Sedangkan alfimeprase memecah fibrin secara langsung dan menghasilkan fibrin degradation product (Baskin et al., 2012). Skematik dari aksi fibrinolitik dapat dilihat pada gambar 1.
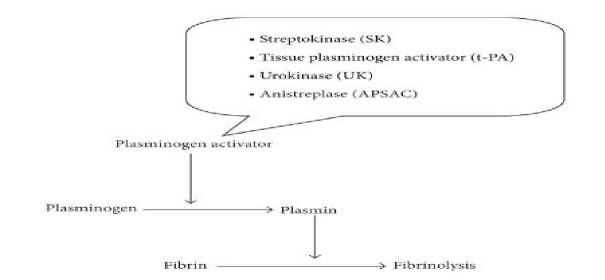
Gambar 1 . Schematic representation of fibrinolysis (Ali et al., 2014)
d) Jenis Fibrinolitik
Fibrinolitik terbagi menjadi 2 yaitu agen yang tidak spesifik fibrin dan agen yang spesifik fibrin. Dimana agen yang tidak spesifik fibrin adalah streptokinase dan urokinase sedangkan yang spesifik fibrin adalah
alteplase, Tenecteplase, dan reteplase, dapat dilihat dalam tabel 1 (Fox et al., 2013; Vivek, 2017). Fibrinolitik yang direkomendasikan PERKI untuk STEMI adalah streptokinase, alteplase dan Tenecteplase (PERKI, 2015).
Tabel. 1 Jenis Fibrinolitik (Ali et al., 2014)
|
Generasi Fibrinolitik |
Spesifik Fibrin Non-spesifik Fibrin |
|
Satu |
…. - Streptokinase - urokinase |
|
Kedua |
plasminogen activator (t-PA) - Sk-plasminogen activating
|
|
Ketiga |
|
Adapun macam-macam dari fibrinolitik yang digunakan pada STEMI adalah :
-
1. Streptokinase
Streptokinase merupakan agen non-spesific fibrin yang berasal dari kelompok streptokokus yaitu β-hemolytic group-C streptococci. Streptokinase bergabung dengan plasminogen bebas disirkulasi untuk
membentuk kompleks aktivator yang menghasilkan plasmin dan akan memecah thrombus (Vivek, 2017; Sekhar et al., 2017).
Streptokinase merupakan original thrombolytic agent yang bekerja dengan mengikat plasminogen untuk membentuk kompleks enzim yang mengubah plasminogen menjadi plasmin. Selain itu, streptokinase juga meningkatkan kadar
protein-C di sirkulasi sehingga meningkatkan pemecahan bekuan atau gumpalan darah. Dosis infus dari streptokinase adalah 1,5 juta IU dalam 100 mL larutan salin selama 30-60 menit. Adapun efek samping yang sering terjadi dari penggunaan streptokinase dibandingkan dengan alteplase adalah hipotensi, alergi dan pendarahan mayor (Fox et al., 2013).
Berdasarkan penelitian Gruppo Italiano Per Lo Studio Della Sopravvivenza Nell’Infarti Miocardico-2 (GISSI-2) tahun 1990 (GISSI-2, 1990) menunjukan bahwa tidak ada efek yang berbeda secara signifikan antara alteplase dan streptokinase. Namun pada penelitian GUSTO-1, 1993 (The GUSTO, 1993) alteplase lebih bersifat superior dari pada streptokinase.
-
2. Alteplase
Alteplase merupakan enzim alami (plasminogen spesifik) yang diproduksi oleh teknologi DNA rekombinan dari kultur jaringan manusia. Altelase bersifat “clot selective,”. Alteplase berikatan dengan fibrin pada permukaan clot yang mengaktifkan plasminogen yang terikat pada fibrin. Plasmin di bentuk dari plasminogen yang terikat fibrin. Molekul fibrin dipecah menjadi plasmin dan gumpalan yang larut (Vivek, 2017).
Pemberian awal dilakukan dengan bolus kemudian diikuti dengan infus intravena lambat karena waktu paruhnya yang sangat singkat. Karena waktu paruh alteplase yang sangat singkat maka harus digunakan bersama dengan antikoagulan intravena untuk menghindari reoklusi. Penggunaan tPA dapat menunjukan angka mortalitas 14% lebih rendah (penurunan absolut 1%) dibandingkan dengan streptokinase. Alteplase lebih banyak
digunkaan pada pasien stroke iskemik dibandingkan pasien STEMI akut (Fox et al., 2013; Vivek, 2017).
Dosis alteplase yang digunakan adalan infusan dengan dosis 100 mg selama 3 jam, dimana 60 mg pada jam pertama (6-10 mg diberikan secara bolus), dan 20 mg selama jam kedua, selanjutnya 20 mg pada jam ketiga. Untuk pasien dengan bobot tubuh lebih kecil <65 kg maka dosis yang digunakan adalah 1,25 mg/kg adalah Seperti halnya fibrinolitik lainnya penggunaan aspirin 300 mg harus diberikan sesegera mungkin dan diikuti clopidogrel 75 mg per hari. Heparin intravena juga harus diberikan setidaknya setidak nya selama 48 jam. (Fox et al., 2013).
Keuntungan dari tPA adalah dapat meningkatkan kelangsungan hidup, lebih baik dibandingkan agen fibrinolitik lainnya, seperti streptokinase dan memiliki resiko yang sedikit lebih tinggi terhadap pendarahan intracerebra. Agen fibrinolitik lainnya yang merupakan analog dari tPA, seperti tenecteplase dan reteplase, memiliki waktu paruh plasma lebih lama dari alteplase dan bisa diberikan secara bolus intravena. Tenecteplase (TNK) sama efektifnya dengan alteplase dalam menurunkan angka kematian (Newby et al., 2010).
Berdasarkan hasil metaanalisis oleh Jinatongthai et al (Jinatongthai et al., 2017), menunjukan bahwa rejimen accelerated alteplase plus antikoagulan parenteral dapat mengurangi resiko moratlitas dibandingkan dengan streptokinase dan antikoagulan parenteral.
-
3. Tenecteplase
Tenecteplase (TNK) merupakan rekayasa genetika dari alteplase dengan
subtansi asam amino di tiga site. Hal ini menyebabkan penurunan waktu eliminasi dan waktu paruh menjadi lebih panjang atau lama, sehingga menyebabkan peningkatan spesifisitas fibrin, dan resistensi terhadap PAI-1. Bolus tunggal tenecteplase dalam dosis yang disesuaikan dengan berat badan yaitu 0,5 mg/kg dibandingkan dengan accelerated alteplase menunjukan angka mortalitas yang sama. Namun resiko pendarahan tenecteplase dan kebutuhan transfusi darah lebih rendah dibandingkan alteplase, selain itu manfaat praktis dari pemberian bolus dapat menjadikan tenecteplase menjadi pilihan di ruang emergensi untuk mengatasi STEMI. (Fox et al., 2013; Vivek, 2017; Thomas & Christoph, 2015).
Tenecteplase telah diuji secara ekstensif dalam uji klinis. Dalam ASSENT-1 (assessment of safety and efficacy of a new thrombolytic agent) percobaan pada pasien dengan infark miokard akut, single bolus dari tenecteplase terbukti bersifat aman sebagai gold standart terapi trombolitik, dibandingkan rejimen accelerated alteplase (bolus awal diikuti oleh infus lebih dari 90 menit). Dalam TIMI-10b (Thrombolysis In Myocardial Infarction) percobaan pemberian dosis bolus tunggal tenectplase 40 mg selama memiliki rata-rata kekuatan yang sama dengan pemberian accelerated alteplase selama 90 menit. Dalam ASSENT-2 Trial tenecteplase dan alteplase keduanya memiliki angka mortalitas yang sama setelah 30 hari. Seperti dengan reteplase, tenecteplase dibandingkan dengan alteplase keduanya memiliki efikasi yang sama dan tenecteplase lebih superior ketika diberikan dala dosis bolus tunggal (Thomas & Christoph, 2015).
-
4. Reteplase
Reteplase (rPA) adalah deletion mutan dari alteplase dengan menghilangkan beberapa hal seperti kringle-1, finger, and faktor pertumbuhan domain dan juga beberapa rantai samping dari karbohidrat. Reteplase dapat memperpanjang waktu eliminasi, sehingga regimen yang digunakan merupakan double-bolus dengan dosis 10 U+10 U secara intravena, dimana pemberiannya dilakukan masing-masing lebih dari 10 menit dan 30 menit secara terpisah. Heparin tidak boleh diberikan melalui jalur intravena yang sama karena bersifat incompatibility. Kasus kematian dengan penggunaan reteplase dan streptokinase bersifat sama atau mirip begitu pula dengan resiko terjadinya stroke reteplase serupa dengan alteplase (Fox et al., 2013). Satu-satunya keunggulan reteplase dibandingkan Alteplase adalah duration of action dari reteplase lebih lama dan pemberiannya juga secara bolus, sehingga tidak membutuhkan infus intravena. Namun, spesifisitasnya untuk plasminogen terikat fibrin bersifat mirip dengan alteplase (Vivek, 2017)
Reteplase telah disetujui untuk pengobatan trombolitik infark miokard akut. Dalam Rapid I (Recombinant Plasminogen Activator Angiographic Phase II international Dose Finding Study) pemberian reteplase lebih unggul dari alteplase (diberikan lebih dari tiga jam) dengan patensi reteplase dicapai lebih awal dan lebih sering dibandingkan accelerated alteplase (lebih dari 1,5 jam). Namun menurut GUSTO-III menunjukan bahwa tidak ada perbedaan dalam hal mortalitas setelah 30 hari antara reteplase dengan alteplase. Kesimpulannya reteplase
dibandinkan dengan alteplase keduanya memiliki efikasi yang sama dalam reperfusi dan retelpase lebih unggul ketika diberikan dalam bolus ganda (Thomas & Christoph, 2015).
Adapun Beberapa perbedaan karakteristik dari fibrinolitik yang sering digunakan di ditampilkan pada tabel 2.
Tabel 2. Karakteristik Fibrinolitik (Fox et al., 2013; Vivek, 2017)
|
Keterangan |
Streptokinase |
Alteplase (tPA) |
Reteplase (rPA) |
Tenecteplase (TNK) |
|
Selektif fibrin |
Tidak |
++ |
+ |
+++ |
|
Ikatan Plasminogen |
Tidak langsung |
Langsung |
Langsung |
Langsung |
|
Lama infuse (menit) |
60 |
90 |
10+10 |
5-10 detik |
|
Waktu paruh |
23 |
<5 |
13-16 |
20 |
|
Pemecah fibrinogen |
4+ |
1-2+ |
Tidak diketahui |
>tPA |
|
Heparin dini |
Kemungkinan |
Ya |
Ya |
Ya |
|
Hipotensi |
Ya |
Tidak |
Tidak |
Tidak |
|
Reaksi alergi |
Ya |
Tidak |
Tidak |
Tidak |
|
T1/2 Plasma (min) |
23-29 |
4-8 |
15 |
20 |
|
Dosis |
1,5 MIU/60 menit |
100 mg/90 menit |
2x10 IU bolus 30 menit apart |
0,5 mg/kg bolus |
Berdasarkan mekanisme aksi dari fibrinolitik yang mengubah plasminogen menajdi plasmin dan kemudian plasmin akan memecah clot yang kaya akan fibrin menjadi fibrin degradation product (Baskin et al., 2012). Selain itu plasmin yang di hasilkan dari fibrinolitik dapat menyebabkan deplesi fibrinogen, deplesi factor V dan VIII dan disfungsi platelet, serta dapat meningkatkan fibrin degradation product. Hal tersebut dapat menyebabkan resiko pendarahan (Candelise et al., 1996). Selain itu streptokinase dapat menyebabkan penurunan plasminogen disirkulasi sehingga dapat meningkatkan resiko pendarahan (Vivek, 2017). Streptokinase
juga merupakan protein asing sehingga dapat menimbulkan reaksi alergi yang diperantarai immunoglobulin E (IgE), dan dapat menimbulkan gejala urtikaria, bronkospasme dan hipotensi (Nazari et al., 1987).
Adapun efek samping dari penggnaan fibrinolitik sebagai berikut:
-
1. Pendarahan
Sejauh ini komplikasi paling umum dari terapi trombolitik adalah perdarahan. Karena tujuan terapi agen trombolitik adalah pemecahan bekuan darah, diharapkan gumpalan dengan atau tanpa fungsi aktif hemostatik dapat dilisiskan oleh obat-obatan. Semua agen fibrinolitik yang tersedia saat ini
akan menghasilkan derajat fibrinolisis sistemik dan menghasilkan gangguan pasca-statis yang dapat menyebabkan perdarahan. Selain itu, antikoagulan diberikan secara rutin setelah trombolisis menambah risiko komplikasi perdarahan (Nazari et al., 1987).
Resiko perdarahan terjadi berkisar antara 0,5% dan 1%. Oleh karena itu, perawatan harus dihentikan jika terdapat risiko pedarahan yang signifikan seperti pendarahan serius, pendarahan internal aktif, pasien sebelumnya memiiki riwayat perdarahan subarachnoid atau intraserebral, hipertensi yang tidak terkontrol, melakukan operasi dalam 1 bulan sebelumnya, trauma terbaru (termasuk resusitasi traumatis), tukak lambung aktif, dan kehamilan. (Newby et al., 2010).
Menurut Vivek (Vivek, 2017) mengemukakan bahwa streptokinase dapat menyebabkan penurunan plasminogen disirkulasi sehingga dapat meningkatkan resiko perdarahan. Sedangkan berdasarkan hasil meta-analisis jinatongthai et al (Jinatongthai et al., 2017) diketahui bahwa resiko pendarahan mayor lebih rendah terjadi pada penggunaan streptokinase dibandingkan accelerated alteplase. Resiko perdarahan juga semakin meningkat ketika ditambahkan antikoagulan parenteral.
-
2. Allergic and Immunological Reactions
Reaksi alergi berhubungan dengan pemberian streptokinase, karena satu-satunya agen yang merupakan protein asing. Reaksi alergi langsung diperantarai oleh IgE termasuk urtikaria, bronkospasme dan hipotensi. Delayed reaction dimediasi oleh IgG termasuk serum sickness dan demam. Beberapa reaksi yang dilaporkan sebagai reaksi alergi meliputi respons demam. Reaksi
alergi pada penggunaan streptokinase jarang terjadi namun potensi reaksi anafilaksis, yang bisa sangat parah, tidak boleh diremehkan. Skin test dengan dosis kecil streptokinase intradermal merupakan prediktor yang baik untuk respons alergi langsung dari jenis anafilaksis, meskipun tidak dapat memprediksi reaksi yang tertunda. Delayed reactions biasanya bersifat ringan dan dapat sembuh dengan sendirinya (Nazari et al., 1987).
-
3. Hipotensi
Hipotensi merupakan efek samping yang paling sering ditemukan pada penggunaan streptokinase. Namun hipotensi ini berbeda dengan yang ditemui pada saat reperfusi. Gejala ini terjadi segera setelah pemberian infus, dapat disertai dengan flushing and anxiety, dan dapat diatasi dengan pemberian cairan dan penghentian infus untuk sementara waktu. Komplikasi ini bersifat sementara dan jinak. Ketika hipotensi telah membaik dan infus diberikan kembali maka efek hipotensi ini tidak akan terjadi kembali. Mortalitas belum dikaitkan dengan hipotensi yang terjadi dengan infus streptokinase (Nazari et al., 1987). Hipotensi pada peggunaan fibrinolitik dapat disebabkan oleh aktivasi sistem bradikinin-kallikrein, vasodilasi langsung dan penurunan viskositas darah (Chang & Yeh, 2014).
-
4. Aritmia Reperfusi
Aritmia yang terjadi selama terapi trombolitik pada infark miokard akut akut digunakan sebagai salah satu dari beberapa marker reperfusi non-angiografi, tetapi sensitivitas dan spesifisitasnya belum didefinisikan secara jelas. Selain respon bradikardi, ritme yang paling umum diamati adalah percepatan irama idioventrikular dan
takikardia ventrikel. Aritmia terjadi pada 70 hingga 100% pasien dengan rekanalisasi. Selain idioventricular rhythm dan ventricular tachycardia fibrilasi ventrikel juga telah dilaporkan, meskipun sulit untuk membedakan antara kejadian nya disebabkan oleh infark miokard atau komlikasi dari reperfusi. Kejadian fibrilasi ventrikel sangat bervariasi, dilaporkan pada 0 hingga 17% kasus (Nazari et al., 1987).
-
5. Guillain-Barre Syndrome
Ada beberapa laporan kasus yang menggambarkan hubungan antara sindrom Guillain-Barre dan terapi streptokinase. Meskipun hubungan kausal belum ditetapkan, insidennya lebih tinggi dari yang ditentukan oleh coincidental association. Streptokinase dapat menginduksi respons imunologis yang dapat memicu sindrom Guillain-Barre (Nazari et al., 1987).
STEMI merupakan penyakit yang dapat mengancam jiwa apabila tidak dilakukan penanganan dengan segera karena dapat menyebabkan nekrosis miokardium yang dapat menyebabkan jantung kehilangan fungsinya. Tujuan dari terapi STEMI adalah mengembalikan perfusi jaringan yang terganggu akibat adanya thrombus. Salah satu pilihan untuk terapi reperfusi adalah fibrinolitik. Fibrinolitik dapat dalam management terapi STEMI fibrinolitik dapat digunakan sebagai terapi reperfusi jaringan apabila terapi PPCI tidak dapat dilakukan dengan mempertimbangkan status kontraindikasi dari pasien. Beberapa penelitain menunjukan bahwa terapi fibrinolitik efektif dalam mengembalikan perfusi jaringan. Meskipun demikian perlu tetap dilakukan pemantauan terhadap efek
samping yang dapat ditimbulkan oleh fibrinolitik itu sendiri seperti resiko terjadinya perdarahan, hipotensi dan resiko alergi yang muncul. Sehingga pemberiannya harus mengikuti protocol yang ada.
DAFTAR PUSTAKA
-
1. Ali, M.R. et al., (2014). Aspect of thrombolytic therapy: A review. Scientific World Journal, (1).
-
2. Antman E, Loscalzo J. ST-Segment Elevation Myocardial Infarction. In D LK, editor. Harrison's Principles of Internal Medicine. 19th ed. New York: McGraw-Hill Education; 2015. p. 1599-1611.
-
3. Antmann, E., Braunwald, E. & Loscalzo, J., (2010). ST Segment Eelevation
Myocardial Infarction. In Harisson’s Cardiovascular Medicine. New york: Mc Graw Hill Inc.
-
4. Baskin, J. et al., (2012). Thrombolytic therapy for central venous catheter occlusion. Haematologica, 97(5), pp.64150.
-
5. Bendary, A., Tawfik, W., Mahrous, M. & Salem, M., (2017). Fibrinolytic therapy in patients with ST-segment elevation myocardial infarction: Accelerated versus standard Streptokinase infusion regimen. Journal of Cardiovascular and Thoracic Research, 9(4).
-
6. Candelise, L. et al., (1996). Thrombolytic therapy From myocardial to cerebral infarction. Ital. J. Neurol. Sci, 17, pp.5-21.
-
7. Chang, L. & Yeh, R., (2014). Evaluation and Management of ST-elevation Myocardial Infarction and Shock. European Cardiology Review, 9(2),
pp.88-91.
-
8. Churchhouse, A. & Ormerod, J., (2017). Infark Miokard Akut. In H. Kalim, ed. Kardiologi dan Kelainan Vaskular. 1st ed. Singapore: Elsevier. pp.177-93.
-
9. Daga, L.C., Kaul, U. & Mansoor, A., (2011). Approach to STEMI and NSTEMI. SUPPLEMENT TO JAPI • decem ber 2011 • VOL. 59, 59, pp.19-25.
-
10. Dipiro, J. et al., (2009). Acute Coronary Syndrome. In Pharmacotherapy: A Pathophysiologic Approach. 8th ed. United States: McGraw-Hill Education. pp.642-575.
-
11. Fox, K., White, H.D., Gersh, B. & Opie, L.H., (2013). Antithrombotic Agents:
Platelet Inhibitors, Acute Anticoagulants, Fibrinolytics, and Chronic
Anticoagulants. In Drugs For The Heart. Eighth Edition ed. Philadelphia: Saunders Elsevier Inc. pp.378-87.
-
12. Ghaffari, S., Kazemi, B. & Golzari, I.G., (2013). Efficacy of a New Accelerated Streptokinase Regime in Acute Myocardial Infarction: A Double Blind Randomized Clinical Trial.
Cardiovascular Therapeutics, 31(1).
-
13. GISSI-2, (1990). GISSI-2: A factorial randomised trial of alteplase versus streptokinase and heparin versus no heparin among 12 490 patients with acute myocardial infarction. THE LANCET, 336.
-
14. Gulati, R. & Gersh, B.J., (2009).
Antithrombotic Therapy for the Prevention of Reinfarction After Reperfusion Therapy: The Price of Success. Revista Española de Cardiología (English Edition), 62(5).
-
15. Hendersoni, M., Carberry, J. & Colin, B., (2019). Targeting an Ischemic Time Journal of the American Heart Association, 8, pp.1-4.
-
16. Hermanides, R.S., Kilic, S. & Van’t Hof, A.W.J., (2018). Optimal pharmacological therapy in ST-elevation myocardial
infarction—a review: A review of
antithrombotic therapies in STEMI. Neth Heart Journal, 26(6).
-
1 7.Ibanez, B. et al., (2018). 2017 ESC
Guidelines for themanagement of acutemyocardial infarction in patients presenting with ST-segment elevation. European Heart Journal, 39, pp.119-77.
-
18 . Jinatongthai, P. et al., (2017). Comparative efficacy and safety of reperfusion therapy with fibrinolytic agents in patients with ST-segment elevation myocardial infarction: a
systematic review and network metaanalysis. Lancet, 390(10096).
-
19 .Kasper, D.L. et al., (2016). ST-Segmen Elevation Miocardial Infarction. In Harrison's Manual Of Medicine. 19th ed. New York: McGraw-Hill Education. pp.658-67.
-
20 .Laksono, B.B., (2015). Literatur Review Efektifitas Terapi Dan PPCI (Primary Percutaneus Corornary Intervention) Sebagai Alternative Terpi Revaskulerisasi Pada Acute Coronary Syndrome (ACS). Jurnal Kesehatan Hesti Wira Sakti, 3(3).
-
21 .Nazari, J., Davidson, R., Kaplan, K. & Fintel, D., (1987). Adverse Reactions to Thrombolytic Agents Implicationsfor Coronary Reperfusion Following Myocardia lInfarction. Medica
lToxicology, 2, p.27286.
-
22 .Newby, D.E., Grubb, N.R. & Bradbury, A., (2010). Cardiovascular Disease. In N.R. Colledge, B.R. Walker & B.H. Ralston, eds. Davidson's Principle and Practice of Medicine. 21st ed. Edinburgh: Elsevier. pp.577-98.
-
23 . O’Gara, P.T. et al., (2013). 2013
ACCF/AHA Guideline for the
Management of ST-Elevation Myocardial Infarction: Executive Summary.
Circulation, 127(4).
-
24 .Pandie, S., Hellenberg, D., Hellig, F. & Ntsekhe, M., (2016). Approach to chest pain and acute myocardial infarction. South African Medical Journal, 106(3).
-
25 .PERKI, Perhimpunan Dokter Spesialis Kardiovaskuler Indonesia., (2015). Pedoman Penatalaksanaan SIndrom Koroner Akut. Jurnal Kardiologi Indonesia.
-
26 .Pu, J. et al., (2017). Efficacy and Safety of a Pharmaco-Invasive Strategy With HalfDose Alteplase Versus Primary Angioplasty in ST-Segment–Elevation Myocardial Infarction. Circulation, 136.
-
27 .Rathore, .V., Singh, N. & Mahat, R.K., (2018). Risk Factors for Acute Myocardial Infarction: A Review. EJMI, 2(1), pp.1-7.
-
28 .Sampson, A.J., Paul, T. & Stouffer, G.A., (2015). Pharmacological Therapy in The Management of Acute Coronary Syndromes. In H. Wang & C. Patterson, eds. Atherosclerosis: Risks, Mechanisms, and Therapies. First Edition ed. NC, USA: John Wiley & Sons, Inc. pp.517-31.
-
29 .Sekhar, G.R. et al., (2017). A Review on Thrombolytic Therapy used in Myocardial Infarction (Streptokinase vs
Tenecteplase). Int. J. Pharm. Sci. Rev. Res, 45(2), pp.29-32.
-
30 .The GUSTO, I., (1993). An international randomized trial comparing four thrombolytic strategies for acute myocardial infarction. N Eng J Med, 329(10), pp.673– 682.
-
31 .Thomas, K.N. & Christoph, B., (2015). Thrombolytic Agents And Their Role In Clinical Medicine. BMJ
-
32 .Tumade B, Jim EL, Joseph VF., (2016) Prevalensi sindrom koroner akut di RSUP Prof. Dr. R. D. Kandou Manado periode 1 Januari 2014 – 31 Desember 2014. Jurnal e-Clinic (eCl); 4(1): p. 223-230.
-
33 .Varma, A., Chillawar, S., Kamble, T. & Acharya, S., (2016). Clinical Markers of Reperfusion in Patients with Acute Myocardial Infarction and Its Prognostic Significance. Int J Recent Surg Med Sci 2016;2(2):90-95., 02(02).
-
34 .Vivek, L., (2017). Fibrinolytic Drug
Therapy in the Management of Intravascular Thrombosis, Especially Acute Myocardial Infarction - A Review. J of Pharmacol & Clin Res, 2(4), pp.00105.
-
35 .Werf, V.d., (2012). Recommendations for an efficient and safe use of fibrinolytic agents. The Bangkok Medical Journal, 3, pp.68-78.
67
Discussion and feedback