STUDI REAKSI SIKLOPENTILSILAN DENGAN 4-IODIDA THIOANISOL MENGGUNAKAN KATALIS PALADIUM
on
ISSN 1907-9850
STUDI REAKSI SIKLOPENTILSILAN DENGAN 4-IODIDA THIOANISOL MENGGUNAKAN KATALIS PALADIUM
Aldes Lesbani, Risfidian Mohadi, dan Elfita
Staf Pengajar Jurusan Kimia FMIPA Universitas Sriwijaya Kampus Inderalaya Km.32 Ogan Ilir Sumatera Selatan 30662 e-mail: aldeslesbani@yahoo.com
ABSTRAK
Studi reaksi siklopentilsilan dengan 4-iodida thioanisol telah dilakukan menggunakan katalis paladium dengan kondisi argon pada temperatur ruang menggunakan tetrahidrofuran sebagai pelarut.
Hasil penelitian menunjukkan bahwa produk reaksi adalah tris(4-thioanisil)siklopentilsilan (1) yang merupakan kristal putih hasil rekristalisasi menggunakan metanol dengan persentase 35%. Senyawa (1) mempunyai titik leleh 91,5-92,0 oC. Analisis dengan GC-MS diperoleh nilai m/z sebesar 466 dengan enam puncak proton ekivalen dan delapan puncak karbon hasil pengukuran dengan 1H dan 13C NMR. Hasil analisis tersebut bersesuaian dengan senyawa (1).
Kata kunci: siklopentilsilan, 4-iodida thioanisol, paladium.
ABSTRACT
A study on cyclopentylsilane reaction in tetrahydrofuran with 4-iodo thioanisol has been carried out using palladium as catalyst under argon atmosphere at room temperature.
The results showed that the product was tris(4-thioanisyl)cyclopentylsilane (1) which was obtained from recrystallization using methanol with the yield 35%. The Compound (1) has a melting point of 91.5-92.0 oC. Analysis using GC-MS found m/z 466 with six equivalent protons and eight carbons peak obtained from 1H and 13C NMR.
Keywords: cyclopentylsilane, 4-iodo thioanisol, palladium
PENDAHULUAN
Sintesis senyawa-senyawa baru yang berguna bagi kehidupan manusia terus dikembangkan seperti sintesis obat-obatan, sintesis bahan pangan, sintesis pestisida maupun sintesis material baru dengan sifat khas (Clayden et.al, 2008). Dalam rangka sintesis senyawa-senyawa baru diperlukan suatu metoda sintesis yang efektif. Efektif diartikan seperti rute sintesis yang pendek, waktu reaksi yang singkat dengan persentase produk yang tinggi dan menggunakan reagen yang seminimum mungkin
(Trost et.al, 1982). Salah satu cara untuk memenuhi syarat diatas yakni menggunakan teknik reaksi kopling (Hegedus, 2002). reaksi kopling merupakan reaksi penggabungan rantai-rantai karbon yang dilakukan dengan menggunakan katalis (Tsuji, 2004). Katalis yang digunakan dalam reaksi kopling pada umumnya merupakan logam-logam transisi baik berupa senyawa garam-garam logam transisi blok d, logam blok f maupun senyawa-senyawa kompleks dari logam-logam tersebut (Negishi, 2002).
Salah satu reaksi kopling yang menarik untuk diteliti yakni reaksi antara organologam grup 14 yang meliputi organosilika, organogermanium, organotimah, dan organotimbal dengan aril halida yang merupakan bagian dari senyawa-senyawa grup 17 (Gilman et.al, 1966). Reaksi organo grup 14 dengan aril halida ini kebanyakan ditujukan bagi kepentingan sintesis obat-obatan, pestisida, serta material baru yang dapat digunakan untuk sensor, komponen-komponen elektronik, serta material lapis tipis (Gross et.al, 1997, Kagechika et.al, 2005). Lesbani et.al (2010a) telah melakukan reaksi kopling antara organosilika primer dengan beberapa aril halida yang menghasilkan rendemen yang tinggi. Aplikasi nyata dari senyawa hasil sintesis yang dilakukan Lesbani dkk yakni material baru yang mempunyai sifat photoluminescence biru-violet (Lesbani et.al, 2010b). Disamping itu Lesbani et.al (2012a) telah mengaplikasikan konsep reaksi kopling tersebut untuk sintesis pestisida seperti pestisida flusilazol yang mempunyai atom silika dalam strukturnya.
Pada penelitian ini akan dikaji lebih lanjut variasi aril halida yang digunakan pada reaksi kopling dengan organosilika primer menggunakan katalis paladium. Lesbani et.al (2012b) telah melaporkan variasi aril halida yakni 2-iodida thiopen, 4-iodida-N,N-dimetil anilin dan 5-metil iodo thiophen dimana rendemen yang dihasilkan rendah bila dibandingkan dengan yang dilakukan sebelumnya. Variasi aril halida yang digunakan dalam penelitian ini yakni 4-iodida thioanisol yang memiliki atom sulfur yang terikat pada gugus metil dengan organosilika primer yakni siklopentilsilan. Produk hasil reaksi diidentifikasi melalui penentuan titik leleh, karakterisasi menggunakan kromatografi gas-spektrometri massa, 1H NMR dan 13C NMR..
MATERI DAN METODE
Bahan
Bahan-bahan kimia yang dipergunakan dalam penelitian ini bekualitas analytical grade buatan Merck, TCI, Aldrich dan Kanto Chemical
Industry dan dipergunakan langsung tanpa pemurnian yang meliputi silkopentilsilan, thioanisil, tetrahidrofuran, paladium tersier tributilfosfin, 1,4-diazabisiklo[2,2,2]oktan, aseton, gas argon, pelat KLT silika, metanol, diklorometan, etilasetat, dan akuades.
Peralatan
Alat-alat yang dipergunakan dalam penelitian ini yakni labu Schlenk 50 mL, syringe 5 mL dan 10 mL, statif dan klem, pompa vakum, rotary evaporator, melting point apparatus, spektrometer 1H dan 13C NMR Jeol, kromatografi gas-spektrometer massa Shimadzu 3201 QP. Untuk analisis dengan 1H dan 13C NMR menggunakan pelarut CDCl3 dan diukur pada frekuensi 500 MHz untuk 1H dan 125 MHz untuk 13C.
Cara Kerja
Sebanyak 5 mmol 1,4-diazabyclo[2,2,2]-oktan dan 0,05 mmol paladium tersier tributilfosfin dimasukkan kedalam labu Schlenk ukuran 50 mL dan divakum selama 15 menit. Selanjutnya proses vakum dihentikan dan dimasukkan kedalam labu Schlenk tersebut 1 mmol siklopentilsilan , 3 mmol 4-iodida thioanisol dan 3 mL tetrahidrofuran melalui syringe ukuran 5 mL secara perlahan. Reaksi dilakukan pada suhu ruang tanpa pemanasan selama 3 hari. Reaksi dihentikan dengan cara penambahan 10 mL akuades kedalam caampuran. Kemudian campuran dipindahkan kedalam corong pisah dan dilakukan ekstraksi menggunakan diklorometan sebanyak 15 mL. Proses pemisahan produk dilakukan setelah didapat ekstrak pekat melalui teknik kromatografi menggunakan fasa diam silika dan eluen etil asetat. Proses rekristalisasi dilakukan menggunakan pelarut metanol. Produk reaksi kopling kemudian dikarakterisasi dikarakterisasi melalui penentuan titik leleh, pengukuran dengan GC-MS, 1H dan 13C NMR.
HASIL DAN PEMBAHASAN
Studi reaksi siklopentilsilan dengan 4-iodida thioanisol menggunakan katalis paladium
membentuk senyawa (1) dapat dilihat pada Gambar 1.
H
I
Si H
I
H
+I
SCH3
SCH3
(1)
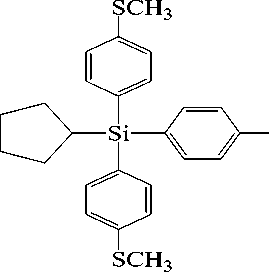
Gambar 1. Reaksi silkopentilsilan dengan 4-iodida thioanisol
Pada Gambar 1 diatas terlihat bahwa tiga mol senyawa 4-iodida thioanisol dibutuhkan untuk membentuk senyawa (1) dengan silkopentilsilan. Reaksi diatas merupakan reaksi tripel arilasi dimana bila tidak menggunakan katalis maka reaksi akan membentuk satu persatu melalui reaksi substitusi 4-iodida thioanisol menjadi senyawa (1) (Solomons et.al, 2008). Dengan menggunakan katalis paladium tahap pertahap tersebut diabaikan karena reaksi silkopentilsilan dengan 4-iodida thioanisol dapat langsung beraksi membentuk senyawa (1).
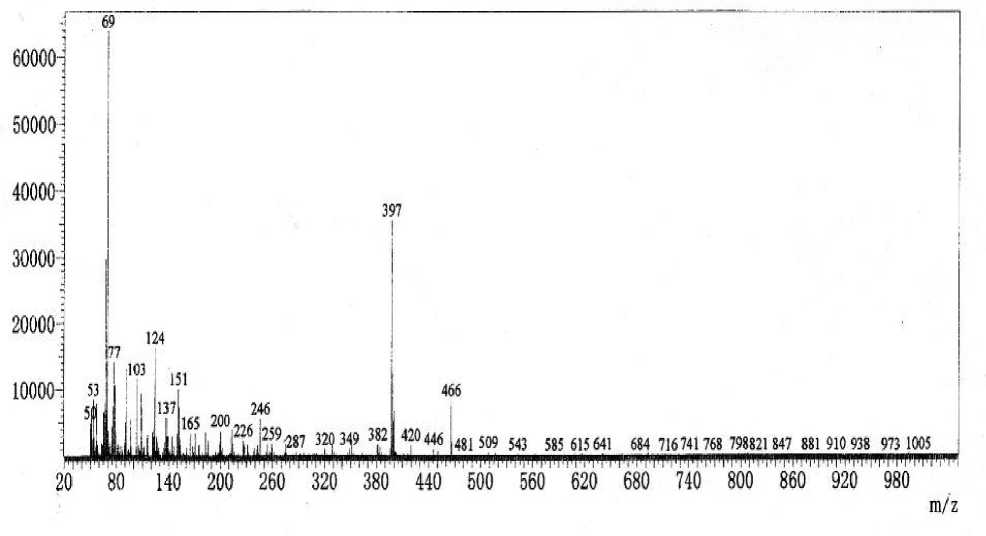
Senyawa (1) hasil reaksi diperoleh berupa kristal putih yang direkristalisasi menggunakan metanol yang kemudian diperoleh senyawa (1) sebanyak 35%. Kristal putih yang diperoleh ditentukan titik lelehnya mennggunakan melting point apparatus dan diperoleh titik leleh senyawa (1) sebesar 91,592,0 oC. Dengan selisih titik leleh yang diperoleh dari hasil pengukuran dapat dipastikan bahwa senyawa (1) memiliki kemurnian yang tinggi yang selanjutnya dianalisis dengan GC-MS. Senyawa (1) dilarutkan dalam aseton untuk diukur dengan GC-MS. Hasil pengukuran GC-MS terhadap senyawa (1) dapat dilihat pada Gambar 2.
Pada Gambar 2 terlihat bahwa senyawa (1) memiliki m/z sebesar 466. Hasil perhitungan bobot molekul senyawa (1) hasil sintesis
diperoleh nilai asebesar 466 g/mol. Hal ini bersesuaian dengan pola GC-MS yang dihasilkan. Bila dilihat pola fragmentasi senyawa (1) seperti yang tersaji pada Gambar 2 terlihat bahwa fragmentasi utama terjadi pada gugus siklopentil (C5H9) dimana terbentuk fragmen dengan m/z sebesar 397 (Clayden et.al, 2008). Selanjutnya dilakukan pengukuran dengan menggunakan 1H dan 13C NMR dengan data yang tersaji pada Gambar 3 dan 4.
Pada Gambar 3 terlihat bahwa terdapat enam puncak proton ekivalen pada senyawa (1) hasil sintesis. Keenam puncak proton tersebut memilik pergeseran kimia (δ) pada 1,50 ppm (m, 6H), 1,81 ppm (m, 1H), 1,98 ppm (m, 2H), 2,48 ppm (s, 9H), 7,21 ppm (d, 6H, J = 8,3 Hz), 7,42 ppm (d, 6H, J = 8,3 Hz). Bila dilihat struktur senyawa (1) hasil sintesis seperti yang tersaji pada Skema 1 teramati bahwa terdapat tigapuluh proton pada senyawa (1) dengan sebaran ekivalen yakni sembilan proton metil pada gugus anisil (a), enam proton pada gugus fenil (b), enam proton pada gugus fenil (c), satu proton pada gugus siklopentil (d), dua proton pada gugus siklopentil (e) dan enam proton pada gugus siklopentil (f), sehingga secara keseluruhan terukur enam puncak proton ekivalen hasil pengukuran dengan 1H NMR. Hal ini menunjukkan bahwa senyawa (1) telah berhasil disintesis dengan kemurnian yang
tinggi. Selanjutnya dilakukan pengukuran dengan menggunakan 13C NMR untuk konfirmasi tambahan terhadap senyawa (1).
165 200 226 ⅛<o
50000:
20000-∙
10000H
382 420 44⅛ ^gj jw ^j 5gj 6∣5641 6g4 7∣6741768 79j82l 847 881 910 938 973 1005
20 80 140 200 260 320 380 440 500 560 620 680 740 800 860 920 980
m/z
60000-;
40000
30000
Gambar 2. Pola fragmentasi massa senyawa (1) hasil pengukuran menggunakan GC-MS
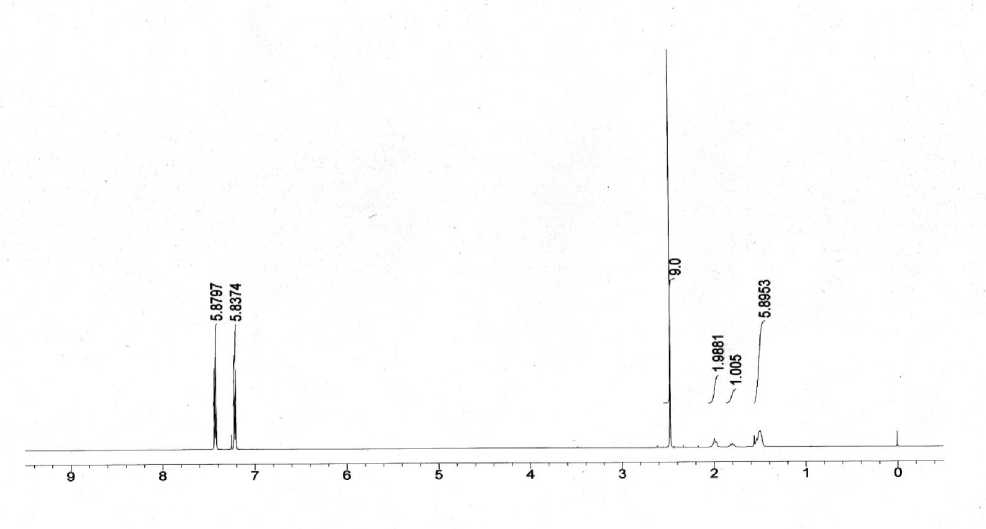
Gambar 3. Spektra 1H NMR senyawa (1).
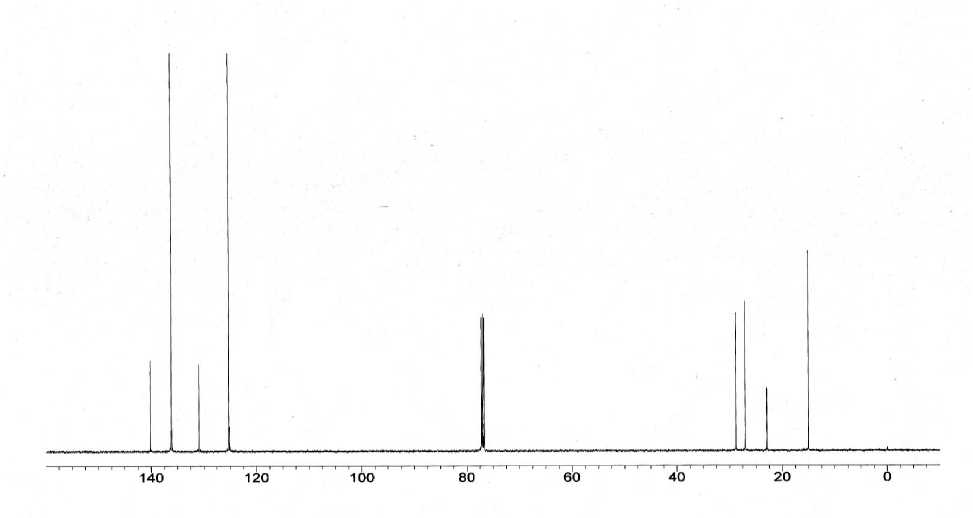
Gambar 4. Spektra 13C NMR senyawa (1).
Spektra 13C NMR senyawa (1) seperti yang tersaji pada Gambar 4 menunjukkan adanya delapan puncak karbon-karbon ekivalen pada senyawa (1) hasil sintesis. Sebaran karbon-karbon ekivalen tersebut tersaji pada Gambar 5.
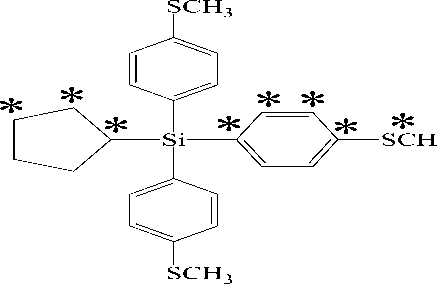
3
Gambar 5. Sebaran karbon-karbon ekivalen dalam senyawa (1). Karbon-
karbon ekivalen dinyatakan
dengan tanda *
Delapan puncak karbon-karbon seperti yang tersaji pada Gambar 5 yakni pada pergeseran kimia ( δ ) 15,0 ppm (CH3), 22,9 ppm (CH2), 27,1 ppm (CH), 28,8 ppm (CH2), 125,2 ppm (CH), 130,9 ppm (Cq), 136,2 ppm (CH), 140,2 ppm (Cq). Secara keseluruhan dari hasil pengukuran diketahui bahwa senyawa (1) dapat disintesis dari siklopentilsilan dengan 4-iodida thioanisol dengan produk yang memiliki kemurnian yang tinggi.
SIMPULAN
Reaksi antara silkopentilsilan dengan 4-iodida thioanisol menggunakan katalis paladium menghasilkan produk tris(4-thioanisil)siklopentilsilan (1) dengan persentase sebesar 35%, titik leleh sebesar 91,5-92,0 oC,
bobot molekul 466, dan mempunyai enam proton ekivalen serta delapan karbon ekivalen didalam strukturnya.
DAFTAR PUSTAKA
Clayden, Greeves, Warren, and Wothers, 2008, Organic Chemistry, Oxford University Press, Oxford, UK
Gilman. H, and Harrell. R. L., 1966, Highly Branched-Chain Methylhalo
Polysilanes, Journal of Organometallic Chemsitry, 5 : 199-200
Gross. T, Kempe. R, and Oehme. H., 1997, 1,2-Di(hypersilyl)-ethylene-The
Unpexpected Result of The Reaction of Tris(trimethylsilyl)Silyllithium With Formic Acid Methyl Ester, Journal of Organometallic Chemistry, 534 : 229231
Hegedus, L. S., 2002. Organometallics in
Synthesis, Wiley, Chichester
Kagechika, H. and Shudo, K., 2005, Synthetic Retinoids: Recent Developments
Concerning Structure and Clinical
Utility, Journal of Medicinal Chemistry, 48 (19) : 5875-5883
Lesbani, A., Kondo, H., Yabusaki, Y., Nakai, M., Yamanoi, Y., and Nishihara, H., 2010a, Integrated Palladium-Catalyzed Arylation of Heavier Group 14
Hydrides, Chemistry A European
Journal, 16 : 13519-13527
Lesbani, A., Kondo, H., Sato, J. I., Yamanoi, Y., and Nishihara, H., 2010b, Facile
Synthesis of Hypersilylated Aromatic Compounds by Palladium-Mediated Arylation Reaction, Chemical
Communications, 46 : 7784-7786
Lesbani, A., Kondo, H., Yamanoi, Y., dan Nishihara, H., 2012a, Sintesis Pestisida Flusilazol. Jurnal Kimia, 6 : 1-7
Lesbani, A. dan Mohadi. R., 2012b, Tripel
Arilasi Organosilika Primer Dengan Beberapa Aril Iodida Menggunakan Katalis Paladium, Chemistry Progress, 5 (2) : 66-69
Negishi, E., 2002, Organopalladium Chemistry, Wiley-Interscience, New York
Solomons, T. W. G. and Fryhle, C. B., 2008, Organic Chemistry 9th Edition. John Wiley & Sons, Inc: USA
Trost, B. M., Verhoeven, T. R., 1982,
Comprehensive Organometallic
Chemistry, Pergamon, Oxford, UK.
Tsuji, J., 2004, Palladium Reagents and
Catalyst, Wiley, Chichester
118
Discussion and feedback