PROFIL BIOAUTOGRAFI DAN UJI PENANGKAP RADIKAL 2,2-DIFENIL-1-PIKRIHIDRAZIL OLEH EKSTRAK ETANOL DAUN BINAHONG (Anredera scandens (L.) Moq.) DAN FRAKSI-FRAKSINYA
on
JURNAL KIMIA (JOURNAL OF CHEMISTRY) 14 (1), JANUARI 2020
DOI: https://doi.org/10.24843/JCHEM.2020.v14.i01.p03
p-ISSN 1907-9850
e-ISSN 2599-2740
PROFIL BIOAUTOGRAFI DAN UJI PENANGKAP RADIKAL 2,2-DIFENIL-1-PIKRIHIDRAZIL OLEH EKSTRAK ETANOL DAUN BINAHONG (Anredera scandens (L.) Moq.) DAN FRAKSI-FRAKSINYA
P. O. Samirana*, D. A. Swastini, A. A. G. R. Y. Putra, I. P. W. Kusuma,
N. P. A. Y. Pratiwi, V. A. Setiawan
Program Studi Farmasi FMIPA Unive rsitas Udayana, Bukit Jimbaran, Bali
*Email: oka_samirana@unud.com
ABSTRAK
Radikal bebas merupakan atom. atau molekul yang mempunyai .satu atau lebih elektron yang tidak berpasangan. dan bersifat sangat reaktif. Antioksidan memiliki kemampuan menginaktifasi berkembangnya reaksi oksidasi berlebihan. Daun binahong (Anredera scandens (L.) Moq.) merupakan salah satu bagian tanaman yang mengandung senyawa flavonoid dan tanin yang secara ilmiah memiliki aktivitas sebagai antioksidan. Penelitian ini bertujuan untuk mengetahui profil bioautografi dan menguji aktivitas antioksidan dari ektrak etanol daun Anredera scandens (L.) Moq. dengan metode penangkap radikal 2,2-difenil-1-pikrilhidrazil. Rendemen yang diperoleh dari proses ekstraksi dalam penelitian ini adalah 19,22%, fraksinasi menghasilkan Rendemen fraksi n-heksan sebesar 11,22% (11,224 gram), fraksi kloroform sebesar 14,68% (14,684 gram), fraksi etil asetat diperoleh rendemen 3,09% (3,094 gram), dan fraksi n-butanol diperoleh rendemen sebesar 23,90% (23,904 gram). Hasil uji profil bioautografi yang menggunakan metode KLT-Densitometri didapat bahwa ekstrak etanol, fraksi kloroform dan fraksi etil asetat memiliki aktivitas penangkap radikal DPPH. Pada penetapan kadar flavonoid total, didapat fraksi etil asetat mengandung kadar flavonoid total yang lebih tinggi dibandingkan dengan fraksi-fraksi lainnya. Pada fraksi etil asetat, didapat kadar flavonoid total yang tinggi dan nilai IC50 yang rendah, sedangkan pada fraksi n-heksan dihasilkan kadar flavonoid yang rendah dan nilai IC50 yang tinggi.
Kata kunci: antioksidan, daun binahong, radikal bebas, flavonoid, IC50.
ABSTRACT
Free radicals are atoms or molecules that have one or more unpaired electrons and are highly reactive. Antioxidants can inhibit the excessive oxidation reaction. The leaves of binahong (Anredera scandens (L.) Moq.) are one part of plants which contain flavonoid compounds and tannins that have scientific activity as antioxidants.This study aims to determine the bioautographic profile and to test the antioxidant activity of the ethanol extract of the leaves of Anredera scandens (L.) Moq. useing 2.2-diphenyl-1-pikrilhidrazil radical capture method. The extraction process produced 19.22% yield, 14.68% (14.684 grams) chloroform fraction, 11.22% (11.224 grams) n-hexane fraction, 3.09% (3.094 grams) ethyl acetate fraction, and 23.90% (23.904 grams) n-butanol fraction. The results of bioautographic profile test using KLT densitometry method proved that ethanol extract, chloroform fraction and ethyl acetate fraction have DPPH radical capture activities. The determination of total flavonoid content found that ethyl acetate fraction contained higher total flavonoids than other fractions. In the ethyl acetate fraction, high total flavonoid level and low IC50 values were obtained, while the n-hexane fraction had low flavonoid level and high IC50 values.
Keywords: antioxidants, binahong leaves, free radicals, flavonoids, IC50.
PENDAHULUAN
Radikal bebas merupakan atom atau molekul yang.mempunyai satu ataupun lebih elektron yang tidak berpasangan dan memiliki sifat sangat reaktif (Fessenden and Fessenden, 1986). Antioksidan memiliki kemampuan
menginaktivasi berkembangnya reaksi substansi dengan cara mencegah terbentuknya radikal atau dengan mengikat radikal bebas dan mendonorkan elektron untuk .menstabilkan radikal bebas (Vaya dan Aviram, 2001; Kumalaningsih, 2006).
Salah satu jenis tanaman yang digunakan dalam pengobatan yaitu daun Binahong
(Anredera scandens (L.) Moq.). Secara empiris binahong digunakan untuk menyembuhkan berbagai gangguan kesehatan dan jenis penyakit seperti mempercepat pemulihan pasca operasi maupun melahirkan, berbagai luka dalam, melancarkan peredaran darah dan tekanan darah, mencegah terjadinya stroke, maag .dan asam urat, menurunkan panas tinggi, dan .diabetes (Manoi, 2009). Penelitian yang dilakukan Samirana dkk, (2016) melaporkan bahwa ekstrak etanol Anredera scandens (L.) Moq. Terbukti menyembuhan luka eksisi yang secara tidak langsung disebabkan oleh adanya antioksidan dari senyawa flavonoid. Senyawa yang diketahui memiliki aktivitas antioksidan pada umumnya adalah senyawa dengan golongan .fenol dan polifenol. Salah satu contohnya adalah flavonoid (Van Acker et al., 1996). Flavonoid berfungsi sebagai antiradikal bebas melalui penekanan radikal bebas atau .Reactive Oxygen Species (ROS), baik .dengan cara menghambat enzim atau pengkelatan ion logam yang berhubungan dengan produksi radikal bebas melalui peredaman radikal .bebas (Subarnas, 2001).
Penelitian yang dilakukan oleh Djamil dkk., (2012) melaporkan aktivitas antioksidan dari ekstrak metanol daun A. cordifolia (Ten.) Steenis merupakan golongan antioksidan kuat dilihat dari nilai IC50 sebesar 53, 11 µg/mL. Namun dalam aplikasinya pada sediaan farmasi, pelarut metanol tidak dipergunakan terkait dengan toksisitasnya. Asam formiat yang terbentuk dari metanol menghambat aktivitas dari oksidase sitokrom yang mengakibatkan degeneratif saraf mata yang mengakibatkan kebutaan dan juga menyebabkan asidosis metabolik hingga kematian. Sehingga digunakan etanol sebagai pelarut sediaan karena lebih aman dibandingkan dengan metanol (Skrzydlewska et al., 1999).
Untuk mengetahui potensi suatu senyawa sebagai antioksidan digunakan metode penangkap radikal DPPH (2,2-difenil-1-pikrihidrazil). Metode DPPH dipilih berdasarkan pada keuntungan yang .dimiliki yaitu murah, cepat, sederhana .serta reagen yang dipergunakan mudah .dipreparasi (Antolovich et al., 2001). Metode penentuan aktivitas antioksidan terbagi menjadi dua yaitu secara kualitatif dan kuantitatif. Dimana secara kualitatif .digunakan profil KLT bioautografi yang merupakan uji kualitatif .senyawa
metabolit .sekunder dengan penyemprotan menggunakan pereaksi pewarna yaitu DPPH (2,2-difenil-1-pikrilhidrazil). Metode kuantitatif yang digunakan adalah metode spektrofotometri dengan pereaksi DPPH.
Tujuan utama dari penelitian .ini adalah untuk mengetahui aktivitas .antioksidan dari ekstrak etanol daun binahong beserta fraksi n-heksan, fraksi kloroform, fraksi etil asetat, dan fraksi n-butanol dengan metode penangkapan radikal DPPH secara kualitatif dan kuantitatif.
MATERI DAN METODE
Bahan
Bahan yang digunakan pada penelitian ini adalah Bahan tanaman yang digunakan adalah daun binahong (Anredera scandens (L.) Moq.) Pelarut yang digunakan untuk ekstraksi daun binahong (Anredera scandens (L.) Moq.) adalah etanol 70% yang berderajat teknis. Bahan yang digunakan untuk uji fitokimia adalah ekstrak etanol daun A. scandens, plat silika gel GF254 (Merck), bahan serbuk DPPH (Sigma), bahan pelarut klorofom P (Merck), metanol P (Merck), n-heksan P (Merck), etil asetat P(Merck), dan n-butanol P (Merck) yang seluruhnya berderajat pro analis. Selain itu, digunakan juga bahan yang berderajat teknis yaitu aquadest. Bahan yang digunakan untuk uji aktivitas antioksidan adalah ekstrak etanol daun A. scandens serbuk DPPH dan vitamin C (Sigma), bahan pelarut metanol (Merck) yang berderajat pro analisis.
Peralatan
Peralatan yang digunakan yaitu toples kaca, blender, mortir, stamper, sudip, cawan porselen, kertas saring, sendok tanduk,.alat gelas, pinset,..timbangan analitik (AND®),.. Rotary evaporator (Eyela®), pipet kapiler, bejana pengembang (CAMAG), lampu UV CAMAG.
Cara Kerja
Penyiapan bahan
Daun Binahong .(Anredera scandens (L.) Moq.) dikumpulkan dan dicuci kemudin disortasi. Daun kemudian dikeringkan dengan cara diangin-anginkan dan dihindarkan dari paparan sinar. matahari secara langsung. Sampel yang telah kering. diserbukkan dengan menggunakan blender. Serbuk yang dihasilkan dibungkus dan disimpan pada tempat kering.
Ekstraksi Daun Binahong.(Anredera Scandens (L.) Moq.)
Serbuk daun binahong.(Anredera scandens (L.) Moq.) kering ditimbang.sebanyak 500 gram, kemudian.dimaserasi.dengan pelarut etanol.70% sebanyak 5 liter.selama ± 24 jam.dengan dilakukan..pengadukan. Maserat kemudian disaring. Residu.dimaserasi.kembali.dengan cara yang. sama dengan 2,5 liter etanol 70% pengulangan sebanyak 2 kali. Filtrat yang dihasilkan.ditampung.menjadi satu diendapkan semalam dan diuapkan.dengan.menggunakan alat vaccum rotary.evaporator dan dioven pada.suhu 40oC, sampai diperoleh ekstrak kental
Fraksinasi ekstrak etanol..daun Anredera scandens (L.).Moq.
Ekstrak etanol.daun A. scandens yang sudah didapat dilarutkan dengan etanol:air (4:1) dan..diaduk hingga semua...ekstrak larut. Selanjutnya campuran..dimasukkan ke..dalam corong pisah..dan dilakukan..fraksinasi dengan pelarut n-heksan,..kloroform, etil asetat,..dan n-butanol. Fraksi yang didapat kemudian diuapkan menggunakan alat..rotary evaporator 68oC, hingga.diperoleh fraksi kering.
Uji Fitokimia Ekstrak.Etanol Daun.Binahong (Anredera scandens (L.) Moq.) dan..Fraksi-Fraksinya
Pemeriksaan steroid dan...triterpenoid dilakukan dengan..reaksi..Liebermann-Burchard. Sebanyak 2 mL..larutan uji diuapkan..dalam cawan penguap. Residu dilarutkan..dengan 0,5 mL kloroform, kemudian..ditambahkan 0,5 mL asam asetat..anhidrat. Selanjutnya..ditambahkan 2 mL asam sulfat..pekat melalui dinding..tabung. Terbentuk cincin kecoklatan..atau violet pada perbatasan...larutan menunjukkan adanya triterpenoid, sedangkan..bila muncul cincin..biru kehijauan menunjukkan..adanya sterol.
Pemeriksaan saponin diawali dengan 10 mL larutan uji..dalam tabung..reaksi dikocok vertical selama 10 detik..dan dibiarkan selama 10 detik. Terbentuknya busa setinggi 1-10 cm yang stabil..selama tidak kurang dari 10 menit, menunjukkan adanya saponin. Dengan penambahan 1 tetes..HCl 2N, busa tidak hilang (Depkes RI, 1989).
Pemeriksaan..tanin dilakukan dengan 1 mL larutan ekstrak uji direaksikan dengan larutan besi (III) klorida 10%, jika terjadi warna..biru tua atau hitam.kehijauan
menunjukkan.adanya.tanin. Pemeriksaan flavonoid..dengan reaksi kimia dengan prosedur. Sebanyak.1 mL larutan ekstrak uji diuapkan..hingga kering, sisanya..dibasahkan dengan..aseton P, ditambahkan0sedikit serbuk halus.asam borat P dan serbuk halus.asam oksalat P,..dipanaskan hati-hati..di atas tangas..air dan dihindari...pemanasan berlebih. Sisa...yang diperoleh..dicampur dengan...10 mL eter P. Diamati dengan..sinar UV 366 nm; larutan berfluoresensi kuning...intensif,
menunjukkan adanya..flavonoid.
Pemeriksaan flavonoid dilakukan..dengan membuat Larutan.uji.dengan cara melarutkan 10 mg..ekstrak dan fraksi-fraksi daun A. scandens (L.) Moq. dalam 5 mL metanol. Larutan..ekstrak uji selanjutnya...ditotolkan sebanyak 6 µL menggunakan pipet.kapiler.pada lempengan KLT silica gel GF254 yang..telah dicuci dan..diaktifkan. Lempengan dielusi.di dalam bejana.pengembang yang telah..dijenuhkan dengan..sistem..pelarut n-butanol:asam
asetat:aquadest (4:1:5) hingga tanda batas. Setelah elusi, lempengan dikeringkan..dalam oven..pada suhu 60oC.selama 5..menit. Bercak yang..diperoleh dideteksi di bawah..sinar UV 366 nm..baik..sebelum maupun sesudah...diuapi ammonia. Dilihat dan diidentifikasi fluoresensi yang terlihat (Markham, 1988).
Uji Aktivitas Antioksidan...Ekstrak Etanol Daun...Binahong (Anredera...scandens (L.) Moq.) dan Fraksi-Fraksinya dengan Spektrofotometri
Kontrol positif...yang digunakan...adalah vitamin..C, dibuat dalam konsentrasi 1..mg/mL dalam..metanol, kemudian diencerkan dengan metanol hingga diperoleh konsentrasi 1; 2; 4; 8; dan 16 µg/mL, Larutan DPPH disiapkan sebagai radikal bebas dalam penelitian ini. Ditimbang 15,8 mg..serbuk DPPH dan dilarutkan dengan metanol dalam labu..ukur 100 mL, ditentukan panjang..gelombang maksimal..DPPH dengan memipet larutan..DPPH 0,4 mM sebanyak 1 mL dan ditambahkan 4 mL..metanol, kemudian campuran..divorteks dan..dibiarkan selama 30 menit.
Campuran diukur absorbansinya
menggunakan spektrofotometer...UV-Vis pada rentang..panjang gelombang 450-550...nm. Diamati nilai panjang...gelombang...maksimal dengan melihat..nilai absorbansi..tertinggi pada satu...titik panjang...gelombang (Samirana Dkk, 2017). Pengukuran aktivitas penangapan radikal...bebas DPPH diawali
dengan.sejumlah.sampel uji.ditambahkan dengan 1 mL DPPH 0,4..mM dan 3,95..metanol. Campuran tersebut...divorteks dan...dibiarkan selama 30..menit. Campuran..lalu..diukur absorbansinya..pada panjang..gelombang 515.nm dengan menggunakan0.blanko metanol. Pengukuran absorbansi..juga dilakukan..terhadap kontrol..yang terdiri dari 1 mL..DPPH..dan 4.mL metanol..(Samirana et al, 2017)
HASIL DAN PEMBAHASAN
Ekstraksi Daun.Binahong (Anredera.scandens (L.) Moq.)
Proses maserasi dilakukan...dengan merendam 1 kg serbuk daun A. scandens...(L.) Moq. dalam 5 Liter pelarut...etanol 70%. Rendemen yang..diperoleh dari..proses ekstraksi dalam..penelitian ini..adalah 19,22% dengan berat..ekstrak yang..diperoleh 192,21 gram..dari 1000 gram.serbuk simplisia..daun A. scandens (L.) Moq. yang..diekstraksi.
Fraksinasi Ektrak Etanol...Daun...Binahong (Anredera.scandens (L.) Moq.)
Rendemen ekstrak diambil sebanyak 100 gram kemudian dilarutkan dengan campuran etanol:air (4:1) hingga terlarut. Larutan tersebut kemudian difraksinasi dengan metode ekstrasi cair-cair menggunakan corong pisah berukuran 250 mL. Proses partisi metode ekstraksi cair-cair berlangsung secara berulang-ulang sebanyak 3 kali.
Pelarut yang digunakan dalam proses fraksinasi terdiri pelarut n-heksan (1:1) dengan volume n-heksan dipergunakan masing-masing sebanyak 100 mL dan air 30 mL. Proses partisi kedua digunakan pelarut kloroform (1:1) digunakan masing-masing 30 mL. Proses partisi ketiga digunakan pelarut etil asetat (1:1) digunakan masing-masing 30 mL. Proses partisi keempat digunakan pelarut n-butanol (1:1) digunakan masing-masing 30 mL. Dilakukan partisi pula digunakan cara yang sama dengan pelarut etil.asetat (1:1) hingga diperoleh..fraksi etil..asetat. Hasil fraksinasi selanjutnya diuapkan pelarutnya didalam oven pada suhu 40oC.
Tabel 1. Hasil Fraksinasi Ekstrak Etanol..Daun
Binahong (Anredera.scandens (L.)
Moq.)
|
Sampel |
Berat (g) |
Rendemen (%) |
|
N-Heksan |
11,224 |
11,22 |
|
Kloroform |
14,684 |
14,68 |
|
Etil Asetat |
3,094 |
3,09 |
|
N-Butanol |
23,904 |
23,90 |
Hasil fraksinasi tersebut menghasilkan beberapa rendemen fraksi terdiri dari fraksi n-heksan sebesar 11,22% (11,224 gram), fraksi kloroform sebesar 14,68% (14,684 gram), fraksi etil asetat diperoleh rendemen 3,09% (3,094 gram), dan fraksi n-butanol diperoleh rendemen sebesar 23,90% (23,904 gram). Fraksi n-butanol merupakan fraksi dengan rendemen terbanyak dikarenakan pelarut n-butanol memiliki tingkat kepolaran semipolar menuju polar sehingga banyak golongan senyawa yang terfraksi ke pelarut ini (Samirana dkk., 2017).
Hasil Uji Fitokimia..Ekstrak Etanol..Daun Binahong (Anredera scandens..(L.) Moq.) Dan Fraksi-Fraksinya
Uji..fitokimia yang dilakukan yaitu pada kandungan..flavonoid,..saponin, triterpenoid..dan tanin. Uji..fitokimia ini dilakukan berdasarkan hasil uji fitokimia pada penelitian Sebelumnya yang menyatakan Bahwa golongan kandungan kimia yang terdapat dalam ekstrak..etanol..daun binahong..(Anredera scandens (L.) Moq.) terdiri dari flavonoid,..saponin, triterpenoid..dan tanin (Samirana, 2010; Karismawan, 2013; Samirana dkk, 2017). Hasil uji fitokimia ekstrak..etanol daun binahong..(Anredera scandens (L.) Moq.) dan..fraksi-fraksinya ditunjukkan pada..tabel 2.
Tabel 2. Hasil Uji Fitokimia.Ekstrak Etanol.Daun Binahong (Anredera scandens (L.) Moq.) dan Fraksi-Fraksinya
..... . Ekstak FiaksiX- Fraksi FraksiEtil FraksiN-jι ιto ιmιa gt3noj He∣tsall Klorofoim A⅞etat Butanol
|
Flavotioid |
- |
- |
+ |
- |
- |
|
Saponin |
- |
- |
- |
- |
+ |
|
Tfiterpenoid |
+ |
- |
+ |
- | |
|
Tanui |
- |
- |
- |
- |
+ |
Ekstrak..etanol daun..binahong (Anredera scandens (L.) Moq.), fraksi kloroform, fraksi..etil asetat dan ..fraksi n-butanol terdapat senyawa golongan flavonoid, saponin, triterpenoid dan tanin. Namun pada fraksi n-heksan tidak ditemukan adanya senyawa golongan flavonoid. Adanya golongan..senyawa yang..terdapat pada ekstrak..dan setiap fraksi dikarenakan tingkat kepolaran dan kelarutannya, senyawa...yang bersifat polar..akan mudah larut..dalam pelarut polar, sedangkan..senyawa non polar..akan mudah larut dalam..pelarut non polar (like dissolves like). Pelarut yang digunakan yaitu etanol yang.bersifat.polar dengan indeks polaritas 5,2..sehingga dapat menarik keempat golongan kandungan kimia tersebut (Snyder, 1997).
Hasil Penetapan Kadar...Flavonoid...Total Ekstrak Etanol...Daun Binahong (Anredera scandens (L.) Moq.) Dan Fraksi-Fraksinya
Kadar flavonoid.total ekstrak.etanol daun A. scandens (L.) Moq. diperoleh sebesar 9,25%b/b ± 0,09 yang dihitung sebagai rutin, dan data perhitungan kadar..flavonoid..total ekstrak dapat dilihat...pada tabel...3. Hasil penetapan kadar flavonoid total menunjukkan bahwa fraksi etil asetat..mengandung kadar..flavonoid total..yang lebih...tinggi dibandingkan..dengan..fraksi-fraksi lainnya.
Tabel 3. Kandungan Flavonoid Total Sampel
Kandungan Flavonoid Total (%b∕b ER)⅜ER rata-
Sampel
|
1 |
2 |
3 | ||
|
Ekstrak Etanol |
9,2 |
9,35 |
9,2 |
9,25 ± 0,09 |
|
Fraksi N-Heksana |
2,3 |
2,02 |
2,58 |
2,3 ± 0,28 |
|
Fraksi Kloroform |
4,41 |
4,27 |
4,7 |
4,46 ± 0,22 |
|
Fraksi N-Butanol |
5,26 |
5,54 |
4,84 |
5,21 ±0,35 |
|
Fraksi Etil Asetat |
10,06 |
10,5 |
10,62 |
10,39 ±0,29 |
Keterangan : % ER = Ekivalen Rutin
Hasil Uji Profil Bioautografi KLT Ekstrak Etanol..Daun..Binahong...(Anredera scandens (L.) Moq.) dan..Fraksi-Fraksinya
Hasil profil bioautografi sebelum disemprot dengan DPPH..0,2% menunjukkan pada..ekstrak etanol, fraksi etil..asetat,..dan fraksi kloroform terdapat bercak yang hampir sama pada Rf 0,73. Bercak-bercak pada Rf 0,73 sebelum diberikan pereaksi penampak bercak menunjukkan warna kuning pudar di bawah sinar tampak, berwarna lembayung gelap di..bawah sinar..UV 254 nm, serta berfluoresensi warna lembayung gelap di..bawah sinar UV..366..nm. Selanjutnya KLT diidentifikasi dengan.disemprot menggunakan larutan.DPPH.0,2%.
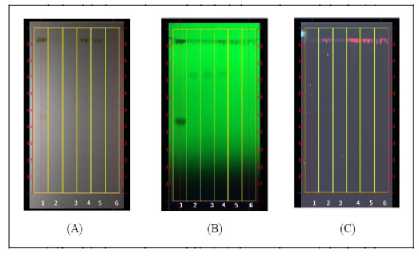
Gambar 1. Hasil Profil KLT Bioautografi Ekstrak Etanol...Daun
Binahong....(Anredera scandens (L.) Moq.) Pada.Sinar.Tampak (A), Sinar.UV 254 nm (B) dan.Sinar UV 366 nm (C) Sebelum Disemprot dengan Larutan.DPPH 0,2%.
Keterangan: 1. Standar Rutin; 2. Ekstrak..Etanol; 3. Fraksi Etil Asetat; 4. Fraksi..Kloroform; 5. Fraksi N-Butanol; 6. Fraksi N-Heksan.
Hasil kromatogram setelah...disemprot dengan..larutan..DPPH 0,2% menunjukkan pada ekstrak etanol,...fraksi etil asetat,...dan fraksi kloroform (Rf 0,73) memiliki warna bercak yang sama yaitu warna kuning dibawah sinar tampak dengan latar berwarna ungu, warna lembayung gelap di bawah..sinar UV 254 nm, dan..di bawah sinar..UV 366...nm berfluoresensi
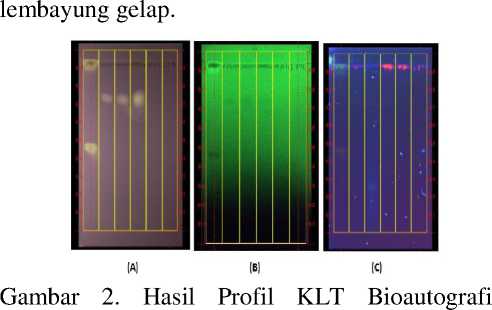
Ekstrak Etanol....Daun
Binahong...(Anredera scandens (L.) Moq.) Pada Sinar.Tampak (A), Sinar UV 254 nm (B) dan Sinar.UV 366 nm (C) Setelah..Disemprot..dengan Larutan DPPH..0,2%.
Keterangan: 1. Standar Rutin; 2. Ekstrak..Etanol; 3. Fraksi Etil Asetat; 4. Fraksi..Kloroform; 5...Fraksi N-Butanol; 6. Fraksi N-Heksan.
Hasil uji profil bioautografi didapat bahwa ekstrak..etanol, fraksi..kloroform dan fraksi..etil asetat memiliki..aktivitas penangkap radikal DPPH yang ditandai..dengan
bercak..berwarna kuning pada latar belakang berwarna..ungu di Rf 0,73 dengan
menggunakan.fase diam.silika gel 60 GF254..dan fase..gerak campuran pelarut etil asetat:.asam.formiat.:.asam.asetat.:.air.(100:11:1 1:26) v/v. Menurut penelitian Andhini (2018), pada metode KLT dengan menggunakan fase.diam silika.gel. GF254 dan.fase gerak menggunakan. campuran pelarut etil.asetat. : asam. formiat. : asam. asetat. : air (100:11:11:26) v/v diperoleh hasil pada nilai Rf 0,71 adalah senyawa flavonoid. Pada. penelitian. ini digunakan fase diam dan fase gerak yang sama yaitu campuran pelarut etil asetat : asam formiat : asam asetat : air (100:11:11:26) v/v menghasilkan bercak dengan nilai Rf 0,73 yang mempunyai aktivitas antioksidan yang diduga merupakan golongan senyawa flavonoid.
Hasil Uji Aktivitas Antioksidan Ekstrak Etanol Daun Binahong (Anredera scandens (L.) Moq.) dan Fraksi-Fraksinya dengan Spektrofotometer
Hasil dari uji penangkap radikal DPPH didapat dari hubungan antara kadar ekstrak etanol beserta fraksi-fraksinya dengan aktivitas penangkap radikal DPPH yang digambarkan pada persamaan regresi linier dengan parameter IC50. Prinsip. dari. metode .uji. aktivitas.antioksidan.ini adalah pengukuran. aktivitas. antioksidan. secara kuantitatif yaitu. dengan pengukuran. penangkapan. radikal DPPH oleh. suatu. Senyawa yang mempunyai. aktivitas. antioksidan. dengan menggunakan. spektrofotometri. UV-Vis. sehingga. dengan. demikian. akan. diketahui. nilai aktivitas. peredaman. radikal. bebas. Yang dinyatakan. dengan. nilai IC50. (Inhibitor Concentration) (Molyneux, 2004).
Nilai. IC50. didefinisikan. sebagai. besarnya. konsentrasi. senyawa. uji. Yang dapat meredam. radikal. bebas sebanyak 50%. Semakin kecil. nilai IC50. maka aktivitas. peredaman radikal. bebas. Semakin. tinggi. Metode. ini juga didasarkan atas pengukuran kemampuan antioksidan untuk menekan atau menghambat radikal DPPH. Kemampuan ini dapat dievaluasi dengan resonansi spin elektron atau dengan mengukur penurunan absorbansinya yang diamati dengan spektrofotometer pada panjang. gelombang…sekitar 515 nm setelah direaksikan dengan senyawa. uji (Prior et al., 2005) Prinsip. kerja. Dari pengukuran. ini. adalah. adanya. radikal. bebas stabil yaitu DPPH yang dicampurkan. dengan senyawa antioksidan. yang
memiliki kemampuan. mendonorkan. hydrogen, sehingga. radikal. bebas. dapat. Diredam (Ridho, 2013).
Tabel 4. Hubungan. antara Konsentrasi. Ekstrak
Etanol…..70% dengan……Aktivitas penangkapan radikal. bebas DPPH
|
Koiiientrasi Sampel (μg⅛L) |
Akfcitas Antioksidan (%) |
Persamaan Garis Regiesi Linier |
|
5 |
20.12 | |
|
10 |
25,63 |
y=0,3089x + 22.107 |
|
20 |
30.78 |
r =0.9938 |
|
40 |
35.81 |
ICso = 90.3 LigniL |
|
80 |
46.47 | |
|
160 |
71.14 |
Pada tabel 4, didapat persamaan regresi linier y = 0,3089x + 22,107 dan memiliki aktivitas. penangkap. radikal DPPH dengan. nilai IC50 sebesar. 90,3 µg/mL. Hasil IC50 ekstrak etanol tersebut dikategorikan sebagai antioksidan kuat dengan nilai IC50 yang terdapat pada rentang 50-100 µg/mL (Putri dan Nurul, 2015).
Tabel 5. Hubungan antara Konsentrasi Fraksi N-Heksan dengan Aktivitas penangkapan radikal bebas DPPH
|
Konsentrasi Sampel (μg⅛nL) |
Aktivitas Antioksidan (%) |
Persamaan Garis Regresi Lmier |
|
5 |
10,66 | |
|
10 |
13.17 |
y= 0.1634x + 11.201 |
|
20 |
14.85 |
r = 0.9963 |
|
40 |
17.96 |
ICso = 237,45 IlgillL |
|
80 |
25.27 | |
|
160 |
36.77 |
Pada tabel 5, didapat persamaan regresi linier y = 0,1634x + 11,201 dan memiliki aktivitas. penangkap. radikal. DPPH dengan nilai IC50 sebesar. 237,45 µg/mL. Hasil IC50. fraksi n-heksan tersebut dikategorikan sebagai antioksidan sedang dengan nilai IC50 yang terdapat pada rentang 100-250 µg/mL (Putri dan Nurul, 2015).
Tabel 6. Hubungan antara Konsentrasi Fraksi Kloroform dengan Aktivitas Penangkap Radikal Bebas DPP
|
Konsentrasi Sampel (μg∕mL) |
Aktivitas Antioksidan (%) |
Persamaan Garis Regresi Linier |
|
5 |
10,9 | |
|
10 |
16,77 |
v= 0,2616x + 16,724 |
|
20 |
26,11 |
r =0,9513 |
|
40 |
32,1 |
ICso= 127.2 μg⅛L |
|
80 |
41.68 | |
|
160 |
55,21 |
Pada tabel 6, didapat persamaan regresi linier y = 0,2616x + 16,724 dan memilik aktivitas. penangkap. radikal. DPPH dengan. nilai IC50. Sebesar. 127,2 µg/mL. Hasil IC50 fraksi kloroform tersebut dikategorikan sebagai antioksidan sedang dengan nilai IC50 yang terdapat pada rentang 100-250 µg/mL (Putri dan Nurul, 2015).
Tabel 7. Hubungan antara Konsentrasi Fraksi N-Butanol dengan Aktivitas Penangkap Radikal Bebas DPPH
|
Konsentrasi Sampel (μg∕mL) |
Aktivitas Antioksidan (%) |
Persamaan Garis Regresi Linier |
|
5 |
13,29 | |
|
10 |
19,16 |
y= 0.2287x+ 17.017 |
|
20 |
23,95 |
r =0,9779 |
|
40 |
28.5 |
ICso = 144,22 μg∕mL |
|
80 |
37,37 | |
|
160 |
51,86 |
Pada tabel 7, didapat persamaan regresi linier y = 0,2287x + 17,017 dan memiliki aktivitas penangkap. radikal. DPPH dengan nilai IC50 sebesar. 144,22 µg/mL.. Hasil IC50 fraksi n-butanol tersebut dikategorikan sebagai antioksi dan sedang dengan nilai IC50 yang terdapat pada rentang 100-250 µg/mL (Putri dan Nurul, 2015).
Tabel 8. Hubungan antara Konsentrasi Fraksi Etil Asetat dengan Aktivitas Penangkap Radikal Bebas DPPH
Konsentrasi Aktivitas Persamaan Garis Regresi Sampel I μg ml.) Antioksidan (%) Linier
|
5 |
22.4 | |
|
10 |
30.3 |
y= 0.9917x + 27.038 |
|
20 |
36.17 |
r =0.9809 |
|
40 |
42.99 |
IC5O = 69.23 μg mL |
|
80 |
57.49 | |
|
160 |
77.37 | |
Pada tabel 8, didapat persamaan regresi linier y = 0,9917x + 27,038 dan memiliki aktivitas penangkap radikal DPPH dengan. nilai .IC50 sebesar. 69,23 µg/mL.. Hasil IC50 fraksi. Etil. Asetat. tersebut dikategorikan sebagai antioksidan kuat dengan nilai IC50 yang terdapat pada rentang 50-100 µg/mL (Putri dan Nurul, 2015).
Pada penelitian ini digunakan vitamin C sebagai senyawa pembanding yang sebelumnya telah diketahui sebagai antioksidan alami. Hubungan antara kadar vitamin C dengan aktivitas penangkapan radikal bebas DPPH digambarkan dalam persamaan regresi linier y = 5,008x + 11,297 dengan nilai. IC50. sebesar. 7,73 µg/mL.
Tabel 9. Hubungan. antara. Konsentrasi.Vitamin C dengan. Aktivitas. Penangkap. Radikal. Bebas. DPPH
|
Kimseniiasi Snιι∣]∣el (μg⅛nl.) |
Akiivitas ATilioksidan ∣⅛) |
Persaniaan Gaiis Regiesi I .inicι |
|
l |
16.53 | |
|
19.28 |
y= 5.008x+ 11.297 | |
|
■1 |
30.30 |
r = 0,9959 |
|
E |
56.05 |
ICw 7.73μg∙nιL |
|
16 |
89.53 |
Hasil penelitian..tersebut menunjukkan bahwa aktivitas. penangkap. radikal. DPPH ekstrak. etanol. daun. Binahong dan fraksi-fraksinya lebih rendah dibandingkan. dengan senyawa pembanding vitamin C. Namun, jika dilihat.. nilai. IC50. dari ekstrak. etanol. dan. fraksi etil. asetat. daun. binahong. (Anredera.scandens. (L.) Moq.), didapat kekuatan aktivitas. antioksidannya digolongkan ke antioksidan kuat.
Pada pengujian skrining.fitokimia,.didapat bahwa…ekstrak…etanol,…dan fraksi-fraksinya memiliki hasil positif pada setiap golongan senyawa yang diuji, kecuali..pada..fraksi.n-heksan yang memiliki hasil negatif pada golongan senyawa.flavonoid.
Penetapan kadar flavonoid total, didapat fraksi..etil..asetat…mengandung..kadar..flavonoi d total..yang..lebih tinggi…dibandingkan dengan fraksi-fraksi lainnya. Hasil uji profil bioautografi didapat bahwa.ekstrak.etanol, fraksi…kloroform dan….fraksi....etil..…asetat…memiliki…aktivita s penangkap radikal DPPH yang ditandai..dengan bercak..berwarna..kuning pada latar…belakang berwarna..ungu..di Rf 0,73
dengan..menggunakan fase..diam..lempeng KLT silika..gel.60 GF254 dan..fase.gerak..campuran pelarut etil..asetat.: asam..formiat..:
asam..asetat..: air.. (100:11:11:26) v/v. Hasil profil bioautografi yang didapat memiliki kemiripan pada penelitian yang dilakukan oleh Andhini (2018) bahwa metode KLT yang menggunakan fase diam lempeng KLT silika gel 60 GF254 dan fase gerak campuran pelarut etil asetat : asam formiat : asam asetat : air (100:11:11:26) v/v menghasilkan bercak yang diduga mengandung flavonoid berada di Rf 0,71. Sehingga, dapat dikatakan bahwa yang bertanggungjawab terhadap aktivitas antioksidan adalah senyawa flavonoid. Hubungan…antara senyawa..flavonoid..dengan..aktivitas.antioksidan ditampilkan pada..Gambar..3.
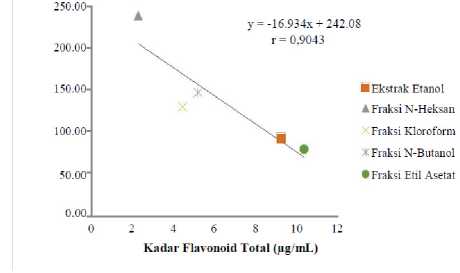
Gambar..3. Kurva..Hubungan..Antara Kandungan Flavonoid Total dan Nilai lC50
Hubungan…antara...kandungan...flavonoid total. dengan. nilai IC50 ekstrak etanol dan fraksi-fraksinya digambarkan dengan persamaan regresi y = -16,934x + 242,08 dan memiliki koefisien korelasi (r) sebesar 0,9043, yang memiliki makna bahwa kandungan flavonoid total dengan nilai IC50 ekstrak etanol dan..fraksi-fraksinya memiliki hubungan yang..sangat..kuat. Semakin besar kandungan flavonoid total dari ekstrak etanol..daun..A. scandens beserta..fraksi-fraksinya, maka nilai IC50 nya akan semakin kecil. Pada fraksi..etil..asetat, didapat
kadar...flavonoid total..yang..tinggi..dan..nilai
IC50 yang rendah, sedangkan pada fraksi n-heksan dihasilkan kadar flavonoid yang rendah dan nilai IC50 yang tinggi.
SIMPULAN DAN SARAN
Simpulan
Profil bioautografi ekstrak etanol daun A. scandens yang berperan sebagai..penangkap radikal…2,2-difenil-1-pikrilhidrazil..adalah pada Rf 0,73 di ekstrak..etanol,..fraksi..kloroform,..dan fraksi..etil..asetat..daun Anredera scandens setelah disemprot…dengan DPPH 0,2%..menunjukkan aktivitas...antioksidan…yang…ditandai…dengan adanya bercak. berwarna kuning dengan..latar.. belakang..ungu..
Saran
Diperlukan penelitian lebih lanjut untuk mengetahui mekanisme antioksidan dari..ekstrak daun..binahong..(Anredera.scandens (L.) Moq.).
UCAPAN TERIMAKASIH
Ucapan..terimakasih penulis…sampaikan kepada..semua..pihak..yang..telah..membantu.dan mendukung..dalam..terlaksananya..penelitian..ini.
DAFTAR PUSTAKA
Antolovich, M., Paul D. P., Emilioa P., Suzanne M. and Kevin R. 2001. Methods for Testing Antioxidant Activity. The Analyst. Vol. 127: 183-198
Departemen Kesehatan Republik Indonesia.
1989. Materia Medika Indonesia Jilid V. Direktorat Pengawasan Obat dan Makanan. Jakarta
Djamil, R., Wahyudi. P.S., Wahono,S. dan Hanafi. 2012. Antioxidant Activity of Flavonoid From Anredera Cordifolia (Ten) steenis Leaves, Journal of Pharmacy.
Fessenden, R. J. dan Fessenden, J. S. 1986. Kimia Organik. Edisi Ketiga. Jakarta: Erlangga
Karismawan, P. N. 2013. Profil Kandungan Kimia dan Uji Aktivitas Antiluka Bakar Ekstrak Etanol Daun Binahong (Anredera Scandens (L.) Moq.) Pada Tikus Jantan Galur Sprague Dawley (Skripsi),. Universitas Udayana. Denpasar
Kumalaningsih, S. 2006. Antioksidan Alami Penangkal Radikal Bebas, Sumber manfaat, Cara penyediaan, dan Pengolahan. Trubus Agrisana.
Surabaya
Manoi, F. 2009. Binahong sebagai Obat. Warta Penelitian dan Pengembangan Tanaman Industri. Vol. 15(1): 3-4.
Markham, K. R. 1988. Cara Mengidentifikasi Flavonoid. Bandung: Penerbit ITB.
Molyneux, P. 2004. The Use of The Stable Free Radical Diphenylpicrylhidrazil (DPPH) for Estimating Antioxidant Activity.J. Sci. Technol. Vol. 26(2): 211-219.
Prabantini, D. 2010. A to Z Makanan Pendamping Asi. Edisi I. Yogyakarta: ANDI.
Prior, R. L, Wu, X., Schaich, K. 2005. Standardized Methods for the Determination of Antioxidant Capacity and Phenolics in Foods and Dietary Supplements. Journal of Agric. And Food Chemistry. Vol. 53(10): 4290-4302.
Putri, A. A. S. dan Nurul H. 2015. Uji Aktivitas Antioksidan Senyawa Fenolik Ekstrak Metanol Kulit Batang Tumbuhan Nyiri Batu (Xylocarpus moluccensis). UNESA Journal of Chemistry. Vol. 4(1): 1-6.
Ridho, E.A. 2013. Uji Aktivitas Antioksida Ekstrak Metanol Buah Bakum (Cayratia trifolia) dengan Metode DPPH. Skripsi. Universitas
Tanjungpura. Pontianak
Samirana, P. O., D. A. Swastini, I. D. G. P. Y. Subartha, dan Ariadi, K. A. 2016. Uji Aktivitas Penyembuhan Luka Ekstrak Etanol Daun Binahong (Anredera scadens (L.) Moq.) pada Tikus Jantan Galur Wistar. Jurnal Farmasi Udayana. 5(2): 19-23.
Samirana, P. O., D. A. Swastini., I. P. R. Ardinanta., I. P. S. D. Suarka. 2017. Penentuan Profil Kandungan Kimia Ekstrak Etanol Daun Binahong (Anredera Scandens (L.) Moq.). Jurnal Farmasi Udayana. 6(1): 24-26.
Samirana, P. O., Swastini., D. A., Satriani, N. W. 2017. Pengaruh Pemberian Ekstrak Etanol 70% Daun Binahong (Anredera Scandens (L.) Moq.) Terhadap Makroskopik Dan Biokimia Ginjal Mencit Jantan Galur Balb/C. Jurnal Farmasi Udayana. 6(2): 29-30.
Samirana, P. O., Taradipta, I. D. M. R., Leliqia, N. P. E. 2016. Penentuan Profil Bioautografi Dan Aktivitas Antioksidan Ekstrak Etanol Daun Bidara (Ziziphus Mauritiana Auct. Non Lamk.) Dengan Metode Penangkapan Radikal Dpph. Jurnal Farmasi Udayana. 6(2): 19-20.
Samirana, P.O., Susidarti, R.A., and Rohman, A. 2017. Isolation and 2,2’-diphenyl-1-picrylhydrazyl radicalscavenging activity of active compound from Jujube tree (Zizyphus mauritiana Auct. non Lamk.). International Journal Of Food Properties. Vol. 20(S2): 1524-1525.
Skrzydlewska, E., Roszkowska A., and Moniuszko-Jakoiuk J. 1999. A Comparison of Methanol and Ethanol Effects on the Activity and Distribution of Lysososmal Proteases. Polish Journal of Environmental Studies. Vol. 8(4): 251257.
Snyder C. R., Kirkland, J. J. and Glajach J. L. 1997. Practical HPLC Method Development. 2th ed. Lnc. 722-723
Subarnas A. 2001. Komponen Aktif Antioksidan Dalam Bahan Alam, Seminar Nasional dan Lokakarya. Pemahaman Konsep Radikal Bebas dan Peranan Antioksidan dalam Meningkatkan Kesehatan Menuju Indonesia Sehat 2010. Pusat Penelitian Kesehatan. Lembaga Penelitian Universitas Padjajaran. Bandung.
Van Acker, S.A., van Den Berg, D.J., Tromp, M.N., Griffioen, D.H.,Van Bennekom, W.P., van der Vijgh, W.J. and Bast A. 1996. Structural aspects of antioxidant activity of flavanoids. Free Radic. Biol. Med. 20(3): 331342.
Vaya, J., dan Aviram, M. 2001. Nutritional Antioxidants: Mechanisms of Action, Analyses of Activities and Medical Applications. Curr. Med. Chem.-Imm, Endoc. and Metab. Agents, 1(1).
18
Discussion and feedback