STUDI PEROMBAKAN ZAT WARNA TEKSTIL REMAZOL RED RB SECARA AEROB MENGGUNAKAN BAKTERI ENTEROBACTER AEROGENES YANG DIISOLASI DARI LUMPUR LIMBAH TEKSTIL
on
ISSN 1907-9850
STUDI PEROMBAKAN ZAT WARNA TEKSTIL REMAZOL RED RB SECARA AEROB MENGGUNAKAN BAKTERI ENTEROBACTER AEROGENES YANG DIISOLASI DARI LUMPUR LIMBAH TEKSTIL
I Dewa Ketut Sastrawidana
Jurusan Pendidikan Kimia FMIPA Universitas Pendidikan Ganesha, Singaraja
ABSTRAK
Tujuan penelitian ini adalah mengkaji potensi bakteri Enterobacter aerogenes yang diisolasi dari lumpur limbah tekstil untuk merombak zat warna azo remazol red RB. Proses perombakan dilakukan dalam reaktor aerob dengan variabel yang teliti yaitu efisiensi perombakan remazol red RB pada variasi pH, konsentrasi zat warna dan lama waktu inkubasi. Hasil penelitian menunjukkan perombakan zat warna azo remazol red RB dengan konsentrasi 75 mg/L berlangsung optimum pada pH 7-8, lama waktu inkubasi 7 hari dengan efisiensi perombakan sebesar 87,9%. Dengan demikian, bakteri Enterobacter aerogenes ini potensial dikembangkan untuk pengolahan limbah tekstil secara aerob pada skala lapang.
Kata Kunci : Enterobacter aerogenes, remazol red RB, lumpur air limbah tekstil
ABSTRACT
The objective of this research is to study the potential use microorganism which is identified as Enterobacter aerogenes isolated from sludge of textile wastewater treatment plant. Reactor was operated to treat remazol red RB azo dyes under aerobic condition. The performance of the bioreactor was evaluated by monitoring color removal within various pH of the medium, dye concentrations and incubation times. The degradation products were characterized by UV–vis techniques. The result showed, Enterobacter aerogenes bacteria was able to successfully decolourize 75 mg/L of remazol red RB azo dyes under aerobic condition, at pH 7-8 and for seven days incubation with biodegradation efficiency of up to 87,9%.
Keywords : Enterobacter aerogenes, remazol red RB, sludge textile wastewater
PENDAHULUAN
Pada proses pewarnaan tekstil lebih banyak menggunakan zat warna sintetik dibandingkan dengan zat warna alam karena zat warna sintetik dapat memenuhi kebutuhan skala besar, warnanya lebih bervariasi dan pemakaiannya lebih praktis (Montano, 2007). Sekitar 70% dari zat warna sintetik yang digunakan adalah zat warna golongan azo yaitu zat warna sintetik yang mengandung paling sedikit satu ikatan ganda N=N. Keunggulan zat warna azo ini adalah terikat kuat pada kain,
memberikan warna yang baik dan tidak mudah luntur (Blackburn & Burkinshaw, 2002).
Remazol red RB merupakan salah satu zat warna sintetik monoazo, karena memiliki satu ikatan ganda N=N. Zat warna remazol red RB ini digunakan sebagai pewarna merah pada industri pencelupan tekstil atau biasanya dicampur dengan zat warna lain untuk menghasilkan warna yang baru. Zat warna azo ini tidak mudah rusak oleh perlakuan kimia maupun fotolitik. Dengan demikian, bila air limbah tekstil yang mengandung zat warna azo terbuang ke lingkungan, maka dapat bertahan lama dan mengalami akumulasi sampai pada
tingkat konsentrasi tertentu dapat menimbulkan dampak negatif terhadap daya dukung lingkungan. Disamping sifatnya cukup toksik, keberadaan zat warna azo dalam perairan dapat menghambat penetrasi sinar matahari ke dalam air sehingga mengganggu aktivitas fotosintesis mikroalga. Dampak lanjutannya adalah pasokan oksigen dalam air menjadi berkurang dan akhirnya memicu aktivitas mikroorganisme anoksik-anaerob yang menghasilkan produk berbau tak sedap (Montano, 2007).
Dalam rangka pengendalian pencemaran lingkungan oleh limbah industri, Pemerintah Republik Indonesia melalui KepMen LH No. 51/MENLH/10/1995 tentang baku mutu limbah industri cair bagi kegiatan industri dan PP No.82 tahun 2001 tentang pengelolaan kualitas air dan pengendalian pencemaran air mewajibkan pelaku industri yang menghasilkan limbah dalam jumlah besar dan berpotensi mencemari lingkungan harus dilengkapi dengan instalasi pengolahan air limbah yang memadai. Selama ini, penanganan air limbah tekstil lebih menekankan pada cara kimia seperti dengan advanced oxidation process dan kuagulasi serta cara fisika seperti iradiasi dengan sinar UV dan adsorpsi menggunakan arang aktif. Perombakan dengan cara kimia dan fisika tersebut belum bisa sepenuhnya diaplikasikan pada skala lapang kerena memerlukan biaya relatif tinggi dan pemakaian bahan-bahan kimia yang banyak serta menimbulkan sludge yang banyak.
Penanganan air limbah tekstil menggunakan bakteri saat ini terus dikembangkan karena diyakini sebagai langkah strategis yang efektif, murah dan ramah lingkungan (Yoo, 2000). Hal ini disebabkan beberapa bakteri yang hidup di alam mampu menggunakan zat warna tekstil sebagai sumber karbon dan energi untuk pertumbuhannya. Menurut Yoo (2000), perombakan zat warna tekstil golongan azo menggunakan bakteri pada dasarnya merupakan reaksi reduksi-oksidasi yang dikatalisis oleh enzim azo reductase. Beberapa jenis bakteri yang digunakan untuk merombak limbah tekstil pada kondisi anaerob diantaranya Sphingomonas sp. BN6 (Russ et al. 2000), Rhizobium Radiobacter MTCC 8161 (Telke et al. 2008). Bakteri umumnya memerlukan glukosa sebagai kosubstrat untuk
mempercepat proses perombakan. Glukosa dalam sistem biologi mengalami proses glikolisis dengan bantuan enzim dehidrogenase menghasilkan nikotinamida adenin dinukleotida (NADH) yang bertindak sebagai pembawa elektron dan berperan penting dalam proses perombakan zat warna azo. Disamping bakteri anaerob, beberapa bakteri aerob seperti Bacillus cereus, Bacillus subtilis, Staphylococcus aureus dan Escherichia coli (Ajibola et al. 2005; Mona and Yusef 2008), Enterobacter agglomerans (Moutaouakkil et al. 2003), Pseudomonas sp., Bacillus sp., Halomonas sp., dan Micrococcus sp. (Padmavathy et al. 2003) yang adapted dengan lingkungan limbah juga dilaporkan mampu merombak zat warna azo dengan bantuan enzim spesifik yaitu aerobic azoreductase. Berdasarkan hasil kajian-kajian terhadap perombakan zat warna azo tersebut dinyatakan zat warna azo lebih sulit mengalami perombakan pada kondisi aerob dibandingkan dengan kondisi anaerob. Namun, titik lemah perombakan anaerob adalah terjadinya biotransformasi zat warna azo menjadi senyawa yang lebih sederhana yaitu amina aromatik yang bersifat lebih toksik dari zat warna azo awalnya.
Berdasarkan permasalahan di atas, penelitian ini ditujukan untuk menelusuri potensi bakteri lokal aerob yaitu bakteri Enterobacter aerogenes hasil isolasi dari lumpur limbah tekstil digunakan dan dikembangkan untuk merombak limbah tekstil. Sebagai tahap awal, dilakukan analisis kemampuannya untuk merombak salah satu zat warna tekstil golongan azo yaitu remazol red RB di berbagai kondisi lingkungan seperti pH, konsentrasi zat warna dan lama waktu kontak antara zat warna dengan bakteri.
MATERI DAN METODE
Bahan
Bahan-bahan yang digunakan meliputi zat warna remazol red RB, lumpur limbah tekstil, garam fisiologis (NaCl 0,85%), agar invitro, buffer fosfat (pH 6-11), NaOH, HCl dan (NH4)2SO4, KH2PO4, Na2HPO4, MgSO4.7H2O, Fe(NH4)sitrat, CaCl2.2H2O, yeast extract, ZnSO4.7H2O, MnCl2.4H2O, CoCl2.6H2O,
NiCl2.6H2O, Na2MoO4.2H2O, H3BO3,
CuCl2.2H2O, dan glukosa.
Peralatan
Alat-alat yang digunakan dalam penelitian ini adalah autoclave, shaker model 350-1, sentrifuge rotofix 32, pH-meter, dan UV-vis Shimadzu 1700. dan alat-alat gelas lainnya.
Cara Kerja
Efisiensi perombakan remazol red RB menggunakan bakteri enterobacter aerogenes di berbagai kondisi lingkungan
Efisiensi perombakan zat warna azo oleh bakteri sangat ditentukan oleh kondisi lingkungan. Faktor-faktor lingkungan yang dikaji meliputi pengaruh pH, konsentrasi zat warna dan lama waktu inkubasi. Semua peralatan dan media cair yang digunakan pada perlakuan ini disterilisasi dengan cara mengautoklaf pada suhu 120oC selama 15 menit.
Perombakan pada variasi pH
Sebanyak 1 mL suspensi bakteri dimasukkan ke dalam Erlenmeyer ukuran 100 mL yang telah berisi 48 mL media cair dan 1 mL zat warna remazol red RB 2500 mg/L(konsentrasi akhir remazol red RB adalah 50 mg/L). Campuran diatur pada pH 6 dengan cara menambahkan larutan HCl dan
ditambahkan buffer fosfat pH 6. Campuran dalam Erlenmeyer tersebut ditutup rapat, selanjutnya diinkubasi pada suhu ruangan selama 5 hari sambil di gojog menggunakan shaker. Setelah 5 hari, cairan diambil untuk disentrifugasi pada 4000 rpm selama 30 menit. Supernatan disaring dengan kertas Whatman kemudian diukur absorbansinya menggunakan spektrofotometer UV-Vis pada panjang gelombang 520 nm. Dengan cara yang sama dilakukan perombakan pada perlakuan variasi pH 7, 8, 9, 10 dan 11. Untuk setiap perlakuan dilakukan pengulangan sebanyak tiga kali. Kontrol dibuat dengan cara yang sama, tanpa ditambahkan suspensi bakteri.
Perombakan pada variasi konsentrasi zat warna
Sebanyak 1 mL suspensi bakteri dimasukkan ke dalam Erlenmeyer ukuran 100
mL yang telah berisi media cair dan konsentrasi zat warna remazol red RB 25 mg/L. Campuran tersebut diatur pada pH optimum yang diperoleh dari perlakuan perombakan pada variasi pH. Selanjutnya diinkubasi pada suhu ruangan selama 5 hari sambil di gojog menggunakan shaker. Setelah 5 hari, cairan diambil untuk disentrifugasi pada 4000 rpm selama 30 menit. Supernatan disaring dengan kertas Whatman kemudian diukur absorbansinya menggunakan spektrofotometer UV-Vis pada panjang gelombang 520 nm. Dengan prosedur yang sama dilakukan perombakan zat warna remazol red RB pada perlakuan konsentrasi 50, 75, dan 100 mg/L. Untuk setiap perlakuan diulang sebanyak tiga kali. Kontrol dibuat dengan cara yang sama, tanpa adanya penambahan suspensi bakteri.
Perombakan pada variasi lama waktu inkubasi
Sebanyak 1 mL suspensi bakteri dimasukkan ke dalam Erlenmeyer ukuran 100 mL yang telah berisi media cair dan zat warna remazol red RB dengan konsentrasi optimum yang diperoleh dari perlakuan perombakan pada variasi konsentrasi zat warna. Campuran tersebut diatur pada pH optimum, selanjutnya diinkubasi pada suhu ruangan selama 1 hari sambil di gojog menggunakan shaker. Setelah 1 hari, cairan disentrifugasi pada 4000 rpm selama 30 menit. Supernatan disaring dengan kertas Whatman kemudian diukur absorbansinya menggunakan spektrofotometer UV-Vis pada panjang gelombang 520 nm. Selanjutnya dilakukan perlakuan perombakan pada variasi lama waktu inkubasi 2, 3, 4, 5, 6, 7, 8, 9, dan 10 hari. Kontrol dibuat dengan cara yang sama tampa penambahan bakteri dan setiap perlakuan dilakukan pengulangan sebanyak tiga kali.
HASIL DAN PEMBAHASAN
Faktor lingkungan yang mempengaruhi aktivitas perombakan bakteri Enterobacter aerogenes dalam merombak zat warna remazol red RB yang dikaji dalam penelitian ini meliputi pH, konsentrasi zat warna, dan lama waktu inkubasi. Hasil perombakan 50 mg/L remazol red RB diberbagai kondisi pH selama 5 hari inkubasi disajikan pada Gambar 1.
Gambar 1 menunjukkan efisiensi perombakan meningkat dengan naiknya pH lingkungan dari 5 sampai 6 kemudian cendrung stabil pada pH 7-8 dan kecendrungan mengalami penurunan dari pH 9 sampai 11. Kondisi pH
optimum untuk berlangsungnya proses perombakan 50 mg/L zat warna remazol red RB selama 5 hari inkubasi pada kisaran pH 7-8 dengan efisiensi perombakan berkisar 78,82 sampai 80,12%.
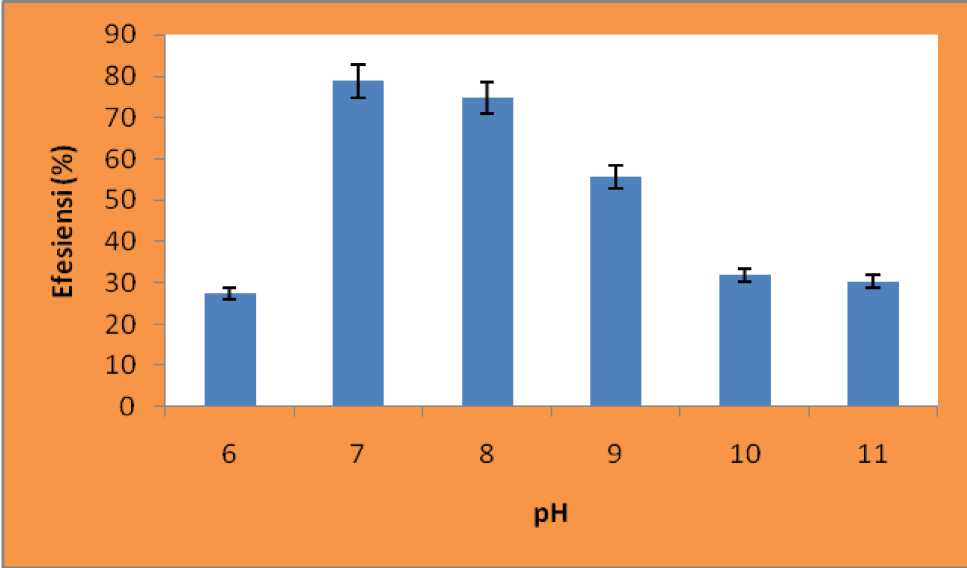
Gambar 1. EfIsiensi perombakan zat warna remazol red RB pada kondisi aerob selama 5 hari inkubasi pada berbagai pH.
Perbedaan efisiensi perombakan pada variasi kondisi pH disebabkan oleh perubahan aktivitas pertumbuhan bakteri.Kebanyakan bakteri hidup dan beraktivitas baik pada kondisi pH netral (Cutright, 2001). Pada kondisi lingkungan tidak menguntungkan, pertumbuhan bakteri menjadi terganggu bahkan mati. Terganggunya pertumbuhan bakteri menyebabkan efisiensi perombakan menjadi rendah. Disamping pertumbuhan bakteri, aktivitas enzim yang terlibat pada proses perombakan juga sangat dipengaruhi oleh pH. Enzim pada sistem biologi sebagian besar merupakan protein yang mempunyai gugus aktif yang bermuatan positif (+) dan negatif (-).
Aktivitas enzim akan optimum jika terjadi keseimbangan antar kedua muatannya. Hasil penelitian ini memperkuat kajian HeFang et al. (2004) yang melaporkan perombakan zat warna azo direct fast scarlet 4BS menggunakan konsorsium white-rot fungus dengan Pseudomonas 1-10 selama 4 hari inkubasi memberikan efisiensi perombakan warna sebesar 73% pada pH 3; 83% pada pH 4; 95% pada pH 7; 90% pada pH 8 dan menjadi 76% pada pH 10.
Kemampuan bakteri Enterobacter aerogenes dalam merombak remazol red RB diberbagai konsentrasi zat warna selama 5 hari inkubasi disajikan pada Gambar 2.
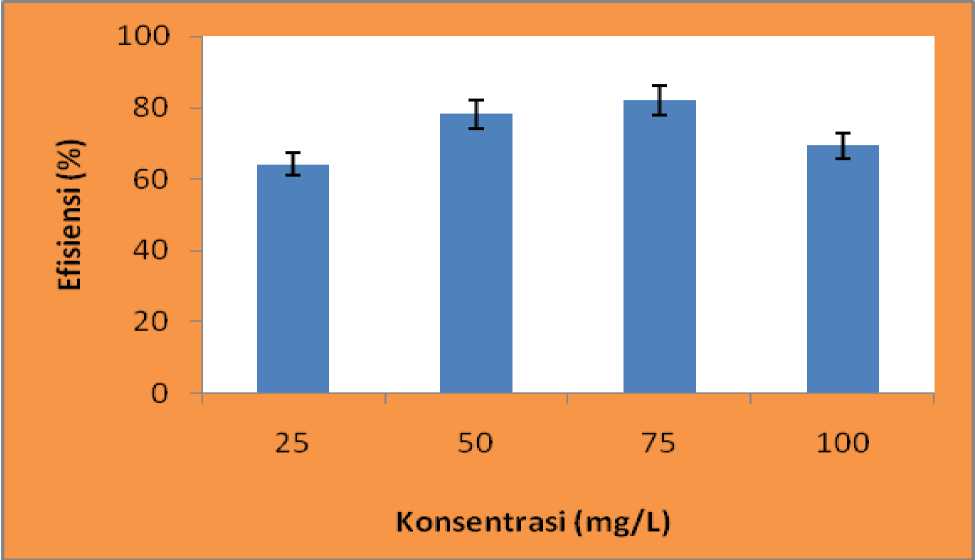
Gambar 2.
secara aerob selama 5 hari inkubasi diberbagai
Efisiensi perombakan remazol red RB konsentrasi zat warna.
Gambar 2. memperlihatkan efisiensi perombakan remazol red RB meningkat dengan naiknya konsentrasi zat warna dari 25 sampai 75 mg/L, kemudian menurun pada konsentrasi 100 mg/L. Konsentrasi maksimum remazol red RB yang mampu dirombak oleh bakteri Enterobacter aerogenes pada pH 7 selama 5 hari inkubasi adalah 75 mg/L dengan efisiensi perombakan sebesar 81,97%.Menurut Cutright (2001), aktivitas bakteri dalam merombak substrat dipengaruhi oleh faktor besarnya konsentrasi substrat yang akan dirombak. Untuk substrat pada rentang konsentrasi rendah, aktivitas perombakan umumnya berlangsung cepat dengan meningkatnya konsentrasi substrat. Pada konsentrasi yang tinggi, gugus-gugus aktif
dari enzim menjadi jenuh sehingga aktivitasnya juga menurun.
Aktivitas bakteri Enterobacter aerogenes dalam merombak zat warna remazol red RB dipengaruhi oleh lama waktu kontak antara bakteri dengan zat warna tersebut. Kurva hubungan efisiensi perombakan terhadap lama waktu inkubasi disajikan pada Gambar 3.
Gambar 3 memperlihatkan efisiensi perombakan 75 mg/L remazol red RB pada kondisi pH 7 meningkat tajam dari hari ke-1 sampai hari ke-7, sedangkan relatif konstan pada hari ke-8 sampai hari ke-10. Perombakan optimum diperoleh pada waktu inkubasi selama 7 hari dengan efisiensi perombakan sebesar 87,90%.
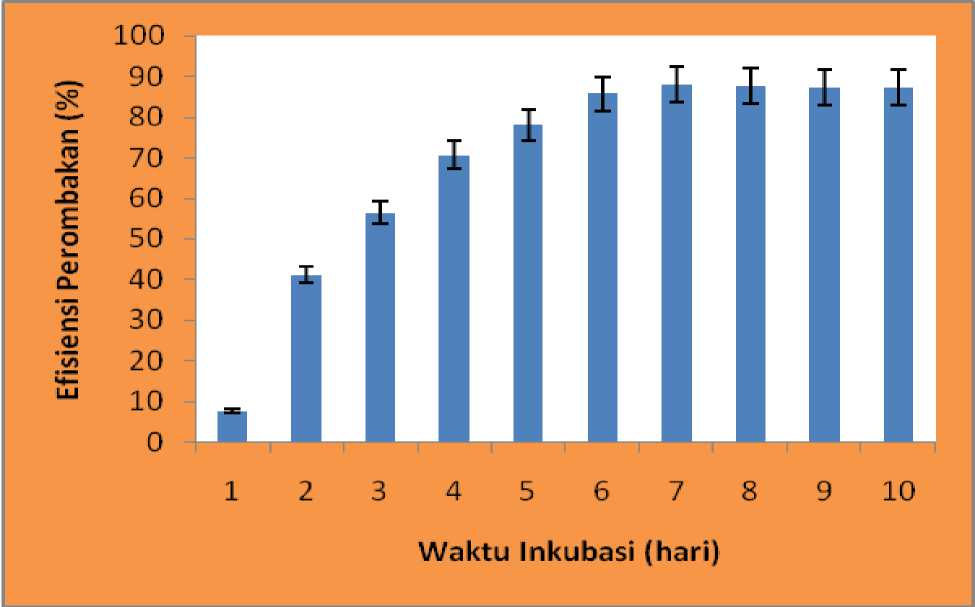
Gambar 3. Perombakan 75 mg/L remazol red RB pada kondisi aerob diberbagai waktu inkubasi
Berdasarkan grafik efisiensi perombakan zat warna remazol red RB pada variasi pH, konsentrasi zat warna, dan lama waktu inkubasi diperoleh efisiensi perombakan tertinggi terjadi pada kondisi pH 7-8, konsentrasi zat warna remazol red RB 75 mg/L dan waktu inkubasi 7 hari dengan efisiensi perombakan sebesar 87,90%.
Analisis terhadap perombakan zat warna remazol red RB dilakukan dengan membandingkan pola spektrum UV-Vis dari zat warna remazol red RB sebelum dan setelah perombakan. Pola spektrum yang diperoleh disajikan pada Gambar 4.
Gambar 4 menunjukkan bahwa terjadi perbedaan spektrum antara remazol red RB sebelum dirombak dengan sesudah dirombak. Puncak serapan remazol red RB sebelum dirombak terjadi pada panjang gelombang 520 nm, sedangkan setelah perombakan tidak terjadi serapan pada panjang gelombang tersebut dan muncul puncak serapan baru pada panjang gelombang 215 nm. Hilangnya puncak serapan pada panjang gelombang 520 nm dan munculnya puncak serapan pada 215 nm menunjukkan zat warna remazol red RB telah mengalami perombakan oleh bakteri Enterobacter aerogenes.
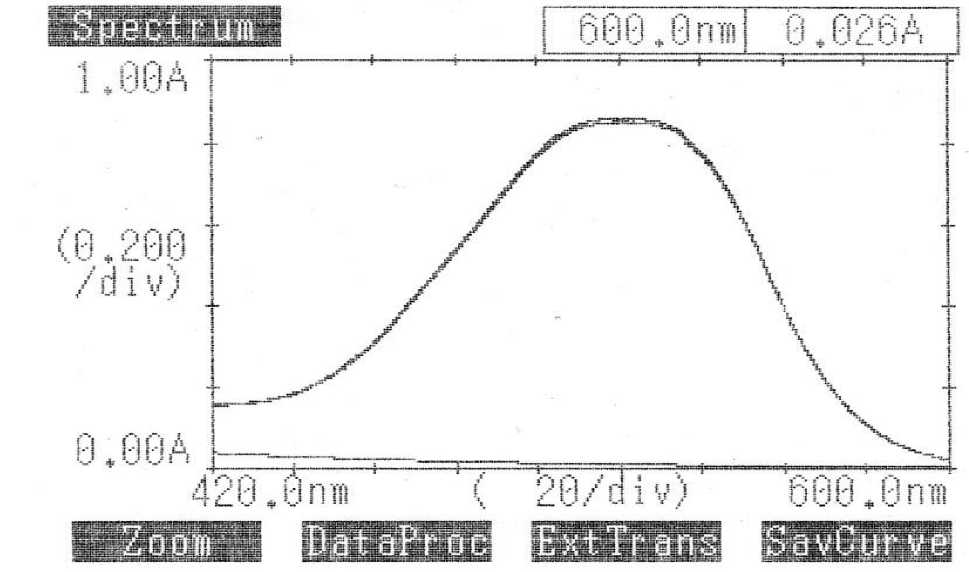
Gambar 4. Pola spektrum zat warna remazol red RB. (a) sebelum dirombak, (b) setelah dirombak menggunakan bakteri Enterobacter aerogenes selam 7 hari inkubasi.
SIMPULAN DAN SARAN
UCAPAN TERIMA KASIH
Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bakteri Enterobacter aerogenes mampu merombak zat warna tekstil secara aerob. Proses perombakan 75 mg/L zat warna remazol red RB berlangsung optimum pada pH 7-8 dan lama waktu inkubasi 7 hari dengan efisiensi perombakan sebesar 87,90%.
Saran
Pemanfaatan sumberdaya alam lokal seperti bakteri Enterobacter aerogenes mampu merombak zat warna tekstil. Berdasarkan potensi tersebut, sangat perlu dilakukan kajian lebih lajut terhadap pemanfaatannya dalam perombakan air limbah tekstil sebagai langkah yang strategis dalam menanggulangi pencemaran air akibat limbah industri.
Terima kasih penulis sampaikan kepada DP2M Dikti atas bantuan sumber dana penelitiannya, Eka Wijayanti yang telah membantu kelancaran pengambilan data, dan Jurusan Pendidikan Kimia FMIPA Universitas Pendidikan Ganesha atas bantuan fasilitas pelaksanaan penelitian.
DAFTAR PUSTAKA
Ajibola, V. O., S. J. Oney, C. E. Odeh, T.
Olugbodi, and U. G. Umeh, 2005, Biodegradation of Indigo Containing Textile Effluent Using Some Strains of Bacteria, Appl Sci. 5(5) : 853-855
Blackburn, R. S. and S. M. Burkinshaw, 2002, A Greener to Cotton Dyeing With
Excellent Wash Fastness, Green Chem, 4 : 47-52
Cutright, T. J., 2001, Biotechnology: Principles and Advances in Waste Control,
Departement of Civil Engineering, University of Akron
HeFang., HuWenrong, and LiYuezhong, 2004, Biodegradation Mechanisms and Kinetics of Azo Dys 4BS by a Micobial Consortium, Chemosphere, 57 : 293-301
Mona E. M., Mabrouk, and H. Yusef, 2008, Decolorization of Fast Red by Bacillus Subtilis HM, Appl Sci Res, 4(3) : 262269
Montano, J. G., 2007, Combination of Advanced Oxidation Processes and Biological Treatments for Commercial Reactive Azo Dyes Removal, Thesis, Universitat Autonoma de Barcelona, Bellaterra
Moutaouakkil, A., Y. Zeroual, F. Z. Dzayri, M. Talbi, K. Lee, and M. Blaghen, 2003, Bacterial Decolorization of The Azo Methyl Red by Enterobacter
agglomerans, Annal Microbiol, 53 : 161169
Padmavathy, S., S. Sandhya, K. Swaminathan, Y. V. Subrahmanyam,T. Chakrabarti, and S. N. Kaul, 2003, Aerobic Decolorization of Reactive Azo Dyes in Presence of Various Cosubstrates, Chem Biochem Eng,. 17 (2) : 147–151
Telke, A., D. Kalyani, J. Jadhav., and S. Govindwar, 2008, Kinetics and Mechanism of Reactive Red 141 Degradation by a Bacterial Isolat Rhizobium Radiobacter MTCC 8161, Acta Chim Slov, 55 : 320-329
Russ, R., J. Rau, and A. Stolz. 2000, The Function of Cytoplasmic Flavin Reductases in The Reduction of Azo Dyes by Bacteria, Appl Environ
Microbiol, 66 (4) : 1429-1434
Yoo, E. S. 2000, Biological and Chemical Mechanisms of Reductive
Decolorization of Azo Dyes, Dissertation, Genehmigte Berlin
124
Discussion and feedback