AKTIVITAS ANTIOKSIDAN ANTOSIANIN DALAM EKSTRAK ETANOL KULIT BUAH NAGA SUPER MERAH (Hylocereus costaricensis) DAN ANALISIS KADAR TOTALNYA
on
ISSN 1907-9850
AKTIVITAS ANTIOKSIDAN ANTOSIANIN DALAM EKSTRAK ETANOL KULIT BUAH NAGA SUPER MERAH (Hylocereus costaricensis) DAN ANALISIS KADAR TOTALNYA
Ni Ketut Meidayanti Putri*, I Wayan Gede Gunawan, dan I Wayan Suarsa
Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran, Bali *Email : meyda.putry93@yahoo.com
ABSTRAK
Buah naga merupakan tumbuhan yang berasal dari daerah beriklim tropis kering. Selain daging buahnya, kulit buah nagadapat dimanfaatkan dalam produksi pangan sebagai pewarna makanan alami dan sebagai bahan dasar pembuatan kosmetik. Hal ini karena kulit buah naga memiliki kandungan senyawa-senyawa yang dapat bermanfaat sebagai antioksidan salah satunya kandungan senyawa pada kulit buah naga adalah antosianin. Penelitian ini bertujuan menentukan aktivitas antioksidan dan kadar total antosianin serta mengetahui jenis antosianin yang terkandung didalam ekstrak etanol kulit buah naga super merah.Penentuan aktivitas antioksidan dilakukan dengan metode DPPH sedangkan, penentuan kadar total antosianinnya dilakukan dengan metode perbedaan pH menggunakan analisis spektrofotometer UV-Visibel.
Hasil penelitian menunjukkan bahwa persentase peredaman optimum sebesar 97,84% dengan nilai IC50 73,2772 mg/L, sedangkan kadar total rata-rata antosianin diperoleh sebesar 58,0720 ± 0,0001 mg/L dan jenis antosianin yang terkandung dalam ekstrak etanol kulit buah naga super merah adalah sianidin dengan membentuk puncak maksimum pada panjang gelombang 547 nm.
Kata kunci : Aktivitas antioksidan, Kadar total antosianin, Antosianin, Buah Naga, Sianidin
ABSTRACT
Dragon fruit is a plant that comes from dry tropical climate zones. Besides the flesh of the dragon fruits,,its skin can be used in food production as a natural food coloring and as the raw materials in cosmetics manufacturing. This is because of that the skin of the dragon fruit contains some compounds such as anthocyanin that can be used as an antioxidant. This study were aimed to determine the antioxidant activity, total anthocyanin content and the type of anthocyanins in the ethanol extract of super red dragon fruit skin. The determination of antioxidant activity of anthocyanin was carried out by the use of DPPH method, whereas the determination of the total content of anthocyanin was performed with a pH difference method using UV-Visibel spectrophotometer.
The results showed that the optimum scavenger percentage of the extract was of 97.84% with IC50 value of 73.2772 mg / L, whereas the average levels of total anthocyanins obtained was of 58.0720 ± 0,0001mg / L. The type of anthocyanins contained in the ethanol extract of the skin of super red dragon fruit was sianidin showing a maximum peak at a wavelength of 547 nm.
Keywords : Antioxidant activity , Total concentration of Anthocyanins , Anthocyanins , Dragon fruit, Cyanidin
PENDAHULUAN
Buah naga merupakan tumbuhan yang berasal dari daerah beriklim tropis kering. Pertumbuhan buah naga dipengaruhi oleh suhu, kelembaban udara, keadaan tanah dan curah hujan.
Habitat asli buah naga berasal dari negara Meksiko, Amerika Utara dan Amerika Selatan bagian utara. Namun buah naga saat ini telah dibudidayakan di Indonesia seperti di Jember, Malang, Pasuruan dan daerah lainnya (Kristanto, 2008).
Hal menarik pada buah naga adalah manfaat dari kulit buahnya. Kulit buah naga dapat bermanfaat dalam produksi pangan maupun industri seperti pewarna alami pada makanan dan minuman. Selain itu dalam industri, kulit buah naga dapat dijadikan bahan dasar pembuatan kosmetik. Dalam bidang farmakologi kulit buah naga juga dapat dijadikan sebagai obat herbal alami yang dapat bermanfaat sebagai antioksidan. Jenis buah naga ada empat, yaitu Hylocereus undatus (buah naga daging putih), Hylocereus costaricensis (buah naga daging super merah), Hylocereus polyrhizus (buah naga daging merah), Selenicereus megalanthus (buah naga kulit kuning daging putih) (Cahyono, 2009).
Kulit buah naga mengandung vitamin C, vitamin E, vitamin A, alkaloid, terpenoid, flavonoid, tiamin, niasin, piridoksin, kobalamin, fenolik, karoten, dan fitoalbumin (Jaafar,et al.,2009). Menurut penelitian Wu ,et al (2006) keunggulan dari kulit buah naga yaitu kaya polifenol dan merupakan sumber antioksidan. Selain itu aktivitas antioksidan pada kulit buah naga lebih besar dibandingkan aktivitas antioksidan pada daging buahnya, sehingga berpotensi untuk dikembangkan menjadi sumber antioksidan alami. Hal ini sesuai dengan penelitian yang dilakukan oleh Nurliyana et al (2010) yang menyatakan bahwa di dalam 1 mg/ml kulit buah naga merah mampu menghambat 83,48 + 1,02% radikal bebas, sedangkan pada daging buah naga hanya mampu menghambat radikal bebas sebesar 27,45 + 5,03 %. Selain itu aktivitas antioksidan kulit buah naga juga didukung dengan penelitian oleh Mitasari (2012) yang menyatakan bahwa ekstrak kloroform kulit buah naga merah memiliki aktivitas antioksidan dengan nilai IC50 sebesar 43,836 µg/mL.
Penelitian yang dilakukan Fajriani (2013) bahwa kulit buah naga super merah memiliki persentase peredaman radikal bebas DPPH sebesar 79,24%, namun pada penelitian tersebut belum menentukan nilai IC50 dari ekstrak kulit buah naga tersebut sehingga pada penelitian ini dilakukan penentuan nilai IC50. Nilai IC50 umum digunakan untuk menyatakan aktivitas antioksidan suatu bahan uji dengan metode peredaman radikal bebas DPPH dimana IC50 yakni konsentrasi suatu larutan uji (sampel) memberikan peredaman DPPH sebesar 50% (Molyneux, 2004).
Penelitian Setyaningrum (2010) juga menyebutkan bahwa kapasitas antiradikal ekstrak buah salam memiliki korelasi yang tinggi terhadap kadar antosianinnya. Berdasarkan uraian tersebut diatas, maka perlu dilakukan penelitian terhadap kulit buah naga super merah karena kandungan antosianin tinggi yang memiliki aktivitas sebagai antioksidan. Penelitian meliputi uji warna sebagai uji fitokimia antosianin (Harborne, 1987), uji aktivitas antioksidan dengan metode DPPH (Santosa et al., 1998) untuk mengetahui persentase peredaman radikal bebas dan nilai IC50 dari ekstrak etanol kulit buah naga super merah dan identifikasi serta penentuan kadar total antosianin pada ekstrak etanol kulit buah naga super merah dengan menggunakan metode perbedaan pH (Giusti dan Worlstad, 2001).
MATERI DAN METODE
Bahan
Bahan baku yang digunakan pada penelitian ini yaitu kulit buah naga super merah yang diperoleh dari Pasar Lokal Anantha Bogha Desa Pemogan, Denpasar. Bahan kimia yang diperlukan adalah Etanol, HCl, Aquades, DPPH, NaOH, KCl, Natrium sitrat.
Peralatan
Alat-alat yang digunakan dalam penelitian ini adalah pisau, blender, stoples, gelas beker, neraca analitik, aluminium foil, botol vial gelap, botol semprot, kertas saring, corong gelas, pH meter, penguap putar vakum, batang pengaduk, pipet mikro, pipet tetes, pipet ukur, labu ukur, gelas ukur, tabung reaksi, Spektrofotometer UV-Visibel.
Cara Kerja
Preparasi sampel
Sampel buah naga super merah dikupas dan dibersihkan untuk memisahkan daging buah dengan kulitnya, selanjutnya kulit buah dicuci kemudian ditiriskan. Setelah air sisa pencucian tiris, kulit buah dipotong kecil-kecil dan diblender hingga halus.
Analisis kadar air sampel
Analisis kadar air kulit buah naga super merah (Hylocereus costaricensis) menggunakan
metode oven pada suhu 105oC. Cawan kosong dikeringkan dalam oven dengan suhu 105oC selama 1 jam dan didinginkan dalam desikator (selama 20-30 menit). Kemudian cawan kering ditimbang dengan neraca analitik (W0).
Sebanyak 1,3411 gram sampel dimasukkan kedalam cawan kering kemudian ditimbang dengan cepat (W1). Cawan beserta sampel tersebut dikeringkan dalam oven 105oC selama 3 jam. Setelah dioven selama 3 jam kemudian masukkan kedalam desikator selama 20-30 menit, lalu timbang kembali. Cawan dimasukkan kembali kedalam oven sampai diperoleh berat yang konstan (W2). Kadar air dalam sampel dapat dihitung dengan rumus berikut:
v W1-VV2
Kadar air = -----x 100%
Wl-WO
Keterangan :
Wo = berat cawan kering yang sudah konstan (g) W1 = berat sampel awal dan cawan (g)
W2 = berat cawan dan sampel kering yang sudah konstan (g)
Ekstraksi kulit buah naga super merah
Sebanyak 1000 g sampel kulit buah yang telah halus diekstraksi dengan teknik maserasi basah menggunakan pelarut etanol 96% dan HCl 1% dengan perbandingan volume 9 : 1 sebanyak 1000 mL. Maserasi dilakukan selama 24 jam kemudian disaring dan filtratnya ditampung. Ekstraksi dilakukan sampai seluruh antosianin pada kulit buah naga super merah terekstraksi sempurna. Filtrat tersebut diuapkan dengan menggunakan rotary vacum evaporator sehingga didapat ekstrak kental etanol kemudian ditimbang beratnya.
Uji fitokimia antosianin
Dilakukan uji warna golongan senyawa antosianin menurut Harborne (1987) yakni 0,5 gram ekstrak etanol kulit buah naga ditambahkan HCl 2M kemudian dipanaskan 100oC selama 5 menit. Hasil positif bila timbul warna merah. Juga ditambahkan NaOH 2M tetes demi tetes sambil diamati perubahan warna yang terjadi. Hasil positif bila timbul warna hijau biru yang memudar berlahan-lahan.
Uji aktivitas antioksidan dengan metode DPPH
Akivitas antioksidan ditentukan dengan metode radikal bebas DPPH (Santosa et al., 1998).
Larutan DPPH 0,004%dibuat dengan cara melarutkan kristal DPPH 0,004 g dalam 100 mL etanol p.a. Sebanyak 200 µl etanol p.a dipipet ke dalam kuvet kemudian ditambahkan larutan DPPH sebanyak 3 mL, aduk rata dengan pipet dan segera dibuat spektra sinar tampak (400-600 nm). Pengukuran antiradikal bebas untuk bahan uji dilakukan dengan cara larutan uji dipipet sebanyak 200 µl ke dalam kuvet, kemudian ditambahkan (reaksikan) larutan DPPH sebanyak 3 mL, selanjutnya dibuat spektra sinar tampak (400-600 nm). Pada menit ke-5 setelah pereaksian dibaca absorban pada 497-517-537 nm dan dilakukan kembali pada menit ke-60. Perhitungan absorbansi antiradikal bebas DPPH dan larutan uji ditentukan menggunakan persamaan 1, sedangkan aktivitas antiradikal bebas sebagai persentase peredaman menggunakan persamaan 2.
Absorban hitung 517 nm = ■^517 - 2 ….(1) %PeredamanDPPH=1- Ahitungbahanuji x100% ..(2)
Penentuan kadar total antosianin dengan metode perbedaan pH
Faktor pengenceran yang tepat untuk sampel harus ditentukan terlebih dahulu dengan cara melarutkan sampel dengan buffer KCl pH 1 hingga diperoleh absorbansi kurang dari 1,2 pada panjang gelombang 510 nm. Selanjutnya diukur absorbansi akuades pada panjang gelombang yang akan digunakan (510 dan 700 nm) untuk mencari titik nol. Panjang gelombang 510 nm adalah panjang gelombang maksimum untuk sianidin-3-glukosida sedangkan panjang gelombang 700 nm untuk mengoreksi endapan yang masih terdapat pada sampel. Jika sampel benar-benar jernih maka absorbansi pada 700 nm adalah 0. Dua larutan dengan sampel disiapkan, pada sampel pertama digunakan buffer KCl dengan pH 1 dan untuk sampel kedua digunakan buffer Na-sitrat dengan pH 4,5. Masing-masing sampel dilarutkan dengan larutan buffer berdasarkan DF (dilution factor) yang sudah ditentukan sebelumnya. Sampel yang dilarutkan menggunakan buffer pH 1 dibiarkan selama 15 menit sebelum diukur, sedangkan untuk sampel yang dilarutkan dengan buffer pH 4,5 siap di ukur setelah dibiarkan bercampur selama 5 menit. Absorbansi dari setiap larutan pada panjang
gelombang 510 dan 700 nm diukur dengan buffer pH 1 dan buffer 4,5 sebagai blankonya. Absorbansi dari sampel yang telah dilarutkan (A) ditentukan dengan persamaan 3.
A = (A510 – A700)pH 1,0 - (A510 – A700)pH 4,5 ............(3)
Kandungan pigmen antosianin pada sampel dihitung dengan persamaan 4.
1 ∖ _ AxBMxDFxIOOO
Total Antosianin (mg/L) = .......(4)
zxl
Keterangan :
BM = berat molekul Sianidin-3-glukosida =
449,2 g/mol
DF = faktor pengenceran
ε = absorptivitas molar sianidin-3-glukosida =
26.900 L/(mol.cm) [ = tebal kuvet (1 cm)
HASIL DAN PEMBAHASAN
Analisis Kadar Air Sampel Kulit Buah Naga Super Merah
Hasil analisis kadar airpada kuli buah naga super merah diperoleh berat konstan sampel sebesar 0,0861 g sehingga diperoleh kadar air sebesar 93,57% hal ini sesuai dengan Kristanto, D (2008) yang mengatakan bahwa kadar air pada kulit buah naga sekitar 90,20% .
Ekstraksi Kulit Buah Naga Super Merah
Ekstraksi kulit buah naga super merah dilakukan dengan metode maserasi menggunakan pelarut etanol 96% yang diasamkan dengan HCl
1%. Etanol merupakan pelarut yang memiliki senyawa yang bersifat polar dan non polar karena etanol memiliki gugus etil yang bersifat non polar dan hidroksi yang bersifat polar. Penambahan pelarut HCl 1% bertujuan untuk memberikan suasana asam pada proses maserasi karena senyawa antosianin bersifat lebih stabil dalam suasana asam. Hasil maserasi 1000 g kulit buah naga super merah yang telah halus dengan 5 L (1000 mL x 5 kali maserasi) dengan etanol 96% yang diasamkan dengan HCl 1% dengan perbandingan volume 9 :1 menghasilkan 10,8502 g ekstrak kental etanol yang berwarna merah pekat.
Uji Fitokimia Antosianin
Uji fitokimia dilakukan untuk mengidentifikasi senyawa antosianin berupa uji warna yang menggunakan pelarut NaOH 2M dan HCl 2M. Hasil dari uji fitokimia antosianin pada ekstrak etanol kulit buah naga super merah dibandingkan dengan Harborne (1987) dapat dilihat pada Tabel 1.
Salah satu faktor yang mempengaruhi warna dari antosianin adalah perubahan pH. Sifat asam akan menyebabkan warna antosianin menjadi merah, sedangkan sifat basa menyebabkan antosianin menjadi biru. Selain faktor perubahan pH, konsentrasi pigmen, adanya campuran dengan senyawa-senyawa lain, jumlah gugus hidroksi dan metoksi juga mempengaruhi warna antosianin (Satyatama, 2008). Gugus hidroksi yang dominan menyebabkan warna cenderung biru dan relatif tidak stabil sedangkan, gugus metoksi yang dominan menyebabkan warna merah dan relatif lebih stabil.
Table 1. Uji fitokimia antosianin ekstrak etanol kulit buah naga super merah
|
Uji |
Hasil | |
|
Penelitian |
Harborne (1987) | |
|
Dipanaskan dengan HCl 2M selama 5 menit pada suhu 100oC |
Warna tetap |
Warna merah (tetap) |
|
Ditambahkan larutan NaOH 2M tetes demi tetes |
Warna berubah menjadi hijau dan memudar perlahan-lahan |
Warna berubah menjadi hijau biru dan memudar perlahan-lahan |
Table 2. Hasil Uji Aktivitas Antioksidan Ekstrak Etanol Kulit Buah Naga Super Merah dengan DPPH
|
Konsentrasi (% b/v) |
Waktu |
A Ukur |
A Hitung |
% Peredaman | |||
|
Z 497 nm |
Z 517 nm |
Z 537 nm | |||||
|
DPPH |
0,004 |
0,6650 |
0,8193 |
0,7827 |
0,0954 |
- | |
|
0,0625 |
0,5281 |
0,6492 |
0,6308 |
0,0697 |
26,93 | ||
|
Sampel |
0,125 |
5’ |
0,4932 |
0,6022 |
0,5860 |
0,0626 |
34,42 |
|
0,25 |
0,4708 |
0,5655 |
0,5471 |
0,0565 |
40,75 | ||
|
0,50 |
0,4145 |
0,4827 |
0,4627 |
0,0441 |
53,80 | ||
|
1 |
0,3409 |
0,3619 |
0,3390 |
0,0219 |
77,01 | ||
|
DPPH |
0,004 |
0,6620 |
0,8189 |
0,7817 |
0,0970 |
- | |
|
0,0625 |
0,5073 |
0,6212 |
0,6028 |
0,0661 |
31,84 | ||
|
Sampel |
0,125 |
60’ |
0,4558 |
0,5531 |
0,5364 |
0,0570 |
41,27 |
|
0,25 |
0,4195 |
0,4973 |
0,4800 |
0,0475 |
51,01 | ||
|
0,50 |
0,3324 |
0,3745 |
0,3554 |
0,0306 |
68,47 | ||
|
1 |
0,2162 |
0,1983 |
0,1762 |
0,0021 |
97,84 | ||
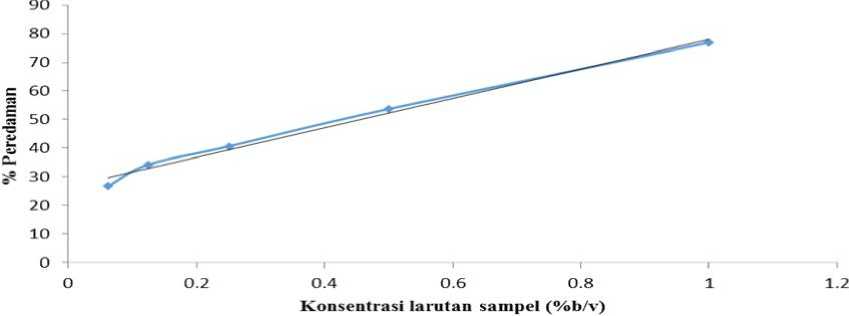
Gambar 1. Kurva Hubungan antara Konsentrasi dengan Persen Peredaman pada menit ke-5
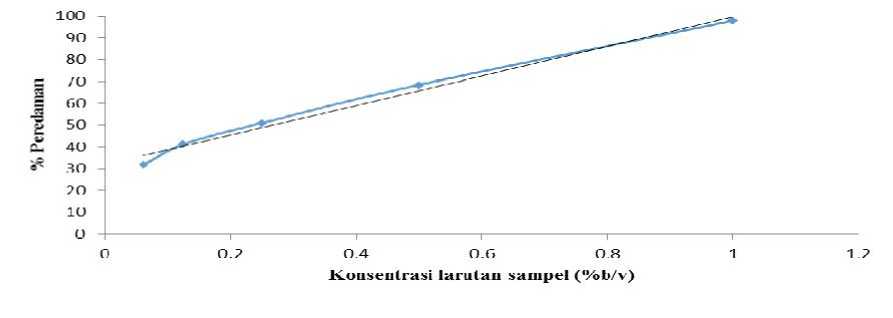
Gambar 2. Kurva Hubungan antara Konsentrasi dengan Persen Peredaman pada Menit ke-60
Uji Aktivitas Antioksidan dengan Metode DPPH
Uji aktivitas antioksidan pada ekstrak etanol kulit buah naga super merah dilakukan untuk mengetahui berapa besar aktivitas antioksidannya. Penentuan aktivitas antioksidan terlebih dahulu dengan cara mengukur panjang gelombang maksimum DPPH. DPPH (Difenilpikril hidrazil) merupakan suatu senyawa radikal bebas yang berperan sebagai oksidator saat bereaksi dengan suatu antioksidan. Pengujian aktivitas antioksidan dengan metode DPPH merupakan prosedur yang sederhana untuk mengetahui suatu senyawa tersebut berfungsi sebagai antioksidan. Berdasarkan hasil pengukuran panjang gelombang maksimum DPPH 0,004% b/v didapat spektrum pada panjang gelombang maksimum 517 nm dengan absorbansi sebesar 0,5570. Pengukuran aktivitas antioksidan dilakukan dengan mereaksikan larutan sampel dengan DPPH. Larutan sampel yang mengandung suatu senyawa yang dapat berfungsi sebagai antioksidan saat direaksikan dengan DPPH maka larutan DPPH yang semula berwarna ungu berubah menjadi warna kuning, hal ini mengidentifikasikan bahwa DPPH telah tereduksi sehingga DPPH berubah menjadi DPPH-H (Difenilpikril hidrazin). Hasil uji aktivitas antioksidan ekstrak etanol kulit buah naga super merah dengan DPPH dapat diamati pada Tabel 2.
Berdasarkan persen peredaman yang diperoleh pada menit ke-5 dan ke-60 diperoleh suatu kurva hubungan antara persen peredaman dengan konsentrasi suatu ekstrak yang ditunjukkan pada Gambar 1 dan 2.
Berdasarkan kurvahubungan antara konsentrasi dengan persen peredaman pada
Gambar 1 diperoleh persamaan garis y= 0,5132x + 0,267, dari persamaan garis tersebut diperoleh nilai IC50. Nilai IC50 merupakan konsentrasi suatu larutan uji (sampel) yang memberikan peredaman DPPH sebesar 50% (Molyneux, 2004). Berdasarkan perhitungan diperoleh nilai IC50 pada menit ke-5 sebesar 96,9454 mg/L, sedangkan nilai IC50 pada menit ke-60 yang ditunjukkan oleh Gambar 2 dari persamaan garis y= 0,6784x + 0,318 diperoleh sebesar 73,2772 mg/L. Menurut Molyneux (2004) suatu senyawa dikatakan sebagai antioksidan yang sangat kuat apabila nilai IC50 kurang dari 50 ppm, aktivitas kuat apabila nilai IC50 antara 50-100 ppm, aktivitas sedang apabila nilai IC50 antara 100-150 ppm dan lemah bila nilai IC50 antara 150-200 ppm. Hal ini menunjukkan bahwa pada ekstrak kulit buah naga memiliki aktivitas yang kuat dalam meredam radikal bebas.
Penentuan kadar total antosianin dengan metode perbedaan pH
Penentuan kadar total antosianin pada ekstrak etanol kulit buah naga super merah dilakukan dengan metode perbedaan pH menurut Giusti dan Worlstad (2001). Pada penentuan kadar antosianin, faktor pengenceran sampel harus ditentukan terlebih dahulu dengan melarutkan sampel pada larutan buffer KCl pH 1,0 sehingga diperoleh absorbansi kurang dari 1,2 pada panjang gelombang 510 nm. Faktor pengeceran yang telah ditentukan adalah 70 kali pengenceran dengan absorbansi yang diperoleh adalah sebesar 0,1274. Berdasarkan hasil perhitungan diperoleh kadar total antosianin rata-rata sebesar 58,0720 mg/L. Kadar total antosianin ekstrak etanol kulit buah naga super merah dipaparkan dalam Tabel 3.
Table 3. Kadar Total Antosianin Ekstrak Kulit Buah Naga Super Merah
|
Pengulangan |
Absorbansi |
Kadar Total Antosianin (mg/L) | |||
|
Buffer pH 1,0 |
Buffer pH 4,5 | ||||
|
λ 510 nm |
λ 700 nm |
λ 510 nm |
λ 700 nm | ||
|
I |
0,1226 |
0,0096 |
0,0739 |
0,0110 |
58,5630 |
|
II |
0,1221 |
0,0089 |
0,0743 |
0,0109 |
58,2123 |
|
III |
0,1219 |
0,0094 |
0,0739 |
0,0107 |
57,6279 |
|
IV |
0,1223 |
0,0087 |
0,0749 |
0,0110 |
58,0954 |
|
V |
0,1214 |
0,0088 |
0,0736 |
0,0105 |
57,8616 |
|
Rata-rata |
58,0720± 0,0001 | ||||
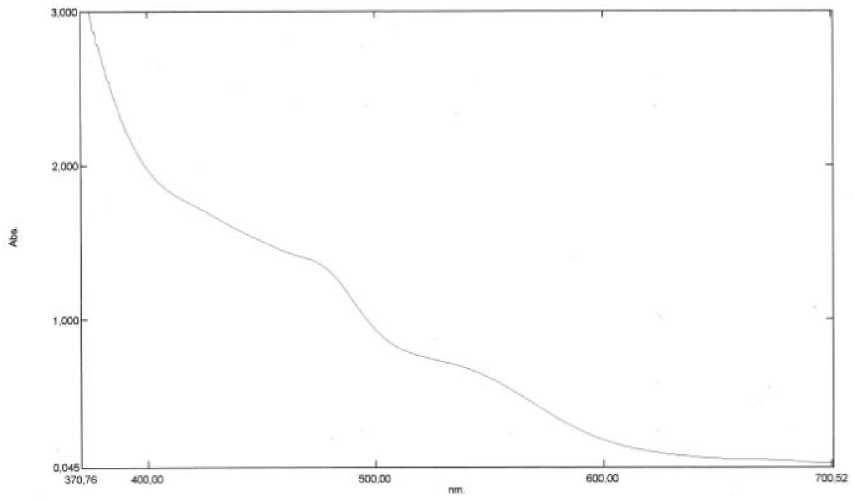
Gambar 3. Spektrum Ekstrak Etanol Kulit Buah Naga Super Merah
Tabel 3 menunjukkan bahwa pada ektrak kulit buah naga super merah memiliki kadar total rata-rata 58,0720 ± 0,0001 mg/L, hal ini disebabkan beberapa faktor diantaranya dalam proses preparasi sampel, kondisi dan masa penyimpanan sampel, serta habitat dari sampel buah naga super merah yang digunakan.
Pada proses preparasi sampel saat melakukan proses evaporasi sampel menggunakan suhu cukup tinggi yakni 50-60oC sehingga pada proses tersebut mempengaruhi kestabilan antosianin, karena dilakukan pemanasan secara kontinu sampai diperoleh ekstrak kental. Sesuai dengan Niendyah (2004), kestabilan antosianin dipengaruhi oleh beberapa faktor antara lain suhu, perubahan pH, sinar dan oksigen, serta faktor lainnya seperti ion logam. Selain itu, proses analisis pada sampel tidak langsung dilakukan saat ekstrak kental telah siap, sehingga kondisi dan masa penyimpanan sampel menyebabkan senyawa antosianin mengalami degradasi. Dilihat dari spektrum yang terbentuk dari larutan ekstrak menunjukkan bahwa ekstrak etanol kulit buah naga super merah mengandung antosianin jenis sianidin, hal ini dapat dilihat pada Gambar 3
Berdasarkan Gambar 3 tersebut menunjukkan bahwa ekstrak etanol kulit buah naga super
merah memberikan serapan pada panjang gelombang 547 nm yang diduga senyawa antosianin jenis sianidin. Hal ini didukung oleh Ribereau Gayon (1959) yang menyebutkan bahwa antosianin jenis sianidin memberikan serapan maksimum pada panjang gelombang 547 nm dengan sistem pelarut etanol yang diasamkan dengan asam klorida. Senyawa sianidin mengalami transisi elektronik n-π*, n-σ* dan π- π* karena terbentuk puncak maksimum pada kisaran panjang gelombang 400-600 nm. Namun, dalam mengidentifikasi jenis senyawa antosianin yang terkandung dalam ekstrak etanol kulit buah naga super merah ini mengalami kesulitan dalam memastikan jenis senyawa tersebut hal ini dikarenakan sampel yang digunakan masih dalam bentuk ekstrak kental sehingga banyak senyawa-senyawa pengganggu memberikan serapan sehingga membentuk suatu spektrum yang tidak sesuai. Hasil ini juga diperkuat oleh Fuleki & Francis (1968) yang menyebutkan bahwa serapan maksimum yang diberikan oleh senyawa antosianin jenis sianidin yakni pada panjang gelombang 547,0 nm. Selain pada panjang gelombang tersebut sianidin juga memberikan serapan pada panjang gelombang 510,5 nm (Schou and Svend Aage, 1927) dan 535,0 nm (Kim, et al,
1973) yang berwarna merah keunguan. Berikut struktur sianidin ditunjukkan pada Gambar 4.
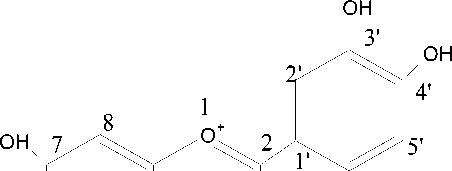
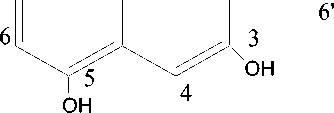
Gambar 4. Struktur sianidin
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian yang telah dilakukan maka dapat disimpulkan yakni :
-
1. Ekstrak etanol kulit buah naga super merah memiliki aktivitas antioksidan yang kuat.
-
2. Kadar total antosianin pada ekstrak kulit buah naga super merah menunjukkan kadar total antosianin dengan kadar rata-rata sebesar 58,0720 ± 0,0001mg/L.
-
3. Senyawa antosianin ysng terkandung dalam ekstrak etanol kulit buah naga super mersh diduga jenis sianidin.
Saran
Perlu dilakukan penelitian pada ekstrak etanol kulit buah naga super merah dengan menggunakan sampel kulit buah naga dalam keadaan kering dan melakukan pemisahan, pemurnian senyawa antosianin pada ekstrak etanol kulit buah naga super merah serta menentukan struktur dari isolat yang diperoleh dengan menggunakan HPLC, FTIR, dan NMR. Perlu diuji aktivitas antikanker sehingga dapat memberikan informasi tentang keaktifan dari kulit buah naga super merah.
UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih kepada Anak Agung Bawa Putra, S.Si., M.Si., selaku Ketua Jurusan Kimia FMIPA Universitas Udayana atas waktu serta saran yang diberikan. Ibu Dra. Ida Ayu Raka Astiti Asih, M.Si., Ibu Dra. Emmy Sahara, M.Sc (Hons)., Ibu Dra Ni Made Puspawati, M.Phil., Ph.D atas segala saran dan masukannya. I Nyoman Suwena dan Ni Ketut Kermi selaku orang tua yang selalu memberikan doa serta dukungan. Orang-orang terdekat saya Kadek Dwi Arya Pramanta, Ni Made Sukma Sanjiwani, Ika Juliana, Luh De Dwi Jayanthi, dan Made Hany Anastasia yang selalu memberikan semangat dan masukannya.
DAFTAR PUSTAKA
Cahyono, B., 2009, Buku Terlengkap Sukses Bertanam Buah Naga, Pustaka Mina, Jakarta
Fuleki, T. and Francis, F.J., 1968, Quantitative methods for anthocyanins, 1,Extraction and determination of total anthocyanin in cranberries, J. Food Sci, 33 : 72-78
Harborne, J. B.,1987, Metode Fitokimia Edisi ke-2, a.b. Padmawinata, K., Soediro, I., Institut Teknologi Bandung, Bandung
Jaafar, Ali, R., Nazri, M., dan Khairuddin, W., 2009, Proximate Analysis of Dragon Fruit (Hylecereus polyhizus), American Journal of Applied Sciences, 6 : 1341-1346
Kim, K. I., Nam, J. H., and Kwon, T. W., 1973, On the proximate composition, organic acids and anthocyanins of Omija, Schizandra chinensis Baillon, Korean Journal of Food Science and Technology, 5 : 178-182
Kristanto, D., 2008, Buah Naga:Pembudidayaan di Pot dan di Kebun, Penebar Swadaya, Jakarta
Mitasari, A., 2012, Uji Aktivitas Ekstrak Kloroform Kulit Buah Naga Merah (Hylocereus polyrhizus Britton & Rose) Menggunakan Metode DPPH (1,1-Defenil-2-Pikril Hidrazil), Skripsi,
Program Studi Farmasi, Universitas Tanjungpura : 37-38
Molyneux, P., 2004, The Use of Stable Free Radical diphenylpicrylhidraxyl (DPPH) for estimating antioxidant activity, Songklanakarin J. Sci. Technol., 26 (2) : 211-219
Niendyah, H., 2004, Efektivitas Jenis Pelarut dan Bentuk Pigmen Antosianin Bunga Kana (Canna coccinea mill.) serta Aplikasinya pada Produk Pangan, Skripsi, Universitas Brawijaya, Malang
Nurliyana, R., Zahir, I. S., Suleiman, K. M., Aisyah, M.R., dan Rahim, K. K., 2010, Antioxidant study of pulps and peels of dragon fruits: a comparative study, International Food Research Journal, 17 : 367-365
Qory Hajrul, Fajriani, 2013, Penentuan Aktivitas Antioksidan Kulit Buah Naga Super Merah (Hylocereus Costaricensis) Dan Produk Olahannya Berupa Permen Jelly, Skripsi, Universitas Pendidikan Indonesia, Jakarta
Ribereau Gayon, P., 1959, Recherches sur les anthocyannes des vegetaux. Application au genre Vitis, Disertasi, University of Bordeaux, Paris
Santosa H.M., Budiati, A.S., Fuad, A., dan Kusumawati, I., 1998. Pengujian
Antiradikal Bebas Difenilpikril Hidrazil (DPPH) Ekstrak Graptophyllum pictum (L). Griff. Secara Spektrofotometri, p.Seminar Nasional Tumbuhan Obat XIII, Malang, h. 84-85
Satyatama, D. I., 2008, Pengaruh Kopigmentasi Terhadap Stabilitas Warna Antosianin Buah Duwet (Syzygium cumini), Tesis, Fakultas Pertanian, Institut Pertanian Bogor, Bogor
Schou and Svend Aage, 1927, Light absorption of several anthocyanins, Helv Chim Acta, 10 : 907-915
Setyaningrum, A., 2010, Kapasitas Antiradikal Ekstrak Antosianin Buah Salam (Syzygium Polyanthum) Segar dengan Variasi Proporsi Pelarut, Jurusan Ilmu dan Teknologi Pangan UNS, Solo
Wrolstad, R. E. and Giusti, M.M., 2001, Characterization and Measurement of Anthocyanin by UV-Visible Spectroscopy : Current Protocols in Food Analytical Chemistry, John Wiley and Son, New York
Wu, L. C., Hsu, H. W., Chen, Y., Chiu, C. C., and Ho, Y. I., 2006, Antioxidant and Antiproliferative Activities of Red Pitaya, Food Chemistry Volume, 95 : 319-327
251
Discussion and feedback