SINTESIS SILIKA GEL TERIMOBILISASI DIFENILKARBAZON DARI ABU SEKAM PADI MELALUI TEKNIK SOL GEL
on
JURNAL KIMIA 9 (2), JULI 2015: 226-234
SINTESIS SILIKA GEL TERIMOBILISASI DIFENILKARBAZON DARI ABU SEKAM PADI MELALUI TEKNIK SOL GEL
Ni Nyoman Sri Nopianingsih*, I Wayan Sudiarta, dan Wahyu Dwijani Sulihingtyas
Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran, Bali *Email : nopianingsih29@gmail.com
ABSTRAK
Penelitian mengenai pembuatan silika gel terimobilisasi difenilkarbazon dari abu sekam padi melalui teknik sol-gel telah dikerjakan. Tujuan dari penelitian ini yaitu untuk membuat silika gel dari abu sekam padi yang diimobilisasi difenilkarbazon melalui teknik sol – gel. Penelitian ini meliputi modifikasi silika gel dari abu sekam padi dan karakterisasinya dengan spektra IR serta X-RD.
Hasil penelitian menunjukan bahwa sintesis silika gel termodifikasi difenilkarbazon berhasil dikerjakan, terbukti dari hasil spektra karakterisasi spektrofotometri IR, yang menunjukkan adanya gugus Si-O-Si, Si-O, dan Si-OH pada bilangan gelombang ±1087,85 cm-1, ±952,84 cm-1, ±3361,93 cm-1 yang merupakan gugus utama silika gel. Gugus N-H, C-H aromatik, C=C aromatik, vibrasi gugus N=N, serta vibrasi gugus C=O yang berada pada bilangan gelombang ±3313,71 cm-1, ±800,46 cm-1, ±1602,85 cm-1, ±1700 cm-1, dan ±1602,85 cm-1. Data X-RD menunjukkan bahwa struktur silika terimobilisasi difenilkarbazon bersifat amorf.
Kata kunci : abu sekam padi, silika gel, ligan difenilkarbazon
ABSTRACT
A research on synthesis diphenylcarbazone immobilized silica gel from rice husk ash by sol-gel technique has been conducted. The purpose of this research was to synthesize the diphenylcarbazone immobilized silica gel from rice husk ash by sol-gel technique. This research included modification of silica gel of rice husk ash and silica gel characterization by IR spectra and X-RD.
The results showed that the diphenylcarbazone immobilized silica gel has been successfully synthesized. It can be seen from the FTIR spectrum that silica-imobilized revealed peaks at wave numbers of ±1087.85cm-1 indicating the presence of Si-O-Si. The peak seen at wave numbers of ±952.84cm-1 indicating the presence of Si-O, at ±3361.93cm-1due to the Si-OH bond which was the main functional group of silica gel. Another peaks at ±3313.71cm-1, ±800.46cm-1, ±1602.85cm-1,±1700 cm-1, and ±1602.85cm-1 suggesting the presence of N-H, aromatic C-H (substituted benzene), aromatic C=C, N=N and C=O stretching. X-RD data showed that the structure of diphenilcarbazone immobilized silica gel was amorphous.
Keywords : rice ash, silica gel, diphenylcarbazone
PENDAHULUAN
Sekam padi bersifat keras dan kasar, tidak memiliki nilai ekonomis dan berkadar gizi rendah (Rohaeti, 1992). Abu sekam padi berasal dari pembakaran sekam padi yang dapat digunakan untuk mensintesis silika gel. Kandungan (SiO2) yang terdapat dalam abu sekam padi yaitu sebesar 87-97% (Nuryono,2004). Dilihat dari tingginya
kandungan silika dalam sekam maka sangat memungkinkan silika untuk digunakan sebagai dasar pembuatan silika gel. Senyawa silika sintetis yang berstruktur amorf serta berbentuk padatan dimana dapat dimanfaatkan sebagai adsorben disebut dengan silika, sehingga silika gel sangat inert serta relatif tidak mengembang dalam pelarut organik. Silika gel memiliki situs aktif berupa gugus silanol dan siloksan. Adanya gugus –OH
memberikan peluang secara luas untuk memodifikasi gugus tersebut menjadi gugus lain yang lebih aktif (Santos, et al.w, 2001).
Modifikasi permukaan silika gel dapat dibedakan menjadi dua yaitu secara fisik dan kimia. Secara kimia modifikasi dapat dilakukan melaui dua cara yaitu reaksi homogen (teknik solgel) dan reaksi heterogen. Proses modifikasi melalui sol-gel terjadi pada bahan dasar pembentuk silika gel (precursor) natrium silikat. Proses modifikasi dilakukan pada saat pembentukan gel (Sulastri, 2010).
Penelitian tentang modifikasi silika gel secara kimia melalui reaksi heterogen oleh Arakaki (2000), dilaporkan bahwa diperoleh hasil yang stabil tetapi reaksi berlangsung lambat dan senyawa yang terimmobilisasi sangat sedikit. Buhani dan Suharso (2010) juga telah melaporkan penelitian tentang sintesis adsorben hibrida amino-silika (HAS) melalui proses sol-gel menggunakan senyawa aktif 3-aminopropiltrimetoksisilan (3-APTMS) dengan prekursor tetraetil ortosilikat (TEOS) untuk adsorpsi ion Cd(II) dari larutan. Hasil yang didapatkan bahwa adsorpsi logam efektif terjadi pada pH 3 hingga 4.
Dari perbandingan metode tersebut, teknik sol – gel mempunyai kelebihan diantaranya proses yang sederhana dan cepat karena reaksi pengikatan berlangsung secara bersamaan dengan proses terbentuknya padatan. Selain itu, teknik modifikasi melalui proses sol – gel lebih mudah dilakukan di laboratorium karena reaksi dapat dilakukan pada temperatur kamar sehingga dapat menggunakan alat -alat sederhana (Astuti, 2012). Sejauh ini belum pernah dilaporkan mengenai modifikasi silika gel dengan ligan difenilkarbazon menggunakan teknik sol gel. Oleh karena itu, pada penelitian ini akan dilakukan sintesis silika gel dari abu sekam padi yang diimobilisasi difenilkarbazon melalui teknik sol – gel. Penelitian ini meliputi modifikasi silika gel dari abu sekam padi dan karakterisasinya dengan spektra IR serta X-RD.
MATERI DAN METODE
Bahan
Bahan yang digunakan adalah sebagai berikut sekam padi, HCl, HNO3, NaOH, toluena p.a merck, ligan difenilkarbazon, piridin, 3
kloropropiltrimetoksisilan, aquades, kertas saring whatman 42.
Peralatan
Alat – alat yang digunakan yaitu peralatan gelas, pengaduk magnet, corong kaca, batang pengaduk, ayakan 250 µm, pipet tetes, pipet volum, kaca arloji, desikator, oven, hot plate, pH meter, oven, tanur, sentrifugasi, Spektrofotometer Inframerah (IR) Shimadzu, XRD.
Cara Kerja
Pengabuan sekam padi
Sebanyak 1 kg sekam padi yang bersih dan kering diabukan pada suhu 7000C. Abu yang diperoleh kemudian digerus dan diayak menggunakan ayakan 250 µm (Aina, et al., 2007). Pembuatan natrium silikat
Abu sekam padi direndam dengan HCl 4M sebanyak 200 mL selama 3 jam selanjutnya dibilas dengan akuades hingga netral. Abu sekam padi dikeringkan pada suhu 1000C. Sebanyak 20 g abu kering ditambahkan dengan 40 mL NaOH 4 M lalu dididihkan sampai mengental, selanjutnya dilebur pada suhu 500 oC selama 30 menit dalam tanur. Hasil leburan dilarutkan dalam 200 mL akuades, kemudian disaring setelah didiamkan semalam. Filtratnya merupakan larutan natrium silikat (Astuti, 2012).
Modifikasi Silika Gel dari Abu Sekam Padi dengan Difenilkarbazon
Modifikasi silika gel dari abu sekam padi diawali dengan mereaksikan larutan natrium silikat sebanyak 20 mL dengan reagen silan 3-kloropropil-trimetoksisilan sebanyak 5 mL dimasukan ke dalam gelas beker, kemudian ditambahkan 100 mL larutan difenilkarbazon 500,0 mg/L dalam toluena, 2 mL piridin, kemudian diaduk sambil ditambahkan HCl 3 M secara bertetes-tetes sampai terbentuk gel dan pH netral. Gel yang dihasilkan dicuci dengan akuades hingga netral. Setelah netral gel dikeringkan pada temperatur 70 °C dalam oven. Gel yang kering kemudian digerus dan diayak menggunakan ayakan 250 μm. Hal yang sama juga dilakukan untuk pembuatan SI-G, SI-CPTMS dan SI-CPTMS-DPZon dengan variasi masa 0,005; 0,5; dan 1,0 g.
Karakterisasi hasil sintesis
Semua silika gel yang diperoleh dikarakterisasi dengan Spektroskopi IR untuk menentukan gugus-gugus fungsional yang ada dan anlisis dengan X-RD untuk mengetahui kristalinitasnya
HASIL DAN PEMBAHASAN
Pengabuan Sekam Padi
Abu sekam padi diperoleh dari pengabuan sekam padi yang sudah bersih dan kering pada suhu 700 oC dalam tanur. Abu sekam padi yang diperoleh berwarna putih sebanyak 202,02 g dari 1000 g sekam padi, sehingga kadar abu dalam sekam adalah 20,20 % b/b. Struktur abu yang dihasilkan berbentuk amorf. Hasil yang diperoleh sama dengan hasil yang dilaporkan oleh Nuryono (2004) dimana abu sekam padi yang diperoleh ketika pengabuan pada suhu 7000C berwarna putih dengan struktur amorf.
Pembuatan Natrium Silikat
Natrium silikat dapat dibuat dari abu sekam padi melalui peleburan dengan natrium hidroksida. Peleburan dilakukan agar reaksi antara SiO2 yang terdapat dalam abu dengan NaOH dapat berjalan lebih sempurna sehingga semua silika bereaksi menghasilkan natrium silikat (Na2SiO3) (Wogo, 2011). Natrium silikat (Na2SiO3) yang dihasilkan kemudian dilarutkan dengan akuades sehingga menghasilkan natrium silikat berwarna bening jernih dan digunakan sebagai prekursor dalam pembuatan silika gel.
Reaksi pembentukan larutan Na2SiO3 dari SiO2 dalam abu sekam padi dengan NaOH adalah sebagai berikut :
SiO2 + 2NaOH ----► Na2SiO3 + H2O
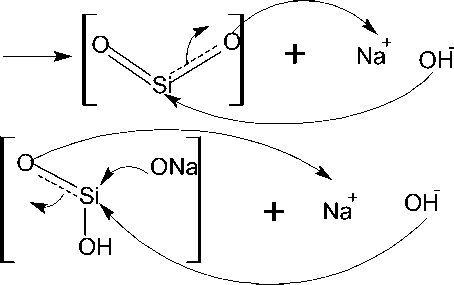
Dengan perkiraan mekanisme reaksi pembentukan natrium silikat sebagai ditunjukkan pada Gambar 1.
O Si O

O Si ONa +
OH
+
NaOH
NaOH
ONa
S

OH
ONa
→ ONa Si ONa +
O
H2O
H
Gambar 1. Mekanisme reaksi pembentukan natrium silikat (Scott, 1993)
Tahapan reaksinya adalah ion hidroksil (OH-) akan menyerang atom Si yang elektropositif sehingga melepaskan ikatan terhadap salah satu atom O yang elektronegatif sehingga terbentuk intermediet SiO2OH- yang tidak stabil. Intermediet mengalami dehidrogenasi membentuk SiO32-, ion hidrogen yang dilepaskan berikatan dengan ion hidroksil membentuk air.
Modifikasi Silika Gel dengan ligan Difenilkarbazon
Pembuatan silika gel terimobilisasi difenilkarbazon melalui teknik sol-gel dilakukan
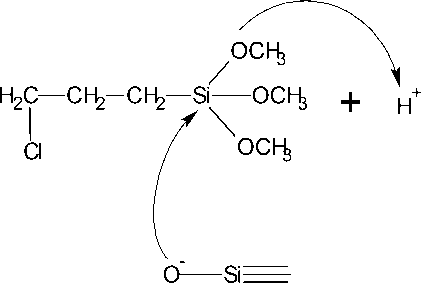
dengan mereaksikan natrium silikat dengan 3-kloropropil-trimetoksisilan (CPTMS), dan difenilkarbazon dalam toluena dengan katalis piridin. Campuran warna merah pekat diaduk sambil ditambahkan HCl 3 M secara bertetes-tetes. Proses pembentukan gel terjadi pada saat netralisasi dengan asam, sehingga menghasilkan silika gel terimobilisasi difenilkarbazon (Si-CPTMS-DPZon). Perkiraan reaksi pada tahap ini ditunjukkan pada Gambar 2.
H
O+CH3
H2C CH2 CH2 Si OCH3 i∖
Cl OCH3
I I
O Si
OCH3
H2C CH2 CH2 Si OCH3
Cl O Si
CH3OH
Gambar 2. Reaksi pembentukan Si-CPTMS
H 3 CO
SiO Si CH 2 CH 2 CH 2 +
SiO £ Cl
H 3CO
SiO Si CH

2 CH 2 CH 2
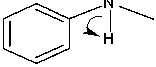
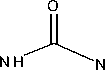

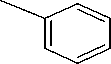
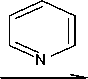
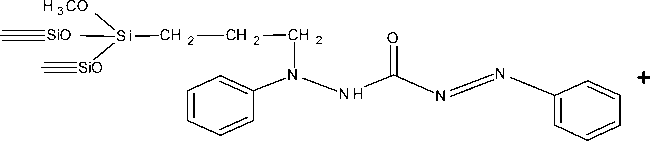
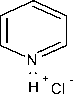
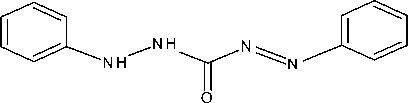
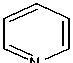
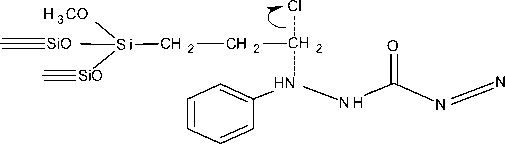
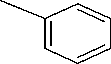
Gambar 3. Mekanisme reaksi pembentukan Si-CPTMS-DPZon
Reaksi imobilisasi difenilkarbazon pada silika gel sebagaimana ditunjukkan pada Gambar 3.
Silika gel yang diperoleh pada penelitian ini menunjukkan warna yang berbeda-beda pada 0,05 ; 0,5 ; dan 1 g adalah berwarna kuning muda, merah bata dan merah muda. Tujuan dari penggerusan dan pengayakan silika gel terimobilisasi difenilkarbazon untuk menghomogenkan serta memperbesar luas permukaan partikel silika gel terimobilisasi difenilkarbazon (Wogo, 2011).
Pada penelitian ini juga dibuat silika gel tanpa modifikasi (SiG) dan silika dengan pereaksi silan (Si-CPTMS). Silika gel yang dihasilkan adalah berwarna putih. Hasil yang diperoleh sesuai
dengan yang dilaporkan Wogo (2011) yaitu terbentuknya gel pada proses pembentukan silika gel melalui teknik sol gel dengan menggunakan larutan natrium silikat sebagai prekursornya dan 3-kloropropiltrimetoksisilan sebagai pereaksi silan.
Gugus Fungsional
Analisis gugus fungsi yang terdapat pada setiap silika gel dilakukan dengan metode spektrofotometri infra merah. Setiap gugus mempunyai spektra IR yang karakteristik sehingga dapat dibedakan satu sama lainnya, oleh karena itu dapat diidentifikasi secara kualitatif (Wogo, 2011). Karakterisasi dilakukan pada silika gel (SiG), Si-CPTMS, Si-CPTMS-DPZon 0,05 g, Si-CPTMS-DPZon 0,5 g, dan Si-CPTMS-DPZon 1 g. Hasil
karakterisasi dapat digunakan untuk mengetahui secara kualitatif keberhasilan pembuatan SI-G, SI-CPTMS dan SI-CPTMS-DPZon melalui perubahan serapan yang karakteristik untuk gugus-
gugus fungsional pada adsorben. Spektra hasil karakterisasi untuk kelima jenis silika gel disajikan dalam Gambar 4.
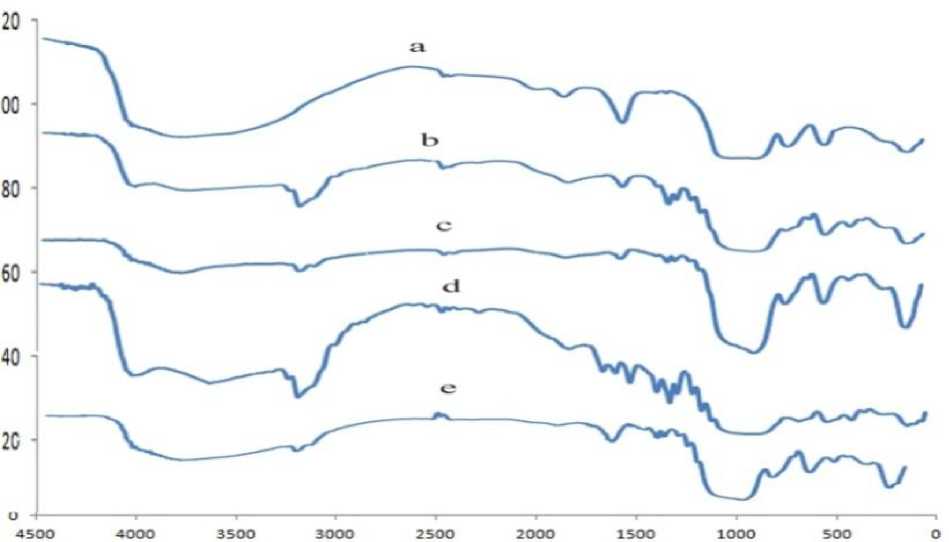
Gambar 4. Spektra IR untuk (a) SiG, (b) Si- CPTMS, (c) Si-CPTMS-DPZon 0,05 g, (d) Si-CPTMS-DPZon 0,5 g, (e) Si-CPTMS-DPZon 1 g
Tabel 1. Interpretasi hasil Spektrum FTIR
|
No. |
Gugus Fungsi |
Bilangan Gelombang (cm-1) | ||||
|
SiG |
Si-CPTMS |
Silika Terimobilisasi | ||||
|
Si-CPTMS-DPZon 0,05 g |
Si-CPTMS-DPZon 0,5 g |
Si-CPTMS-DPZon 1 g | ||||
|
1 |
Vibrasi ≡ Si — O - Si ≡ |
1087,85 |
1093,64 |
1087,85 |
1083,99 |
1082,07 |
|
2 |
Vibrasi ≡ Si - OH |
952,84 |
966,34 |
958,62 |
914,26 |
954,76 |
|
3 |
Vibrasi ulur OH dari Si-OH |
3361,93 |
±3400 |
3437,15 |
3313,71 |
3390,86 |
|
4 |
Vibrasi ulur C-H |
- |
2954,95 |
2954,95 |
2954,95 |
2956,87 |
|
5 |
Vibrasi gugus –C-C dari CH2 |
- |
1438,90 |
1440,83 |
1440,83 |
1438,90 |
|
6 |
Vibrasi ulur C-Cl |
- |
700,16 |
- |
- |
- |
|
7 |
Vibrasi gugus N=N |
- |
- |
- |
±1700 |
- |
|
8 |
Vibrasi gugus C=O |
- |
- |
- |
±1602,85 |
- |
|
9 |
Vibrasi tekuk C-H (aromatik) |
- |
- |
±800,46 |
±800,46 |
±800,46 |
|
11 |
Vibrasi tekuk C=C (aromatik) |
- |
- |
- |
±1602,85 |
±1629,85 |
|
12 |
Vibrasi tekuk N-H |
- |
- |
±1440,83 |
±1440,83 |
±1438,90 |
Analisis spektra FTIR dari spektrum silika gel, SiG (Gb.4.a) memperlihatkan munculnya serapan gugus siloksan pada ±1087,85 cm-1 dan gugus silanol pada bilangan gelombang ±952,84 cm-1, diperkuat oleh munculnya vibrasi ulur –OH pada bilangan gelombang ±3361,93 cm-1. Analisis Spektra IR menunjukkan bahwa pada sampel silika gel tanpa modifikasi terdapat gugus fungsional siloksan (Si-O-Si) dan gugus silanol (Si-OH), yang merupakan gugus fungsional utama dalam silika gel (Silverstein, 1986).
Pada silika gel termodifikasi 3-kloro-propiltrimetoksisilan (Si-CPTMS) (Gb.4.b), hasil karakterisasi dengan FTIR menunjukkan adanya gugus Si-OH pada bilangan gelombang ±966,34 cm-1, vibrasi ulur –OH dari Si-OH pada bilangan gelombang ±3400 cm-1, gugus Si-O-Si pada bilangan gelombang ±1093,64 cm-1 dan munculnya vibrasi ulur C-H pada ±2954 cm-1, vibrasi gugus –C-C dari CH2 pada daerah ±1438,90 cm-1 serta vibrasi ulur C-Cl pada bilangan gelombang ±700,16 cm-1 (Silverstein, 1986). Berdasarkan interpretasi spektra IR b dapat diprediksi bahwa silika dengan pereaksi silan (Si-
CPTMS) telah berhasil disintesis, dimana gugus-gugus tersebut tidak muncul pada silika tanpa modifikasi (SiG) dan hasil spektra dari Si-CPTMS diatas juga membuktikan silika gel telah terikat dengan senyawa 3-kloropropiltrimetoksisilan sebagai senyawa penghubung yang akan menyempurnakan proses imobilisasi ligan pada silika gel.
Interpretasi spektra IR silika gel terimobilisasi difenilkarbazon, Si-CPTS-DPZon, (Gambar 4) dijelaskan bahwa interpretasi spektra inframerah silika gel terimobilisasi ligan difenilkarbazon 0,05 g, 0,5 g, dan 1 g (Si-CPTMS-DPZon 0,05; Si-CPTMS-DPZon 0,5; Si-CPTMS-DPZon 1,0) menunjukkan adanya Si-OH pada bilangan gelombang ±900 cm-1, vibrasi ulur – OH dari Si-OH pada bilangan gelombang ±3300 cm-1, gugus Si-O-Si pada bilangan gelombang ±1080 cm-1, vibrasi ulur C-H pada ±2954 cm-1, vibrasi gugus –C-C dari CH2 pada daerah ±1440 cm-1, vibrasi gugus N-H pada daerah gelombang ±1400 cm-1, vibrasi tekuk C-H (aromatik) pada ±800 cm-1, vibrasi tekuk C=C (aromatik) pada daerah ±1600 cm-1 (Silverstein, 1986).
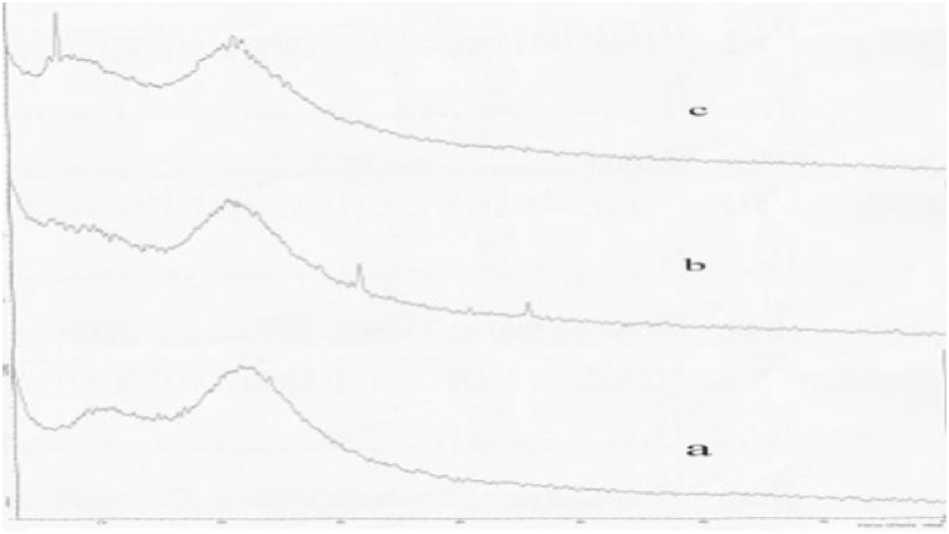
Gambar 5. Difraksi Sinar X dari (a) SiG (b) Si-CPTMS, (c) Si-CPTMS-DPZon 0,5 g
Pada Si-CPTMS-DPZon 0,5 g menunjukkan adanya gugus tambahan seperti munculnya gugus C=O pada daerah bilangan gelombang ±1602,85 cm-1dan vibrasi gugus N=N pada daerah bilangan gelombang ±1700 cm-1. Hasil interpretasi spektra pada Si-CPTMS-DPZon 0,05 g, 0,5 g dan 1 g memperlihatkan bahwa silika gel berhasil diimobilisasikan dengan ligan difenilkarbazon (Silverstein, 1986). Si-CPTS-DPZon 0,5 g yang menunjukkan serapan yang paling lengkap bila dibandingkan dengan Si-CPTS-DPZon 0,05 g dan 1 g. Sehingga Si-CPTS-DPZon 0,5 dipilih untuk tahap selanjutnya yaitu karakterisasi X-RD.
Difraksi Sinar-X (X-RD)
Spektroskopi XRD (Difraksi sinar-X) digunakan untuk mengidentifikasi struktur padatan yang dianalisis berupa pola difraksi sesuai dengan tingkat kristalinitasnya. Pola difraksi yang dianalisis yaitu silika gel tanpa modifikasi (SiG), silika dengan pereaksi silan (Si-CPTMS) dan silika terimobilisasi 0,5 ligan difenilkarbazon (Si-CPTMS-DPZon 0,5). Berdasarkan gambar 5 terlihat bahwa ketiga difraktogram memiliki pola difraksi dengan puncak melebar di sekitar 2θ = 21220. Sesuai dengan penelitian Kalaphaty (2000), silika dengan puncak melebar disekitar 20 = 20-22° menunjukkan struktur amorf. Puncak-puncak kecil yang muncul paga Gb.5b mengindikasikan adanya klorida dalam silika gel Si-CPTMS membentuk garam (Wogo, 2011). Sedangkan puncak tajam kecil pada Gambar 5 (c) kemungkinan disebabkan oleh kehadiran senyawa difenilkarbazon. Proses modifikasi dari silika gel dengan ligan organik tidak menyebabkan perubahan struktur dari silika gel yaitu sama-sama amorf.
SIMPULAN DAN SARAN
Simpulan
Pembuatan silika gel terimobilisasi difenilkarbazon dari abu sekam padi dapat dikerjakan dengan teknik sol-gel, terbukti dari spektra IR yang menunjukkan adanya vibrasi Si-OH, Si-O-Si, vibrasi ulur N-H yang diperkuat dengan vibrasi tekuk N-H, C-H (aromatik), vibrasi tekuk C=C (aromatik), munculnya gugus N=N, dan gugus C=O. Selain itu dibuktikan dengan
karakterisasi menggunakan spektroskopi X-RD yang menunjukkan bahwa proses modifikasi dari silika gel dengan ligan organik yaitu difenilkarbazon tidak menyebabkan perubahan struktur dari silika gel yaitu memiliki struktur sama-sama amorf dengan puncak melebar pada 2θ = 21-220.
Saran
Berdasarkan hasil penelitian, maka dapat disarankan agar melakukan penelitian lebih lanjut untuk memanfaatkan silika gel terimobilisasi ligan difenilkarbazon ini sebagai adsorben untuk mengadsorpsi ion-ion logam dalam larutan.
UCAPAN TERIMA KASIH
Ucapan terima kasih kami sampaikan kepada Drs. I Made Siaka M.Sc (Hons)., Drs. I Wayan Suirta M.Si, dan I Made Sutha Negara S.Si., M.Si. atas saran dan masukannya dalam penulisan artikel ini.
DAFTAR PUSTAKA
Aina, H., Nuryono, and Tahir, I., 2007, Sintesis Aditif Semen 2Ca2SiO4 dari Abu Sekam Padi dengan Variasi Temperatur Pengabuan, Makalah Seminar Nasional” Aplikasi Sains Dan Matematika Dalam Industri, UKSW, Salatiga
Arakaki, L. N. H. and Airoldi, C., 2000, Ethylenimine in the Synthetic Routes of a New Silylating agent: Chelating Ability of Nitrogen and Sulfur donor Atoms after Anchoring onto the Surface of Silica Gel, Polyhedron, 19 (1) : 367-737
Astuti, M.D., Nurmasari, R., dan Mujiyanti, D.R., 2012, Imobilisasi 1,8-Dihidroxyanthraqui-non Pada Silika Gel Melalui Proses SolGel, Sains dan Terapan Kimia, 6 (1) : 25 – 34
Buhani, dan Suharso, 2010, Modifikasi Silika dengan 3-Aminopropiltrimetoksisilan Melalui Proses Sol-Gel untuk Adsorpsi Ion Cd (III) dari Larutan, J.Sains MIPA, 16 (3) : 177-183
Dewi, L., 2005, Termodinamika Adsorpsi Zn(II) dan Cd(III) pada Adsorben Hibrida Amino-Silika Hasil Pengolahan dari Abu Sekam Padi, Skripsi, FMIPA UGM, Yogyakarta
Harsono, H., 2002, Pembuatan Silika Amorf dari Limbah Sekam Padi, Jurnal Ilmu Dasar, 3 (2) : 98 -103
Kalapathy, U., Proctor, A; and Shultz, J; 2000, A Simple Method for Production of Silica from Rice Hull Ash, Bioresource
Technology, 73 : 257-262
Nuryono, Narsito, dan Astuti, E., 2004, Pengaruh Temperatur Pengabuan Sekam Padi terhadap Karakter abu dan Silika gel Sintetik, Review Kimia, 7 (2) : 67-81
Rohaeti, E., 1992, Studi Pemanfaatan Abu Sekam Padi Sebagai Bahan Dasar Silikon untuk Bahan Semi Konduktor, FMIPA IPB, Bogor
Santos, E.A., Pagono, R.L., Simoni, J.A., Airoldi, C., Cestari, A.R., and Viera, E.F.S., 2001, The Influence of the Counter Ion
Competition and Nature of Solvent on the Adsorption of Mercury Halides on
SHmodified Silica Gel, Colloid and Surface, 201 : 259-282
Scott, R.P.W., 1993, Silica Gel and Bonded Phases, Willey & Sons Ltd, Chichester, : P. 2-14, 23-25, 43-54
Silverstein, Bassler, and Morrill, 1986, Penyidikan Spektrometrik Senyawa Organik, 4th ed., a.b. A.J. Hartomo, Erlangga, Jakarta
Sulastri, S., Kristianingrum, S., 2010, Berbagai Macam Senyawa Silika : Sintesis, Karakterisasi, dan Pemanfaatan, Prosiding Seminar Nasional Penelitian Pendidikan dan Penerapan MIPA, Fakultas MIPA, Universitas Negeri Yogyakarta, 15 Mei 2010
Wogo, H.E., Segu, J.O., and Ola, P.D., 2011, Sintesis Silika Gel Terimobilisasi Dithizon Melalui Proses Sol-Gel, Sains dan Terapan Kimia, 5 (1) : 84 – 95
234
Discussion and feedback