KAPASITAS ANTIOKSIDAN SENYAWA GOLONGAN TRITERPENOID PADA DAUN PRANAJIWA (Euchresta horsfieldii lesch benn)
on
ISSN 1907-9850
KAPASITAS ANTIOKSIDAN SENYAWA GOLONGAN TRITERPENOID PADA DAUN PRANAJIWA (Euchresta horsfieldii lesch benn)
Kadek Ayu Intan Sari, I Wayan Gede Gunawan, dan Ketut Gede Dharma Putra
Jurusan Kimia FMIPA Universitas Udayana, Bukit Jimbaran, Bali
Email : gede_gunawan@unud.ac.id
ABSTRAK
Telah dilakukan isolasi, identifikasi, dan uji aktivitas antioksidan senyawa golongan triterpenoid pada daun pranajiwa (Euchresta horsfieldii lesch benn). Maserasi 600 g serbuk kering daun pranajiwa dengan pelarut n-heksana menghasilkan 6,1 g ekstrak kental n-heksana. Skrining fitokimia dengan pereaksi Lieberman-Burchard menunjukkan reaksi positif untuk triterpenoid dengan perubahan warna dari kuning menjadi merah ungu. Pemisahan dengan kromatografi kolom diperoleh 3 kelompok fraksi (F1, F2, dan F3), ketiga kelompok fraksi tersebut dilakukan uji triterpenoid. Fraksi yang positif triterpenoid (F1) menghasilkan isolat sebanyak 2 g yang berwarna kuning. Hasil identifikasi menggunakan spektrofotometer inframerah menunjukkan bahwa isolat diduga mengandung senyawa triterpenoid dengan karakteristik gugus fungsi –OH, –CH, C=O, –C=C, –CH2, –CH3, dan C–O alkohol, serta memberikan serapan maksimum di daerah UV-Vis pada panjang gelombang 217 nm. Hasil uji aktivitas antioksidan terhadap isolat triterpenoid memberikan presentase peredaman DPPH sebesar 94,67 %. Hal ini menunjukkan bahwa isolat triterpenoid pada daun pranajiwa memiliki potensi sebagai antioksidan.
Kata kunci : Kapasitas Antioksidan, Euchresta horsfieldii lesch benn, Triterpenoid
ABSTRACT
Isolation, identification, and anti-oxidant assay of triterpenoid compound from Euchresta horsfieldii lesch benn) have been conducted. Maseration of 600 g pranajiwa leaves powder with n-hexane produced 6,1 g n-hexane extract which gave yellow to purple colour change with Lieberman-Burchard reagent. The separation with column chromatography using silica gel 60 obtained 3 fractions (F1, F2, F3) which were then analyzed with triterpenoid test. The positive fraction of triterpenoid (F1) produced 2 g yellow isolate. Infrared spectra indicated that the isolate was a triterpenoid, with characteristic functional groups of OH, –CH, C=O, –C=C, –CH2, –CH3, and C–O alcohol. Ultraviolet-visible spectra showed broad peak at 217 nm. The result of anti-oxidant capacity test of triterpenoid was 94,67%, showing that triterpenoid from pranajiwa leaves can be use as an anti-oxidant.
Keywords : Antioxidant Capacity, Euchresta horsfieldii lesch benn, Triterpenoid
PENDAHULUAN
Spesies tanaman di Indonesia diketahui memiliki ragam khasiat sebagai obat tradisional. Keanekaragaman yang dimiliki Indonesia dapat digunakan sebagai pustaka kimia alam yang dapat diberdayakan secara maksimal melalui proses isolasi senyawa aktif maupun skrining bioaktivitasnya (Farnsworth,1996; Hariana, 2004).
Salah satu keanekaragaman hayati yang dapat dimanfaatkan sebagai obat tradisional adalah tanaman Pranajiwa (Euchresta horsfieldii lesch benn). Tanaman pranajiwa dapat digunakan untuk melegakan pernapasan yang tersumbat, penyakit asma, batuk darah, batuk kering maupun gangguan rongga dada lainnya. Sedangkan kegunaan lainnya bisa dimanfaatkan sebagai penawar bisa ular dan alfrodisiakum, yakni mampu meningkatkan gairah seksual (Heyne, 1987; Kloppenburgh, 2006).
Berdasarkan uji pendahuluan yang telah dilakukan menunjukkan bahwa dalam ekstrak daun pranajiwa mengandung senyawa steroid dan triterpenoid. Secara kualitatif, intensitas perubahan warna untuk reaksi golongan triterpenoid sangat kuat dengan reaksi fitokimia. Selain mengandung triterpenoid diduga dalam daun pranajiwa juga mengandung senyawa antioksidan alami yang sangat tinggi sebesar 126,94 ppm (Tirta,2010). Hal ini didukung pula oleh hasil penelitian yang telah dilakukan pada biji pranajiwa dengan nilai kapasitas antioksidan sebesar 82,90% (Gunawan, 2013).
Berdasarkan hasil uji pendahuluan yang telah dilakukan, maka penulis tertarik melakukan penelitian untuk mengisolasi dan mengidentifikasi senyawa golongan triterpenoid dari daun pranajiwa serta menguji kapasitas antioksidan.
MATERI DAN METODE
Bahan
Bahan yang digunakan dalam penelitian ini adalah daun tumbuhan Pranajiwa (Euchresta hors-feildii (Lesch.) Benn), yang diperoleh dari daerah Pemogan Denpasar Selatan, Bahan- bahan kimia yang digunakan dalam penelitian ini adalah n-heksana, kloroform, etilasetat, DPPH (1,1-Difenil-2-pikril hidrasil), silika gel GF254 untuk kromatografi lapis tipis dan silika gel 60 untuk uji kromatografi kolom, kalium bromida (KBr), dan pereaksi uji fitokimia triterpenoid Lieberman-Burchard (asetat anhidrida dan H2SO4 pekat).
Peralatan
Peralatan yang digunakan dalam penelitian ini adalah blender, neraca elektronik, gelas erlenmeyer, gelas beker, batang pengaduk, labu ukur, pipet volume, pipet tetes, kertas saring, aluminium foil, penguap vakum (rotary vacum evaporator), Kromatografi lapis tipis (KLT), kromatografi kolom, Spektrofotometer UV-Vis dan Spektrofotometer IR.
Cara Kerja
Ekstraksi Pada Daun Pranajiwa
Sebanyak 600 g daun pranajiwa dipotong kecil-kecil kemudian diblender hingga berbentuk serbuk. Serbuk ini kemudian dimaserasi menggunakan pelarut n-heksana selama ± 24 jam
kemudian disaring., filtratnya ditampung, dan ampasnya dimaserasi lagi dengan pelarut n-heksana. Ekstrak n-heksana yang didapat dipisahkan dari pelarutnya dengan menggunakan rotary vacuum evaporator sehingga didapat ekstrak kental n-heksana dan ditimbang beratnya.
Kromatografi Lapis Tipis dan Kromatografi Kolom
Sebelum pemisahan dengan kromatografi kolom, terlebih dahulu dilakukan kromatografi lapis tipis untuk mencari eluen terbaik yang digunakan pada kromatografi kolom. Pemilihan eluen dilakukan dengan berbagai sistem pelarut dengan polaritas yang berbeda sehingga menghasilkan pemisahan noda terbanyak dengan harga Rf yang relatif baik.
Pemisahan pada kromatografi kolom menggunakan fase diam silika gel 60, sedangkan eluen yang digunakan adalah eluen yang memberikan pola terbaik pada analisis KLT. Sebelum sampel dimasukkan, eluen diatur setiap 3 mL dan eluat ditampung setiap 3 mL dalam botol vial. Setelah eluat yang diperoleh kemudian dilihat pola pemisahannya dengan menggunakan plat KLT. Eluat yang mempunyai pola yang sama digabungkan dengan menjadi 1 fraksi. Fraksi yang didapat, diuji dengan pereaksi Lieberman-Burchard. Kelompok fraksi paling positif triterpenoid dapat dilanjutkan dengan uji kemurnian. Jika isolat menunjukkan noda tunggal pada plat KLT menunjukkan isolat relatif murni secara KLT.
Fraksi yang relatif paling baik dan murni (isolat aktif) kemudian diidentifikasi dengan spektrofotometer inframerah (IR) dan ultraviolet-visibel (UV-Vis).
Uji Aktivitas Antioksidan dengan Metode DPPH
Persiapan sampel dilakukan dengan mengencerkan sebanyak 0,08 gram isolat triterpenoid dengan n-heksana pada labu ukur 10 mL sehingga kadarnya 8000 ppm. Kristal DPPH ditimbang sebanyak 0,004 gram untuk dilarutkan dalam n-heksana dengan menggunakan labu ukur 100 mL sehingga kadarnya 0,004 % (b/v). Uji kapasitas antioksidan dilakukan dengan cara 1 mL sampel dimasukkan ke dalam kuvet lalu tambahkan kedalamnya 2 mL larutan DPPH 0,004%. Campuran tersebut kemudian diaduk rata dengan menggunakan pipet. Larutan blanko pada sampel adalah n-heksana. Pencatatan absorbansi
pada panjang gelombang 497 nm, 517 nm, dan 537 nm.
HASIL DAN PEMBAHASAN
Ekstraksi
Hasil maserasi terhadap 600 g serbuk kering daun pranajiwa (Euchresta horsfieldii lesch benn) dengan n-heksana diperoleh ekstrak kental n-heksana berwarna hijau kehitaman seberat 6,1 g. Ekstrak kental n-heksana diuji fitokimia menggunakan pereaksi Lieberman-Burchard menunjukkan positif mengandung senyawa golongan triterpenoid yang dapat dilihat dari perubahan warnanya yaitu kuning menjadi merah ungu.
Kromatografi Kolom
Pemisahan Komponen-komponen aktif pada ekstrak n-heksana dilakukan dengan kromatografi kolom. Dengan silika gel 60 sebagai fase diam, dan fase gerak yang digunakan adalaah campuran eluen terbaik yang diperoleh dari analisis KLT yaitu etil asetat. Hasil pemisahan 1,5 g ekstrak kental n-heksana menghasilkan 60 botol eluat. Eluat-eluat yang diperoleh kemudian yang dianalisis dengan KLT dan eluat-eluat yang mempunyai noda pemisahanyang sama yaitu jumlah noda yang sama dan Rf yang sama digabungkan sehingga diperoleh tiga kelompok fraksi gabungan yaitu fraksi F1, F2, dan F3 dipaparkan pada Tabel 1.
Tabel 1. Hasil pemisahan komponen fraksi n-heksana dengan kromatografi kolom
|
Fraksi (F) |
Berat (g) |
Warna |
Jumlah Noda |
Harga Rf |
|
F1(1-20) |
31,04 |
Kuning |
1 |
0,91 |
|
F2(21-45) |
88,37 |
Abu-Abu |
1 |
0,86 |
|
F3(46-60) |
15,77 |
Hitam |
1 |
0,83 |
Identifikasi
Hasil uji triterpenoid menggunakan pereaksi Lieberman-Burchard terhadap fraksi F1, F2 dan F3 menunjukkan bahwa fraksi F1 positif triterpenoid. Fraksi yang dianalisis lebih lanjut adalah fraksi F1, Karena secara kualitatif intensitas perubahan warna yang dihasilkan pada
penambahan pereaksi Lieberman-Burchard yaitu dari kuning menjadi merah ungu dengan intensitas warna yang kuat. Uji kemurnian terhadap fraksi F1 dengan teknik kromatografi lapis tipis menggunakan beberapa campuran eluen dengan polaritas yang berbeda-beda menunjukkan hasil bahwa fraksi F1 mengandung satu senyawa yang ditunjukkan dengan tidak bertambahnya jumlah noda pada berbagai campuran eluen yang digunakan. Hal ini menunjukkan bahwa fraksi F1 relatif murni secara kromatografi lapis tipis.Hasil uji triterpenoid ketiga kelompok fraksi tersebut dipaparkan pada Tabel 2.
Tabel 2. Hasil uji triterpenoid pada ketiga
kelompok fraksi (F1-F3)
|
Fraksi |
Perubahan warna |
Ket. |
|
F1 |
Kuning menjadi ungu |
+ |
|
F2 |
Abu menjadi hijau |
- |
|
F3 |
Hitam menjadi ungu kehitaman |
- |
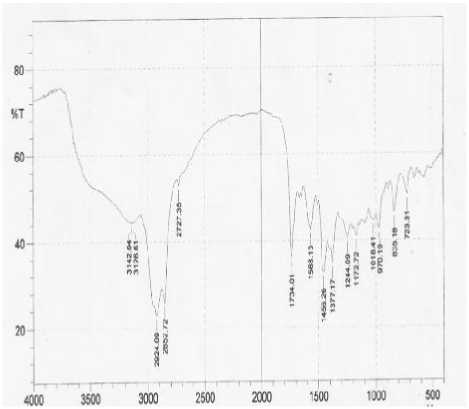
Gambar 1. Spektrum inframerah isolat F1
Isolat aktif triterpenoid ini selanjutnya dianalisis sifat fisikokimianya dengan spektrofotometer inframerah dan ultraviolet-visible. Spektrum inframerah isolat aktif triterpenoid ditunjukkan pada gambar 1, sedangkan data bilangan gelombang, bentuk pita, intensitas, dan penempatan gugus terkait dipaparkan pada Tabel 3.
Tabel 3. Data Spektrum inframerah isolat F1
|
Bilangan Gelombang ʋ (cm-1) |
Bentuk pita |
Intensitas |
Kemungkinan gugus fungsi | |
|
Spektra |
Pustaka | |||
|
3142,04 |
3450-3200 |
Lebar |
Sedang |
-OH terikat (stretching) |
|
2924,09 |
2850-3000 |
Tajam |
Kuat |
-CH alifatik (-CH3stretching) |
|
2852,72 |
2850-3000 |
Tajam |
Kuat |
-CH alifatik (-CH2stretching) |
|
1734,01 |
1650-1900 |
Tajam |
Kuat |
-C=O |
|
1568,13 |
1566-1653 |
Tajam |
Sedang |
-C=C |
|
1456,26 |
1300-1475 |
Tajam |
Kuat |
-CH alifatik (-CH2bending) |
|
1377,17 |
1300-1475 |
Tajam |
Sedang |
-CH alifatik (-CH3bending) |
|
1244,09 |
1300-1000 |
Tajam |
Sedang |
-C-O alkohol (bending) |
Hasil analisis spektra Inframerah menunjukkan adanya pita serapan melebar dengan intensitas kuat pada daerah bilangan gelombang 3142,04 cm-1 yang diduga serapan dari gugus – OH terikat. Adanya gugus –OH ini didukung dengan munculnya serapan kuat pada bilangan gelombang 1244,04 cm-1 dari C–O alkohol. Pita serapan yang tajam dengan intensitas kuat pada bilangan gelombang 2924,09 cm-1 dan 2852,72 cm-1 diduga mengandung gugus –CH alifatik stretching yang biasanya muncul pada daerah bilangan gelombang 2850 cm-1 dan 3000 cm-1. Dugaan ini diperkuat oleh adanya serapan pada daerah bilangan gelombang 1456,26 cm-1 dan 1377,17 cm-1 yang merupakan serapan dari –CH2 dan –CH3 bending. Serapan tajam dengan intensitas kuat pada daerah bilangan gelombang 1734,01 cm-1 diduga karena adanya gugus fungsi C=O (Lambert, dkk, 1976), sedangkan munculnya pita serapan dengan intensitas lemah pada daerah bilangan gelombang 1568,13 cm-1 menunjukkan adanya gugus fungsi C=C alifatik stretching (Silverstein,1981; Sastrohamidjojo, 1991). Hasil dari spektrum inframerah maka isolat diduga mempunyai gugus fungsi O-H, –CH alifatik, C=O dan C=C alifatik, Sedangkan hasil analisis spektrum UV-Vis dari isolat dapat dilihat pada gambar 2.
Hasil analisis isolat dengan menggunakan spektrofotometer UV-Vis memberikan 1 puncak serapan. Munculnya serapan pada panjang gelombang 217 nm diduga diakibatkan oleh adanya transisi elektron n→ π* yang disebabkan oleh adanya suatu kromofor C=O. Hal ini didukung dari hasil inframerah yang menunjukkan isolat mempunyai gugus fungsi C=O pada daerah bilangan gelombang 1734,01cm-1 (Silverstain, 1981; Sastrohamidjojo,1991).
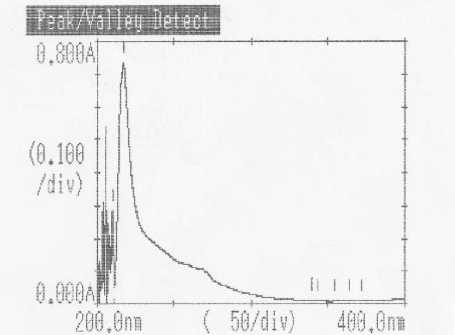
Gambar 2. Spektrum UV-vis dari isolat F1
|
Tabel 4. |
Hasil kapasitas antioksidan ekstrak n-heksana daun pranajiwa |
|
No |
Uji sor ans ( ) AbsorbansiHitung % Peredaman 517 nm 537 nm 497 nm |
|
1 |
DPPH 0,6168 0,4599 0,5901 0,0918 Sampel 0,4243 0,3960 0,4476 0,0025 97,28 % |
|
Tabel 5. |
Hasil kapasitas antioksidan isolat triterpenoid |
|
No |
Uji sor ans ( ) AbsorbansiHitung % Peredaman 517 nm 537 nm 497 nm |
|
1 |
DPPH 0,6168 0,4599 0,5901 0,0918 Sampel 0,3218 0,2685 0,3654 0,0049 94,67 % |
Uji Aktivitas Antioksidan dengan Metode DPPH
Hasil uji antioksidan menunjukkan bahwa ekstrak n-heksana dari isolat F1 aktif sebagai antioksidan karena menunjukkan persentase peredaman yang besar yaitu sebesar 97,28 % untuk ekstrak n-heksana dan persentase peredaman untuk isolat triterpenoid yaitu sebesar 94,67 %. Tingginya aktivitas antioksidan pada ekstrak n-heksana disebabkan karena pada ekstrak n-heksana terdapat lebih dari satu senyawa yang kemungkinan memiliki potensi sebagai antioksidan namun rendahnya aktivitas antioksidan pada isolat aktif disebabkan oleh adanya aktivitas sinergis dari senyawa-senyawa yang terdapat pada ekstrak n-heksana. Suatu bahan dikatakan aktif sebagai antioksidan jika memiliki presentase peredaman lebih besar atau sama dengan 50% (Cooper, 2001).
SIMPULAN DAN SARAN
Simpulan
Isolat (F1) dari ekstrak n-heksana daun pranajiwa diduga mengandung senyawa golongan triterpenoid yang memberikan serapan landai pada panjang gelombang 217 nm dengan transisi elektron n→ π* dan mempunyai gugus-gugus fungsi karakteristik yaitu –OH terikat, –CH, C=O, –C=C, –CH2, –CH3, dan C–O alkohol. Isolat F1 dari daun pranajiwa mempunyai aktivitas antioksidan dengan persentase peredaman sebesar 94,67 % pada 8000 ppm.
Saran
Penelitian lebih lanjut perlu dilakukan untuk menentukan struktur dari isolatetriterpenoid daun pranajiwa dengan menggunakan GCMS. Selain itu Perlu diuji aktivitas lain sehingga dapat menambah informasi tentang keaktifan dari isolat.
UCAPAN TERIMA KASIH
Melalui kesempatan ini penulis menyampaikan banyak-banyak terima kasih kepada Bapak Dr.I Wayan Gede Gunawan,S.Si,M.Si dan Dr. Ketut Dharma Putra,M.Sc atas saran dan masukannya, serta pihak-pihak lain yang telah membantu dalam penyelesaian penelitian ini.
DAFTAR PUSTAKA
Cooper, K. H., 2001, Sehat Tanpa Obat: Empat langkah Revolusi Antioksidan yang mengubah hidup anda, Edisi I, Kaifa, Bandung
Fransworth, N. R., 1966, Biological and Phytochemical Screening of Plant, J. Pharm. Sci, 55 (3) : 225-276
Gunawan, I W. G., 2013, Pemberian Ekstrak Biji Pranajiwa Memperbaiki Kerusakan Sel-Β Pankreas Melalui Penurunan Kadar Glukosa Darah, Advanced Glycation End Product, Malondialdehid, Dan 8-Hidroksi-2- Dioksiguanosin Pada Tikus Wistar Hiperglikemia, Disertasi, Universitas Udayana, Denpasar
Hariana, A., 2004, Tumbuhan Obat dan Khasiatnya, Seri I, Penerbit Swadaya, Jakarta
Heyne, K., Tumbuhan Berguna Indonesia III, Badan Lidbang Departeman Kehutanan, Jakarta
Kloppenburgh – Versteegh, 2006, Tanaman Berkhasiat Indonesia, Volume I., IPB Press, Bogor
Robinson, T., 1995, Kandungan Organik Tumbuhan Tinggi, edisi ke-6, ITB, Bandung
Sastrohamidjojo, H., 1991, Spektroskopi, Liberty, Yogyakarta
Silverstein, R. M., Basler, G.C., dan Morril, T.C., 1991, Spectrometric Identification of Organic compound, John Willey & Sons, Inc, Singapore
Tirta, I. G., I. M. Ardaka., dan I Dw. Pt. Darma., 2010, Studi fenologi dan senyawa kimia pronojiwo (Euchresta horsfieldii (Lesch.) Benn.), Bul, Littro, 21 (1) : 28 -36
66
Discussion and feedback