Review Terapi Bisfosfonat pada Pasien Kanker Payudara, Berapa Lamakah Diberikan?
on

Review Terapi Bisfosfonat pada Pasien Kanker Payudara, Berapa Lamakah
Diberikan?
Ni Gusti Ayu Agung Manik Yuniawaty Wetan*, Hendry Irawan
Divisi Bedah Onkologi, Departemen Ilmu Bedah, Fakultas Kedokteran Universitas Udayana.
*Penulis korespondensi: manikyw@gmail.com.
ABSTRAK
Tujuan: Untuk mengetahui efektivitas, efek samping serta durasi yang optimal dalam pemberian bisfosfonat pada pasien kanker payudara. Metode: Pencarian komprehensif dilakukan pada database PubMed, Science Direct, dan CENTRAL dari tahun 2012 hingga 2022 yang dilakukan selama 10 tahun. Hasil: Tinjauan saat ini, yang termasuk tiga studi randomized controlled trials, yang melibatkan 7.162 kasus kanker payudara, menilai efek bisfosfonat pada risiko kanker payudara serta durasi penggunaan bisfosfonat. Ditemukan adanya pengurangan risiko kanker payudara dengan paparan bisfosfonat. Penggunaan bisfosfonat jangka pendek (<1 tahun) tidak menyebabkan perubahan yang signifikan, sementara penurunan risiko kanker payudara yang signifikan sebesar 26% tercatat dengan penggunaan jangka panjang (>1 tahun). Efek perlindungan bisfosfonat ditunjukkan pada kanker payudara kontralateral. Simpulan: Tinjauan ini menunjukkan bahwa penggunaan bisfosfonat dikaitkan dengan penurunan risiko payudara kanker, termasuk kanker payudara kontralateral. Dibandingkan dengan jenis bisfosfonat lainnya, hanya etidronat yang menunjukkan signifikansi hubungan terbalik. Selain itu, penggunaan bisfosfonat jangka panjang (>1 tahun) lebih signifikan dalam mengecilkan risiko kanker payudara.
Kata kunci: bifosfonat, kanker payudara, terapi adjuvan, efek samping, efikasi.
DOI: https://doi.org/10.24843/JBN.2023.v07.i01.p05
ABSTRACT
Aim: To determine the effectiveness, side effects and optimal duration of bisphosphonate administration in breast cancer patients. Methods: A comprehensive search was performed on the PubMed, Science Direct, and CENTRAL databases from 2012 to 2022 over a 10 years period. Results: The current review, which included three randomized controlled trials, involving 7,162 cases of breast cancer, assessed the effect of bisphosphonates on breast cancer risk and duration of bisphosphonate use. Found a reduction in the risk of breast cancer with bisphosphonate exposure. Short-term (<1 year) bisphosphonate use resulted in no significant change, while a significant 26% reduction in breast cancer risk was noted with long-term use (>1 year). The protective effect of bisphosphonates has been demonstrated in contralateral breast cancer. Conclusion: This review shows that bisphosphonate use is associated with a reduced risk of breast cancer, including cancer of the contralateral breast. Compared with other types of bisphosphonates, only etidronate showed a significant inverse relationship. In addition, long-term use of bisphosphonates (> 1 year) is more significant in reducing breast cancer risk.
Keywords: bisphosphonate, breast cancer, adjuvant therapy, adverse event, efficacy.
PENDAHULUAN terutama di kalangan wanita pascamenopause.
Bisfosfonat banyak digunakan untuk Beberapa penelitian in vitro telah mengobati osteoporosis, seperti digunakan menunjukkan bahwa bisfosfonat memiliki untuk mencegah dan mengobati lesi destruktif serangkaian efek antitumor secara langsung tulang yang disebabkan oleh keganasan, dan tidak langsung, seperti induksi apoptosis
30 | JBN (Jurnal Bedah Nasional)
sel tumor, pencegahan adhesi dan invasi tumor, serta penghambatan angiogenesis tumor dan proliferasi sel.1 Selain itu, sebuah studi praklinis menemukan bahwa bisfosfonat dapat menginduksi kematian sel karsinoma payudara dan menghambat proliferasi sel MCF-7 yang sensitif terhadap estrogen, yang membuat bisfosfonat menjadi golongan obat yang menarik untuk dipelajari lebih lanjut untuk pencegahan kanker payudara.2
Sejumlah studi epidemiologi telah menyelidiki hubungan antara penggunaan bisfosfonat dan risiko kanker payudara. Misalnya, wanita yang memiliki risiko kanker payudara invasif dan telah mendapatkan bisfosfonat untuk pengobatan, dimana didapatkan osteoporosis berkurang sebesar 32%. Sebaliknya, Chiang et al. menggunakan data National Health Insurance Research Database (NHIRD), menemukan bahwa bisfosfonat tidak menurunkan risiko kanker payudara, meskipun demikian penelitian ini dilakukan dengan ukuran penelitian yang terbatas dan hasil yang kurang kuat.2,3 Selain itu, dua meta-analisis peer-review diterbitkan secara konsisten melaporkan bahwa penggunaan bisfosfonat dikaitkan dengan adanya penurunan risiko kanker payudara. Namun, publikasi berikutnya dari dua studi besar telah menunjukkan hasil yang berlawanan, dan sejauh ini, penelitian serta tinjauan sistematis belum membahas apakah penggunaan bisfosfonat dapat menurunkan risiko kanker payudara.3
Hingga saat ini, hal tersebut masih menjadi perdebatan yang sedang berlangsung dan telah memberikan dorongan baru oleh studi terbaru tanpa kesimpulan yang jelas. Oleh karena itu, untuk memberikan ringkasan bukti terkini, kami melakukan tinjauan secara sistematis untuk meringkas semua studi saat ini untuk mengukur secara tepat apakah penggunaan bisfosfonat dikaitkan dengan risiko pengurangan kanker payudara dan untuk
mengeksplorasi berbagai jenis efek bisfosfonat pada kanker payudara, durasi penggunaan bisfosfonat, dan efek dari bisfosfonat pada berbagai jenis kanker payudara.
METODE
Tinjauan ini melaporkan penelitian yang mengevaluasi penggunaan bisfosfonat pada pasien kanker payudara dengan melihat manfaat dan efek samping yang ditimbulkan serta mengetahui berapa lama waktu pemberian dari bisfosfonat kepada pasien kanker payudara. Penulisan systematic review ini mengacu pada pedoman preferred reporting for systematic reviews and metaanalysis (PRISMA). Populasi yang terlibat dalam tinjauan ini adalah pasien yang telah terdiagnosis dengan kanker payudara pada berbagai stadium dengan tanpa adanya batasan usia. Luaran yang diharapkan dalam tinjauan ini adalah diketahuinya manfaat dan
efek samping dari pemberian bisfosfonat pada pasien kanker payudara.
Pencarian literatur dilakukan pada database PubMed, Science Direct, dan CENTRAL
dengan seluruh literatur yang digunakan berbahasa Inggris. Pencarian ini dilakukan
dengan mengidentifikasi jurnal yang
diterbitkan dalam jurnal kedokteran selama 10
tahun kebelakang dari Januari 2012 hingga
Juni 2022 yang berfokus pada penelitian
mengenai tentang subjek manusia diidentifikasi menggunakan istilah berikut:
(payudara atau kelenjar
susu),
tumor∗atau
(neoplasma∗atau kanker∗atau (difosfonat∗atau alendronat∗atau clodronate∗atau
karsinoma∗), dan
bisfosfonat∗atau etidronate∗atau zoledronate∗atau
risedronate∗ atau ibandronate∗atau
pamidronate∗atau tiludronate∗).
Data strategi penelusuran dilakukan dengan menerapkan boolean operator yang dikombinasikan dengan kata kunci terkait. Kata kunci yang digunakan dalam penelusuran literatur terkait yaitu bisphosphonate, breast cancer, adjuvant therapy, adverse event, efficacy. Batas pencarian yang ditetapkan untuk penelusuran jurnal adalah jenis desain studi dan periode penerbitan jurnal. Kriteria inklusi dalam systematic review ini adalah 1) jurnal berbahasa Inggris, 2) jurnal dengan teks lengkap, 3) penelitian yang dilakukan pada manusia, dan, 4) penelitian yang terfokus pada penggunaan bisfosfonat pada pasien kanker payudara dengan memperlihatkan hasil dari efektivitas maupun efek samping serta durasi penggunaan yang efektif. Sementara kriteria eksklusi dalam penelitian ini adalah semua penelitian yang tidak memenuhi kriteria inklusi yang disebutkan di atas seperti penelitian pada hewan dan tinjauan.
Pencarian jurnal terkait dilakukan dengan menggunakan kata kunci spesifik. Penyaringan jurnal dilakukan dua kali. Pada penyaringan pertama, jurnal yang didapat akan ditinjau berdasarkan judul, abstrak dan kata kunci. Jurnal terkait dipilih berdasarkan kriteria inklusi, selanjutnya jurnal yang tidak memenuhi kriteria inklusi dan tidak dapat di akses akan di eksklusi secara langsung. Jurnal yang memenuhi kriteria inklusi selanjutnya dilakukan pengunduhan teks lengkap dan dilakukan telaah kritis untuk menilai kualitas jurnal dengan melihat aspek validitas, kepentingan, dan aplikabilitas. Telaah kritis jurnal dilakukan dengan menggunakan systematic review critical appraisal sheets dari centre for evidence based medicine (CEBM).
Jurnal yang kurang mendukung penyusunan tinjauan seperti data tidak lengkap akan secara langsung di eksklusi. Jurnal yang selanjutnya akan digunakan untuk
penyusunan tinjauan ini akan diekstraksi untuk mendapatkan informasi terkait penulis, desain penelitian, metode pemberian intervensi, evaluasi luaran, hasil, dan kesimpulan. Data disarikan secara independen oleh pengulas, dengan ketidaksesuaian ditangani dengan konsensus dan diskusi dengan reviewer ketiga. Informasi berikut dikumpulkan dari masing-masing percobaan termasuk, seperti yang pertama pengarang, tahun terbit, bangsa, rancangan penelitian, periode, database penelitian, usia partisipan, status menopause, jumlah kasus kanker payudara, jumlah partisipan, prevalensi kanker payudara, jenis kanker payudara, jenis bisfosfonat, definisi paparan, ukuran bisfosfonat penggunaan, periode paparan rata-rata.
HASIL
Pada pencarian sistematis yang dilakukan pada tiga database dengan menggunakan kata kunci spesifik yang telah ditetapkan sebelumnya didapatkan 63 jurnal terkait yang selanjutnya duplikat dari jurnal yang serupa dihapus. Penyaringan jurnal dilakukan dengan melakukan tinjauan awal terhadap judul, abstrak, dan kata kunci. Pada penyaringan awal didapatkan 17 jurnal terkait. 22 jurnal lainnya tidak dapat diakses sedangkan 24 jurnal lainnya tidak memenuhi kriteria inklusi yang telah ditetapkan sebelumnya berdasarkan abstrak yang disajikan. Selanjutnya 17 jurnal akan ditinjau berdasarkan teks lengkap dan dilakukan telaah kritis untuk menilai kualitas jurnal. Pada penyaringan kedua ini didapatkan 3 jurnal yang relevan terhadap studi terdahulu. Sehingga terdapat 3 jurnal yang akan ditinjau lebih lanjut dan digunakan dalam penyusunan tinjauan sistematis ini. Jurnal yang digunakan dalam tinjauan ini diterbitkan antara tahun 2012 sampai 2022 dan seluruh studi merupakan penelitian randomized controlled trials. Seluruh penelitian dilakukan pada
wanita yang telah terdiagnosis dengan kanker payudara dengan bebagai stadium dengan setting penelitian dilakukan di rumah sakit.
Total dari tiga studi, termasuk 7.162 wanita dengan kanker payudara, diterbitkan antara 2012 dan 2012, dengan fokus pada bisfosfonat dan risiko kanker payudara. Tabel 1 menunjukkan secara rinci karakteristik studi. terdapat 3 studi yang merupakan studi randomized controlled trials yang digunakan dalam tinjauan ini dan studi tersebut dilakukan di Amerika Serikat, Italia dan Inggris. Dua penelitian melibatkan pasien dengan status pre-menopause dan satu penelitian melibatkan kelompok pasca menopause. Usia rata-rata peserta di studi yang memenuhi syarat bervariasi dari 54,2 hingga 73,5 tahun. Selain itu, Tabel 1 merinci penggunaan bisfosfonat dari studi yang termasuk atau relevan dengan topik. Sehubungan dengan jenis kanker payudara, ketiga studi menggunakan populasi yang berbeda, yaitu kanker payudara dengan stadium berapapun, kanker payudara stadium dini hingga kanker payudara stadium II dan III. Untuk jenis bisfosfonat, zoledronic acid adalah bisfosfonat yang paling banyak digunakan dalam semua penelitian. Dalam hal pengukuran penggunaan bisfosfonat, tiga studi didasarkan pada peserta yang melakukan self-report. Rata-rata penggunaan bisfosfonat pada ketiga studi bervariasi mulai dari 12 bulan, 3 tahun hingga 5 tahun. Hasil yang ditunjukkan pada ketiga studi bervariasi, hal ini juga dipengaruhi oleh populasi yang dilibatkan pada masing-masing studi.
DISKUSI
Bisfosfonat umumnya ditoleransi dengan baik, dengan risiko serius yang relatif rendah. Efek samping gastrointestinal umum terjadi pada pasien yang mendapatkan terapi formulasi oral. Bisfosfonat intravena dikaitkan dengan efek samping toksisitas
ginjal, ketidakseimbangan elektrolit, dan first-infusion acute phase reactions.4 Uji klinis telah mengevaluasi apakah bisfosfonat adjuvant dapat mencegah metastasis kanker payudara dimana beberapa melaporkan perbaikan dalam kekambuhan dan kematian, sementara yang lain tidak menunjukkan manfaat.5
Gralow6 dalam penelitiannya melaporkan tidak ada perbedaan yang signifikan secara statistik dalam efektivitas berdasarkan jenis bisfosfonat. Berdasarkan jenis bisfosfonat, pada mereka yang berusia 55 tahun atau lebih besar atau kurang dari usia 55 dilaporkan tidak adanya perbedaan efektivitas bisfosfonat yang dihasilkan. Toksisitas bisfosfonat dilaporkan relatif rendah dan jumlah toksisitas pada saluran cerna cukup tinggi pada pasien yang menggunakan bisfosfonat oral dan timbulnya rasa nyeri yang dilaporkan lebih tinggi pada pasien yang mendapatkan asam zoledronat dan ibandronat.
Perubahan Coleman7 dalam penelitiannya melaporkan menopause tetap menjadi pengubah pengobatan yang substansial, dengan kejadian yang lebih sedikit pada wanita dengan menopause yang sudah mapan (>5 tahun sejak menstruasi terakhir) yang diobati dengan asam zoledronat. Wanita premenopause dengan kanker payudara reseptor estrogen positif dengan prognosis baik diobati dengan goserelin menginduksi menopause dan kombinasi dengan baik tamoxifen ataupun aromatase inhibitor. Manfaat pada wanita pasca menopause tampaknya berbeda daripada estrogen-receptor tumor primer.
Perrone8 dalam penelitiannya melaporkan zoledronic acid dan letrozole (ZL) secara signifikan meningkatkan disease free survival (DFS) pasien premenopause dengan kanker payudara dini dengan tumor reseptor hormon positif, menjalani ovarian function supression (OFS) dengan triptorelin.
Tabel 1. Karakteristik Studi Hasil Tinjauan
|
Studi |
Status menopause |
Tipe Kanker Payudara |
Tipe Bisphosphonat |
Paparan |
Pelaporan Pengunaan Biphosphonate |
Rata-Rata Waktu Penggunaan |
Hasil |
|
Perrone4 |
Pre-menopause |
Kanker Payudara |
Zoledronic acid |
Semua pasien menerima triptorelin intramuskular 3,75 mg pada awal pengobatan dan kemudian setiap 4 minggu, selama 5 tahun atau sampai usia 55 tahun. Pasien menerima baik T (20 mg/hari secara oral selama 5 tahun), L (2,5 mg/hari selama 5 tahun) atau ZL (Z 4 mg dalam infus intravena selama 15 menit pada awal pengobatan dan setiap 6 bulan ditambah L 2,5 mg/hari, selama 5 tahun). |
self-report |
12 bulan |
Pasien pre-menopause dengan kanker payudara dini menjalani penekanan fungsi ovarium dengan triptorelin, ZL secara signifikan meningkatkan DFS, sementara kepatuhan dan toksisitas yang memburuk, dibandingkan dengan T. |
|
Gralow5 |
Postmenopause |
Kanker payudara stadium dini |
Bisphosphonat |
Pasien dengan kanker payudara stadium I-III diacak hingga 3 tahun dan mendapatkan asam zoledronat intravena, klodronat oral, atau ibandronat oral. |
self-report |
3 tahun |
Mayoritas wanita yang didiagnosis dengan kanker payudara stadium awal akan sembuh, tetapi risiko kekambuhan jauh dan kematian masih ada. |
|
Coleman6 |
Pramenopause, perimenopause, dan status tidak diketahui) |
Stadium II dan III kanker payudara |
Zoledronic acid |
Setelah diagnosis kanker payudara invasif, pasien menerima operasi standar yang sesuai untuk payudara dan perawatan aksila dan adjuvan termasuk pengobatan endokrin untuk penyakit reseptor-estrogen- positif, kemoterapi adjuvan, radioterapi lokoregional, dan, setelah Juni 2005, trastuzumab untuk penyakit HER2+, di sesuai dengan protokol standar dan masing-masing berpartisipasi. |
self-report |
5 tahun |
Tidak ada manfaat keseluruhan dari penambahan asam zoledronat ke bahan pembantu standar pengobatan untuk kanker payudara dini. Namun, asam zoledronat mengurangi perkembangan metastasis tulang dan, untuk wanita dengan menopause yang mapan, hasil penyakit yang lebih baik. |
T: tamoxifen L: letrozole ZL: zoledronic acid dan letrozole
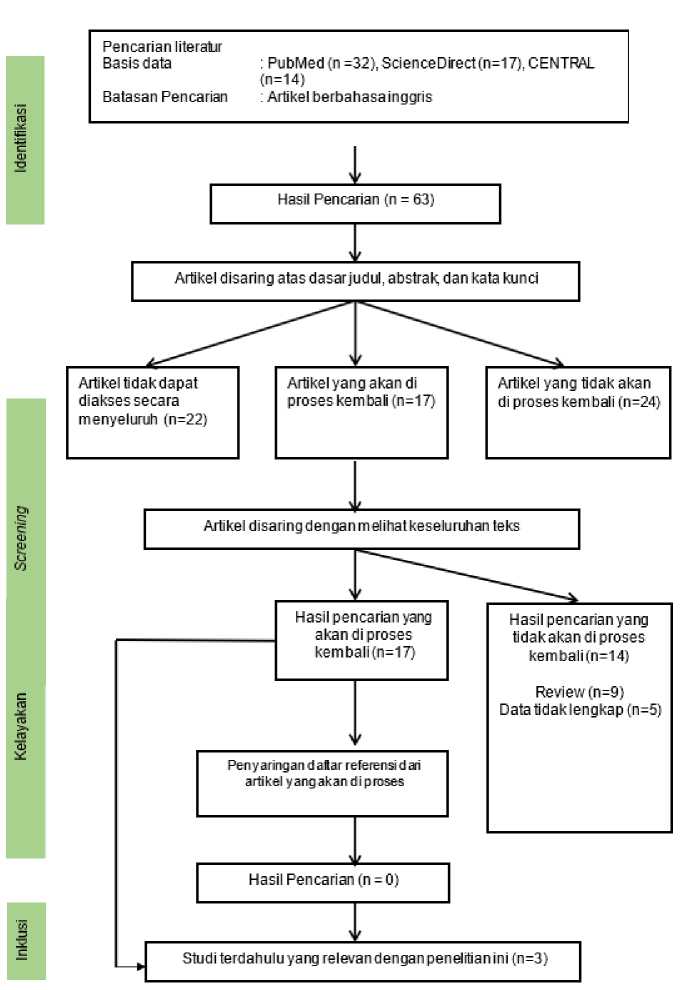
Gambar 1. Bagan Prisma dalam Metode Penyusunan Tinjauan
Dalam sebuah meta analisis melaporkan bahwa adanya efek protektif bisfosfonat pada wanita yang menggunakan bisfosfonat dengan penggunaan jangka panjang (>1 tahun).9,10 Manfaat bervariasi antara berbagai jenis bisfosfonat, khususnya etidronate, yang secara signifikan menurunkan risiko kanker payudara sebesar 13%.9
Secara struktural, bisfosfonat dikategorikan menjadi older first- generation non-nitrogen-containing moieties dan newer second- generation nitrogen-containing
moieties, termasuk etidronate, clodronate, dan tiludronate serta pamidronate, alendronate, ibandronate, risedronate, dan zoledronate.10 Dalam sebuah meta analisis menemukan bahwa hanya etidronate, bukan alendronate, yang menunjukkan efek protektif pada pasien kanker payudara.11
Efektivitas antitumor dari penggunaan bisfosfonat pada risiko kanker payudara diamati hanya setelah lebih dari 1 tahun menerima bisfosfonat. Asosiasi waktu paparan antara bisfosfonat dan risiko kanker
payudara kecenderungan yang hampir linier. Berkenaan dengan apakah menggunakan bisfosfonat dengan jangka panjang sebenarnya bermanfaat untuk risiko kanker payudara, profil efek samping harus dipertimbangkan.12,13
Efek samping dari pengguna bisfosfonat telah dilaporkan, termasuk osteonekrosis rahang, patah tulang femoralis atipikal, fibrilasi atrium, gangguan pencernaan, dan gangguan ginjal.14 Oleh karena itu, efek samping penggunaan bisfosfonat jangka panjang perlu dianalisis lebih lanjut dengan studi prospektif, untuk menentukan apakah manfaat dari terapi benar-benar lebih besar daripada risikonya dan untuk mengoptimalkan waktu penggunaan bisfosfonat.15
Dalam hal efektivitas bisfosfonat untuk kanker payudara dengan berbagai jenis dan stadium, analisis stratifikasi risiko kami menunjukkan bahwa bisfosfonat memiliki efek anti kanker payudara yaitu hanya pada kanker payudara kontralateral (tingkat yang berkurang, 59%) daripada kanker payudara invasif.16
Dalam tinjauan ini jumlah studi yang digunakan cukup terbatas sehingga berpotensi menimbulkan terjadinya bias. Kedepannya diperlukan penelitian yang dapat menjangkau populasi dalam jumlah yang lebih besar sehingga dapat menunjukkan efektivitas dan efek samping dari penggunaan bisfosfonat pada pasien kanker payudara.
SIMPULAN
Paparan bisfosfonat dikaitkan dengan penurunan kejadian kanker payudara, termasuk kanker payudara kontralateral. Dibandingkan dengan jenis bisfosfonat lainnya, hanya etidronate yang menunjukkan hubungan terbalik yang signifikan. Sebagai tambahan, penggunaan bisfosfonat jangka panjang (>1 tahun) lebih signifikan dalam menurunkan risiko kanker payudara.
Diperlukan penelitian longitudinal yang lebih mendalam untuk menghasilkan perkiraan yang lebih tepat mengingat semua perancu potensial, berbagai jenis bisfosfonat, dosis kumulatif, durasi penggunaan bisfosfonat, dan efek bisfosfonat pada berbagai jenis kanker payudara.
UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih yang tulus kepada keluarga dan para pembimbing penelitian.
PERNYATAAN
Tidak ada konflik kepentingan dalam penelitian ini.
DAFTAR PUSTAKA
-
1. Black DM, Rosen CJ. Clinical Practice. Postmenopausal Osteoporosis. N Engl J Med. 2016;374:254-62.
-
2. Van Acker HH, Anguille S, Willemen Y, dkk. Bisphosphonates for cancer treatment: Mechanisms of action and lessons from clinical trials. Pharmacol & Ther. 2016;158:24-40.
-
3. Fournier A, Mesrine S, Gelot A, dkk. Use of Bisphosphonates and Risk of Breast Cancer in a French Cohort of Postmenopausal Women. J Clin Oncol. 2017;35:3230-39.
-
4. Ou YJ, Chiu HF, Wong YH, dkk. Bisphosphonate use and the risk of breast cancer: a meta-analysis of observational studies. Pharmacoepidemiol Drug Saf. 2017;26:1286-95.
-
5. Hue TF, Cummings SR, Cauley JA, dkk. Effect of bisphosphonate use on risk of postmenopausal breast cancer: results from the randomized clinical trials of alendronate and zoledronic acid. JAMA Intern Med. 2014;174:1550-7.
-
6. Gralow JR, Barlow WE, Paterson AHG, dkk. Phase III Randomized Trial of Bisphosphonates as Adjuvant Therapy in Breast Cancer: S0307. J Natl Cancer Inst. 2020;112:698-707.
-
7. Coleman R, Cameron D, Dodwell D, et al. Adjuvant zoledronic acid in patients with early breast cancer: final efficacy analysis of the AZURE (BIG 01/04) randomised open-label phase 3 trial. Lancet Oncol. 2014;15:997-1006.
-
8. Perrone F, De Laurentiis M, De Placido S, dkk. Adjuvant zoledronic acid and letrozole plus ovarian function suppression in premenopausal breast cancer: HOBOE phase 3 randomised trial. Eur J Cancer. 2019;118:178-86.
-
9. Zhang XS, Zhang YM, Li B, dkk. Risk reduction of endometrial and ovarian cancer after bisphosphonates use: A metaanalysis. Gynecol Oncol. 2018;150:509-14.
-
10. Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Adjuvant bisphosphonate treatment in early breast cancer: meta-analyses of individual patient data from randomised trials. Lancet. 2015;386:1353-61.
-
11. Amoroso V, Petrelli F, Pedersini R, dkk. Adjuvant bisphosphonates in patients with breast cancer: does the potency matter? Futur Oncol. 2015;11:2853-6.
-
12. Francis PA, Pagani O, Fleming GF, dkk. Tailoring Adjuvant Endocrine Therapy
for Premenopausal Breast Cancer. N Engl J Med. 2018;379:122-37.
-
13. Coleman RE, Finkelstein D, Barrios C, dkk. Adjuvant denosumab in early breast cancer: First results from the international multicenter randomized phase III placebo controlled D-CARE study. J Clin Oncol. 2018;36:501.
-
14. Pan H, Gray R, Braybrooke J, dkk. 20-Year Risks of Breast-Cancer Recurrence after Stopping Endocrine Therapy at 5 Years. N Engl J Med. 2017;377:1836-46.
-
15. Gnant M, Pfeiler G, Steger GG, dkk. Adjuvant denosumab in postmenopausal patients with hormone receptor-positive breast cancer (ABCSG-18): disease-free survival results from a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2019;20:339-51.
-
16. Coleman R, Hall A, Albanell J, dkk. Effect of MAF amplification on treatment outcomes with adjuvant zoledronic acid in early breast cancer: a secondary analysis of the international, open-label, randomised, controlled, phase 3 AZURE (BIG 01/04) trial. Lancet Oncol. 2017;18:1543-52.
37

Discussion and feedback