PENGARUH WAKTU MASERASI TERHADAP AKTIVITAS ANTIOKSIDAN EKSTRAK RIMPANG TEMULAWAK (Curcuma xanthorriza Roxb.)
on
ISSN : 2527-8010 (ejournal)
Jurnal Ilmu dan Teknologi Pangan Vol. 7, No.4, 165-174, Desember 2018
PENGARUH WAKTU MASERASI TERHADAP AKTIVITAS ANTIOKSIDAN EKSTRAK RIMPANG TEMULAWAK (Curcuma xanthorriza Roxb.)
The Effect of Maceration Time on Antioxidant Activity of Java Turmeric (Curcuma Xanthorriza Roxb.) Rhizome Extract
Ega Amelinda¹), I Wayan Rai Widarta²), Luh Putu Trisna Darmayanti²) ¹)Mahasiswa Program Studi Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Unud ²)Dosen Program Studi Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Unud Kampus Bukit Jimbaran, Badung-Bali
ABSTRACT
This research aimed to find effect of maceration time on antioxidant activity of java turmeric rhizome extract and to get the right maceration time with highest antioxidant activity of java turmeric rhizome extract. This study used The Completely Randomized Design with the treatment of maceration time of 6 levels: 18 hours, 24 hours, 30 hours, 36 hours, 42 hours and 48 hours. The experiment was repeated in three replication, so that 18 experimental units were obtained. Data were analyzed by Analysis of Variance (ANOVA) and then continued with Duncan Multiple Range Test (DMRT). The result showed that the treatment of maceration time had very significant effect on extraction yield, total curcumin, total phenol and antioxidant activity of java turmeric rhizome extract. The best treatment was 24 hours with extraction yield was 18.88%, total phenol 205.86 mg GAE/g, total curcumin 21.22 mg/g extract, antioxidant activity 84.45% and IC50 36.96 mg/L.
Keywords : curcumin, antioxidant activity, maceration time, java turmeric.
PENDAHULUAN
Indonesia merupakan salah satu negara agraris yang sebagian besar penduduknya bertumpu pada bidang pertanian. Salah satu komoditas bahan alam andalan Indonesia yakni temulawak (Curcuma xanthorriza Roxb.) (Anggoro et al., 2015).Produksi temulawak di Indonesia pada tahun 2015 tercatat sebanyak 27.840.185 kg(Anon., 2015). Temulawak masih sangat berpotensi untuk dikembangkan karena memiliki bahan aktif kurkumin di dalamnya. Kurkumin termasuk senyawa fenolik yang memberikan pigmen berwarna kuning yang diperoleh dari rimpang tanaman family Jahe (Zingiberaceae) (Akram et al., 2010).
Menurut Hayani (2006) dari hasil analisis
mutu rimpang temulawak secara kuantitatif diperoleh kadar kurkuminnya sebesar 2,29 % sedangkan secara kualitatif diketahui bahwa di dalam rimpang temulawak terdapat alkaloid, flavonoid, fenolik, saponin, triterpennoid dan glikosida. Rimpang temulawak mengandung antioksidan. Komponen senyawa yang bertindak sebagai antioksidan dari rimpang temulawak adalah fenol dan kurkumin (Jayaprakhasha et al., 2006). Rao (1997) melaporkan bahwa kurkumin dapat berperan sebagai antioksidan karena mampu menangkal radikal hidroksil, anion superoksida, dan oksigen singlet.
Fenolik merupakan senyawa metabolit sekunder yang dapat disintesis tumbuhan, sebagai respon terhadap berbagai kondisi antara lain infeksi dan radiasi UV (Arif dan
*Korespondensi Penulis:
Email: egaamelinda03@gmail.com1
Tukiran, 2015). Senyawa fenolik telah banyak diteliti sebagai senyawa yang bertanggungjawab terhadap berbagai aktivitas biologis tanaman, salah satunya yaitu antioksidan (Cartea et al., 2011). Hasil penelitian Nurcholis dan Bintang (2017) menyatakan bahwa temulawak memiliki kandungan total fenolik dan aktivitas antioksidan yang lebih tinggi dibandingkan dengan temu ireng.
Ekstrak temulawak dapat dimanfaatkan sebagai pewarna alami pada pengolahan makanan, minuman instan temulawak dan tablet effervecent. Cara untuk mendapatkan ekstrak temulawak dapat dilakukan dengan ekstraksi. Ekstraksi adalah proses pemisahan komponen-komponen dalam larutan berdasarkan perbedaan kelarutannya. Faktor– faktor yang mempengaruhi laju ekstraksi adalah tipe persiapan sampel, waktu ekstraksi, jumlah sampel, suhu, dan jenis pelarut (Utami, 2009).Selama proses ekstraksi, bahan aktif akan terlarut oleh zat penyari yang sesuai sifat kepolarannya. Ekstraksi dapat dilakukan dengan metode maserasi. Maserasi merupakan metode sederhana yang paling banyak digunakan. Cara ini sesuai, baik untuk skala kecil maupun skala industri (Agoes, 2007). Metode maserasi dapat menghindari rusaknya senyawa-senyawa yang bersifat termolabil (Mukhriani, 2014).
Maserasi dilakukan dengan memasukkan bubuk tanaman dan pelarut yang sesuai ke dalam wadah inert yang tertutup rapat pada suhu kamar. Pelarut yang dapat digunakan untuk ekstraksi senyawa bioaktif pada temulawak salah satunya adalah etanol. Etanol merupakan pelarut organik dengan polaritas medium dengan sifat mudah menguap. Somaatmadja (1981) menyatakan bahwa etanol merupakan pelarut paling aman karena tidak beracun. Menurut Hayani (2006), ekstrak rimpang temulawak terbanyak diperoleh dengan menggunakan pelarut alkohol yaitu sebesar 20,40% sedangkan dengan menggunakan heksan diperoleh ekstrak
sebesar 8,20% dan etil asetat sebesar 17,00%.Penggunaan etanol untuk ekstraksi kurkumin dan fenol telah dilaporkan oleh Hincapie et al. (2011) padakunyit (Curcumadomestica) yang menghasilkantotal fenol dan aktivitas antioksidan yang lebih tinggi dari petroleum eter. Hasil penelitian Prasetya dan Yuliani (2014) melaporkan bahwa kurkumin pada ekstrak temulawak yang diperoleh sebesar 16,40% dengan menggunakan pelarut etanol 80% dengan lama waktu ekstraksi 28 jam dan perbandingan ekstrak dengan pelarut adalah 1:4.
Menurut Budiyanto dan Yulianingsih (2008) waktu ekstraksi sangat berpengaruh terhadap senyawa yang dihasilkan. Waktu maserasi yang tepat akan menghasilkan senyawa yang optimal.Waktu maserasi yang terlalu singkat dapat mengakibatkan tidak semua senyawa terlarut dalam pelarut yang digunakan. Fauzana (2010) melaporkan bahwa hasil rendemen ekstrak rimpang temulawak dengan waktu maserasi kurang dari 18 jam menghasilkan rendemen yang rendah yaitu dibawah 12,60%. Lebih lanjut dilaporkan bahwa semakin lama waktu maserasi yaitu dari 4 jam hingga 24 jam, hasil rendemen ekstrak semakin meningkat. Menurut Ramdja et al., 2009 melaporkan bahwawaktu maserasi yang terlalu lama tidak akan berpengaruh lagi karena jumlah pelarut dalam zat terlarut telah jenuh . Oleh karena itutujuan dari penelitian ini adalah untuk mengetahui pengaruh waktu maserasi terhadap aktivitas antioksidan ekstrak rimpang temulawak dan mendapatkan waktu maserasi yang tepat sehingga menghasilkan ekstrak rimpang temulawak dengan aktivitas antioksidan tertinggi.
METODE PENELITIAN
Bahan dan Alat
Bahan yang digunakan adalah rimpang temulawak yang diperoleh dari petani temulawak di Kecamatan Gondang, Kabupaten Mojokerto, Jawa Timur dengan
umur panen 9 bulan. Bahan kimia yang digunakan adalah etanol 80 %
(Merck),aquadest, 1,1-diphenyl-2-
picrylhydrazil (DPPH) (SigmaAldrich),etanol PA (Merck), reagen Folin Ciocalteu (Merck), natrium karbonat (Merck), dan Kurkumin (Merck).
Alat yang digunakan yaitu oven (Labo DO 225), pisau, blender (Philip), kertas saring Whatman no.1, timbangan analitik (Shimadzu ATY224), aluminium foil, ayakan 60 mesh, mikropipet (Socorex), vortex, rotary vacuum evaporator (Ika Labortechnik),
spektrofotometer UV –Vis (Genesys 10s Uv-Vis), rak tabung, corong dan alat-alat gelas lainnya.
Rancangan Percobaan
Penelitian ini menggunakan rancangan acak lengkap (RAL) dengan perlakuan waktu ekstraksi. Perlakuan waktu ekstraksi (W) terdiri dari 6 taraf yaitu : W1 : 18 jam, W2 : 24 jam, W3 : 30 jam, W4 : 36 jam, W5 : 42 jam dan W6 : 48 jam. Perlakuan ini diulang
sebanyak 3 kali sehingga diperoleh 18 unit percobaan. Data dianalisis menggunakan metode analisis ragam (Analysis of Variant atau ANOVA), apabila terdapat pengaruh antar perlakuan terhadap parameter yang diamati maka dilanjutkan dengan uji Duncan (Steel and Torrie, 1993).
Pelaksanaan Penelitian
Pembuatan Bubuk Temulawak
Temulawak segar dipilih dan dicuci hingga bersih kemudian di angin-anginkan selama ± 15 menit. Setelah itu temulawak diiris dengan ketebalan ± 1 mm lalu dikeringkan
menggunakan oven dengan suhu 55ºC selama 24 jam selanjutnya diblender hingga halus lalu diayak dengan menggunakan ayakan 60 mesh dan diapatkan bubuk temulawak. (Widarta dan Arnata (2017), yang dimodifikasi).
Proses Pembuatan Ekstrak Rimpang Temulawak
Ekstraksi dilakukan dengan metode maserasi. Ditimbang sebanyak 10 gram bubuk sampel, kemudian di masukkan kedalam erlenmeyer. Ditambahkan pelarut etanol 80% sebanyak 100 ml atau perbandingan sampel dengan pelarutnya adalah 1:10. Erlenmeyer ditutup dengan aluminium foil kemudian dimaserasi pada suhu kamar sesuai perlakuan yaitu waktu maserasi 18 jam, 24 jam, 30 jam, 36 jam, 42 jam dan 48 jam. Selanjutnya disaring menggunakan kertas saring Whatman no. 1. Filtrat yang diperoleh kemudian dipekatkan dengan rotary vacuum merk IKA dengan suhu 40ºC dan tekanan 100 mBar dan didapatkan ekstrak kasar (Widarta dan Arnata (2014), yang dimodifikasi).
Variabel yang Diamati
Variabel yang diamati dalam penelitian ini, diantaranya adalah rendemen (AOAC, 1999), kadar total kurkumin (Harini et al., 2012), kadar total fenol dengan metode Folin-Ciocalteau (Garcia et al., 2007), dan aktivitas antioksidan dengan metode DPPH (Shah dan Modi, 2015)
HASIL DAN PEMBAHASAN
Rendemen
Hasil analisis ragam menunjukkan bahwa waktu maserasi berpengaruh sangat nyata terhadap rendemen ekstrak (P<0,01). Grafik hasil pengaruh waktu maserasi terhadap rendemen ekstrak dapat dilihat pada Gambar 1.
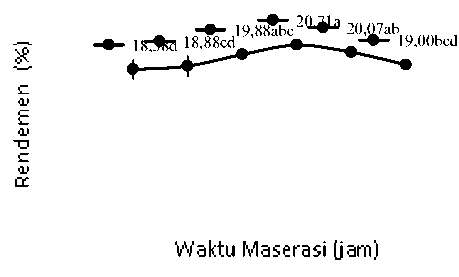
Gambar 1. Grafik hubungan antara waktu maserasi terhadap rendemen (%)
Keterangan : Notasi yang berbeda pada kolom yang sama menunjukkan
perlakuan berpengaruh nyata (P<0,05).
Gambar 1. menunjukkan bahwa rendemen tertinggi diperoleh dari perlakuan dengan waktu maserasi 36 jam yaitu 20,70% yang tidak berbeda nyata dengan rendemen ekstrak dari perlakuan waktu maserasi selama 30 jam dan 42 jam yaitu sebesar 19,88% dan 20,07%. Rendemen terendah diperoleh dari perlakuan waktu maserasi 18 jam yaitu 18,58% yang tidak berbeda nyata dengan rendemen ekstrak dari perlakuan waktu maserasi selama 24 jam dan 48 jam yaitu sebesar 18,,88% dan 19,00%. Hasil rendemen temulawak pada penelitian ini lebih tinggi dibandingkan hasil rendemen kunyit yang dilaporkan oleh Dewi et al. (2016) dengan waktu maserasi 24 jam menggunakan pelarut etanol 96% menghasilkan rendemen sebesar 18,17%.
Semakin lama waktu ekstraksi maka semakin tinggi rendemen yang dihasilkan hingga mencapai titik optimum ekstraksi, setelah mencapai titik optimum hasil rendemen mengalami penurunan. Utami (2009) melaporkan bahwa waktu ektraksi yang terlalu lama dan melewati batas optimum proses ekstraksi akan menyebabkan rusaknya senyawa fitokimia yang terekstrak sehingga mempengaruhi hasil ekstrak yang
didapatkan.Srijanto (2010) menyatakan bahwa semakin lama waktu ekstraksi yang digunakan, waktu kontak antara sampel dan pelarut semakin lama sehingga jumlah senyawa yang terekstraksi semakin banyak. Kondisi ini akan terus berlanjut hingga tercapai kondisi kesetimbangan antara konsentrasi senyawa didalam bahan baku dengan konsentrasi senyawa di pelarut. Waktu maserasi yang melewati waktu optimum akan merusak zat terlarut yang ada didalam bahan dan berpotensi meningkatkan proses hilangnya senyawa-senyawa pada larutan karena penguapan (Cikita et al., 2016)
Total Fenol
Hasil analisis ragam menunjukkan bahwa waktu maserasi berpengaruh sangat nyata (P<0,01) terhadap total fenol ekstrak rimpang temulawak. Grafik hasil pengaruh waktu maserasi terhadap total fenol dapat dilihat pada Gambar 2.
Waktu Maserasi Qam)
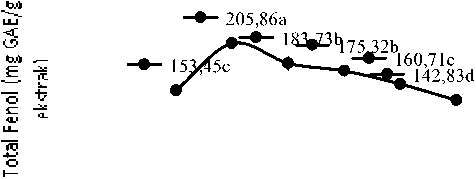
Gambar 2. Grafik hubungan antara waktu maserasi terhadap total fenol (mg GAE/g ekstrak)
Keterangan : Notasi yang berbeda pada kolom yang sama menunjukkan perlakuan berpengaruh nyata (P<0,05).
Gambar 2 menunjukkan total fenol tertinggi terdapat pada perlakuan waktu maserasi selama 24 jam (W2) yaitu 205,86 mg GAE/g dan total fenol terendah terdapat pada perlakuan waktu maserasi paling lama yaitu 48 jam (W6) sebesar 142,83 mg GAE/g ekstrak.Waktu ekstraksi sangat berpengaruh terhadap kadar total fenolik ekstrak rimpang
temulawak. Hal ini sesuai dengan yang dilaporkan Devi dan Arumughan (2007) bahwa waktu maserasi berpengaruh terhadap rendemen ekstrak senyawa fitokimia termasuk senyawa fenolik. Semakin lama waktu ekstraksi menyebabkan semakin banyak senyawa fenol yang larut kedalam pelarut sampai titik tertentu.
Menurut Kemit et al. (2015) semakin lama waktu maserasi maka kesempatan kontak antara bahan dan pelarut semakin besar sehingga hasilnya akan terus meningkat sampai pada titik jenuh dari pelarut tersebut. Waktu ekstraksi yang singkat belum menunjukkan reaksi yang optimal terhadap senyawa fenolik (Tananuwong dan Tewaruth, 2010). Penurunan kadar total fenol setelah waktu maserasi 24 jam mengindikasikan adanya kemungkinan senyawa fenol mengalami kerusakan atau terdegradasi seiring dengan lamanya waktu ekstraksi. Peningkatan waktu ekstraksi menaikkan kemungkinan terjadinya dekomposisi atau oksidasi senyawa fenolik karena kontak yang relative lama dengan faktor lingkungan seperti oksigen (Kristiani dan Halim, 2014).
Total Kurkumin
Hasil analisis ragam menunjukkan bahwa waktu maserasi berpengaruh sangat nyata (P<0,01) terhadap total kurkumin ekstrak rimpang temulawak. Grafik hasil pengaruh waktu maserasi terhadap total kurkumin dapat dilihat pada Gambar 3.
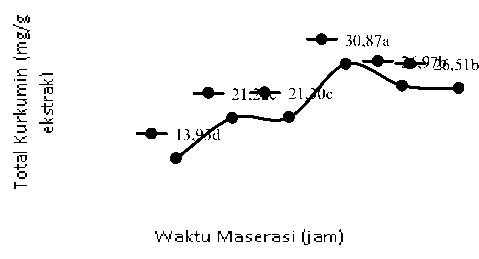
Gambar 3. Grafik hubungan antara waktu maserasi terhadap total kurkumin
(mg/g ekstrak)
Keterangan : Notasi yang berbeda pada kolom yang sama menunjukkan perlakuan berpengaruh nyata (P<0,05).
Gambar 3 menunjukkan total kurkumin tertinggi terdapat pada perlakuan waktu maserasi 36 jam (W4) yaitu 30,87 mg/g ekstrak dan total kurkumin terendah terdapat pada perlakuan waktu maserasi paling singkat yaitu 18 jam (W1) sebesar 13,93 mg/g ekstrak.
Senyawa kurkumin mengalami peningkatan pada waktu maserasi 18 sampai 36 jam. Semakin lama waktu ekstraksi, maka kadar total kurkumin yang diperoleh semakin besar. Hal ini disebabkan karena waktu kontak antara kurkumin dengan pelarutnya semakin lama. Kondisi ini akan terus berlanjut hingga waktu kontak yang diperlukan pelarut dengan bahan sudah cukup dan mencapai kesetimbangan (Harjanti, 2008).
Hasil penelitian menyatakan bahwa kontak yang terlalu lama yaitu lebih dari 36 jam menyebabkan kandungan kurkumin semakin menurun. Hal ini disebabkan oleh kontak kurkumin yang semakin lama dengan oksigen mengakibatkan laju oksidasi meningkat. Degradasi kurkumin dapat terjadi karena reaksi autooksidasi (Zhu, 2016). Degradasi kurkumin menghasilkan produk utama yaitu biciclopentadion. Biciclopentadion adalah senyawa radikal yang terbentuk dari oksigenasi dan siklus berulang dari rantai heptadiendion yang berhubungan dengan dua cincin metoksi fenol dari kurkumin (Schneider et al., 2016).
Aktivitas Antioksidan
Aktivitas antioksidan ditentukan
menggunakan metode DPPH. Hasil analisis ragam menunjukkan bahwa waktu maserasi berpengaruh sangat nyata (P<0,01) terhadap aktivitas antioksidan ekstrak rimpang
temulawak. Grafik hasil pengaruh waktu maserasi terhadap aktivitas antioksidan dapat dilihat pada Gambar 4.
dapat dilihat pada Gambar 5.
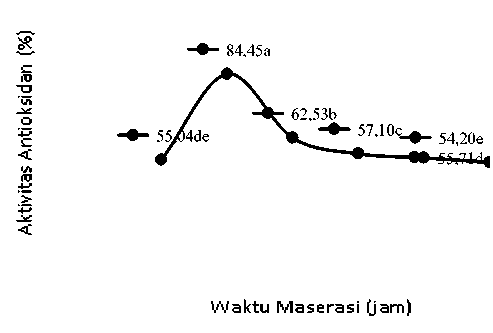
Gambar 4. Grafik hubungan antara waktu maserasi terhadap aktivitas
antioksidan (%)
Keterangan : Notasi yang berbeda pada kolom yang sama menunjukkan perlakuan berpengaruh nyata (P<0,05).
Gambar 4 menunjukkan aktivitas antioksidan tertinggi diperoleh pada perlakuan waktu maserasi selama 24 jam (W2) yaitu sebesar 84,45% dan aktivitas terendah terdapat pada perlakuan waktu maserasi paling lama yaitu 48 jam (W6) sebesar 54,20%. Namun hasil aktivitas antioksidan perlakuan waktu maserasi 48 jam tidak berbeda nyata dengan aktivitas antioksidan waktu maserasi 18 jam yaitu sebesar 55,04%. Aktivitas antioksidan semakin tinggi hingga mencapai hasil optimal pada waktu maserasi 24 jam, setelah waktu maserasi 24 jam aktivitas antioksidan mengalami penurunan.
Aktivitas antioksidan meningkat seiring dengan meningkatnya total fenolik yang terdapat pada ekstrak, namun setelah mencapai hasil optimum maka aktivitas antioksidan akan menurun selaras dengan penurunan total fenolik. Hasil penelitian menunjukkan bahwa terdapat korelasi yang positif antara aktivitas antioksidan dengan total fenolik. Korelasi aktivitas antioksidan dengan total fenolik
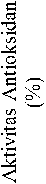
y = 0.451x - 15.301
R² = 0.7827
∙. ∙* ∙
Total Fenolik (mg GAE/g)
Gambar 5. Grafik hubungan antara total fenolik (mg GAE/g ekstrak) terhadap aktivitas antioksidan (%)
Gambar 5 menyatakan bahwa semakin tinggi total fenolik maka aktivitas antioksidan juga semakin meningkat. Kaur dan Kapoor (2002) menyatakan bahwa senyawa fenolik memiliki berbagai efek biologis seperti aktivitas antioksidan melalui mekanisme sebagai pereduksi, penangkap radikal bebas, pengkelat logam, peredam terbentuknya oksigen singlet serta pendonorelektron.
Menurut Sarwono (2006) koefisien korelasi (R2) yang mempunyai nilai >0,75-0,99 dapat dikategorikan sebagai berkorelasi sangat kuat. Berdasarkan data yang diperoleh, koefisien korelasi (R2) antara total fenolik dan aktivitas antioksidan ekstrak rimpang temulawak yaitu 0,78. Khadijah et al. (2017) juga melaporkan bahwa aktivitas antioksidan daun samama memiliki koefisien korelasi yang positif terhadap total fenolik dengan nilai koefisien korelasi (R2) sebesar 0,9996.
Kurkumin juga berpengaruh terhadap aktivitas antioksidan ekstrak rimpang temulawak. Penelitian Jitoe et al. (1992) menunjukkan bahwa aktivitas antioksidan ekstrak temulawak lebih besar dibandingkan dengan aktivitas antioksidan tiga jenis kurkuminoid yang diperkirakan terdapat dalam temulawak. Hal ini diduga terdapat zat lain selain ketiga kurkuminoid tersebut yang
mempunyai efek antioksidan di dalam ekstrak temulawak. Menurut Hayani (2006) dari hasil pengujian skrining fitokimia terlihat dalam rimpang temulawak terdapat kandungan alkaloid, flavonoid, fenolik, triterpenoid. Sesuai dengan penelitian Kurniati (2013) senyawa flavonoid, fenolik, dan alkoloid yang terdapat pada fraksi etanol 70% daun buas-buas (Premna cordifolia Linn.) diperkirakan merupakan senyawa yang bertanggung jawab terhadap aktivitas antioksidan daun buas-buas. Berdasarkan penelitian yang dilakukan oleh Ismarti (2011), senyawa triterpenoid pada kulit batang meranti merah (Shorea singkawang (Miq).Miq) yang diuji dengan radikal DPPH memiliki aktivitas antioksidan kuat dengan nilai IC50 sebesar 82 ppm.
IC50
Berdasarkan hasil analisis aktivitas antioksidan, diperoleh bahwa perlakuan waktu maserasi 24 jam memiliki persentase aktivitas antioksidan tertinggi sehingga perlakuan ini dipilih untuk uji lanjutan yaitu penentuan IC50.Hasil pengujian aktivitas antioksidan ekstrak rimpang temulawak dapat dilihat pada Gambar 6.
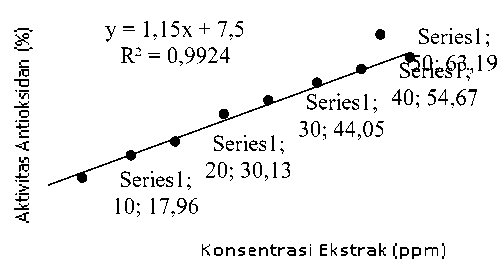
Gambar 6. Grafik hubungan antara konsentrasi ekstrak terhadap aktivitas
antioksidan.
Gambar 6 menunjukkan hubungan antara konsentrasi ekstrak (x) dengan aktivitas antioksidan yang diperoleh (y). Semakin tinggi konsentrasi ekstrak maka semakin tinggi
persentase aktivitas antioksidan. Berdasarkan analisis regresi linier diperoleh persamaan y = 1,15x + 7,5 dengan nilai IC50 sebesar 36,96 mg/L.
Nilai IC50 yang rendah menunjukkan bahwa senyawa tersebut memiliki kemampuan menangkap radikal bebas yang tinggi (Riaz et al, 2012). Menurut Jun et al. (2003)
mengatakan suatu senyawa memiliki aktivitas antioksidan kuat apabila IC50< 50 mg/L,
antioksidan aktif IC50 50-100 mg/L, antioksidan sedang IC50 101-250 mg/L, antioksidan lemah IC50 250-500 mg/L dan antioksidan tidak aktif IC50> 500 mg/L
SIMPULAN DAN SARAN
Simpulan
-
1. Perlakuan waktu maserasi berpengaruh sangat nyata terhadap rendemen, kadar total fenolik, kadar total kurkumin dan aktivitas antioksidan ekstrak rimpang temulawak.
-
2. Pelakuan terbaik adalah perlakuan waktu maserasi 24 jam (W2) dengan rendemen sebesar 18,88%, total fenolik sebesar 205,86 mg GAE/g, total kurkumin sebesar 21,22 mg/g ekstrak, aktivitas antioksidan sebesar 84,45%, dan nilai IC50 sebesar 36,96 mg/L.
Saran
Berdasarkan hasil penelitian yang telah dilakukan disarankan untuk dilakukan proses purifikasi senyawa yang paling berperan sebagai antioksidan dalam ekstrak rimpang temulawak.
DAFTAR PUSTAKA
Agoes, G. 2007. Teknologi Bahan Alam. ITB Press, Bandung
Akram, M., S. Uddin, A. Ahmed, K. Ushmanghani, A. Hannan, E. Mohiuddin dan M. Asif. 2010. Curcuma longa and
curcumin. Journal Plant Biol.55(2) : 6570
Anggoro, D., R.S. Rezki, M.Z. Siswarni. 2015. Ekstraksi Multi Tahap Kurkumin Dari Temulawak (Curcuma xanthorriza Roxv.) Menggunakan Pelarut Etanol. Jurnal Teknik Kimia USU. 4(2) : 39-45
Anonimus. 2015. Statistik Tanaman Biofarmaka Indonesia. Badan Pusat Statistik, Jakarta
Arif, R.S. dan Tukiran. 2015. Identifikasi senyawa fenolik hasil isolasi dari fraksi semi polar ekstrak etil asetat kulit batang tumbuhan nyiri baru (Xylocarpus
moluccencis). Journal of Chemistry. 4(2) : 105-110
Budiyanto, A. dan Yulianingsih. 2008. Pengaruh suhu dan waktu ekstraksi terhadap karakter pektin dari ampas jeruk siam (Citrus nobilis L.). J.
Pascapanen. 5(2) : 37-44
Cartea, M.E., M. Francisco, P. Soegas dan P. Velasco. 2011. Phenolic compounds in brassica vegetables. Molecules. 16 : 251280
Cikita, I., I. H. Hasibuan dan R. Hasibuan. 2016. Pemanfaatan Flavonoid Ekstrak Daun Katuk Sauropusandrogynous (L) Merr) Sebagai Antioksidan pada Minyak Kelapa. Jurnal Teknik Kimia USU: 1-7.
Devi, R.R dan C. Arumughan. 2007. Phytochemical characterization of defatted rice bran and optimization of a process for their extraction and enrichment. Bioresource Technol. 98: 3037-3043
Dewi, P.J.N, A. Hartiati, dan S. Mulyani. 2016. Pengaruh umur panen dan tingkat maserasi terhadap kandungan kurkumin
dan aktivitas antioksidan ekstrak kunyit (Curcuma domestica Val.). Jurnal Rekayasa dan Manajemen Agroindustri. 4(2) : 101-111
Fauzana, D. L. 2010. Perbandingan Metode Maserasi, Remaserasi, Perkolasi dan Reperkolasi Terhadap Rendemen Ekstrak Temulawak (Curcuma
xanthorrhiza Roxb.). Skripsi. Tidak Dipublikasikan. Fakultas Teknologi Pertanian IPB, Bogor
Harjanti, R.S. 2008. Pemungutan kurkumin dari kunyit (curcuma domestica val.) dan pemakaiannya sebagai indikator analisis volumetri. Jurnal Rekayasa Proses.2(2). Hal 49-54
Hayani, E. 2006. Analisis Kandungan Kimia Rimpang Temulawak. Departemen Pertanian, Bogor
Hincapie, C.A., Z. Monsalve, D.S. Seigler, J. Alarco dan C.L. Cespedes. 2011. Antioxidant activity of Blechnum chilense (Kaulf.) Mett.,Curcuma
domestica Valeton and Tagetes verticillata Lag. Boletin latinoamericano y del Caribe de Plantas Medicinales y Aromáticas. 10(4): 315-324.
Ismarti. 2011. Isolasi Triterpenoid dan Uji Antioksidan dari Fraksi Etil Asetat Kulit Batang Meranti Merah (Shorea singkawan (Miq).Miq). Tesis. Tidak Dipublikasikan. Program Studi Kimia Pascasarjana, Universitas Andalas
Jayaprakasha, G. K., J.M. Rao. and K.K. Sakariah. 2006. Antioxidant activities of curcumin, demethoxycurcumin and bisdemethoxcurcumin. Food
Chemistry.98 : 720-724.
Jitoe, A., T. Masuda, I.G.P. Tengah, D.N. Suprapta, I.W. Gara, dan N. Nakatani.
1992. Antioxidant activity of tropical ginger extracts and analysis of the contained curcuminoids. J Agric Food Chemistry. 40: 1337-1340.
Jun, M., H.Y. Fu, J. Hong., X. Wan, C.S. Yang, C.T. Ho. 2003. Comparison of antioxidant activities of isoflavones from kudzu root (Pueraria labata Ohwl). J. Food Sci. 68: 2117–2122.
Kaur, C. H. dan C. Kapoor. 2002. Antioxidant activity and total phenolic content of some asian vagetables. Journal of Food Science and Technology. 37 : 153-161
Kemit, N., I W.R. Widarta dan K.A. Nocianitri. Pengaruh jenis plarut dan waktu maserasi terhadap kandungan senyawa flavonoid dan aktivitas antioksidan ekstrak daun alpukat (Persea Americana Mill). E. Jurnal Itepa Universitas Udayana. 1 : 130-141
Khadijah, A.M. Jayali, S. Umar, I. Sasmita. 2017. Penentuan Total Fenolik dan Aktivitas Antioksidan Ekstrak Etanolik Daun Samama (Anthocephalus
macrophylus) Asal Ternate, Maluku Utara. Jurnal Kimia Mulawarman. 5(1) : 11-18Murtiningsih, S. 2011. Membuat Tepung Umbi dan Variasi Olahannya. Agromedia Pustaka, Jakarta.
Kristiani, V. dan F.I. Halim. 2014. Pengaruh Konsentrasi Etanol dan Waktu Maserasi Terhadap Perolehan Fenolik, Flavonoid dan Aktivitas Antioksidan Ekstrak
Rambut Jagung. Skripsi. Tidak Dipublikasikan. Fakultas Teknik.
Universitas Katolik Widya Mandala, Surabaya
Kurniati, R.I. 2013. Uji Aktivitas Antioksidan Fraksi Etanol Daun Buas-Buas (Premna cordifolia Linn.) Dengan Metode DPPH (2,2-difenil-1-pikrlhidrazil). Skripsi.
Tidak Dipublikasikan. Fakultas
Kedokteran Universitas Tanjungpura, Pontianak
Mukhriani. 2014. Ekstraksi, pemisahan Senyawa, dan Identifikasi Senyawa Aktif. Jurnal Kesehatan. 7(12) : 361-367
Nurcholis, W. dan M. Bintang. 2017. Perbandingan aktivitas antioksidan dan kandungan fenolik temulawak dan temu ireng. Jurnal Jamu Indonesia. 2(1) : 2529
Prasetya, D.Y. dan S. Yuliani. 2014. Aktivitas ekstrak rimpang temulawak (Curcuma xanthirrhiza Roxb.) pada radial arm maze dan pasive avoidance test tikus model demensia. Pharmaciana. 4(2) :
157-164
Ramdja, A.F., R.M.A. Aulia dan P. Mulya. 2009. Ekstraksi kurkumin dari temulawak dengan menggunakan etanol. Jurnal Teknik Kimia. 16(3) : 52-58
Rao, M.N.A. 1997. Antioxidant properties of curcumin. Proceedings of the International
Riaz, T., M.A. Abbasi, A. Rehman, T. Shahzadi, M. Ajaib, dan K.M. Khan. 2012. Phytochemical screening, free radical scavenging, antioxidant activity and phenolic content of Dodonaea viscose Jacq. J Serb Chem Soc. 77(4):423–435
Sarwono, J. 2006. Metode Penelitian Kuantitatif dan Kualitatif. Graha Ilmu, Yogyakarta
Schneider, C., O.N. Gordon and P.B. Luis. 2016. Degradation of curcumin: from mechanism to biological implications. J. Agric Food Chem. 63(35) : 7606-7614
Somaatmadja, D. 1981. Prospek
Comparative Effects on Inflammation. Tesis. Tidak Dipublikasikan. University of Massachusetts Amherst, Boston
Perkembangan Industri Oleoresin di Indonesia. Balai Besar Industri Hasil Pertanian, Bogor
Srijanto, B. 2010. Pengaruh Waktu, Suhu Dan Perbandingan Bahan Baku-Pelarut Pada Ekstraksi Kurkumin Dari Temulawak (Curcuma xanthorriza Roxb.) Dengan Pelarut Aseton. Skripsi. Tidak Dipublikasikan. Jurusan Teknik Kimia Universitas Pembangunan Nasional Veteran, Yogyakarta
Steel, R.G.D dan J.H. Torrie. 1993. Prinsip dan prosedur statistika Suatu Pendekatan Biometrik. Penerjemah B. Sumantri. PT. Gramedia Pustaka, Jakarta
Symposium on Curcumin Pharmacochemistry (ISCP). 39-47
Tananuwong, K. dan W. Tewaruth. 2010. Extraction and application of antioxidants from black glutinous rice. J Food Sci and Tech. 43 : 476–481
Utami. 2009. Potensi daun alpukat (Persea americana Mill) sebagai sumber antioksidan alami. Jurnal Teknik Pertanian. 2(1) : 58-64.
Widarta, I W.R. dan I W. Arnata. 2014. Stabilitas aktivitas antioksidan ekstrak bekatul beras merah terhadap oksidator dan pemanasan pada berbagai pH. Jurnal Teknologi dan Industri Pangan. 25(2) : 193-199
Widarta, I W.R. dan I W. Arnata. 2017. Ekstraksi komponen bioaktif daun alpukat dengan bantuan ultrasonik pada berbagai jenis dan konsentrasi pelarut. Jurnal Agritech. 37 (2) : 158-166
Zhu, J. 2016. Curcumin and Its Oxidative Degradation Products: Their
174
Discussion and feedback