SINTESIS DAN KARAKTERISASI KATALIS CaO-BENTONIT UNTUK REAKSI TRANSESTERIFIKASI MINYAK JELANTAH MENJADI BIODIESEL
on
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 8 Nomor 1, Mei 2020

SINTESIS DAN KARAKTERISASI KATALIS CaO-BENTONIT UNTUK REAKSI TRANSESTERIFIKASI MINYAK JELANTAH MENJADI BIODIESEL
James Sibarani* , Martha Zulfihardini, I Wayan Suarsa
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Udayana, Bukit Jimbaran-Badung, Bali-Indonesia *james_sibarani@unud.ac.id
ABSTRAK: Katalis basa heterogen paling banyak digunakan dalam produksi biodiesel. Tujuan penelitian ini untuk mendapatkan konsentrasi Ca(NO3)2 dan suhu optimum dalam sintesis katalis basa CaO-Bentonit sebagai katalis heterogen dalam proses reaksi transesterifikasi minyak jelantah menjadi biodesel. Bentonit terlebih dahulu diaktivasi dengan larutan NaOH 5% (b/v) kemudian dipanaskan pada suhu 500oC. Pembuatan CaO-Bentonit dilakukan dengan proses impregnasi larutan Ca(NO3)2 dengan konsentrasi 0,10M; 0,25M; dan 0,50M pada bentonit teraktivasi tersebut dan dikalsinasi pada suhu 500oC sampai 700oC selama 5 jam. Karakterisasi CaO-Bentonit dilakukan dengan FTIR, XRD dan BET. Hasil karakterisasi CaO-Bentonit menunjukkan bahwa konsentrasi Ca(NO3)2 dan suhu kalsinasi optimum berturut-turut adalah 0,10 M dan 700oC. Aplikasi dari katalis CaO-Bentonit tersebut pada proses transesterifikasi minyak jelantah menghasilkan biodiesel dengan rendemen sebesar 66,74% dan telah memenuhi standar baku mutu nasional Indonesia SNI.
Kata kunci: CaO-Bentonit, reaksi transesterifikasi, minyak jelantah, biodiesel
ABSTRACT: Heteregeneous base catalysts are commonly used in biodiesel production. The purpose of this study is to obtain the optimum concentration of aqueous solution of Ca(NO3)2 and the optimum temperature in the synthesis of CaO-Bentonite catalysts for transesterification reaction of waste cooking oil to produce biodiesel. Firstly, the bentonite was activated with NaOH 5% (w/v) following by calcination at 500oC. Secondly, the activated bentonite was impregnated with Ca(NO3)2 solution with various concentration of 0.10M, 0.25M, and 0.50M and calcinated at temperature of 500oC, 600oC, and 700oC. The characterizations of the CaO-bentonite were conducted by FTIR, RXD, and BET. The results revealed that the optimum concentration of Ca(NO3)2 and the optimum calcination temperature were 0.1 M and 700oC, respectively. Application of the CaO-bentonite catalyst on transesterification reaction of waste cooking oil to biodiesel yielded 66.74% of biodiesel fulfilling the Indonesian Standard Qualities.
Keywords: CaO-Bentonite, transesterification, waste cooking oil, biodiesel
Biodiesel adalah salah satu bahan bakar alternatif yang digunakan untuk mesin diesel. Hasil-hasil penelitian menunjukkan bahwa berbagai minyak nabati maupun hewani digunakan sebagai bahan bakar alternatif (biodiesel). Biodiesel atau metil ester dapat diperoleh dengan
melalui reaksi transesterifikasi menggunakan katalis asam atau basa. Katalis basa merupakan katalis yang paling banyak digunakan pada proses transesterifikasi untuk memproduksi biodiesel. Terdapat dua jenis katalis basa yang dapat digunakan dalam pembuatan biodiesel, yaitu katalis basa homogen dan
katalis basa heterogen. Katalis basa heterogen seperti CaO, memiliki kemampuan katalisator yang sedikit lebih rendah dibandingkan dengan katalis basa homogen tetapi dapat menjadi alternatif yang baik dalam proses pembuatan biodiesel [1]. Stojković [2] telah menggunakan CaO pada reaksi transesterifikasi minyak bunga matahari dengan yield 98%. Namun, ketika CaO direaksikan langsung, ion oksigen (O2-) pada permukaannya mudah membentuk ikatan hidrogen dengan metanol atau gliserol yang akan meningkatkan viskositas gliserol dan membentuk suspensi dengan CaO. Sehingga CaO maupun gliserol akan sulit dipisahkan [3]. Solusi yang bisa dilakukan adalah melakukan proses penambahan penunjang katalis pada CaO. Bentonit salah satu katalis heterogen yang sangat potensial sebagai penunjang katalis dalam pembuatan biodiesel. Selain penunjang katalis, bentonit ini membantu dalam pemisahan dengan asam lemak dalam minyak nabati.
Bahan yang digunakan adalah bentonit alam yang berasal dari Jawa Barat, minyak jelantah yang berasal dari minyak sisa rumahan, larutan Ca(NO3)2, NaOH, CH3OH, C2H5OH 95%, KOH, H2C2O4, dan HCl 37%.
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat alat refluks, hot plate, tanur, pengaduk magnet, oven, cawan porselen, mortar, ayakan dengan ukuran 200 mesh, pipet mikro, timbangan analitik, desikator, piknometer, viskometer oswald, termometer, FTIR, NOVA 1000 Gas Sorbtion Analyzer dan X’PertProPANalytical.
Bentonit dipanaskan pada suhu 500oC kemudian diaktivasi dengan NaOH 5% dengan rasio 1:10 (bentonit:NaOH) [4].
Campuran diaduk menggunakan pengaduk magnet selama 12 jam pada suhu 60oC, lalu disaring dan dikeringkan didalam oven. Bentonit teraktivasi kemudian dikalsinasi pada suhu 500oC selama 3 jam.
Sintesis CaO-Bentonit
Sebanyak 10 g bentonit teraktivasi diimpregnasi dengan larutan Ca(NO3)2 dengan konsentrasi 0,10 M; 0,25 M; 0,50 M selama 12 jam pada suhu 60oC menggunakan pengaduk magnet dengan modifikasi dari Jurnal Kouzu [4,5]. Kemudian, campuran bentonit disaring dan bubur Ca(NO3)2 dikeringkan di dalam oven pada suhu 110oC. Setelah itu bentonit kering dikalsinasi dengan variasi suhu 500oC, 600oC, dan 700oC selama 5 jam. Lalu, katalis CaO-Bentonit digerus, diayak dan dikarakterisasi dengan XRD, FTIR, dan BET.
Penentuan situs basa katalis
Sebanyak 0,1 g katalis CaO-Bentonit dimasukkan ke dalam erlenmeyer dan ditambahkan 10 mL HCl 0,10 M sambil diaduk dengan menggunakan pengaduk magnet selama 15 menit [5]. Lalu, ditambahkan 3 tetes indikator phenolphetalin dan dititrasi dengan larutan NaOH 0,10 N hingga terjadi perubahan warna menjadi merah muda. Volume NaOH yang didapatkan dicatat.
Sintesis biodiesel dari minyak jelantah
Sebanyak 1,5 g katalis CaO-Bentonit dan 51,3761 g metanol direfluks selama 1 jam pada suhu 60oC diatas hot plate [6]. Lalu, 30 g minyak jelantah dimasukkan ke dalam campuran sambil tetap dipanaskan selama 3 jam. Kemudian, campuran didinginkan pada suhu kamar dan dipisahkan menggunakan corong pisah. Setelah terjadi pemisahan, biodiesel disaring dengan kertas saring dan dilakukan pengujian biodiesel viskositas, densitas, angka asam, kadar air.
-
2.3. Karakterisasi biodiesel
Penentuan densitas
Piknometer kosong ditimbang lalu dicatat beratnya. Kemudian, piknometer diisi dengan biodiesel lalu ditimbang, dicatat beratnya dan dilakukan pengulangan sebanyak tiga kali [7].
Penentuan viskositas
Viskometer otswald dibersihkan dengan aseton, lalu dimasukkan 5 mL sampel biodiesel dan dibiarkan cairan turun, dicatat waktu yang diperlukan untuk melewati 2 tanda batas pada viskometer [8].
Penentuan angka asam
Sebanyak 2 g sampel biodiesel dimasukkan ke dalam erlenmeyer. Lalu, ditambahkan 20 mL etanol 95% [9].
Ditambahkan 2 tetes indikator PP kemudian dititrasi dengan larutan KOH 0,1 N dititrasi hingga terbentuk warna merah jambu yang stabil selama 10 detik dan dilakukan pengulangan tiga kali.
Penentuan kadar air
Sampel minyak jelantah sebanyak 2 g ditempatkan pada cawan porselin lalu dikeringkan dalam oven pada suhu 104-106oC selama 2 jam [9]. Sampel diangkat dari oven dan didinginkan dalam desikator, setelah itu minyak ditimbang. Dilakukan penimbangan sampai bobotnya stabil (tidak berbeda lebih dari 0.005 %).
-
3. HASIL DAN PEMBAHASAN
Karakterisasi struktur katalis dengan X-ray diffraction (XRD)
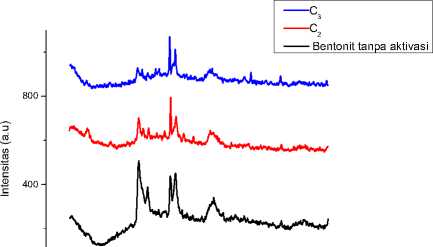
Pada Gambar 1 difraktogram bentonit tanpa katalis terdapat puncak 2θ : 9,0159o; 19,6161o; 26,3434o. Refleksi 2θ : 9o, 20o, 26o, 30o, 62o mengindikasikan keberadaan montmorilonit dalam bentonit [10]. Sedangkan, difraktogram katalis CaO-Bentonit dengan penambahan konsentrasi Ca(NO3)2 0,25 M pada suhu kalsinasi
500oC (C2) terdapat puncak pada 2θ: 21,81o
yang mengindikasikan puncak kuarsa dan puncak pada 2θ: 31,36o mengindikasikan puncak kristobalit. Refleksi sekitar 2θ : 34o menunjukkan adanya kristal Na2O yang terbentuk selama aktivasi dengan NaOH [4]. Pada difaktogram katalis CaO-Bentonit dengan penambahan konsentrasi Ca(NO3)2 0,50 M dengan suhu kalsinasi 700oC (C3) terdapat puncak pada 2θ: 27,80o yang mengindikasikan puncak mineral illit sesuai dengan JCPDS (Joint Committee on Powder Diffraction Standards) No.24-0495 yang digunakan sebagai data pembanding [11].
04----------------------------------------------1-----------------------,-----------------------1-----------------------,-----------------------1-----------------------,
0 20 40 60
2Theta
Gambar 1. Spektra XRD dari bentonit, CaO- bentonit dengan penambahan konsentrasi larutan Ca(NO3)2 0,25 M (C2), CaO-bentonit dengan penambahan konsentrasi larutan Ca(NO3)2 0,50 M (C3).
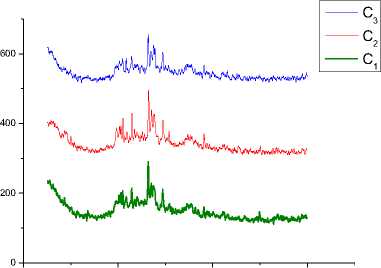
Pada Gambar 1 terlihat bahwa kristalinitas pada katalis CaO-Bentonit dengan penambahan konsentrasi Ca(NO3)2 0,1 M dan 0,25 M memiliki ukuran partikel yang lebih kecil dibandingkan dengan ukuran partikel dari bentonit tanpa aktivasi. Hal ini bisa diperkuat karena intensitas pada pola difraksi XRD berhubungan dengan tingkat kristalinitas dimana umumnya semakin tinggi kristalinitas maka semakin besar ukuran partikelnya [12]. Spektra XRD dari katalis CaO-Bentonit dengan penambahan konsentrasi larutan Ca(NO3)2 0,10 M (C1), 0,25 M (C2) dan 0,50 M (C3) menunjukkan puncak yang cenderung sama setelah diimpregnasi dengan katalis CaO yang mengindikasikan bahwa sampel tersebut
memiliki fase yang sama. Hal ini terjadi karena CaO tidak merubah struktur dari bentonit tersebut.
Intensitas (a.u)
0 20 40 60
2 Theta
Gambar 2. Spektra XRD CaO-Bentonit dari proses impregnasi menggunakan konsentrasi Ca(NO3)2 0,10 M (C1), 0,25 M (C2), 0,50 M (C3)
Karakterisasi gugus fungsi dengan FTIR
Analisis FTIR dilakukan pada bilangan gelombang 4000-500 cm-1. Spektra inframerah bentonit murni pada Gambar 3 adanya pita gugus OH di daerah sekitar 3631,96 cm-1, pita C=C aromatik muncul pada bilangan gelombang 1535,34 cm-1 dan pita CH asitilen pada bilangan gelombang 2345,44 cm-1[13]. Pada spektra inframerah kalsium oksida (CaO) standar menunjukkan adanya pita gugus OH di daerah sekitar 3732,26 cm-1, pita C=O stretching muncul pada bilangan gelombang 1697,36 cm-1 hal ini diperkuat dengan C=O bending pada bilangan gelombang 1245,61 cm-1 dan pita Ca=O pada daerah sekitar 491,85 cm-1. Pada Gambar 3 menunjukkan adanya puncak yang muncul pada ketiga katalis CaO-Bentonit yang dihasilkan dari variasi suhu 500oC, 600oC dan 700oC pada proses kalsinasi secara umum hampir sama.
Gambar 4 menunjukkan spektra hasil katalis CaO-Bentonit yang dihasilkan dari variasi konsentrasi dengan suhu kalsinasi 700oC terlihat bahwa puncak OH berturut-turut sebesar 3597,24 cm-1, 3604,96 cm-1, dan 3595,31 cm-1. Puncak tersebut
mengalami pergeseran yang tidak terlalu signifikan. Bilangan gelombang pada daerah serapan 2347,37 cm-1 yang menunjukkan adanya ikatan CH pada katalis CaO-Bentonit yang dihasilkan dari penambahan konsentrasi Ca(NO3)2 0,1 M dengan suhu kalsinasi 700oC pada Gambar 4 menunjukkan puncak yang tajam. Berdasarkan variasi konsentrasi katalis CaO-Bentonit semakin bertambah konsentrasi hanya mengalami pergeseran bilangan gelombang saja dengan gugus fungsi yang sama.
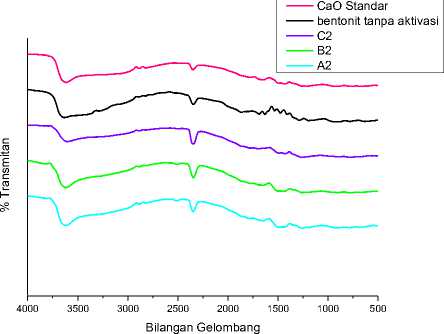
Gambar 3. Spektra FTIR Bentonit murni, CaO standar, dan atalis CaO-Bentonit
yang dihasilkan dari variasi suhu kalsinasi 500oC (A2), 600oC (B2) dan
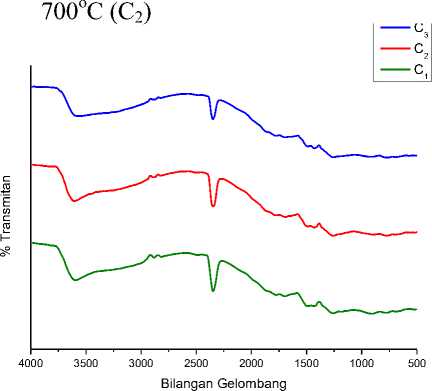
Gambar 4. Spektra Katalis CaO-Bentonit yang dihasilkan dari variasi penambahan konsentrasi larutan Ca(NO3)2 0,10 M (C1), 0,25 M (C2) dan 0,50 M (C3) dengan suhu kalsinasi 700oC.
Tabel 1. Nilai Kebasaan Permukaan dan Situs Aktif Basa Katalis
|
Sampel Katalis |
Kebasaan Permukaan (mmol/g) |
Situs aktif basa (atom/g) |
|
A1 |
19,6690 ± 0,0056 |
11,8446 x 1021 |
|
A2 |
19,6735 ± 0,0205 |
11,8473 x 1021 |
|
A3 |
19,6590 ± 0 |
11,8386 x 1021 |
|
B1 |
18,9760 ± 0,9446 |
11,4273 x 1021 |
|
B2 |
18,9835 ± 0,9553 |
11,4318 x 1021 |
|
B3 |
19,6585 ± 0,0205 |
11,8383 x 1021 |
|
C1 |
19,7240 ± 0,0232 |
11,8777 x 1021 |
|
C2 |
19,6875 ± 0,0205 |
11,8558 x 1021 |
|
C3 |
19,6880 ± 0 |
11,8561 x 1021 |
A1 = Katalis CaO-Bentonit dengan konsentrasi 0,10 M pada suhu kalsinasi 500oC A2 = Katalis CaO-Bentonit dengan konsentrasi 0,25 M pada suhu kalsinasi 500oC A3 = Katalis CaO-Bentonit dengan konsentrasi 0,50 M pada suhu kalsinasi 500oC B1 = Katalis CaO-Bentonit dengan konsentrasi 0,10 M pada suhu kalsinasi 600oC B2 = Katalis CaO-Bentonit dengan konsentrasi 0,25 M pada suhu kalsinasi 600oC B3 = Katalis CaO-Bentonit dengan konsentrasi 0,50 M pada suhu kalsinasi 600oC C1 = Katalis CaO-Bentonit dengan konsentrasi 0,10 M pada suhu kalsinasi 700oC C2 = Katalis CaO-Bentonit dengan konsentrasi 0,25 M pada suhu kalsinasi 700oC C3 = Katalis CaO-Bentonit dengan konsentrasi 0,50 M pada suhu kalsinasi 700oC
Kebasaan permukaan katalis
Kebasaan permukaan katalis pada reaksi transesterifikasi dapat meningkatkan aktifitas katalis sehingga berpengaruh terhadap yield biodiesel. Semakin tinggi kebasaan katalis, maka semakin tinggi yield biodiesel yang dihasilkan. Selain itu kekuatan basa katalis memberikan pengaruh yang lebih besar terhadap yield biodiesel dibandingkan dengan pengaruh luas permukaan katalis[14]. Karakterisasi kebasaan permukaan katalis dilakukan dengan titrasi asam basa. Nilai kebasaan permukaan tertinggi yaitu pada sampel B1 yaitu sebesar 18,9760 ± 0,9446 mmol g-1 dengan jumlah situs aktif basa sebesar 11,4273 x 1021 atom g-1
Luas permukaan spesifik
Luas permukaan spesifik katalis ditentukan dengan metode BET dimana prinsipnya yaitu menghitung jumlah gas yang teradsorpsi pada permukaan bahan yang dikarakterisasi. Berdasarkan hasil dari kebasaan permukaan yang tidak terlalu
memberikan efek yang signifikan, luas permukaan spesifik katalis CaO-Bentonit hanya salah satu sampel katalis yang dikarakterisasi dengan metode BET. Hasil karakterisasi luas permukaan spesifik katalis menunjukkan bahwa katalis CaO-Bentonit yang dihasilkan dari penambahan konsentrasi Ca(NO3)2 0,25 M dengan proses suhu kalsinasi 700oC (C2) memiliki luas permukaan sebesar 1,974 m2/g. Kecilnya luas permukaan katalis ini mungkin disebabkan karena proses preparasi katalis dan proses kalsinasi [15]. Ukuran pori rata-rata dari katalis meningkat karena runtuhnya pori-pori kecil dari dukungan bentonit selama langkah impregnasi. Peningkatan luas permukaan pada material yang difungsikan sebagai katalis, umumnya akan meningkatkan kinerja katalis tersebut dalam hal aktivitasnya.
Karakterisasi biodiesel hasil reaksi transesterifikasi minyak jelantah menggunakan katalis CaO-Bentonit
Tabel 2. Karakterisasi Biodiesel Hasil Transesterifikasi Minyak Jelantah Menggunakan Katalis dan Tanpa Katalis yang Dibandingkan dengan SNI
|
Densitas (kg/m3) |
Viskositas (cSt) |
Angka Asam (mg-KOH/g) |
Kadar Air (%) | |
|
Bentonit |
923 |
19,00 |
1 |
0,1 |
|
Bentonit teraktivasi |
921 |
16,61 |
0,8 |
0,06 |
|
NaOH | ||||
|
C1 |
890 |
6,7 |
0,6 |
0,01 |
|
C2 |
890 |
7,6 |
0,6 |
0,03 |
|
C3 |
889 |
7,3 |
0,7 |
0,04 |
|
Tanpa katalis |
935 |
22,00 |
2,4 |
0,1 |
|
SNI |
850-890 |
2,3-9,0 |
Maks 0,8 |
Maks 0,05 |
Pada reaksi transesterifikasi, mula-mula katalis direaksikan dengan metanol agar terbentuk spesi metoksi yang merupakan inisiator reaksi transesterifikasi. Selama reaksi berlangsung suhu harus tetap dijaga karena suhu merupakan salah satu faktor yang mempengaruhi reaksi. Suhu reaksi diatur sesuai dengan zat yang memiliki titik didih terendah yakni metanol (titik didih metanol 65oC) apabila reaksi dilakukan pada suhu penangas diatas titik didih metanol maka metanol akan lebih cepat habis menguap, namun apabila suhu reaksi terlalu rendah reaksi pembentukan metil ester menjadi lebih lambat. Setelah melalui reaksi transesterifikasi sifat fisik yang terlihat pada minyak jelantah mengalami perubahan menjadi lebih jernih dan encer. Perubahan tersebut mengindikasikan bahwa minyak jelantah sudah menjadi biodiesel. Biodiesel pada rasio molar minyak:metanol adalah 1:15 dengan katalis CaO-Bentonit 5% menghasilkan rendemen sebesar 66,74%.
Biodiesel yang dianalisis adalah biodiesel yang dihasilkan dengan penambahan larutan Ca(NO3)2 dengan variasi konsentrasi 0,10 M (C1), 0,25 M (C2) dan 0,50 M (C3) pada suhu kalsinasi 700oC, bentonit tanpa katalis dan bentonit teraktivasi NaOH. Berdasarkan Tabel 2 biodiesel yang diperoleh dari penggunaan ketiga katalis hasil transesterifikasi mampu melakukan proses reaksi transesterifikasi minyak jelantah menjadi metil ester. Hal ini bisa dilihat dari nilai densitas, viskositas,
angka asam dan kadar air yang mengalami penurunan sesuai dengan standar baku mutu yang ditetapkan dalam SNI-04-7128-2006. Untuk bentonit tanpa katalis dan bentonit teraktivasi NaOH masih belum berada dalam standar, hal ini dikarenakan bentonit hanya digunakan sebagai support atau adsorben. Berikut hasil pengujian biodiesel yang dibandingkan dengan minyak jelantah (tanpa katalis) disajikan dalam Tabel 2 dihasilkan dengan penambahan larutan Ca(NO3)2 dengan variasi konsentrasi 0,1 M (C1), 0,25 M (C2) dan 0,5 M (C3) pada suhu kalsinasi 700oC.
Pembuatan katalis hetereogen CaO-Bentonit untun reaksi transesterifikasi minyak jelantah menjadi biodiesel sudah berhasil dilakukan. Konsentrasi larutan Ca(NO3)2 dan suhu kalsinasi yang optimum untuk mendapatkan katalis CaO-Bentonit adalah larutan Ca(NO3)2 0,10 M dan suhu kalsinasi sebesar 700oC. Karakterisasi biodiesel hasil reaksi transesterifikasi minyak jelantah menggunakan katalis CaO-Bentonit telah memenuhi SNI-04-7182-2006
DAFTAR PUSTAKA
-
[1] Wei Z., Xu C., Liu B., 2009.
Application of Waste Eggshell as LowCost Solid Base Catalyst for Biodiesel Production, Journal Bioresouce Technology, 100 (11): 6362-6368.
-
[2] Stojković, Ivan J., Stamenković O., S., Dragan S., Povrenović, Veljković V., B., 2014. Purification Technologies For Crude Biodiesel Obtained By Alkali-Catalyzed Transesterification,
Renewable and Sustainable Energy Reviews, 32 (3): 1-15.
-
[3] Liu C., L., V., Pengmei, Yuan Z., F., Yan, W., Luo, 2009. The Nanometer Magnetic Solid Base Catalyst For Production of Biodiesel, Journal Renewable Energy, 35 (7): 1531-1536.
-
[4] Ali B., Yusup S., Armando T., Quitain, Alnarabiji M., S., Ruzaimah N., M.,
Kamil., Kida T., 2018. Synthesis of
Novel Graphene Oxide/Bentonite bifunctional Heterogeneous Catalyst for One-pot Esterification and
Transesterification Reactions, Journal Elsevier Energy Conversion and Management, 171 (1): 1801-1812.
-
[5] Kouzu, M., Kazuno T., Tajika M., Sugimoto Y., Yamanaka S., Hidaka J., 2008. Calcium Oxide as a Solid Base Catalyst for Transesterification of Soybean Oil and its Application to Biodiesel Production, Journal Fuel, 87 (12): 2798- 2806.
-
[6] Setiowati R., Nurhayati, Linggawati A., 2014. Produksi Biodiesel Dari
Minyak Goreng Bekas Menggunakan Katalis CaO Cangkang Kerang Darah Kalsinasi 900oC, Jurnal Online
Mahasiswa FMIPA Universitas Riau, 1 (2): 383-388.
-
[7] Yusuf M., M., F., 2010. Sintesis dan Karakterisasi Biodiesel dari Minyak Biji Karet (Hevea Brasiliensis) Melalui Proses Estrans (Esterifikasi-
Transesterifikasi), Skripsi, Institut Pertanian Bogor, Bogor.
-
[8] Laila L., Oktavia L., 2017. Kaji
Eksperimen Angka Asam dan Viskositas Biodiesel Berbahan Baku Minyak Kelapa Sawit dari PT. Smart TBK, Jurnal Teknologi Proses dan Inovasi Industri, 2 (1): 27-31.
-
[9] Badan Standarisasi Nasional, 2013. SNI No. 01-3741 Minyak Goreng, <http://sispk.bsn.go.id/SNI/DetailSNI/ 9013> tanggal akses 30 April 2019.
-
[10] Soetaredjo F., A., Ayucitra A., Ismadji S., Maukar A., L., 2011.
KOH/Bentonite Catalysts for
Transesterification of Palm Oil to Biodiesel, Journal Elvesier Applied Clay Science, 53 (2): 341-346.
-
[11] Hidayat M., T., Nugraha I., 2018. Kajian Kinerja Ca-Bentonit Kabupaten Pacitan-Jawa Timur Teraktivasi Asam Sulfat Sebagai Material Lepas Lambat (Slow Release Material) Pupuk Organik Urin Sapi, Indonesian Journal of Materials Chemistry, 1 (1): 27-37.
-
[12] Horiba Scientific, 2010. A Guidebook to Particle Size Analysis, Horiba Instruments Inc, USA
-
[13] Ruiz M.G., Hernández J., Baños L., Montes J.N., and García M.E.R., 2009. Characterization of Calcium
Carbonate, Calcium Oxide, and Calcium Hydroxide as Starting Point to the Improvement of Lime for Their Use in Construction, Journal of Materials in Civil Engineering, 21
(11): 694- 698.
-
[14] Helwani Z., Yoesepha W., Saputra E., 2016. Produksi Biodiesel dari Minyak Sawit Off Grade Menggunakan Katalis Na2O/Fe3O4 Pada Tahap
Transesterfikasi, Jurnal Online Mahasiswa Fakultas Teknik
Universitas Riau, 3 (2): 1-8.
-
[15] Wistanto E., Trisuryananti W., Triyono., 2010. Preparasi dan Karakterisasi Katalis Ni/Zeolit Alam Aktif, Prosiding: Seminar Nasional VI SDM Teknologi Nuklir, Yogyakarta.
65
Discussion and feedback