MICROBIAL CONTAMINATION STANDARD OF PEGAGAN LEAVES SAMPLE AS QUALITY REQUIREMENTS FOR RAW MEDICINAL PREPARATIONS
on
Volume 14 No. 4: 319-326
Agustus 2022
DOI: 10.24843/bulvet.2022.v14.i04.p01
Buletin Veteriner Udayana
pISSN: 2085-2495; eISSN: 2477-2712
Online pada: http://ojs.unud.ac.id/index.php/buletinvet
Terakreditasi Nasional Sinta 4, berdasarkan Keputusan Direktur Jenderal
Pendidikan Tinggi, Riset, dan Teknologi No. 158/E/KPT/2021
Standarisasi Cemaran Mikroba Sampel Daun Pegagan sebagai Persyaratan Mutu Bahan Baku Sediaan Obat
(MICROBIAL CONTAMINATION STANDARD OF PEGAGAN LEAVES SAMPLE AS QUALITY REQUIREMENTS FOR RAW MEDICINAL PREPARATIONS)
Luh Made Sudimartini1*, Genta Dhamara Adam Putranto2, I Gusti Ketut Suarjana3, I Made Merdana1
-
1Laboratorium Farmakologi dan Farmasi Veteriner, Fakultas Kedokteran Hewan, Universitas Udayana, Jl. PB. Sudirman, Denpasar, Bali, Indonesia;
-
2Praktisi Dokter Hewan, Jl. Mekar Baru 1 No. 70 Cireundeu, Ciputat Timur, Tangerang Selatan, Banten
-
3Laboratorium Mikrobiologi Veteriner, Fakultas Kedokteran Hewan, Universitas Udayana, Jl. PB. Sudirman, Denpasar, Bali, Indonesia.
*Email: md_sudimartini@unud.ac.id
Abstrak
Daun pegagan merupakan tanaman yang sangat baik digunakan sebagai bahan baku obat tradisional. Kandungan bioaktif pada daun pegagan berperan dalam proses penyembuhan luka, menyembuhkan dermatitis kompleks pada anjing, neuroprotektif, serta dapat menurunkan stres oksidatif pada sel tubuh. Khasiat yang banyak membuat daun pegagan berpotensi untuk diproduksi menjadi berbagai bentuk sediaan obat. Penelitian ini bertujuan untuk mengetahui kualitas sampel daun pegagan yang akan dibuat menjadi sediaan obat melalui standarisasi cemaran mikroba kuantitatif menurut Parameter Standar Umum Ekstrak Tumbuhan Obat Departemen Kesehatan Republik Indonesia tahun 2000 dan Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 32 tahun 2019 tentang Persyaratan Keamanan dan Mutu Obat Tradisional. Pemeriksaan cemaran mikroba dilakukan melalui Uji Angka Lempeng Total dan Uji Angka Kapang Khamir. Data penelitian yang diperoleh adalah data kuantitatif yang dianalisis dengan cara penghitungan jumlah mikroba yang tumbuh pada media Plate Count Agar dan media Potato Dextrose Agar setelah diinkubasi pada suhu pertumbuhan yang sesuai. Hasil penelitian ini menunjukkan bahwa Angka Lempeng Total pada sampel daun pegagan 3250 CFU/gr dan Angka Kapang Khamir 450 CFU/gr. Nilai Angka Lempeng Total telah memenuhi persyaratan bentuk sediaan obat dalam (≤105 koloni/gr) dan memenuhi persyaratan sediaan obat luar semi padat (≤107 koloni/gr). Sedangkan nilai Angka Kapang Khamir telah memenuhi persyaratan sediaan obat dalam (≤103 koloni/gr) serta memenuhi persyaratan sediaan obat luar semi padat (≤104 koloni/gr).
Kata kunci: Angka Lempeng Total; Angka Kapang Khamir; daun pegagan; sediaan obat; standarisasi
Abstract
Pegagan is an excellent plant used as a raw material for traditional medicine. The bioactive content in pegagan leaves plays a role in the wound healing process, able to cure complex dermatitis in dogs, proven as neuroprotective, and can reduce oxidative stress of body cells. Many efficacies make pegagan leaves have the potential to be produced into various forms of medicinal preparation. This study will calculate the number of microbes’ contamination in pegagan leaves which will be used as various drug preparations and then compare it to the General Standard Parameters for Medical Plant Extracts of the Ministry of Health of Republic Indonesia in 2000 and Regulation of the Head of BPOM RI Number 32 of 2019. The examination of microbial contamination was carried out through the Total Plate Count and Yeast Fungus Test. The research data obtained were quantitative data that were analyzed by counting the number of microbes that grow on PCA and PDA after incubation at the appropriate growth temperatures. The results of this study show that the Total Plate Count from the sample was 3250 CFU/gr and the Yeast Fungus Test was 450 CFU/gr. The number of Total Plate Count has fulfilled the requirements for the Oral Drugs (≤105 colony/gr) and required for Semi Solid Drugs (≤107 colony/gr).
The number of Yeast Fungus Test are required for Oral Drugs (≤103 colony/gr) and required for Semi Solid Drugs (≤104 colony/gr).
Keywords: pegagan leaves; medicinal preparation; standardization; Total Plate Count; Yeast Fungus Test
PENDAHULUAN
Peningkatan kesadaran masyarakat mengenai penggunaan obat berbahan dasar tanaman herbal semakin berkembang. Sebagai budaya dan warisan bangsa, obat tradisional Indonesia perlu dilestarikan dan dikembangkan. Pengembangan yang dimaksud meliputi aspek pembuktian khasiat, keamanan, jaminan mutu, pengemasan, serta teknologi produksi. Tanaman pegagan (Centella asiatica (L.) Urban) terbukti secara empiris maupun ilmiah mampu menyembuhkan penyakit. Jenis tanaman liar ini hidup di daerah tropis, ditemukan di daerah perkebunan, tepi jalan, pematang sawah, atau di ladang yang agak basah. Daun pegagan bersifat hepatoprotektor, tidak menimbulkan efek samping, dan dapat dicerna dengan baik oleh tubuh (Lotulung et al., 2015). Manfaat yang banyak juga membuat tanaman pegagan dibudidayakan dan diproduksi menjadi berbagai bentuk sediaan obat. Kandungan terpenting yang terkandung pada daun pegagan adalah triterpenoid saponin yang meliputi asiaticoside, centelloside, madecoside, dan asam asiatik.
Daun pegagan digunakan menjadi obat herbal untuk mengobati penyakit kulit dan menyembuhkan luka (Singh et al., 2010). Daun pegagan yang digerus secara langsung dan ditambahkan sedikit air dapat digunakan untuk menyembuhkan luka. Kandungan yang berperan dalam proses penyembuhan luka pada daun pegagan adalah asiaticoside (Widianingtyas et al., 2014). Asiaticoside berperan dalam peningkatan proliferasi, sintesis kolagen, dan epitelisasi pada bagian yang mengalami luka (Josi dan Chaturvedi, 2013). Selain itu asiaticoside berfungsi meningkatkan daya regenerasi kulit, menstimulasi pembentukan sel darah merah, sebagai sistem imun, antibiotik
alami (Sutardi, 2016), serta menstimulasi percepatan pembentukan lapisan epidermis kulit tanpa membentuk jaringan scar pada bekas luka (Bhavna dan Jyoti, 2011). Kelainan kulit merupakan masalah utama pada anjing yang memerlukan perhatian khusus (Widyastuti et al., 2012). Ekstrak etanol yang terkandung pada daun pegagan terbukti mampu menghambat pertumbuhan bakteri penyebab dermatitis kompleks pada anjing (Megariyanthi et al., 2018), serta ekstrak metanol pada daun pegagan mampu menghambat pertumbuhan bakteri M. tuberculosis (Yusran et al., 2016).
Sediaan oral daun pegagan berpotensi memberikan efek neuroprotektif bagi sistem saraf (Orhan, 2012). Penggunaan serbuk daun pegagan yang dicampur dengan susu digunakan pada beberapa daerah di India untuk meningkatkan daya ingat (Lisiswanti dan Fiskasari, 2017). Kandungan triterpenoid saponin pada daun pegagan mampu memperlancar sistem peredaran darah dan mengurangi stres oksidatif pada sel tubuh. Daun pegagan berkhasiat dalam pengobatan penyakit Alzheimer dan Parkinson serta telah dikonfirmasi dalam studi pada manusia maupun pada model in vivo (Lokanathan et al., 2016). Penelitian terbaru menyebutkan bahwa konsumsi kapsul pegagan dapat digunakan sebagai upaya perbaikan disfungsi otot rangka pada manusia berusia lanjut sehat melalui tes kekuatan massa otot (Pramantara et al., 2018).
Standarisasi cemaran adalah suatu prosedur yang dilakukan untuk menjamin bahan baku dan produk akhir obat yang diproduksi mempunyai nilai parameter tertentu yang konstan dan telah ditetapkan terlebih dahulu (Depkes RI, 2000). Diperlukan suatu standarisasi kuantitatif cemaran mikroba pada sampel daun pegagan yang akan dijadikan bahan baku
obat menurut Parameter Standar Umum Ekstrak Tumbuhan Obat Departemen Kesehatan Republik Indonesia (2000) dan Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 32 (2019) melalui Uji Cemaran Mikroba yang meliputi penentuan Angka Lempeng Total dan Angka Kapang Khamir. Ketentuan maksimal Angka Lempeng Total untuk obat dalam ≤105 koloni/gr dan obat luar semi padat ≤107 koloni/gr. Ketentuan maksimal Angka Kapang Khamir untuk obat dalam ≤103 koloni/gr dan obat luar semi padat ≤104 koloni/gr. Jika Angka Lempeng Total dan Angka Kapang Khamir atau salah satunya melebihi batas yang telah ditentukan untuk bentuk sediaan tertentu maka disimpulkan bahwa sampel daun tidak layak dilanjutkan ke proses selanjutnya.
METODE PENELITIAN
Preparasi Sampel
Daun pegagan (Centella asiatica (L.) Urban) dipetik secara langsung dari Dusun Kangin Desa Tusan, Kecamatan Banjarangkan, Kabupaten Klungkung, Bali. Dipilih daun pegagan yang hidup secara liar di daerah perkebunan sehingga dipastikan tidak ada kontaminasi pestisida yang terkandung pada daun. Hal ini juga dilakukan untuk menghindari adanya faktor cemaran lain yang dapat mengganggu efek terapi kandungan bioaktif daun. Daun pegagan yang sudah dipetik kemudian diseleksi lalu dicuci menggunakan air mengalir dan dibilas dengan aquades. Daun yang sudah dicuci kemudian dirajang kasar lalu dilakukan proses pengeringan menggunakan oven dengan suhu 50oC selama 24 jam. Daun pegagan yang sudah kering dibuat menjadi serbuk menggunakan mortar and pestle untuk selanjutnya diencerkan dengan NaCl 0,9%. Disiapkan gelas ukur berisi NaCl 0,9% sebanyak 45 ml dan tiga buah tabung reaksi dengan masing-masing berisi 9 ml NaCl 0,9%. Proses pengenceran dilakukan sampai tabung reaksi terakhir sehingga didapatkan pengenceran 10-4. Hasil setiap pengenceran
yang telah dilakukan akan ditanam pada media pertumbuhan.
Persiapan Media
Sebanyak 1,75 gr OXOID® Plate Count Agar dilarutkan dalam 100 ml aquades pada erlenmeyer kemudian dipanaskan sambil diaduk perlahan sampai tidak ada endapan. Tabung erlenmeyer diangkat lalu mulut botol disumbat dengan kapas dan dilapisi dengan alumunium foil. Larutan PCA pada erlenmeyer kemudian disterilisasi menggunakan autoclave pada suhu 121oC dengan tekanan 1 atm selama 15 menit (Wati, 2018). Larutan media PCA kemudian dibagi ke dalam 8 cawan petri masing-masing sebanyak ±12 ml. Proses pengerjaan dilakukan di dalam laminar air flow agar tidak terjadi kontaminasi. Media PCA yang sudah dingin dan memadat dapat disimpan di lemari es dalam posisi terbalik sebelum digunakan. Prosedur di atas dilakukan juga pada pembuatan media PDA, dengan komposisi 3,9 gr MERCK® Potato Dextrose Agar (PDA) dalam 100 ml aquades. Ditambahkan Amoxicillin sebanyak 1 gr ke dalam 100 ml larutan media PDA yang digunakan. Hal ini berfungsi untuk menghambat pertumbuhan bakteri sehingga dapat dipastikan yang tumbuh pada media PDA hanya kapang dan khamir saja. Jika proses sterilisasi pada larutan media PDA selesai maka larutan media tersebut dapat dibagi ke dalam 8 cawan petri masing-masing sebanyak ± 12 ml (Basarang et al., 2018).
Uji Angka Lempeng Total
Prosedur uji Angka Lempeng Total dilakukan dengan menyebar inokulum sebanyak 0,1 ml ke masing-masing media PCA dan dibuat duplo lalu sampel diratakan ke seluruh permukaan media. Untuk mengetahui sterilitas media dan pengencer dilakukan uji kontrol. Cawan petri diinkubasi pada suhu 35-37oC selama 24 jam dengan posisi terbalik, lalu jumlah koloni yang tumbuh diamati dan dihitung (Depkes RI, 2000). Penghitungan dan pencatatan koloni dilakukan dalam satuan CFU/gr.
Uji Angka Kapang Khamir
Prosedur uji Angka Kapang Khamir dilakukan seperti di atas pada media PDA. Media PDA diinkubasi pada suhu 20-25oC selama 3-5 hari dengan posisi terbalik. Setelah 3 hari inkubasi dicatat jumlah koloni kapang dan khamir yang tumbuh dengan pengamatan terakhir dilakukan pada hari ke-5. Pemeriksaan cemaran mikroba dilakukan dengan metode enumerasi bakteri.
Analisis Data
Data hasil penelitian dianalisis secara deskriptif kualitatif.
HASIL DAN PEMBAHASAN
Hasil
Hasil uji Angka Lempeng Total dari sampel daun pegagan pada masing-masing pengenceran setelah diinkubasi selama 36 jam disajikan pada Tabel 1 dan Gambar 1. Sementara hasil uji Angka Kapang Khamir dari sampel daun pegagan pada masing-masing pengenceran setelah diinkubasi selama 120 jam dijelaskan pada Tabel 2 dan Gambar 2.
Pembahasan
Cawan petri yang memenuhi standar penghitungan hanya pada cawan pengenceran pertama. Pengenceran kedua, ketiga, dan keempat tidak memenuhi kriteria penghitungan menurut Depkes RI (2000) karena jumlah koloni berada di bawah syarat penghitungan (antara 30-300 koloni). Rata-rata jumlah koloni pada pengenceran pertama yaitu 32,5 koloni. Rata-rata koloni kemudian dihitung sesuai rumus perhitungan Angka Lempeng Total menurut Depkes RI (2000). Angka koloni pada pengenceran pertama kemudian disebut sebagai nilai Angka Lempeng Total sehingga didapatkan hasil 3250 CFU/gr. Morfologi koloni bakteri pada setiap cawan pengenceran terlihat seragam, berbentuk bulat dengan diameter 3-7 mm, mengkilat, memiliki permukaan yang datar dan halus, serta berwarna keputih-putihan.
Berdasarkan hasil di atas, nilai Angka Lempeng Total memenuhi persyaratan yang ditentukan oleh BPOM RI (2019) untuk bentuk sediaan obat dalam yaitu ≤105 koloni/gr dan memenuhi persyaratan obat luar semi padat yaitu ≤107 koloni/gr. Kontaminasi mikroba pada bahan baku sediaan obat perlu diminimalisir. Pada sediaan obat luar semi padat untuk luka, kehadiran mikroba perlu diminimalisir karena cemaran mikroorganisme akan masuk ke luka dan membentuk koloni di tempat yang tidak seharusnya. Kontaminasi bakteri akan menyebabkan terjadinya infeksi sekunder yang justru membuat keadaan menjadi buruk dan mengganggu proses kesembuhan.
Salah satu faktor yang menyebabkan tingginya nilai Angka Lempeng Total adalah kadar air yang tinggi dalam serbuk daun karena air merupakan salah satu faktor pertumbuhan yang terpenting bagi mikroba. Pengeringan menggunakan oven tidak menjamin dapat menghilangkan keberadaan mikroba apabila kadar air yang terkandung pada daun masih dalam persentase yang tinggi. Semakin tinggi kadar air yang ada pada ekstrak daun maka semakin tinggi kemungkinan terjadinya pertumbuhan bakteri. Pengeringan daun pegagan yang tidak sempurna dan lingkungan penyimpanan sekitar yang lembab dapat meningkatkan pertumbuhan mikroba. Ekstrak daun yang sudah dibuat dalam bentuk serbuk perlu disimpan pada wadah yang tertutup, diletakkan pada suhu kamar atau di tempat yang kering serta terlindung dari paparan sinar matahari (Kepmenkes RI, 1994).
Karena tidak ada cawan petri yang memiliki koloni 40-60 maka angka sebenarnya dicatat dari pengenceran terendah dan dihitung sebagai Angka Kapang Khamir perkiraan (Depkes RI, 2000). Pada cawan 1 pengenceran pertama terlihat dengan jelas 5 koloni (3 kapang, 2 khamir) dan pada cawan 2 (duplo) pengenceran pertama terdapat 4 koloni (3 kapang, 1 khamir). Rata-rata koloni cawan
pertama yaitu 4,5 koloni kemudian dikalikan dengan faktor pengenceran dan volume sesuai rumus perhitungan oleh Depkes RI (2000) sehingga didapatkan nilai pengenceran pertama berjumlah 450 CFU/gr. Pada pengenceran ketiga dan keempat tidak ada pertumbuhan koloni yang terlihat. Hasil penghitungan pengenceran pertama kemudian disebut dengan nilai Angka Kapang Khamir perkiraan yang berjumlah 450 CFU/gr.
Kapang (mould) adalah fungi multiseluler berbentuk serabut seperti kapas yang dapat menghasilkan metabolit beracun yang disebut mikotoksin yang akan menimbulkan berbagai penyakit sehingga perlu dihindarkan kehadirannya. Khamir (yeast) adalah mikroba bersel tunggal dari golongan fungi yang dapat bersifat saprofit maupun parasitik (Widiastutik dan Alami, 2014). Koloni kapang yang tumbuh berbentuk seperti filamen yang disebut hifa dengan pigmen warna putih-kekuningan sedangkan khamir yang tumbuh berbentuk bulat seperti koloni bakteri berukuran 3-10 mm dengan pigmen putih pekat. Nilai Angka Kapang Khamir telah memenuhi persyaratan yang ditentukan oleh BPOM RI (2019) untuk obat dalam yaitu ≤103 koloni/gr, serta memenuhi persyaratan obat luar semi padat, yaitu ≤104 koloni/gr.
Tingginya Angka Kapang Khamir disebabkan oleh kadar air dalam serbuk ekstrak daun pegagan yang masih tinggi. Hal ini berhubungan dengan proses pengeringan yang tidak sempurna, yang akan menyebabkan kadar air pada ekstrak daun masih tinggi meskipun sudah dilakukan pengeringan menggunakan oven. Tingginya kadar air akan memfasilitasi pertumbuhan kapang dan khamir. Salah satu usaha untuk mengurangi kontaminasi kapang dan khamir yaitu perlu dilakukan proses pencucian sampel daun berulang sampai bersih. Metode penyimpanan serbuk daun yang sudah dibuat juga penting, serbuk harus diletakkan dalam wadah tertutup pada suhu kamar tanpa paparan sinar matahari (Kepmenkes RI, 1994).
SIMPULAN DAN SARAN
Simpulan
Angka Lempeng Total sampel daun pegagan 3250 CFU/gr dan Angka Kapang Khamir 450 CFU/gr. Nilai Angka Lempeng Total memenuhi persyaratan sediaan obat dalam (≤105 koloni/gr) dan memenuhi persyaratan sediaan obat luar semi padat (≤107 koloni/gr). Nilai Angka Kapang Khamir memenuhi persyaratan sediaan obat dalam (≤103 koloni/gr) dan memenuhi persyaratan sediaan obat luar semi padat (≤104 koloni/gr). Sampel daun pegagan (Centella asiatica (L.) Urban) yang diproduksi telah memenuhi persyaratan cemaran mikroba kuantitatif menurut BPOM RI (2019) dan layak untuk diproduksi menjadi sediaan obat.
Saran
Sterilisasi sampel daun menggunakan radiasi sinar Gamma dapat dilakukan untuk menurunkan jumlah cemaran mikroba apabila peralatan produksi memadai. Pemberian bahan aktif alami tambahan dapat diberikan untuk meningkatkan kualitas mutu sediaan. Diperlukan penelitian lebih lanjut untuk mengetahui keberadaan cemaran mikroba patogen pada sampel daun pegagan yang telah diproduksi.
UCAPAN TERIMA KASIH
Ucapan terima kasih ditujukan kepada dosen pembimbing dan dosen penguji atas segala masukan dan bimbingan yang telah diberikan serta staf Laboratorium Mikrobiologi Pangan Fakultas Teknologi Pertanian, Universitas Udayana.
DAFTAR PUSTAKA
Basarang M, Naim N, Rahmawati. 2018. Perbandingan pertumbuhan jamur pada media Bekatul Dextrose Agar (BDA) dan Potato Dextrose Agar (PDA). Proc. Seminar Hasil Penelitian (SNP2M). 2018: 121-125.
Bhavna D dan Jyoti K. 2011. Centella asiatica: The elixir of life. Int. J. Res. Ayurveda Pharm. 02(2): 431-38.
BPOM RI. 2019. Peraturan kepala badan pengawas obat dan makanan Republik Indonesia Nomor 32 tahun 2019 tentang persyaratan keamanan dan mutu obat tradisional. Badan Pengawas Obat dan Makanan Republik Indonesia. Jakarta.
Departemen Kesehatan Republik
Indonesia. 2000. Parameter standar umum ekstrak tumbuhan obat. Edisi I. Jakarta.
Josi K, Chaturvedi P. 2013. Therapeutic efficiency of centella asiatica (l.) urb. an underutilized green leafy vegetable: an overview. Int. J. Pharm. Bio. Sci. 04(1): 135-149.
Keputusan Menteri Kesehatan RI. 1994. Keputusan Menteri Kesehatan Republik Indonesia Nomor:
661/MENKES/SK/VII/1994 tentang
persyaratan obat tradisional. Menteri Kesehatan Republik Indonesia. Jakarta.
Lisiswanti R, Fiskasari SR. 2017. Manfaat pegagan (centella asiatica) terhadap pengobatan penyakit alzheimer. J. Majority. 06(2): 132-136.
Lokanathan Y, Omar N, Ahmad PNN, Saim A, Idrus R. 2016. Recent updates in neuroprotective and neuroregenerative potential of Centella asiatica. The Malaysian J. Med. Sci. 23(1): 4-14.
Lotulung PDN, Handayani S, Ernawati T, Yuliani T, Artanti N, Mozef T. 2015. Standarisasi ekstrak pegagan (Centella asiatica) sebagai obat herbal terstandar hepatoprotektor. J. Kimia Terapan Indon. 17: 185-193.
Megariyanthi NPA, Wirawan IG, Suartha IN, Sudimartini LM. 2018. Efektivitas ekstrak etanol daun pegagan terhadap bakteri Micrococcus luteus diisolasi dari dermatitis kompleks anjing. Indon. Med. Vet. 07(5): 475-481.
Orhan IE. 2012. Centella asiatica (L.) urban: from traditional medicine to
modern medicine with neuroprotective potential. Evidence-Based
Complement. Altern. Med. 2012: 1-8.
Pramantara IDP, Kertia N, Wahyuningsih MSH, Arfian N. 2018. Efek kapsul pegagan (Centella asiatica L.) terhadap disfungsi otot rangka pada relawan usia lanjut sehat. Traditional Med. J. 23(2): 142-148.
Singh S, Gautam A, Sharma A, Batra A. 2010. Centella asiatica (L.): a plant with immense medicinal potential but threatened. Int. J. Pharm. Sci. Rev. Res. 04(2): 9-17.
Sutardi. 2016. Kandungan bahan aktif tanaman pegagan dan khasiatnya untuk meningkatkan sistem imun tubuh. J. Penelitian dan Pengembangan Pertanian. 35(3): 121-130.
Wati RY. 2018. Pengaruh pemanasan media plate count agar (PCA) berulang terhadap uji total plate count (TPC) di laboratorium mikrobiologi teknologi hasil pertanian unand. J. Teknol. Manajemen Pengelolaan Lab. 01(2): 44-47.
Widianingtyas D, Wihastuti TA, Setijowati N. 2014. Pengaruh perawatan dengan ekstrak daun pegagan (Centella asiatica) dalam mempercepat
penyembuhan luka bakar derajat 2 dangkal pada tikus putih (Rattus norvegicus) strain Wistar. Maj. Kesehatan FKUB. 01(4): 223-227.
Widiastutik N, Alami NH. 2014. Isolasi dan identifikasi yeast dari rhizosfer Rhizophora mucronata wonorejo. J. Sains Seni Pomits. 3(01): 11-16.
Widyastuti SK, Dewi NMS, Utama IH. 2012. Kelainan kulit anjing jalanan pada beberapa lokasi di Bali. Bul. Vet. Udayana. 04(2): 81-86.
Yusran I, Asriani S, Asri H. 2016. Bioaktivitas ekstrak metanol daun pegagan (Centella asiatica (L.) Urban) terhadap pertumbuhan bakteri
Mycobacterium tuberculosis. J. Al-Kimia. 04(1): 54-61.
|
Tabel 1. Hasil uji Angka Lempeng Total sampel serbuk daun pegagan | ||||
|
Pengenceran |
1 |
Jumlah koloni masing-masing cawan petri |
Nilai ALT (CFU/gr) | |
|
2 (Duplo) |
Rata-rata | |||
|
10-1 |
34 |
31 |
32,5 |
3250 |
|
10-2 |
8 |
5 |
6,5 |
- |
|
10-3 |
0 |
0 |
- |
- |
|
10-4 |
0 |
0 |
- |
- |
|
Nilai ALT (CFU/gr) |
3250 | |||
|
Tabel 2. Hasil uji Angka Kapang Khamir sampel serbuk daun pegagan | ||||
|
Pengenceran |
Jumlah koloni masing-masing Nilai AKK cawan petri | |||
|
1 |
2 (Duplo) |
Rata-rata |
(CFU/gr) | |
|
10-1 |
5 |
4 |
4,5 |
450 |
|
10-2 |
0 |
1 |
0,5 |
400 |
|
10-3 |
0 |
0 |
0 |
0 |
|
10-4 |
0 |
0 |
0 |
0 |
|
Nilai AKK (CFU/gr) |
450 | |||
Pengenceran 10-1
Pengenceran 10-2
Gambar 1. Hasil uji Angka Lempeng Total
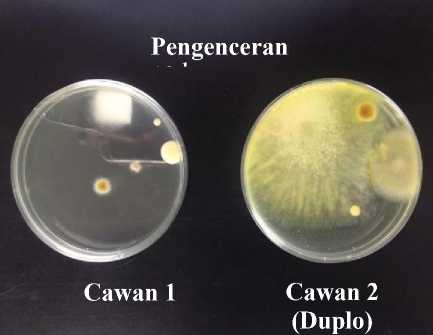
Cawan 1
Cawan 2 (Duplo)
Pengenceran
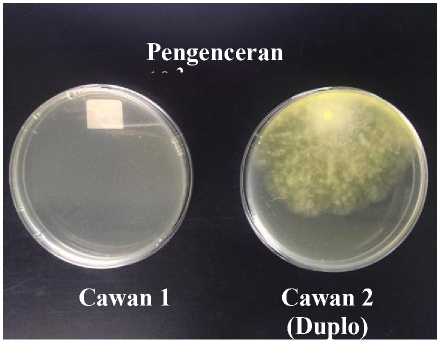
Gambar 2. Hasil uji Angka Kapang Khamir
326
Discussion and feedback