PENGARUH JUMLAH PEG 200 DAN TEMPERATUR ANNEALING TERHADAP MORFOLOGI DAN STRUKTUR NANOPARTIKEL TiO2 DENGAN METODE SINTESIS SIMPLE HEATING
on
PENGARUH JUMLAH PEG 200 DAN TEMPERATUR ANNEALING TERHADAP MORFOLOGI DAN STRUKTUR NANOPARTIKEL TiO2 DENGAN METODE SINTESIS SIMPLE HEATING
Tuty Emilia Agustina1, Fitri Suryani Arsyad2, Mikrajuddin Abdullah3
1Jurusan Teknik Kimia, Fakultas Teknik, Universitas Sriwijaya 2Jurusan Fisika, Fakultas MIPA, Universitas Sriwijaya 3Jurusan Fisika, Fakultas MIPA, Institut Teknologi Bandung Email: tutycurtin@yahoo.com
Abstract
The surface area of a photocatalyst is an important factor that effect decomposition process of colored wastewater. Increasing the catalyst particle surface area will increase the UV light absorbed thus enhance the photacatalysis process. Bulk TiO2 will have the higher surface area if it is made in the nano size. As a photocatalyst, nanoparticle of TiO2 is more efficient than bulk of TiO2. The nanoparticle of TiO2 can be made in various ways, for example by simple heating method. In this study, the synthesis of nanoparticle TiO2 was investigated by optimize the amount of polyethilene glycol (PEG 200) used and the annealing temperature. The amount of PEG 200 was varied between 6-18 ml. Moreover, the annealing temperature was varied in the range of 600-700oC. After synthesizing, the nanoparticles of TiO2 then characterize by using scanning electron microscope (SEM) to observe the morphology, and by using the X-ray difraction (XRD) to find the crystal structure and the particle size. Based on the characterization, it was found that the smallest nanoparticle of TiO2 have a 29 nm in size was produced by using the 12 ml of PEG at the annealing temperature of 600oC.
Keywords: photocatalyst, wastewater treatment, nanoparticle of TiO2, simple heating method
Saat ini, pencemaran lingkungan akibat limbah industri sudah cukup memprihatinkan. Salah satu limbah yang sangat mengganggu kelestarian lingkungan adalah limbah cair yang mengandung pewarna sintetis yang dihasilkan oleh industri tekstil skala besar maupun industri kecil dan menengah (IKM) (Utami, 1994). Limbah cair pewarna sintetis yang bersumber dari pabrik tekstil maupun tenun dapat mengakibatkan perubahan warna dan derajat keasaman badan penerima air. Limbah ini didominasi oleh pencemaran karena penggunaan zat warna sintetis dalam proses produksinya (Agustina dan Badewasta, 2009). Limbah ini dikategorikan sebagai limbah B3 (bahan berbahaya dan beracun). Meningkatnya kekeruhan air karena adanya polusi zat warna akan menghalangi masuknya cahaya matahari ke dasar perairan dan mengganggu
keseimbangan proses fotosintesis, ditambah lagi adanya efek mutagenik dan karsinogen dari zat warna tersebut, membuatnya menjadi masalah yang serius (Agustina dan Badewasta, 2009). Selain itu air limbah pabrik tekstil di Indonesia rata-rata mengandung 750 mg/l padatan tersuspensi dan 500 mg/l BOD. Perbandingan COD : BOD adalah dalam kisaran 1,5 : 1 sampai 3 : 1 (Manurung, 2002). Nilai ini jauh melebihi standar baku mutu lingkungan. Oleh karena itu limbah ini harus diolah dengan baik.
Untuk itu perlu disiapkan teknologi pengolahan limbah agar dampak pencemaran dapat dicegah dan dikendalikan. Beberapa teknologi pengolahan telah banyak dikembangkan untuk mengatasi permasalahan limbah pewarna sintetis seperti adsorpsi dengan menggunakan karbon aktif (Agustina, 2011), koagulasi dengan bahan kimia (Mujiadi dan Nieke, 2001) ataupun koagulasi dengan
penyaringan (Astuti, 2004), lumpur aktif (Sudarjanto, 2008), semikonduktor fotokatalisis (Agustina, 2012), maupun teknik peresapan alami (Purwadi, 2004). Namun, seringkali teknologi tersebut membutuhkan biaya operasional yang sangat mahal, baik dari segi pembelian bahan-bahan kimia, instalasi, dan penggunaan lahan, maupun dari segi waktu proses yang relatif lama (Agustina dkk, 2011). Tentu saja hal ini kurang efisien diterapkan pada Industri kecil dan menengah (IKM) karena biaya hasil produksi tidak sebanding dengan biaya pengolahan limbahnya.
Dalam dua dekade terakhir, telah banyak sekali dilakukan penelitian terhadap limbah industri tekstil dengan apa yang disebut AOPs. Oksidasi lanjutan terbentuk diantaranya system fotokatalisis heterogen dengan media TiO2 yang terinduksi cahaya matahari, terlihat telah memiliki kemampuan untuk menghilangkan warna secara sempurna dan setidaknya telah memineralisasi secara sebagian limbah warna industri tekstil dalam waktu reaksi yang singkat tanpa menghasilkan gas sisa pembakaran ataupun sludge yang berbahaya. Selain itu, tidak ada produk samping yang beracun dan atau bersifat karsinogenik yang teramati ketika menerapkan AOPs pada penghilangan warna air limbah tekstil (Arslan-Alaton, 2004).
Sedangkan untuk kandungan logam berat yang mungkin terkandung di dalam senyawa organik dapat teroksidasi sehingga dapat dengan mudah dilakukan proses pemisahan dari air yang telah diolah, dan selanjutnya logam berat akan dapat didaur ulang kembali dengan menggunakan proses selanjutnya. Hal ini menjadikan AOPs sebagai teknologi bersih dalam proses pengolahan air limbah pada industri tekstil (Sugiarto, 2009). Selain itu, pemanfaatan AOPs memiliki beberapa keunggulan di antaranya areal instalasi pengolahan air limbah yang tidak luas, waktu pengolahan cepat, penggunaan bahan kimia sedikit, dan air hasil pengolahannya dapat dipergunakan kembali (Agustina, 2009).
Dapat disimpulkan penggunaan metode alternatif ini dalam proses pengolahan air limbah industri tekstil merupakan pilihan yang lebih hemat energi (Agustina, 2009). Oleh sebab itu, metode fotokatalisis sebagai salah satu dari AOPs akan diterapkan dalam pengolahan limbah cair pewarna sintetis dalam penelitian ini.
Dalam metode semikonduktor fotokatalisis, sering digunakan bulk TiO2 sebagai bahan semikonduktor yang tidak transparan tetapi dapat menyerap radiasi ultraviolet (Abdullah, 2008). Jika dibuat dalam ukuran nano, maka nanopartikel TiO2 berubah menjadi sangat transparan dan menyerap radiasi ultraviolet lebih banyak (Abdullah, 2008). Karena sifatnya yang transparan dan mudah menyerap radiasi ultraviolet itulah maka nanopartikel TiO2 sangat efektif digunakan sebagai semikonduktor fotokatalis untuk mendekomposisi polutan limbah cair pewarna sintetis.
Banyak metode sintesis nanopartikel yang telah dikembangkan para peneliti. Di antara metode sintesis nanopartikel yang sederhana adalah menggunakan metode simple heating (pemanasan sederhana) dalam larutan polimer (Abdullah, 2008).
Secara sederhana, prinsip kerja metode ini adalah mencampurkan larutan logam nitrat di dalam air dengan larutan polimer dengan berat molekul tinggi (high molecular weight polymer, HMWP), seperti Polyethylene glycol, H(OCH2-CH2)nH yang disingkat PEG. Kedua larutan dicampur dan diaduk secara merata disertai pemanasan sehingga kandungan air hampir habis dan diperoleh larutan kental polimer. Di dalam larutan tersebut diperkirakan ion-ion logam menempel secara merata pada rantai polimer. Larutan polimer kemudian ditempatkan dalam krusibel alumina dan dipanaskan pada suhu di atas suhu dekomposisi polimer. Suhu operasi di atas 500oC sudah cukup untuk mendekomposisi sejumlah polimer. Suhu pemanasan dinaikkan secara perlahan-lahan. Keberadaan polimer menghindari pertemuan antar partikel yang terbentuk melalui proses nukleasi sehingga tidak terjadi agglomerasi. Ketika polimer telah terdekomposisi didapatkan partikel-partikel yang hampir terpisah satu dengan lainnya. Ukuran partikel dikontrol dengan mengatur konsentrasi polimer, mengatur suhu pemanasan, dan mengatur lama waktu pemanasan dalam oven (Abdullah, 2008).
PEG merupakan sekelompok polimer sintetik yang larut air dan memiliki kesamaan struktur kimia berupa adanya gugus hidroksil primer pada ujung rantai polieter yang mengandung oksietilen (-CH2-CH2-O-) (Kuixiong, 1993). Struktur PEG dapat digambarkan seperti pada gambar 1.
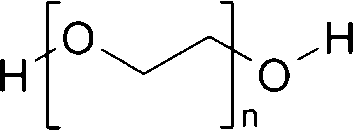
Gambar 1. Struktur Polyethylene glycol (PEG). Sumber : Kahovec, et al. (2002).
Perdana (2009) dalam penelitiannya mengenai sintesis dan karakterisasi nano Fe3O4 menggunakan PEG 1000 sebagai template. PEG adalah satu zat yang dapat dipakai untuk membentuk dan mengontrol ukuran dan struktur pori. Dalam hal ini PEG berfungsi sebagai template, dan juga pembungkus partikel besi sehingga tidak terbentuk agregat, hal ini dikarenakan PEG terjebak pada permukaan partikel dan menutupi ion positif besi, dan pada akhirnya akan diperoleh hasil partikel dengan bentuk bulatan yang seragam. Angka-angka yang sering termasuk dalam nama-nama PEG menunjukkan berat molekul rata-rata mereka, misalnya, PEG dengan n = 9 akan memiliki berat molekul rata-rata sekitar 400 daltons dan akan diberi label PEG 400 (Perdana, 2009).
Dalam penelitian ini digunakan PEG 200 dan dipelajari pengaruh jumlah PEG 200 dan temperatur annealing dalam sintesis nanopartikel TiO2 yang dibuat dengan metode simple heating. Nanopartikel TiO2 yang diperoleh diharapkan dapat diterapkan sebagai fotokatalis yang murah dan efisien.
Metode sintesis nanopartikel TiO2 yang digunakan dalam penelitian ini adalah metode simple heating. Titanium (IV) cloride tetrahidrofuran (Ti(ClH)4) dan polyetylene glycol (PEG 200) digunakan sebagai bahan sintesa nanopartikel Titanium dioksida (TiO2). Titanium (IV) cloride tetrahidrofuran (Ti(ClH)4) dengan jumlah molaritas tertentu, dilarutkan kedalam deionized water. Polyethylene glycol (PEG 200) dalam jumlah yang cukup ditambahkan kedalam larutan disertai pengadukan hingga diperoleh larutan jernih. Larutan kemudian dipanaskan pada suhu di atas 100oC hingga menjadi kental yang kemudian dilanjutkan dengan pemanasan pada suhu diatas suhu dekomposisi PEG 200 selama 30 puluh menit di dalam oven sehingga dihasilkan partikel dengan ukuran beberapa puluh nanometer hingga beberapa ratus nanometer. Ukuran
partikel dikontrol dengan mengatur jumlah PEG 200 yang digunakan dan mengatur suhu pemanasan. Jumlah PEG 200 divariasikan 6-18 ml dan temperatur annealing divariasikan 600-700oC. Nanopartikel TiO2 yang sudah terbentuk kemudian dikarakterisasi menggunakan SEM untuk mengamati morfologinya, dan XRD untuk mengetahui stuktur kristal dan ukuran
Dalam penelitian ini, nanopartikel TiO2 akan dibuat dengan metode simple heating dengan mengoptimasi parameter sintesis yaitu jumlah pemakaian PEG 200 dan temperatur. Nanopartikel TiO2 yang sudah disintesis kemudian dikarakterisasi morfologi dan struktur serta ukuran butirnya masing-masing dengan menggunakan scanning electron microscope (SEM) dan X-ray difraction (XRD). Pengaruh jumlah pemakaian PEG 200 terhadap ukuran butir nanopartikel TiO2 dilaporkan berdasarkan analisa dari hasil pengamatan menggunakan XRD. Untuk memastikan bahwa sampel yang dihasilkan adalah nanopartikel TiO2 digunakan analisis elemen atau karakterisasi kimia dengan teknik analisis energy-dispersive X-ray spectroscopy (EDX) berdasarkan struktur atom yang terbentuk (Goldstein, 2003). Berdasarkan hasil analisa EDX, terbukti bahwa dengan menggunakan (Ti(ClH)4) dan PEG 200 dapat dihasilkan nanopartikel TiO2 dengan menggunakan metode simple heating.
Gambar 2 dan 3 adalah gambar pola XRD dan foto SEM sampel nanopartikel TiO2 yang disintesa dengan PEG 200 masing-masing sejumlah 6 ml, 12 ml, dan 18 ml.
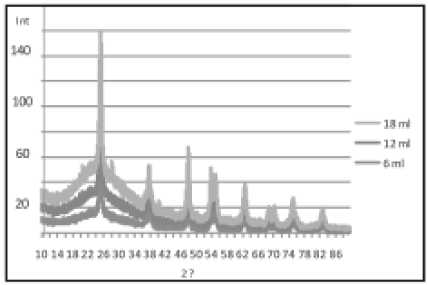
Gambar 2. Hasil XRD untuk nanopartikel TiO2 dengan pemakaian PEG 200 a) 6 ml, b) 12 ml, dan c) 18 ml.

Gambar 3. Foto SEM nanopartikel TiO2 dengan pemakaian PEG 200
-
a) 6 ml, b) 12 ml, dan c) 18 ml.
Dari Gambar 2 terlihat bahwa semakin banyak PEG 200 yang ditambahkan, semakin tinggi intensitasnya dan semakin lebar puncak-puncak difraksi yang dihasilkan. Hal ini disebabkan karena semakin banyak rantai PEG 200, maka semakin merata distribusinya melapisi butiran-butiran atom TiO2. Distribusi PEG 200 yang merata menutupi permukaan atom-atom TiO2 akan menghalangi terjadinya aglomerasi atom-atom TiO2, sehingga memperkecil ukuran butirnya (3.2a dan 3.2b). Ukuran butir yang mengecil akan memperlebar Full Width at Half Maximum (FWHM) pada pola difraksi sinar-X yang dihasilkan (Linerlinah, 2009). Dari hasil perhitungan ukuran butir dengan metoda Scherrer diperoleh nanopartikel yang disintesa dengan pemakaian PEG 200 sebanyak 6 ml, 12 ml, dan 18 ml, masing-masing memiliki ukuran butir rata-rata sebesar 31 nm, 29 nm, dan 26 nm. Meskipun ukuran butir nanopartikel TiO2 yang disintesa dengan pemakaian PEG 200 sebanyak 18 ml memiliki ukuran paling kecil, namun berdasarkan hasil foto SEM (3.2c) teramati adanya penggumpalan partikel. Hal ini menunjukan bahwa ada batas optimum jumlah pemakaian PEG yang dibutuhkan untuk melapisi atom-atom TiO2 secara sempurna. Karena jika terlalu banyak, maka PEG akan menutupi seluruh permukaan atom dan menghalangi terbentuknya butiran-butiran nano TiO2, seperti terlihat pada Gambar 3c. Oleh karena itu dalam penelitian ini, optimasi temperatur annealing dilakukan pada pemakaian PEG sebanyak 12 ml.
-
3.1. Pengaruh Temperatur Annealing
Untuk melihat pengaruh temperatur terhadap perubahan struktur dan morfologi permukaan nanopartikel TiO2 yang disintesa dengan metode simple heating, digunakan digunakan PEG 200 sebanyak 12 ml. Optimasi temperatur annealing dilakukan dengan memvariasikan temperatur dari 600 sampai 7000C. Gambar 4 dan 5 adalah pola XRD dan foto SEM dari nanopartikel TiO2 yang disintesa dengan temperatur annealing masing-masing sebesar a) 600oC, b) 650oC, dan c) 700oC.
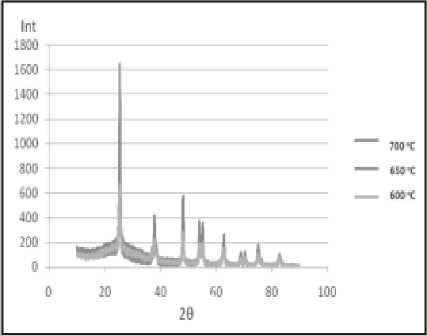
Gambar 4. Pola difraksi sinar-X dari nanopartikel TiO2 yang disintesa dengan temperatur annealing masing-masing sebesar 600oC, 650oC, dan 700oC

Gambar 5. Foto SEM dari nanopartikel TiO2 yang disintesa dengan temperatur annealing masing-masing sebesar 600oC, 650oC, dan 700oC
Dari Gambar 4 terlihat bahwa semakin besar temperatur annealing, semakin menurun intensitasnya puncak-puncak difraksi yang dihasilkan. Dari perhitungan metode Scherrer berdasarkan data XRD tersebut diperoleh ukuran butir nanopartikel untuk temperatur annealing 600oC, 650oC, dan 700oC masing-masing diperoleh sebesar 29 nm, 42 nm, dan 47 nm. Terlihat bahwa semakin tinggi temperatur annealing semakin besar ukuran butir nanopartikel TiO2. Hal ini disebabkan karena temperatur annealing yang tinggi dapat meningkatkan distribusi ion-ion PEG. Ion-ion PEG akan bermigrasi ke kisi-kisi struktur kristal sehingga menyebabkan terjadinya penggumpalan atom-atom titania, seperti terlihat pada Gambar 5b dan 5c. Dari hasil optimasi pemakaian PEG dan temperatur annealing tersebut di atas terlihat bahwa kondisi optimum diperoleh untuk nanopartikel TiO2 yang disintesa dengan pemakaian PEG sebanyak 12 ml dan temperatur annealing 600oC.
Berdasarkan hasil analisa dapat disimpulkan bahwa semakin banyak jumlah pemakaian PEG 200 akan semakin kecil ukuran nanopartikel TiO2 yang dihasilkan, akan tetapi pada penggunaan PEG 18 ml teramati adanya gumpalan partikel. Selain itu, semakin tinggi temperatur annealing semakin besar ukuran butir nanopartikel TiO2 yang dihasilkan, sehingga pemakaian temperatur annealing yang rendah lebih baik di dalam sintesis nanopartikel dengan metode simple heating. Kondisi optimum sintesis nanopartikel TiO2 dicapai dengan penggunaan PEG 200 sebanyak 12 ml dan temperatur annealing 600oC, dimana diperoleh nanopartikel TiO2berukuran 29 nm.
Ucapan Terima Kasih
Penulis mengucapkan terima kasih kepada Direktorat Jendral Pendidikan Tinggi yang telah mendanai penelitian ini melalui Hibah Bersaing tahun 2011.
Daftar Pustaka
Abdullah, M. 2008. Pengantar Nanosains. Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung.
Agustina, T.E. 2009. Alternatif Pengolahan Air Limbah Industri Tekstil dengan Teknologi Bersih Hemat Energi: Suatu Tinjauan Pustaka. Prosiding Added Value of Energy Resources (AVOER) 2009. Palembang, 27-28 Juli 2009, 169-176.
Agustina, T.E. dan Badewasta, H. 2009. Pengolahan Limbah Cair Industri Batik Cap Khas Palembang dengan Proses Filtrasi dan Adsorpsi. Prosiding Seminar Nasional Teknik Kimia Indonesia 2009. Bandung, 19-20 Oktober 2009.
Agustina, T.E. 2011. “Pengolahan Air Limbah Pewarna Sintetis dengan Metode Adsorpsi Menggunakan Karbon Aktif”. Jurnal Rekayasa Sriwijaya, No. 1 Vol. 20, 36-42.
Agustina, T.E, Nurisman, E., Prasetyowati, Haryani, N., Cundari, L., Novisa, A. dan Khristina, O. 2011. Pengolahan Air Limbah Pewarna Sintetis dengan Menggunakan Reagen Fenton. Prosiding Added Value of Energy Resources (AVOER) 2011. Palembang, 26-27 Oktober 2011, 260-266
Agustina, T.E. 2012. Degradasi Pewarna Sintetis Procion Biru Menggunakan Metode Fotokatalisis dengan bantuan Sinar Matahari. Prosiding Added Value of Energy Resources (AVOER) 2012. Palembang, 28-29 November 2012.
Arslan-Alaton, I. 2004. “Advanced oxidation of textile industry dyes”. In Parson, S. Advanced Oxidation Processes for Water and Wastewater Treatment (pp 302-328). IWA Publishing, London, UK.
Astuti, F. 2004. Pengolahan Limbah Cair Industri Batik dengan Koagulan dan Penyaringan. Tesis. Program Pascasarjana Universitas Gadjah Mada, Yogyakarta
Kahovec, J., Fox, R.B., and Hatada, K. 2002. “Nomenclature of regular single-strand organic polymers”. Pure and Applied Chemistry, 74. 1921–1956.
Kuixiong, G. 1993. Polyethylene glycol as an embedment for microscopy and histochemistry. CRC Press, Oxfordshire, UK.
Goldstein, J. 2003. Scanning Electron Microscopy and X-Ray Microanalysis. Springer. New York, USA
Linerlinah, Abdullah, M dan Khairurrijal. 2009. “Sintesis nanokatalis CuO/ZnO/Al2O3 untuk mengubah metanol menjadi hidrogen untuk bahan bakar kendaraan fuel cell”. Jurnal Nanosains dan Nanoteknologi, Edisi khusus, 90-95.
Manurung, R. 2002. “Perombakan Zat Warna Azo Reaktif dengan Proses Anaerob-Aerob.” Jurnal Komunikasi Penelitian,14 No.6.
Mujiadi, S. dan Nieke, K. 2001. “Kemampuan Koagulan Poli Aluminium Khloride untuk Menurunkan Warna Effluent Pengolahan Limbah PT Sier.” Jurnal Purifikasi, 2, 271-276.
Nguyen, V. 2009. “Research on TiO2-Based Photocatalyst Thin Film and Its Application in a Pilot-Scale Supply Water Treatment System”. Environment Asia, 2. issue 1, 35-40.
Pavasupree, S., Ngamsinlapasathian, S., Nakajima. M., Suzuki, Y., Yoshikawa, S. and Kawahata, R. 2006. “Synthesis, characterization, photocatalytic activity and dye sensitized solar cell performance of nanorods/nanoparticles TiO2 with mesoporous structure”. J. Photochem. Photobio. A: Chem., 184, 163-169
Perdana, F. A. 2009, Sintesis dan karakterisasi partikel nano Fe3O4 dengan template PEG 1000, Jurusan Fisika, FMIPA, Institut Teknologi Sepuluh November, Surabaya
Purwadi, T. 30 Juni 2004. Teknik Peresapan Alami : UPL Jenggot Jadi Percontohan di Jateng. Suara Merdeka
Sudarjanto, G. 2008. Penyisihan Zat Warna CIRO-16 serta Kinetikanya Menggunakan Kombinasi Proses Kontak Stabilisasi dan Adsorpsi Karbon Aktif Jenis Granular. Thesis. Institut Teknologi Bandung, Bandung
Sugiarto, A.T. 2009. Pengolahan Air Limbah dengan Teknologi Bersih. http://task-list.blogspot.com/2008/ 03/pengolahan-air-limbah-dengan-teknologi.html, diakses tanggal 6 Mei 2009.
Utami, A. 22 September 1994. Industri-industri Penghasil Limbah B3. KOMPAS
57
Discussion and feedback